Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ЛЕЙКОЗЫ В ПРАКТИКЕ ПЕДИАТРА
Содержание
- 1. ЛЕЙКОЗЫ В ПРАКТИКЕ ПЕДИАТРА
- 2. Острые лейкозы — это злокачественные опухолевые заболевания
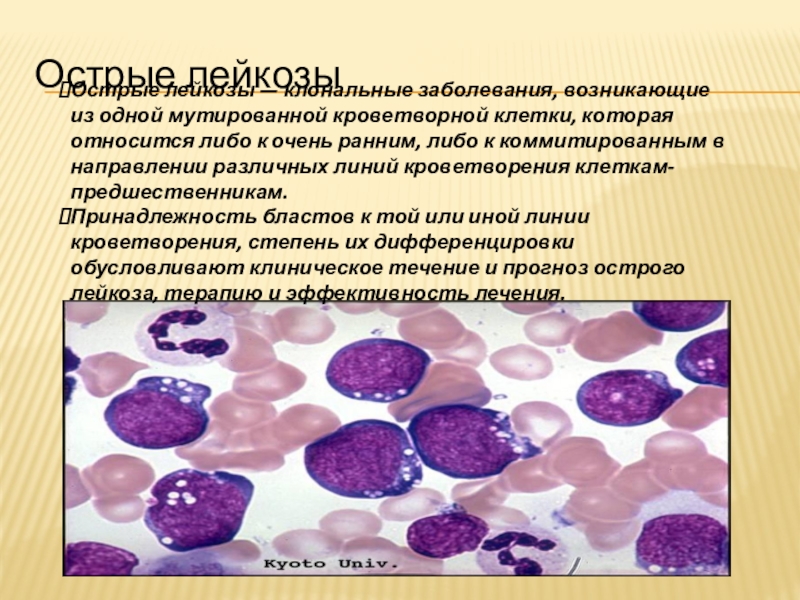
- 3. Острые лейкозы Острые лейкозы — клональные заболевания,
- 4. Статистика по РоссииСреди злокачественных новообразований кроветворной и
- 5. Статистика в архангельской областиПроведен предварительный анализ заболеваемости
- 6. Статистика в архангельской областиСреднегодовые показатели заболеваемости составили:
- 7. Статистика в архангельской областиПоказатели смертности для всех
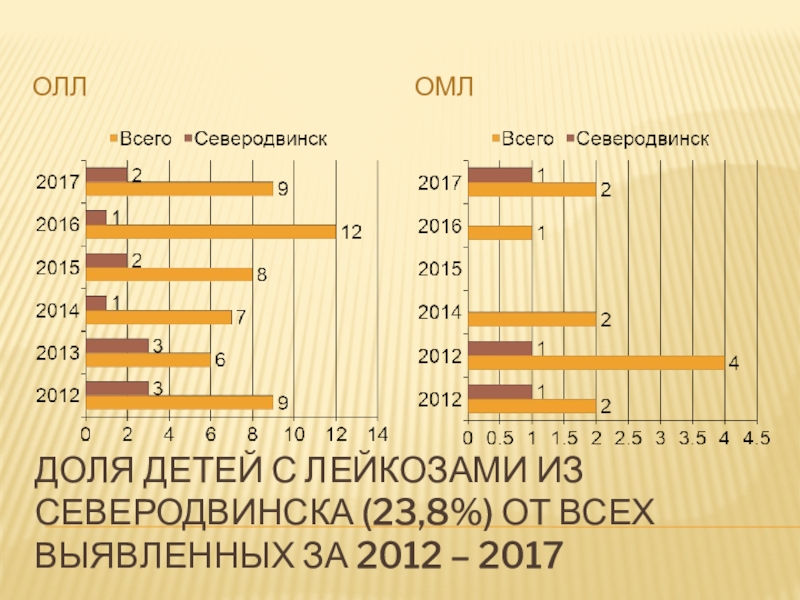
- 8. Доля детей с лейкозами из северодвинска (23,8%) от всех выявленных за 2012 – 2017 ОЛЛОМЛ
- 9. Клинические проявленияВ анализах периферической крови у детей
- 10. Клинические проявленияНаиболее ранними являются симптомы общей интоксикации,
- 11. Клинические проявленияК редким проявлениям ОЛЛ, но довольно
- 12. Клинические проявленияНесмотря на прогресс в лечении ОЛ,
- 13. Клинические проявления рецидиваКостномозговой рецидив обычно проявляет себя
- 14. Клинические проявления рецидиваЯички у мальчиков являются второй
- 15. омлБольшинство симптомов при ОМЛ отражает недостаточность нормального
- 16. Дифференциальный диагноз ОЛ у детейНезлокачественные заболевания:Ювенильный ревматоидный
- 17. Лечение Олл в аодкбЛечение детей с ОЛЛ
- 18. Лечение олл в аодкбС июля 2008 г.
- 19. Лечение олл в аодкбЖивы в ремиссии к
- 20. Слайд 20
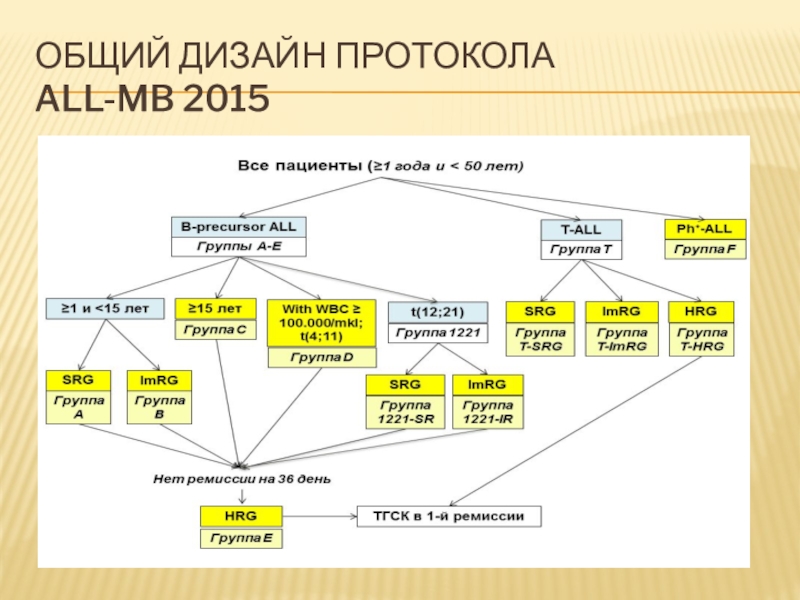
- 21. Общий дизайн протокола ALL-MB 2015
- 22. выводыУчастие в мультицентровом исследовании и терапия по
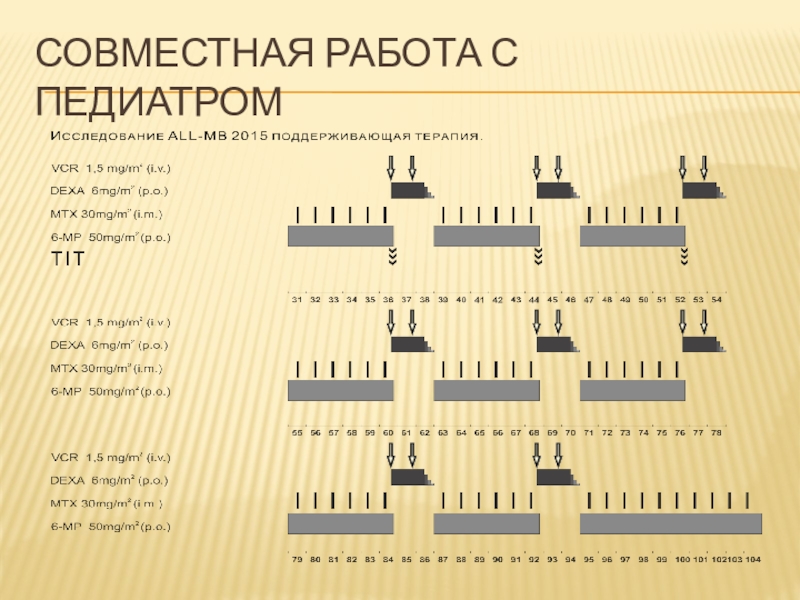
- 23. Совместная работа с педиатром
- 24. Поддерживающая терапияВажно помнить, что терапия 6-MP в
- 25. Поддерживающая терапияКонтроль лейкоцитоза в диапазоне от 2 000
- 26. Поддерживающая терапияВ первую неделю после реиндукции доза
- 27. Поддерживающая терапияПерерывом в приеме 6-MP считается только
- 28. Поддерживающая терапияСпециальная терапия во время сопутствующего острого
- 29. Поддерживающая терапияКатегорически противопоказано применение индукторов интерферона! Центральные
- 30. Благодарю за внимание
- 31. Скачать презентанцию
Острые лейкозы — это злокачественные опухолевые заболевания системы крови, первично поражающие костный мозг. Субстрат опухоли представлен незрелыми бластными клетками с «нежной» структурой ядерного хроматина, вытесняющими нормальные элементы и инфильтрирующими различные органы
Слайды и текст этой презентации
Слайд 2Острые лейкозы
— это злокачественные опухолевые заболевания системы крови, первично
поражающие костный мозг.
с «нежной» структурой ядерного хроматина, вытесняющими нормальные элементы и инфильтрирующими различные органы и ткани.Слайд 3Острые лейкозы
Острые лейкозы — клональные заболевания, возникающие из одной
мутированной кроветворной клетки, которая относится либо к очень ранним, либо
к коммитированным в направлении различных линий кроветворения клеткам-предшественникам.Принадлежность бластов к той или иной линии кроветворения, степень их дифференцировки обусловливают клиническое течение и прогноз острого лейкоза, терапию и эффективность лечения.
Слайд 4Статистика по России
Среди злокачественных новообразований кроветворной и лимфоидной ткани, составляющих
половину всех злокачественных опухолей детей, на долю лейкозов приходится 38—40%.
Частота острых лейкозов у детей до 15 лет составляет 4,1 ± 0,4 случаев на 100 000 детского населения, с пиком заболевания в возрасте от 2 до 5 лет. Болеют преимущественно мальчики.
У детей на ОЛЛ приходится 80%, на ОМЛ — 15-17%, на бифенотипический и недифференцированные формы около 1-2%.
Слайд 5Статистика в архангельской области
Проведен предварительный анализ заболеваемости и смертности при
острых лейкозах (ОЛ) у детей (от 0 до 17 лет)
в Архангельской области за 16-тилетний период (с 2002 по 2017гг.).Всего за период наблюдения было зарегистрировано 138 случаев острого лейкоза у детей.
Из них 110 (79,7%) случаев острого лимфобластного лейкоза (ОЛЛ) и 21 случаев (20,3%) острого нелимфобласного лейкоза (ОНЛЛ).
Соотношение заболевших мальчиков и девочек оказалось следующим: при всех ОЛ-1,9:1; для ОЛЛ – 2,3:1; для ОНЛЛ – 1:1.
Слайд 6Статистика в архангельской области
Среднегодовые показатели заболеваемости составили: для всех ОЛ
– 3,81±0,21; для ОЛЛ – 2,75±0,18; для ОНЛЛ 1,06±0,24 на
100000 детского населения указанной возрастной категории.Заболеваемость ОЛЛ в Архангельской области составляет 1,04-4,99 на 100000 детского населения (2002 – 2016 гг.).
Слайд 7Статистика в архангельской области
Показатели смертности для всех случаев ОЛ: наибольший
в 2009 г. составил 1,68 на 100 000 детского населения;
наименьший – составил 0 в 2002 г.Средний показатель смертности от лейкозов составил 0,52±0,18.
Таким образом, на фоне оптимизации программной терапии со строгим соблюдением регламента протоколов отмечается значительное снижение смертности и повышение выживаемости пациентов с данным заболеванием.
Слайд 9Клинические проявления
В анализах периферической крови у детей с ОЛ обычно
наблюдается снижение уровня гемоглобина, количества эритроцитов, тромбоцитов.
В зависимости от
лейкоцитоза различают случаи с нормальным, сниженным (1 *109/л и менее) и повышенным (20 *109/л и более, вплоть до 500 109/л) количеством лейкоцитов. Повышенное количество лейкоцитов (> 10*109/л) определяется приблизительно у 1/2 больных, а более 50* 109/л — у 1/5 пациентов.
Основным показателем заболевания является появление бластных клеток, количество которых может варьировать (от 1-2 до 90% и более).
Однако могут быть случаи с отсутствием бластных клеток в периферической крови.
Иногда первым проявлением ОЛЛ является гиперэозинофилия.
Слайд 10Клинические проявления
Наиболее ранними являются симптомы общей интоксикации, анорексия без значительной
потери массы тела и боли в костях, обусловленные леикозной инфильтрацией
периоста и костной ткани; чаще при этом поражаются трубчатые кости (диафиз), особенно бедренная и большеберцовая, но в процесс может быть вовлечен и позвоночник с развитием синдрома бревиспондилии.Артралгии связаны с лейкемической инфильтрацией суставов, что бывает порой трудно дифференцировать от таких заболеваний, как ревматоидный артрит или остеомиелит.
Кожные покровы и видимые слизистые у большинства больных отличаются бледностью.
Характерным признаком острого лейкоза является геморрагический синдром, проявляющийся полиморфными кровоизлияниями (от петехий до кровоизлияний крупных размеров) на коже и кровотечениями со слизистых оболочек (носовые, желудочно-кишечные, почечные).
Одним из характерных симптомов ОЛ у детей является безболезненное увеличение периферических лимфатическихузлов, наиболее часто — шейных, подмышечных, паховых.
Слайд 11Клинические проявления
К редким проявлениям ОЛЛ, но довольно частым при ОМЛ,
относятся изменения на коже и в подкожной клетчатке в виде
лейкемидов, некротические поражения кожи и слизистой ротовой полости (гингивит, стоматит от катарального до язвенно-некротического) и кишечника (энтеропатия).Развитие их связано с лейкемической инфильтрацией слизистых, тканей и сосудов, наличием кровоизлияний и присоединением инфекций.
При ОЛ у детей возможно вовлечение в процесс ЦНС, половых органов, глаз и легких.
Слайд 12Клинические проявления
Несмотря на прогресс в лечении ОЛ, в 15—20% случаев
наблюдаются рецидивы заболевания.
Рецидивы могут характеризоваться различной локализацией: костномозговой, экстрамедуллярный
с поражением ЦНС (нейролейкоз), половых органов и др. (кожа, кости, орбита, легкие, миндалины). Вместе с тем, возможны комбинированные рецидивы (сочетание лейкемического поражения костного мозга с другими локализациями).
Слайд 13Клинические проявления рецидива
Костномозговой рецидив обычно проявляет себя как первичный лейкоз.
Нейролейкоз
встречается обычно между 1-м и 3-м годами от момента установления
диагноза и проявляется симптомами повышенного внутричерепного давления, а именно, головными болями, диплопией тошнотой и рвотой, и/или отеком диска зрительного нерва. В редких случаях, поражением ЧМН, гипоталамическим синдромом или полифагией.Слайд 14Клинические проявления рецидива
Яички у мальчиков являются второй по частоте локализацией
экстрамедуллярного лейкозного поражения. Определяется пальпаторно по безболезненному увеличению, уплотнению яичек
и семенных канатиков. У девочек может быть поражение яичников.Кожные поражения проявляются в виде высыпаний, чаще папулезного характера, пигментного или безпигментного типа, отличаются упорной перманентностью течения и постепенным нарастанием проявлений несмотря на предпринимаемую терапию.
Слайд 15омл
Большинство симптомов при ОМЛ отражает недостаточность нормального кроветворения (изменения в
ОАК) и более быструю инвазию опухолевых клеток в экстрамедуллярные органы
и ткани: кожу, слизистые полости рта (гингивит), орбиту, головной и спинной мозг.При ретроспективном анализе клинические проявления ОМЛ обычно начинают отмечаться родителями пациента за 2—4 нед., иногда за 1—2 мес. до установления диагноза.
Слайд 16Дифференциальный диагноз ОЛ у детей
Незлокачественные заболевания:
Ювенильный ревматоидный артрит
Инфекционный мононуклеоз
Идиопатическая тромбоцитопеническая
пурпура
Коклюш, паракоклюш
Апластическая анемия
Острый инфекционный лимфоцитоз
Опухоли:
Нейробластома
Ретинобластома
Рабдомиосаркома
Неходжкинская лимфома
Саркома Юинга
Остеосаркома
Редкие состояния:
Синдром
гиперэозинофилииСлайд 17Лечение Олл в аодкб
Лечение детей с ОЛЛ в АОДКБ проводится
с 1982 года по различным схемам. Для сравнения: общая выживаемость
в 1982-1991 гг. составляла около 8,9%. В 1991-2003 гг. применялся протокол ALL–BFM –90, выживаемость возросла до 56%.С апреля 2003 г. наша клиника вступила в мультицентровое кооперативное исследование ALL – MB – 2002, при этом 5-тилетняя выживаемость пациентов к 2014 г. составляла 63,3%.
Слайд 18Лечение олл в аодкб
С июля 2008 г. пациенты с ОЛЛ
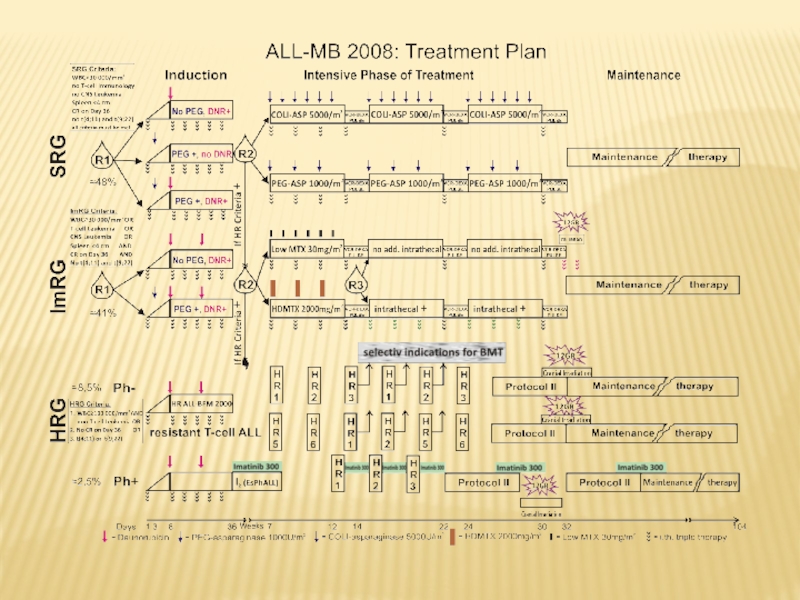
получали терапию по протоколу ALL – MB – 2008. Всего
пролечено 40 больных в возрасте 1,6 – 16 лет (медиана - 3 года). Ремиссия достигнута у 39 (97,4%); 1 (2,5%) – умер в индукции. Рецидивы (4) оказались все изолированными костномозговыми, из них очень ранний - у 1 пациента (2,5%), ранний – 1 (2,5%), поздний – 2 (5,1%). Выбыло из-под наблюдения 3 (7,7%) пациента. Умерло на разных этапах терапии и в продолжительной ремиссии всего 7 (17,9 %). ТГСК проведена – 2 (5,1%), из них родственная - 1 (умер от осложнений); неродственная – 1 (жив в полной ремиссии-2).Слайд 19Лечение олл в аодкб
Живы в ремиссии к настоящему времени (под
наблюдением) 30 детей.
5-тилетняя выживаемость пациентов (по Kaplan-Meyer) общая 86,0%;
бессобытийная -79,3%.С декабря 2014 г. клиника перешла на лечение детей с ОЛЛ по протоколу ALL–MB–2015. Всего зарегистрировано 30 пациентов, возраст от 1 лет до 17.
1 пациент развил очень ранний ЦНС – рецидив.
1 пациент погиб от токсичности терапии в ремиссии.
Слайд 22выводы
Участие в мультицентровом исследовании и терапия по протоколам ALL–MB привело
к значимому повышению выживаемости пациентов с ОЛЛ (общая 86,0%; бессобытийная
-79,3%).Оптимизация лечения по протоколу ALL–MB–2008 и 2015 привела к снижению смертности (в первую очередь, индукционной) и числа рецидивов.
Слайд 24Поддерживающая терапия
Важно помнить, что терапия 6-MP в ранние сроки после
индукции является критически важной для предотвращения, в том числе, ранних
рецидивов.Задачей является такая юстировка доз, прежде всего 6-MP, чтобы лейкоциты стабильно держались в пределах от 2 000 до 3 000/мкл, не допуская как развития аплазии, так и увеличения лейкоцитов выше 3 500/мкл. Эта доза и должна считаться для данного больного его индивидуальной терапевтической (она может составлять от 10% до 150% от стартовой, в зависимости от индивидуальных особенностей метаболизма).
Слайд 25Поддерживающая терапия
Контроль лейкоцитоза в диапазоне от 2 000 до 3 500/мкл является
основным ориентиром при подборе дозы 6-MP и MTX.
При подборе
доз особенно 6-MP следует стараться «играть на опережение», прогнозируя динамику изменения количества лейкоцитов в крови у конкретного больного, и, по возможности, не допуская перерывов в приёме 6-MP. Слайд 26Поддерживающая терапия
В первую неделю после реиндукции доза 6-MP и метотрексата
должна составлять не более 100% (даже, если лейкоциты более 3 000/мкл).
Коррекция дозы 6-MP и метотрексата может происходить асинхронно. Поэтому, при снижении лейкоцитов следует в первую очередь снижать дозу метотрексата.
Слайд 27Поддерживающая терапия
Перерывом в приеме 6-MP считается только пропуск препарата в
течение недели и более.
Даже, если пациент получает препарат только
2 раза в неделю, это уже не считается перерывом в терапии. Поэтому для адекватного дозирования 6-MP его нужно рассчитывать не на один день, а на неделю, и распределять эту дозу таким образом в течение недели, чтобы каждый день пациент получал рассчитанную дозу. При этом допускается пауза в приеме в какие-то дни недели
Слайд 28Поддерживающая терапия
Специальная терапия во время сопутствующего острого заболевания должна быть
приостановлена, если у пациента есть симптомы интоксикации, повышение Т тела
более 37,5С.Как только состояние пациента стабилизируется возобновляем химиотерапию с обязательным контролем ОАК, нередко под *прикрытием* антибиотиков.
Необходимо в более ранние сроки назначать антибиотики широкого спектра, т.к. у иммунокомпроментированных детей быстро развивается генерализация процесса с развитием сепсиса.
Слайд 29Поддерживающая терапия
Категорически противопоказано применение индукторов интерферона! Центральные клиники отказались от
применения даже препаратов, содержащих интерфероны, но обоснованных клинических исследований о
вреде их применения у детей с ОЛ до настоящего времени не представлено, поэтому мы при тяжелом течении вирусных инфекций их применяем.Необходимо помнить о подверженности данных пациентов грибковой инфекции, вплоть до инвазивных форм, поэтому раннее назначение и противогрибковых препаратов будет оправдано.