Слайд 1Методы окрашивания микроорганизмов
Слайд 2Особенности разных видов микроскопии
Основными задачами микроскопии являются следующие:
Выявление микроорганизмов в
различных материалах.
Ориентировочная идентификация микроорганизмов в образце.
Изучение некоторых морфологических признаков и
структур микроорганизмов (например, капсул, жгутиков и т. д.).
Изучение окрашенных мазков из колоний и чистых культур.
На сегодняшний день наиболее используемой является световая микроскопия.
Слайд 3Световая микроскопия обеспечивает увеличение до 2–3 тысяч раз, цветное и
подвижное изображение живого объекта, возможность микрокиносъемки и длительного наблюдения одного
и того же объекта, оценку его динамики и химизма.
Слайд 4Световая микроскопия включает обычную просвечивающую микроскопию (светло-, темнопольную), фазово-контрастную, люминесцентную.
В последнее время разработаны и другие способы микроскопии и микроскопы
– инверсионная и конфокальная лазерная сканирующая микроскопия.
Слайд 5Светлопольная микроскопия позволяет исследовать объекты в проходящем свете в светлом
поле. Данный вид микроскопии предназначен для исследования морфологии, размеров клеток,
их взаимного расположения, структурной организации клеток и других особенностей.
Слайд 6Фазово-контрастное приспособление дает возможность увидеть в микроскоп прозрачные объекты. Они
приобретают высокую контрастность изображения, которая может быть позитивной или негативной.
Благодаря применению этого способа микроскопии контраст живых неокрашенных микроорганизмов резко увеличивается и они выглядят темными на светлом фоне (позитивный фазовый контраст) или светлыми на темном фоне (негативный фазовый контраст).
С помощью фазово-контрастной микроскопии изучают форму, размеры, взаимное расположение клеток, их подвижность, размножение, прорастание спор микроорганизмов и т. д.
Слайд 7Темнопольная микроскопия основана на освещении объекта косыми лучами света. При
таком освещении лучи не попадают в объектив, поэтому поле зрения
выглядит темным. Темнопольная микроскопия является очень простым, но эффективным методом и хорошо подходит для получения изображения живых и неокрашенных биологических образцов. Учитывая простоту установки, качество получаемых изображений весьма хорошее.
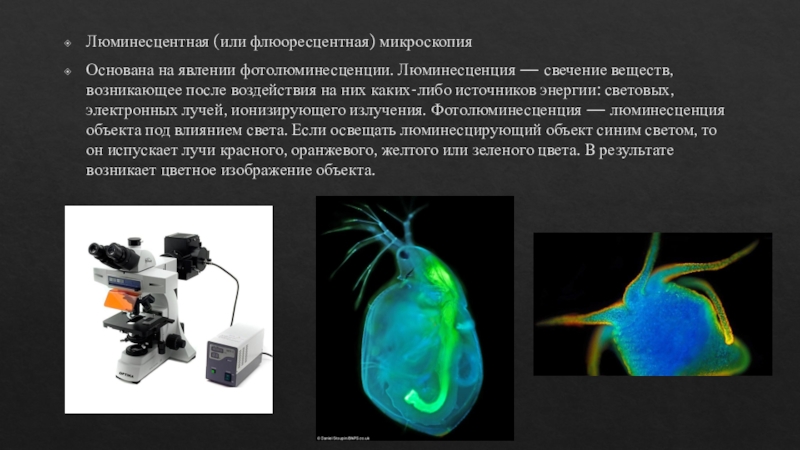
Слайд 8Люминесцентная (или флюоресцентная) микроскопия
Основана на явлении фотолюминесценции. Люминесценция — свечение
веществ, возникающее после воздействия на них каких-либо источников энергии: световых,
электронных лучей, ионизирующего излучения. Фотолюминесценция — люминесценция объекта под влиянием света. Если освещать люминесцирующий объект синим светом, то он испускает лучи красного, оранжевого, желтого или зеленого цвета. В результате возникает цветное изображение объекта.
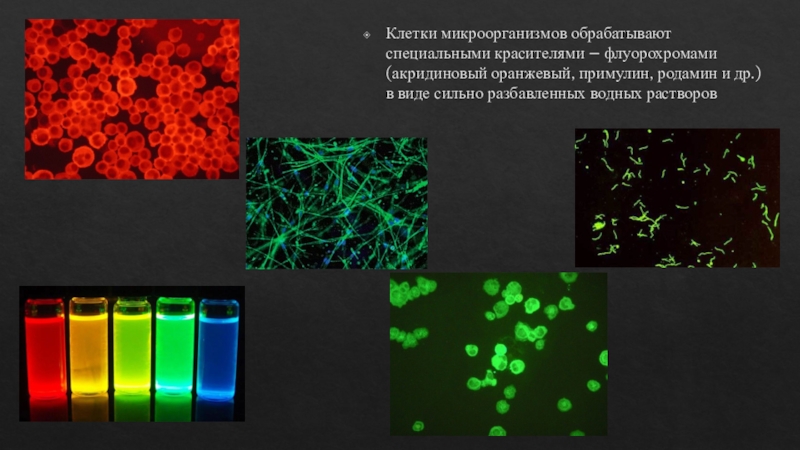
Слайд 9Клетки микроорганизмов обрабатывают специальными красителями – флуорохромами (акридиновый оранжевый, примулин,
родамин и др.) в виде сильно разбавленных водных растворов
Слайд 10Электронная микроскопия позволяет обнаружить объекты, которые не разрешаются при использовании
световых или ультрафиолетовых лучей.
Электронный микроскоп применяется для изучения вирусов,
тонкого строения различных микроорганизмов, макромолекулярных структур и других субмикроскопических объектов.
Слайд 11Приемы микроскопирования микроорганизмов
Прижизненные (нативные):
Метод «висячей» капли
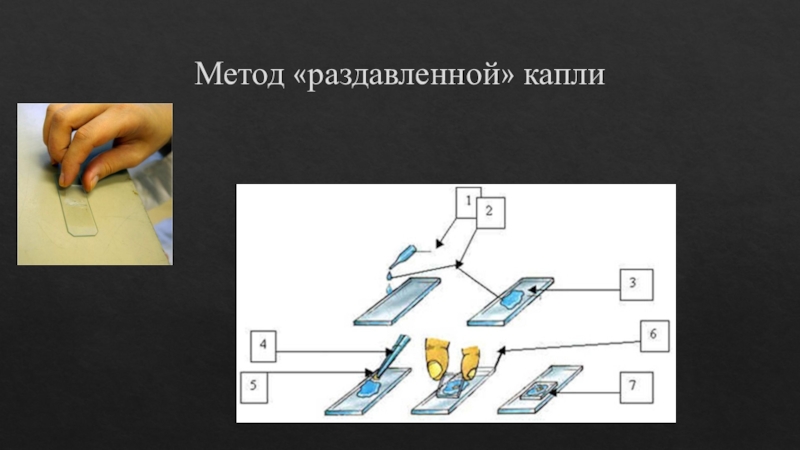
Метод «раздавленной» капли
Прижизненная окраска
Фиксированные:
Простые
методы окраски
Сложные методы окраски
Люминесцентные красители (акридиновый желтый, ауромин, корифосфин)
Электронная микроскопия
Слайд 14Методы окраски
фиксированных препаратов
Простые
окраска метиленовым синим
фуксином Пфейфера
Генциан-виолетом
Сложные
окраска по методу
Грама
окраска по Цилю — Нельсену
окраска по Романовскому —
Гимзе
Слайд 15В основе окраски лежат сложные химические и физико-химические реакции.. Окрашивание
препаратов проводится с помощью красителей, которые можно разделить на:
позитивные (метиленовый
синий, фуксин и др.) и негативные (нигрозин, тушь). Позитивными называются красители, окрашивающие микроорганизмы, негативными – красители, заполняющие пространство, окружающее микроорганизмы, в результате чего последние становятся видимыми как силуэты на фоне красителя;
килые (эозин, кислый фуксин, конго красный) и щелочные (основные) (гематоксилин, азур, сафранин, основной фуксин). Кислые красители связываются с веществами, имеющими щелочную реакцию (например, цитоплазматическими белками), щелочные – связываются с кислыми компонентами клеток (нуклеиновыми кислотами, рибосомами). Высокая концентрация ДНК и рибосомальной РНК в клетке бактерии делает ее более чувствительной к основным красителям. В связи с этим в микробиологической практике применяются почти исключительно основные красители.
Основные цвета окрашивания могут быть следующими: красный (основной фуксин, кислый фуксин, сафранин, конго красный); фиолетовый (генциановый фиолетовый, метиловый фиолетовый, кристаллический фиолетовый); синий (метиленовый синий, толуидиновый синий, водный синий); зеленый (малахитовый зеленый, бриллиантовый зеленый).

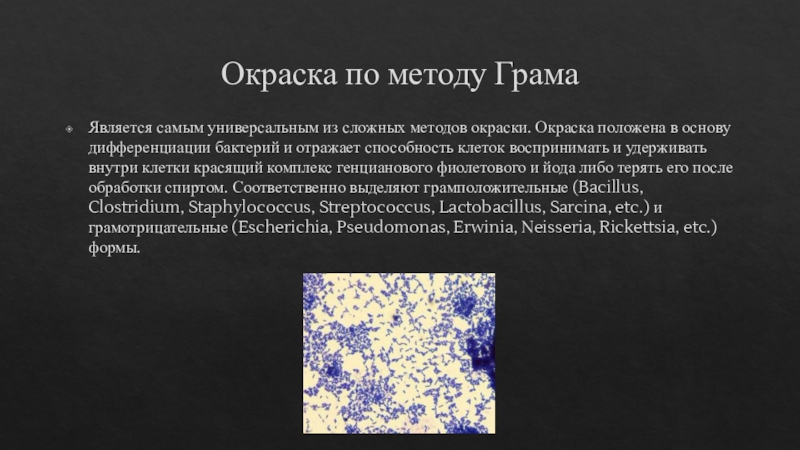
Слайд 16Окраска по методу Грама
Является самым универсальным из сложных методов окраски.
Окраска положена в основу дифференциации бактерий и отражает способность клеток
воспринимать и удерживать внутри клетки красящий комплекс генцианового фиолетового и йода либо терять его после обработки спиртом. Соответственно выделяют грамположительные (Bacillus, Clostridium, Staphylococcus, Streptococcus, Lactobacillus, Sarcina, etc.) и грамотрицательные (Escherichia, Pseudomonas, Erwinia, Neisseria, Rickettsia, etc.) формы.
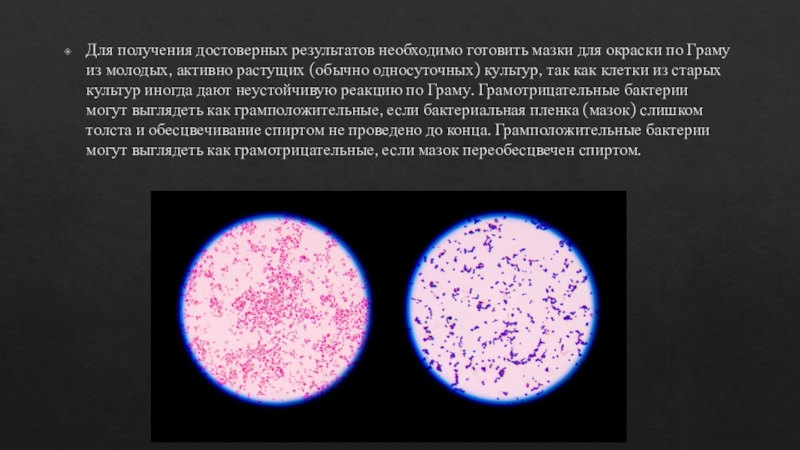
Слайд 17Для получения достоверных результатов необходимо готовить мазки для окраски по
Граму из молодых, активно растущих (обычно односуточных) культур, так как
клетки из старых культур иногда дают неустойчивую реакцию по Граму. Грамотрицательные бактерии могут выглядеть как грамположительные, если бактериальная пленка (мазок) слишком толста и обесцвечивание спиртом не проведено до конца. Грамположительные бактерии могут выглядеть как грамотрицательные, если мазок переобесцвечен спиртом.
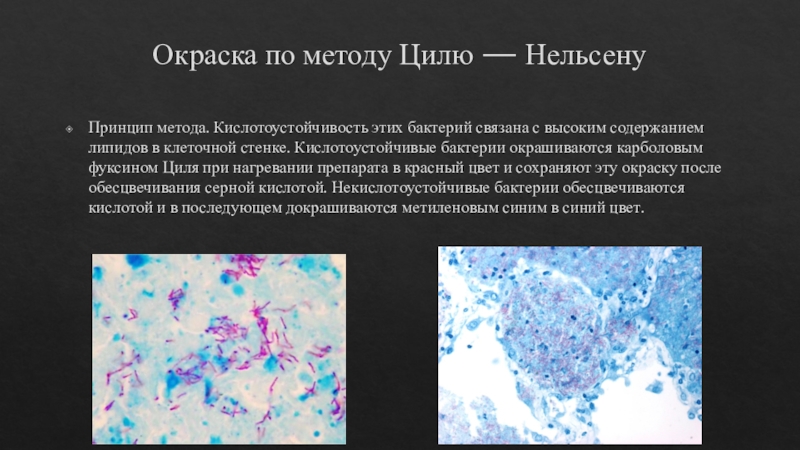
Слайд 19Окраска по методу Цилю — Нельсену
Принцип метода. Кислотоустойчивость этих
бактерий связана с высоким содержанием липидов в клеточной стенке. Кислотоустойчивые
бактерии окрашиваются карболовым фуксином Циля при нагревании препарата в красный цвет и сохраняют эту окраску после обесцвечивания серной кислотой. Некислотоустойчивые бактерии обесцвечиваются кислотой и в последующем докрашиваются метиленовым синим в синий цвет.