Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Молекулярная физика и термодинамика
Содержание
- 1. Молекулярная физика и термодинамика
- 2. Методы исследованияТермодинамический метод исследованияСтатистический метод исследованияразделы физики,
- 3. Основные понятияT = 273,15 + tТермодинамическая системасовокупность
- 4. Основные положения МКТИдеальный газ1. Все тела состоят
- 5. Основное уравнение МКТОсновное уравнение МКТ идеальных газовсредняя
- 6. Уравнение состояния идеального газаУравнение Менделеева-КлапейронаМ –
- 7. Внутренняя энергия идеального газаСпособы изменения внутренней энергииРаботаТеплопроводностьэнергия
- 8. Работа газа при изменении его объемаРSdlQсправедливо при
- 9. Первое начало термодинамикиU1V1 T1илиQ > 0Количество теплоты
- 10. ТеплоемкостьУДЕЛЬНАЯ теплоемкость веществаЧисленно равна количеству теплоты, необходимому
- 11. ИзопроцессыИзохорныйV=const=0Молярная теплоемкость при постоянном объемеС учетомВсе
- 12. ИзопроцессыИзобарныйР=const=CV=Rработа при изобарном нагревании 1 моля на
- 13. ИзопроцессыИзотермическийРоберт Бойль, 1662 г.Эдм Мариотт, 1676 г.Т=const=0Для
- 14. Адиабатический процессПроцесс, проходящий без теплообмена с окружающей средойпоказатель адиабатыАдиабатический (адиабатный)Q = 0Уравнение Пуассона
- 15. Термодинамический циклКруговой процесс (термодинамический цикл)Периодически повторяющийся процесс
- 16. Использование цикловрабочее телоТепловой двигательустройство, способное превращать полученное
- 17. Цикл КарноЦикл Карноизотермаадиабата1-2:изотермическое расширениегаз получает теплогаз совершает
- 18. Использование цикла КарнохолодильникЛюбой участок цикла Карно и
- 19. Второе начало термодинамикиКлаузиус: Невозможен процесс, единственным результатом
- 20. ЭнтропияЭнтропияФункция состояния системы, мера неупорядоченности,
- 21. Явления переноса в термодинамически неравновесных системахТеплопроводностьобусловлена переносом
- 22. ТеплопроводностьОбусловлена переносом энергииЗакон ФурьеЕсли в одной области
- 23. ДиффузияЗакон ФукаСамопроизвольное проникновение и перемешивание частиц
- 24. Внутреннее трение (вязкость)Закон НьютонаЕсли параллельные слои жидкости
- 25. ВязкостьВязкость (внутреннее трение)Свойство жидкостей (газов) оказывать сопротивление
- 26. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Молекулярная физика
и термодинамика
Курс лекций по общей физике
Вечерний факультет МГАКХиС
Бахтина
Елена Юрьевна,
к.ф-м.н., доц. каф. физики
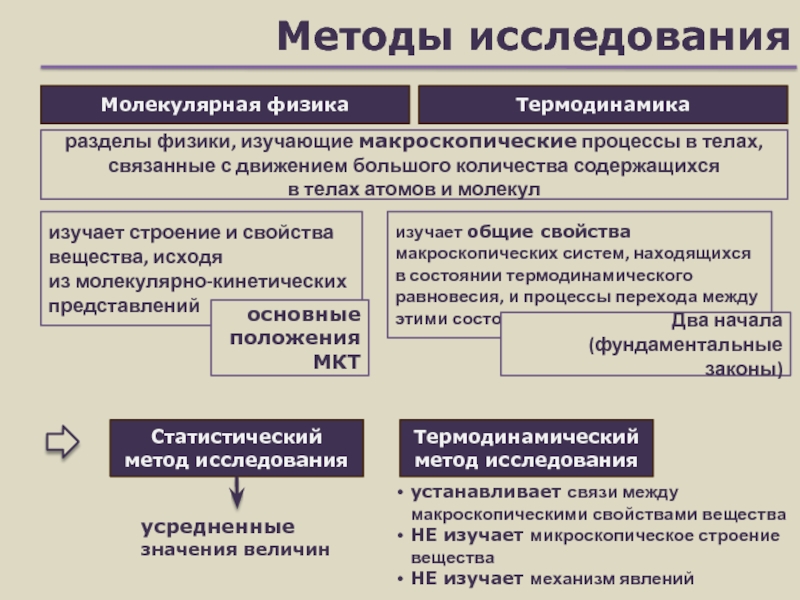
Слайд 2Методы исследования
Термодинамический метод исследования
Статистический метод исследования
разделы физики, изучающие макроскопические процессы
в телах, связанные с движением большого количества содержащихся в телах
атомов и молекулМолекулярная физика
Термодинамика
изучает строение и свойства вещества, исходя
из молекулярно-кинетических представлений
основные положения МКТ
усредненные значения величин
изучает общие свойства макроскопических систем, находящихся
в состоянии термодинамического равновесия, и процессы перехода между этими состояниями
Два начала (фундаментальные законы)
устанавливает связи между
макроскопическими свойствами вещества
НЕ изучает микроскопическое строение вещества
НЕ изучает механизм явлений
Слайд 3Основные понятия
T = 273,15 + t
Термодинамическая система
совокупность макроскопических тел,
которые
взаимодействуют и обмениваются энергией как между собой, так и с
другими теламиТермодинамические параметры
давление
P
объем
V
температура
Т
Моль
количество вещества, содержащее столько же частиц, сколько содержится атомов
в 0,012 кг углерода 12C
NA = 6,022·1023 моль–1
число Авогадро
абсолютным нулем температуры – точка нулевого давления газа
Реперные точки
температура тройной точки воды: лед, вода и пар –
в тепловом равновесии
в шкале Кельвина
0,01° С
273,16 К
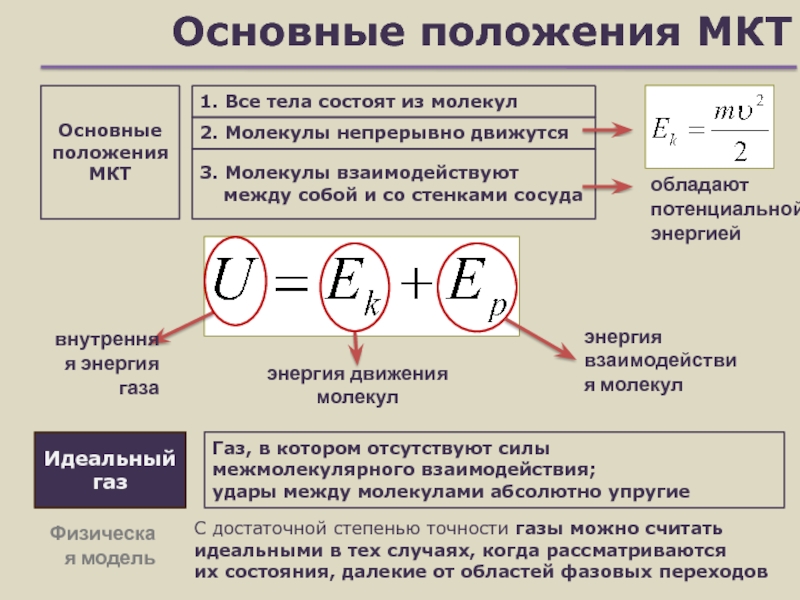
Слайд 4Основные положения МКТ
Идеальный газ
1. Все тела состоят из молекул
Основные положения
МКТ
Газ, в котором отсутствуют силы
межмолекулярного взаимодействия;
удары между молекулами абсолютно
упругие2. Молекулы непрерывно движутся
3. Молекулы взаимодействуют между собой и со стенками сосуда
энергия движения молекул
энергия взаимодействия молекул
внутренняя энергия газа
С достаточной степенью точности газы можно считать идеальными в тех случаях, когда рассматриваются
их состояния, далекие от областей фазовых переходов
Физическая модель
обладают потенциальной энергией
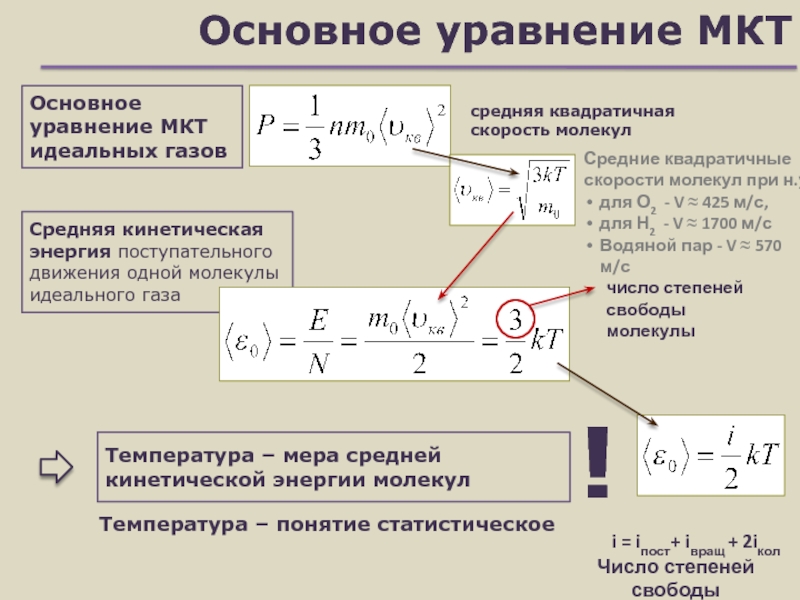
Слайд 5Основное уравнение МКТ
Основное уравнение МКТ идеальных газов
средняя квадратичная скорость молекул
Средние
квадратичные скорости молекул при н.у.
для О2 - V ≈ 425
м/с, для Н2 - V ≈ 1700 м/с
Водяной пар - V ≈ 570 м/с
Средняя кинетическая энергия поступательного движения одной молекулы идеального газа
Температура – мера средней кинетической энергии молекул
Температура – понятие статистическое
!
число степеней свободы молекулы
i = iпост+ iвращ + 2iкол
Число степеней свободы
Слайд 6Уравнение состояния идеального газа
Уравнение
Менделеева-Клапейрона
М – молярная масса
– количество
вещества
R=8,31 Дж/(моль∙К) –
универсальная газовая постоянная
k=R/NA= 1,38 ∙10-23 Дж/К
– постоянная
Больцманаn – концентрация молекул
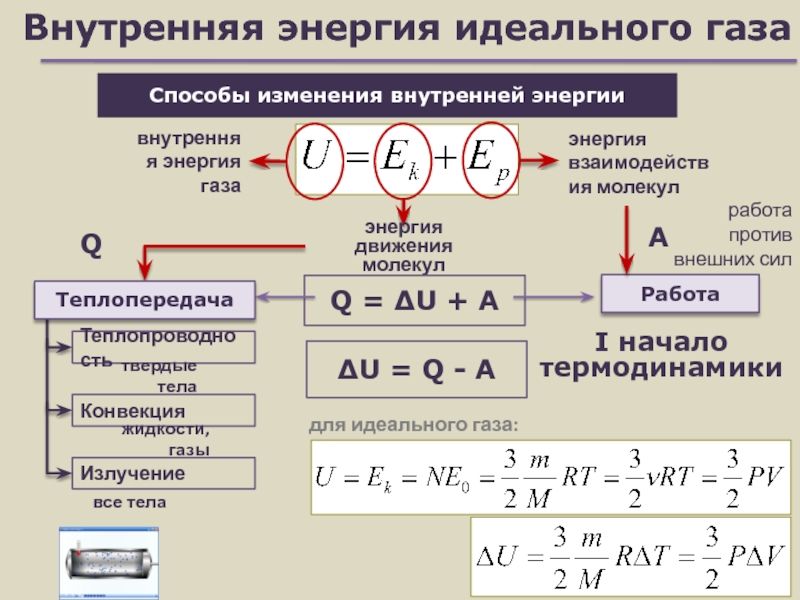
Слайд 7Внутренняя энергия идеального газа
Способы изменения внутренней энергии
Работа
Теплопроводность
энергия
движения молекул
энергия взаимодействия
молекул
внутренняя энергия газа
Q
A
Конвекция
Излучение
твердые тела
жидкости, газы
все тела
Q = U + A
I
начало термодинамикидля идеального газа:
U = Q - A
Теплопередача
работа
против внешних сил
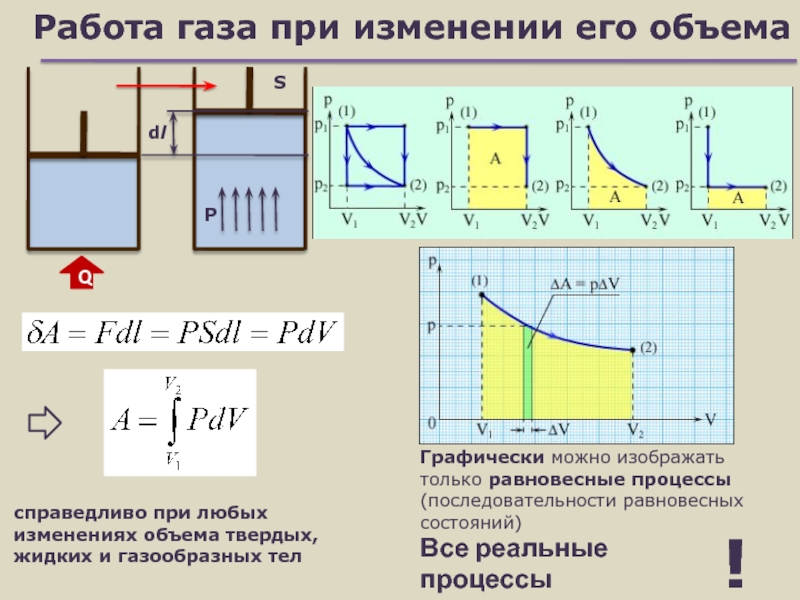
Слайд 8Работа газа при изменении его объема
Р
S
dl
Q
справедливо при любых изменениях объема
твердых, жидких и газообразных тел
Графически можно изображать
только равновесные процессы
(последовательности равновесных состояний)Все реальные процессы неравновесны
!
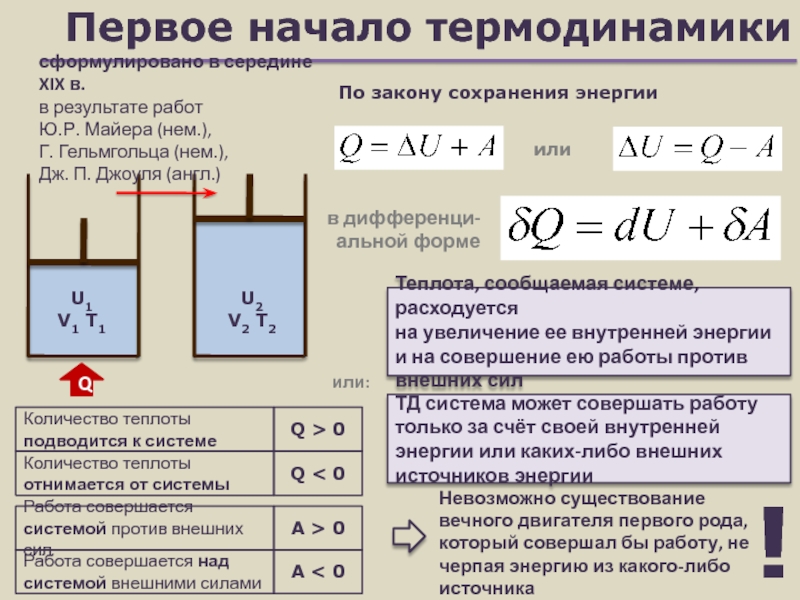
Слайд 9Первое начало термодинамики
U1
V1 T1
или
Q > 0
Количество теплоты подводится к системе
Q
< 0
Количество теплоты отнимается от системы
Работа совершается системой против внешних
силРабота совершается над системой внешними силами
А > 0
А < 0
По закону сохранения энергии
U2
V2 T2
Q
в дифференци-альной форме
Теплота, сообщаемая системе, расходуется
на увеличение ее внутренней энергии и на совершение ею работы против внешних сил
ТД система может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источников энергии
сформулировано в середине XIX в.
в результате работ
Ю.Р. Майера (нем.),
Г. Гельмгольца (нем.),
Дж. П. Джоуля (англ.)
Невозможно существование вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника
или:
!
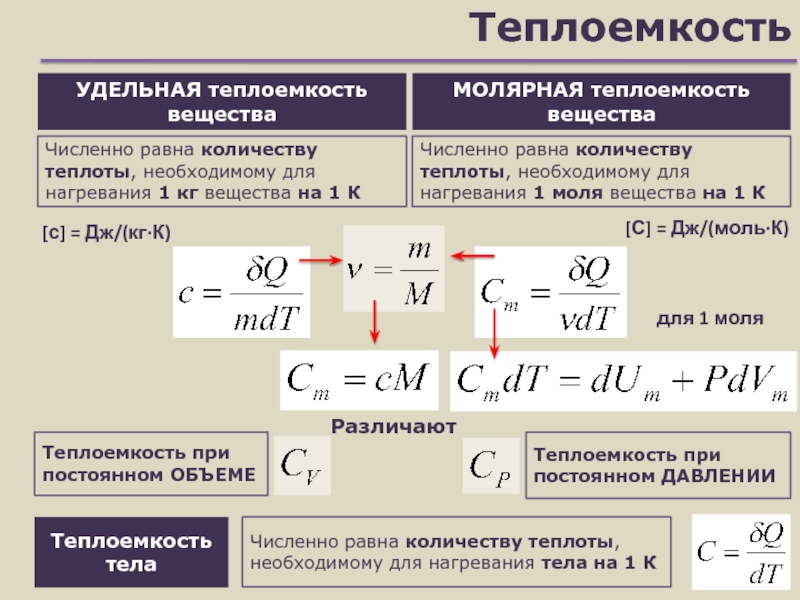
Слайд 10Теплоемкость
УДЕЛЬНАЯ теплоемкость вещества
Численно равна количеству теплоты, необходимому для нагревания 1
кг вещества на 1 К
Теплоемкость при постоянном ОБЪЕМЕ
Теплоемкость при постоянном
ДАВЛЕНИИ[с] = Дж/(кг∙К)
МОЛЯРНАЯ теплоемкость вещества
Численно равна количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К
[С] = Дж/(моль∙К)
Различают
для 1 моля
Теплоемкость тела
Численно равна количеству теплоты, необходимому для нагревания тела на 1 К
Слайд 11Изопроцессы
Изохорный
V=const
=0
Молярная теплоемкость
при постоянном объеме
С учетом
Все количество теплоты, полученное телом,
идет на изменение внутренней энергии
равна Q, необходимому для нагревания 1
моль вещества на 1 КЖак Александр Сезар Шарль, 1808 г.
Слайд 12Изопроцессы
Изобарный
Р=const
=CV
=R
работа при изобарном нагревании 1 моля на 1 К
Жозеф Луи
Гей-Люссак, 1862 г.
уравнение Майера
Все количество теплоты, полученное телом, идет на
изменение внутренней энергии
и совершение работы теломСлайд 13Изопроцессы
Изотермический
Роберт Бойль, 1662 г.
Эдм Мариотт, 1676 г.
Т=const
=0
Для того, чтобы при
расширении газа Т не понижалась, к газу в течение изотермического
процесса необходимо подводить Q, эквивалентное внешней работе расширенияВсе количество теплоты, полученное телом, идет на совершение работы телом
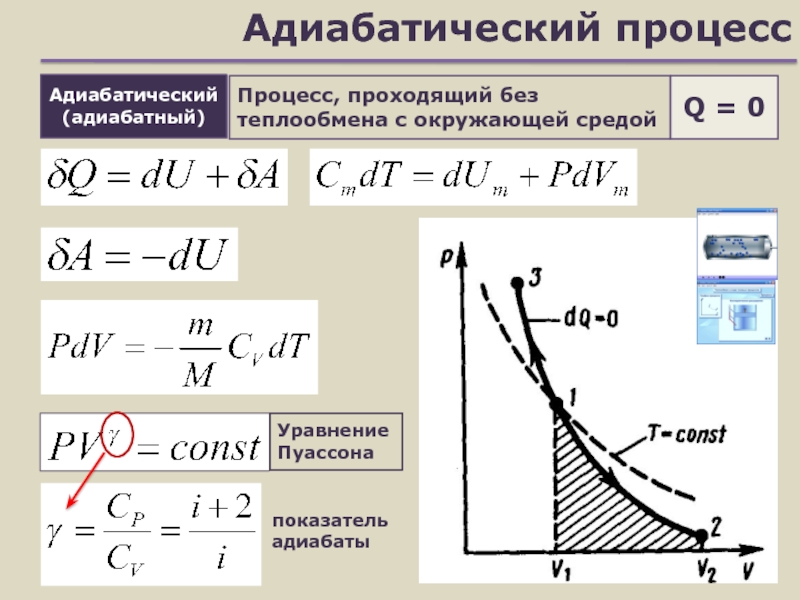
Слайд 14Адиабатический процесс
Процесс, проходящий без теплообмена с окружающей средой
показатель адиабаты
Адиабатический (адиабатный)
Q
= 0
Уравнение Пуассона
Слайд 15Термодинамический цикл
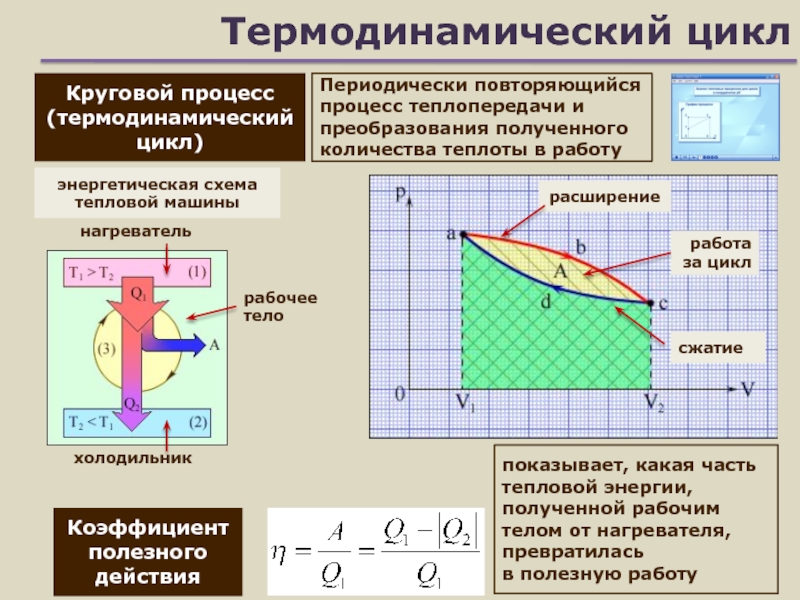
Круговой процесс (термодинамический цикл)
Периодически повторяющийся процесс теплопередачи и преобразования
полученного количества теплоты в работу
Коэффициент полезного действия
рабочее тело
нагреватель
холодильник
расширение
сжатие
работа
за цикл
показывает,
какая часть тепловой энергии, полученной рабочим телом от нагревателя, превратилась
в полезную работуэнергетическая схема тепловой машины
Слайд 16Использование циклов
рабочее тело
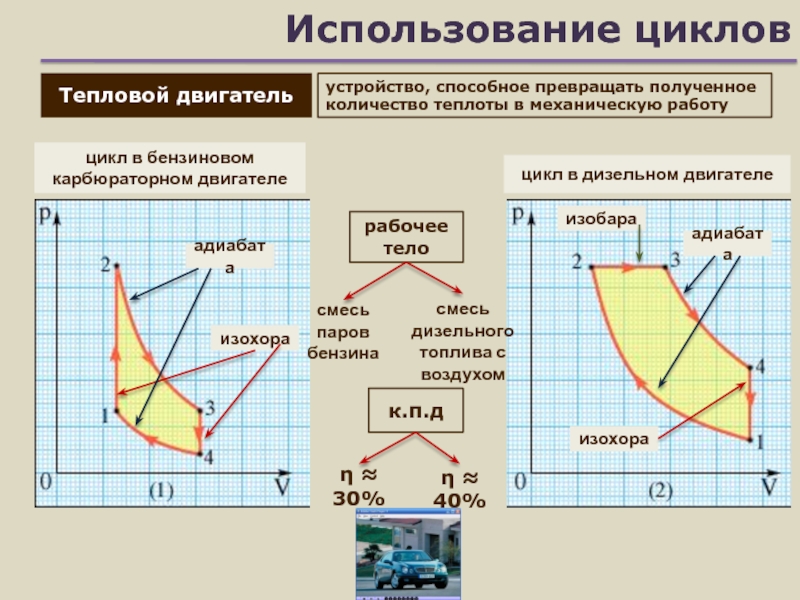
Тепловой двигатель
устройство, способное превращать полученное количество теплоты в
механическую работу
цикл в бензиновом карбюраторном двигателе
цикл в дизельном двигателе
смесь паров
бензина смесь дизельного топлива с воздухом
изохора
адиабата
адиабата
изохора
изобара
30%
40%
к.п.д
Слайд 17Цикл Карно
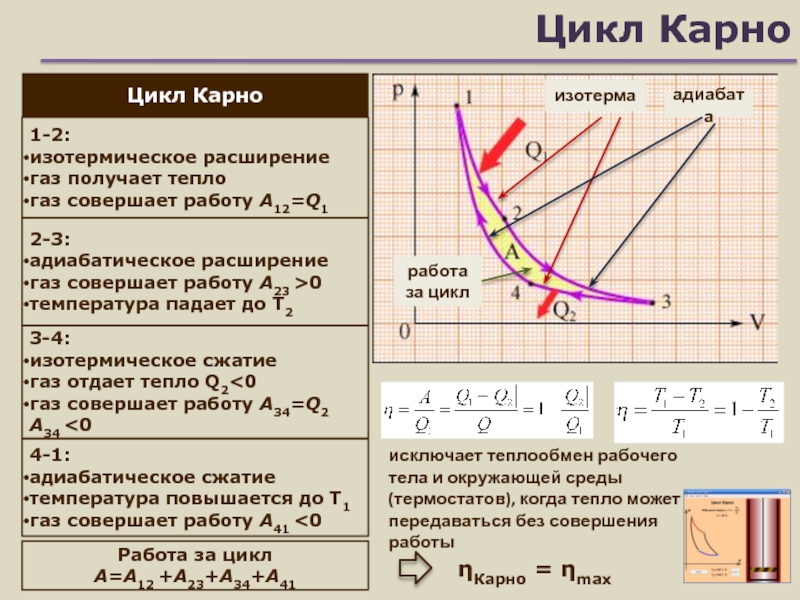
Цикл Карно
изотерма
адиабата
1-2:
изотермическое расширение
газ получает тепло
газ совершает работу A12=Q1
2-3:
адиабатическое расширение
газ
совершает работу A23 >0
температура падает до T2
3-4:
изотермическое сжатие
газ отдает
тепло Q2<0газ совершает работу А34=Q2 A34 <0
4-1:
адиабатическое сжатие
температура повышается до T1
газ совершает работу A41 <0
Работа за цикл
A=A12 +А23+А34+А41
работа за цикл
ηКарно = ηmax
исключает теплообмен рабочего тела и окружающей среды (термостатов), когда тепло может передаваться без совершения работы
Слайд 18Использование цикла Карно
холодильник
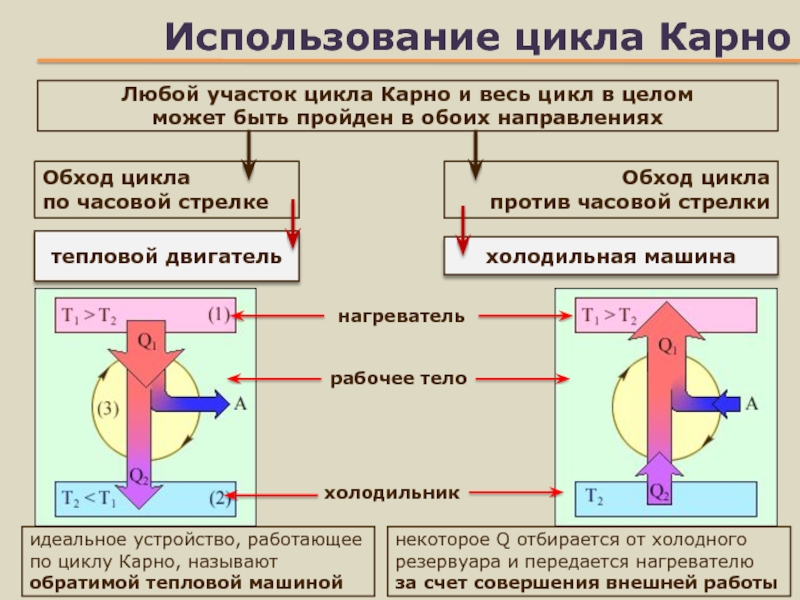
Любой участок цикла Карно и весь цикл в
целом
может быть пройден в обоих направлениях
идеальное устройство, работающее по
циклу Карно, называют обратимой тепловой машинойОбход цикла
по часовой стрелке
некоторое Q отбирается от холодного резервуара и передается нагревателю
за счет совершения внешней работы
тепловой двигатель
Обход цикла
против часовой стрелки
холодильная машина
рабочее тело
нагреватель
Слайд 19Второе начало термодинамики
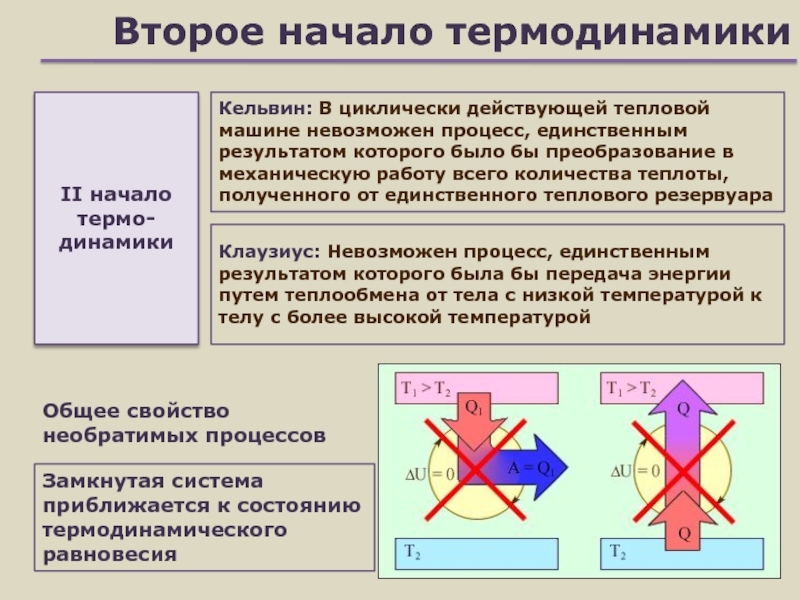
Клаузиус: Невозможен процесс, единственным результатом которого была бы
передача энергии путем теплообмена от тела с низкой температурой к
телу с более высокой температуройII начало термо-динамики
Замкнутая система приближается к состоянию термодинамического равновесия
Общее свойство
необратимых процессов
Кельвин: В циклически действующей тепловой машине невозможен процесс, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара
Слайд 20Энтропия
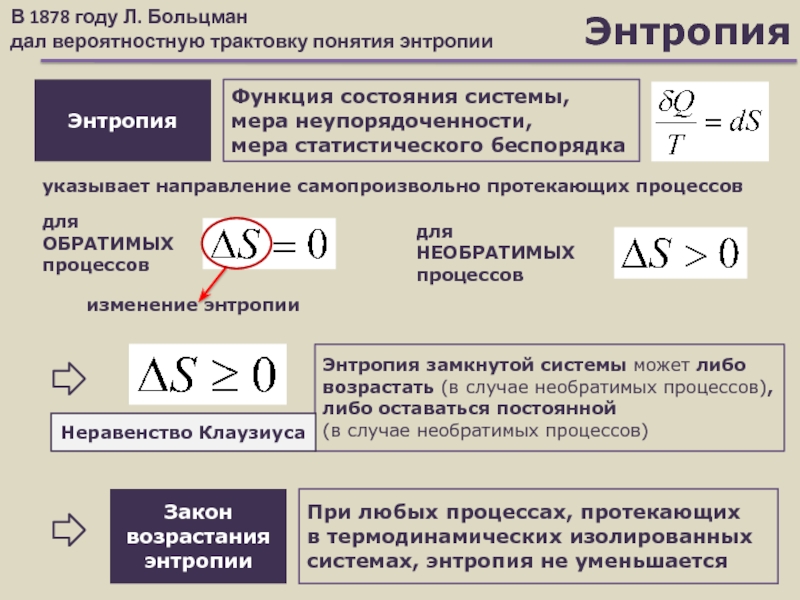
Энтропия
Функция состояния системы,
мера неупорядоченности,
мера статистического беспорядка
указывает направление самопроизвольно
протекающих процессов
В 1878 году Л. Больцман
дал вероятностную трактовку понятия энтропии
для ОБРАТИМЫХ
процессовЗакон возрастания энтропии
При любых процессах, протекающих
в термодинамических изолированных системах, энтропия не уменьшается
изменение энтропии
для
НЕОБРАТИМЫХ процессов
Энтропия замкнутой системы может либо возрастать (в случае необратимых процессов), либо оставаться постоянной
(в случае необратимых процессов)
Неравенство Клаузиуса
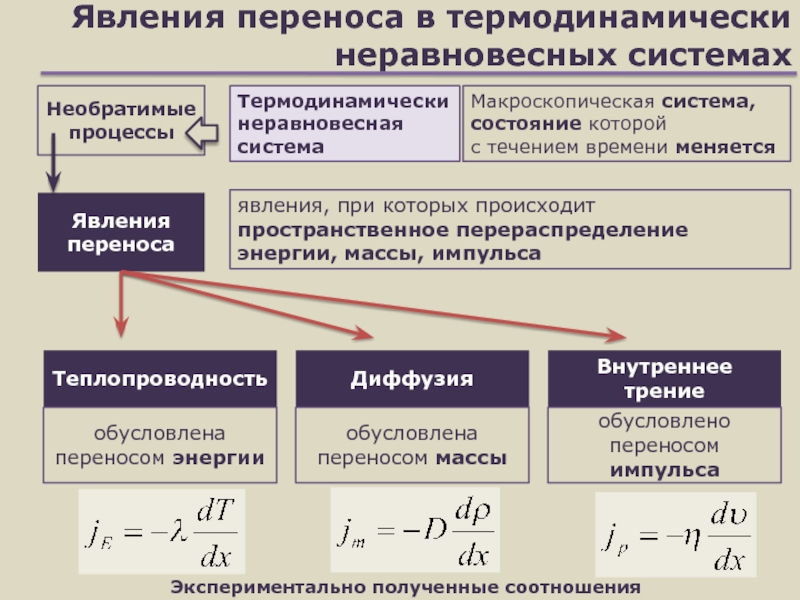
Слайд 21Явления переноса в термодинамически неравновесных системах
Теплопроводность
обусловлена переносом энергии
Внутреннее трение
обусловлено переносом
импульса
Диффузия
обусловлена переносом массы
Необратимые процессы
Макроскопическая система, состояние которой
с течением времени
меняется Термодинамически неравновесная система
Явления переноса
явления, при которых происходит пространственное перераспределение энергии, массы, импульса
Экспериментально полученные соотношения
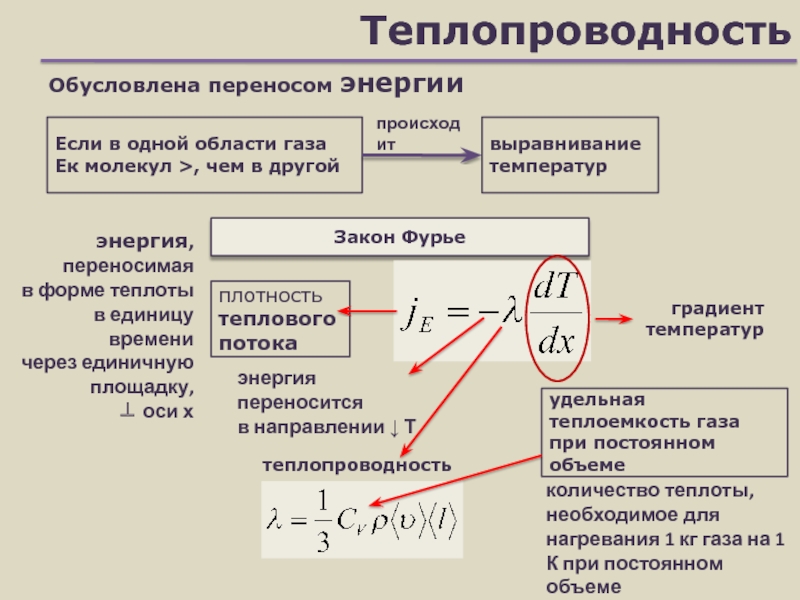
Слайд 22Теплопроводность
Обусловлена переносом энергии
Закон Фурье
Если в одной области газа Ек молекул
>, чем в другой
выравнивание температур
плотность
теплового потока
градиент температур
энергия переносится
в
направлении ↓ Ттеплопроводность
происходит
удельная теплоемкость газа при постоянном объеме
количество теплоты, необходимое для нагревания 1 кг газа на 1 К при постоянном объеме
энергия, переносимая
в форме теплоты
в единицу времени
через единичную площадку,
оси х
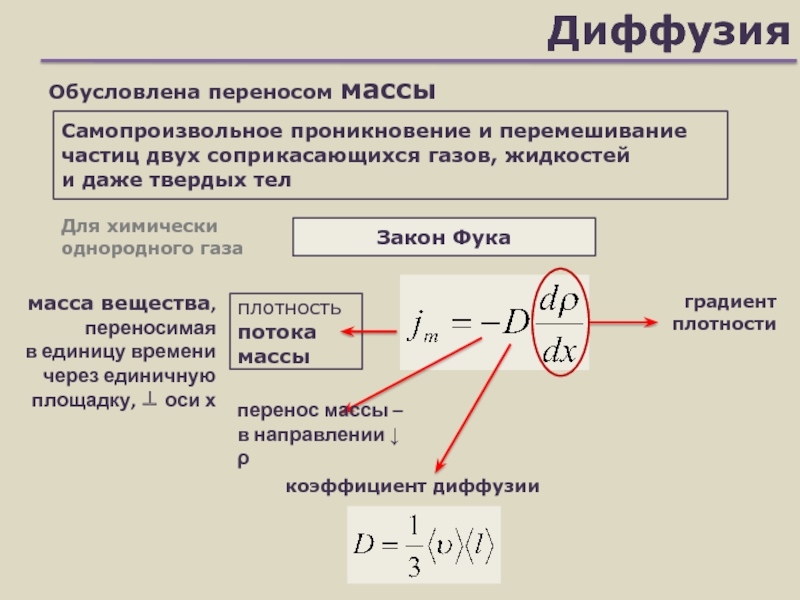
Слайд 23Диффузия
Закон Фука
Самопроизвольное проникновение и перемешивание
частиц двух соприкасающихся газов, жидкостей
и даже твердых тел
плотность
потока массы
градиент плотности
Для химически однородного газа
коэффициент диффузии
Обусловлена переносом массы
масса вещества, переносимая
в единицу времени через единичную площадку, оси х
перенос массы –
в направлении ↓
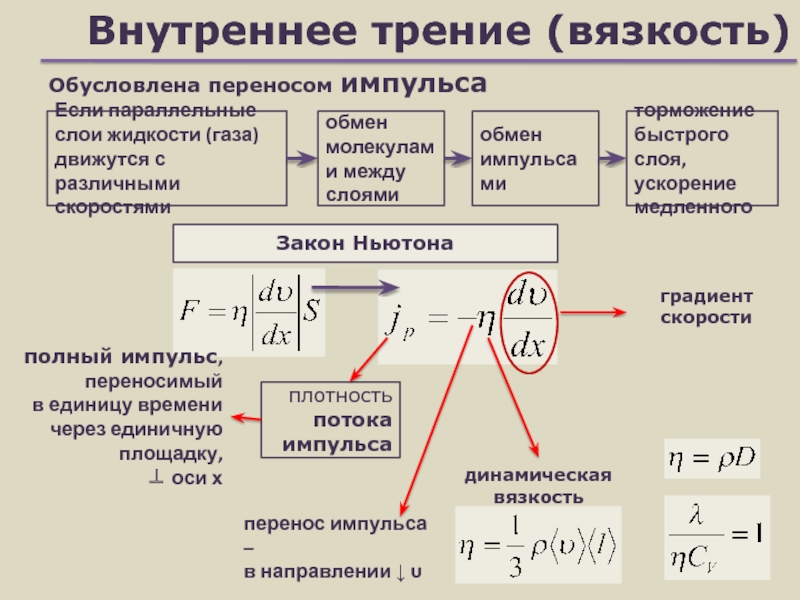
Слайд 24Внутреннее трение (вязкость)
Закон Ньютона
Если параллельные
слои жидкости (газа) движутся с различными
скоростями
плотность
потока импульса
градиент скорости
динамическая вязкость
Обусловлена переносом импульса
перенос импульса –
в
направлении ↓ обмен молекулами между слоями
обмен импульсами
торможение быстрого слоя, ускорение медленного
полный импульс, переносимый
в единицу времени через единичную площадку,
оси х
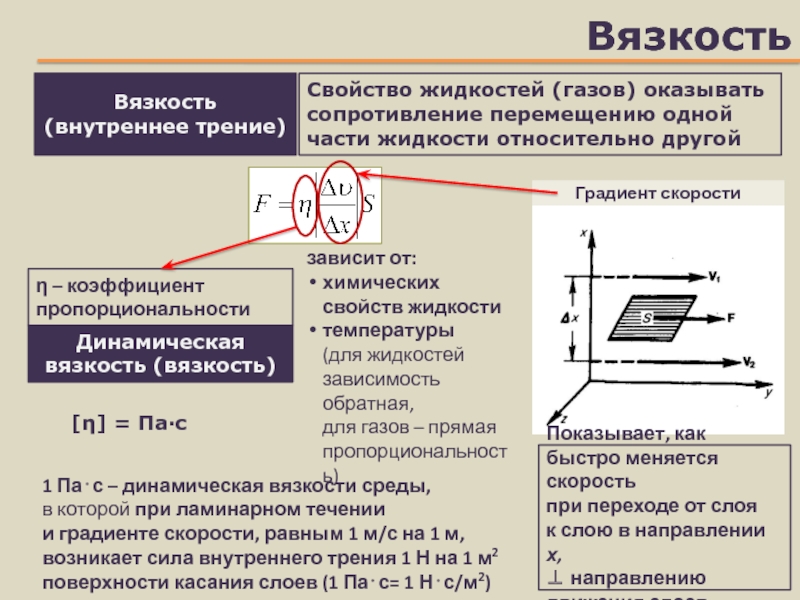
Слайд 25Вязкость
Вязкость
(внутреннее трение)
Свойство жидкостей (газов) оказывать сопротивление перемещению одной части жидкости
относительно другой
Градиент скорости
Показывает, как быстро меняется скорость
при переходе от
слоя
к слою в направлении х,
направлению
движения слоев – коэффициент пропорциональности
зависит от:
химических свойств жидкости
температуры
(для жидкостей зависимость обратная,
для газов – прямая пропорциональность)
Динамическая вязкость (вязкость)
[] = Па∙с
1 Пас – динамическая вязкости среды,
в которой при ламинарном течении
и градиенте скорости, равным 1 м/с на 1 м,
возникает сила внутреннего трения 1 Н на 1 м2 поверхности касания слоев (1 Пас= 1 Нс/м2)