Слайд 1Нанофармакология: биохимические основы, достижения и перспективы.
Слайд 2СТРУКТУРА УЧЕБНОГО СОДЕРЖАНИЯ
Определение
Общие принципы направленной доставки лекарственных препаратов
Направленная доставка
в миокард
Наночастицы кремнезема
4.1. Влияние наночастиц кремнезема на гемодинамические и биохимические параметры
4.2. Биораспределение
наночастиц кремнезема
4.3. Вопросы безопасности наночастиц кремнезема
Направленная доставка в миокард с помощью наночастиц кремнезема
Направленная доставка с помощью магнитных наночастиц
Дилемма направленной доставки препаратов
Слайд 4Определение
Нанофармакология - раздел фармакологии, изучающий механизмы действия, биологические эффекты
и фармакокинетику нанолекарств
Слайд 5ОБЩИЕ ПРИНЦИПЫ НАПРАВЛЕННОЙ ДОСТАВКИ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ
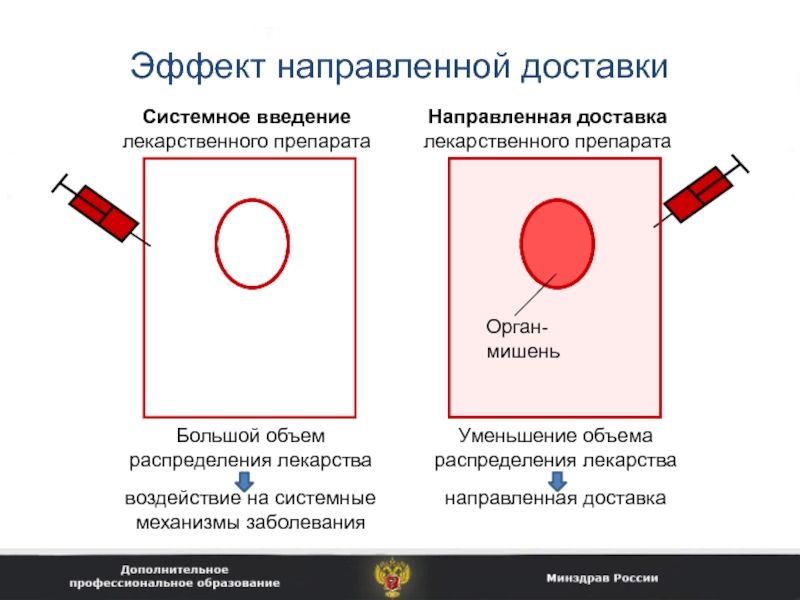
Слайд 6Эффект направленной доставки
Системное введение лекарственного препарата
Направленная доставка лекарственного препарата
Большой объем
распределения лекарства
воздействие на системные механизмы заболевания
Уменьшение объема распределения лекарства
направленная доставка
Слайд 7Преимущества направленной доставки
Направленная доставка лекарственных препаратов с помощью наночастиц имеет
целый ряд существенный преимуществ:
Уменьшение объема распределения препаратов;
Снижение системной токсичности препаратов;
Повышение
растворимости гидрофобных препаратов;
Повышение стабильности препаратов (белки, пептиды, олигонуклеотиды);
Улучшение биосовместимости.
Слайд 8Пассивный и активный механизмы направленной доставки
Направляющий лиганд («якорь»)
Пассивный механизм
Активный (таргетный)
механизм
Наночастицы с лекарством выхо-дят за пределы сосудистого русла преимущественно в
зонах повы-шенной проницаемости сосудов
Накопление наночастиц с лекарством в зоне интереса за счет специфического связывания лиганда и маркера повреждения
Наночастица
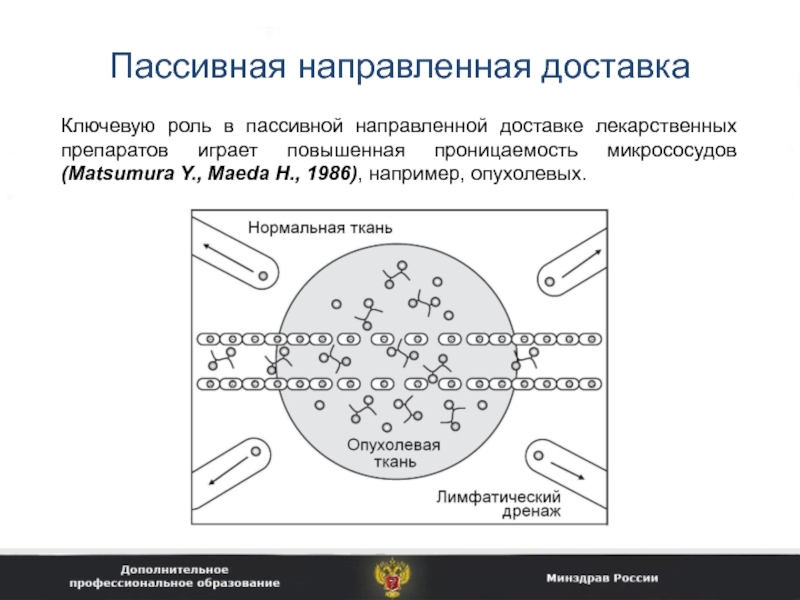
Слайд 9Пассивная направленная доставка
Ключевую роль в пассивной направленной доставке лекарственных препаратов
играет повышенная проницаемость микрососудов (Matsumura Y., Maeda H., 1986), например,
опухолевых.
Слайд 10Основные типы направляющих лигандов
для таргетной доставки лекарств
Моноклональные антитела
Антиген-распознающие фрагменты
антител (Fab-фрагменты, одноцепочечные вариабельные фрагменты, наносомы)
Аптамеры (олигонуклеотиды)
Пептиды
Низкомолекулярные соединения (фолиевая кислота)
Слайд 11Примеры активной направленной доставки
Доставка упакованного в липосомы сосудистого эндотелиального фактора
роста (VEGF) за счет присоединения к поверхности липосом моноклональных антител
против Р-селектина
Доставка в миокард АТФ с помощью липосом, имеющих на своей поверхности моноклональные антитела против миозина
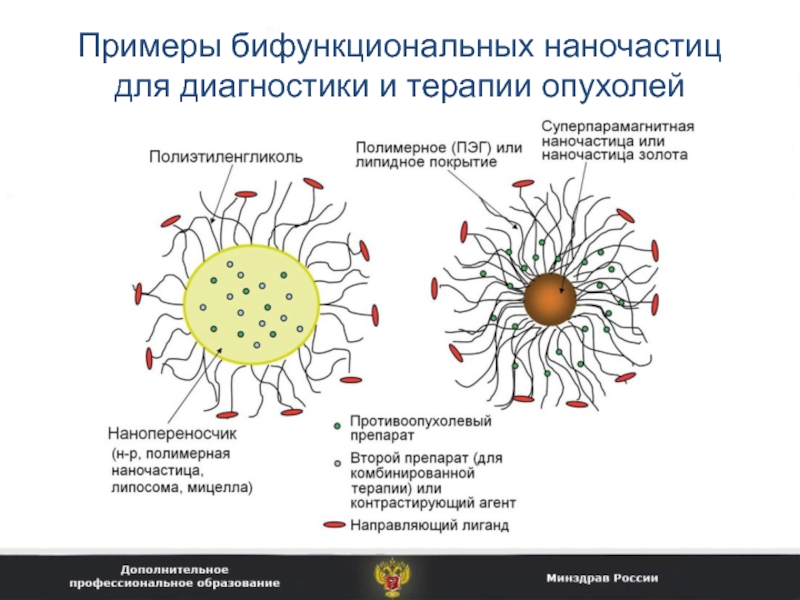
Слайд 12Примеры бифункциональных наночастиц для диагностики и терапии опухолей
Слайд 13Направленная доставка в онкологии: текущие клинические исследования
Слайд 15Пассивная направленная доставка в поврежденный миокард
Протокол и результаты первого опубликованного
исследования пассивной направленной доставки в миокард после ишемии (Takahama H.
et al., 2009)
Контроль
Липосомы
Введение липосомального аденозина сопровождалось:
Накоплением липосом в зоне риска (область некроза и пограничная зона);
Менее выраженными побочными гемодинамическими эффектами;
Более выраженным инфаркт-лимитирующим эффектом
Слайд 16Патологические изменения в ишемизированном миокарде
Цитоплазма
Сарколемма
Аннексин V
Транслокация фосфатидилсерина
Специфическое связывание аннексина V
с сарколеммой
Норма
Обратимое повреждение
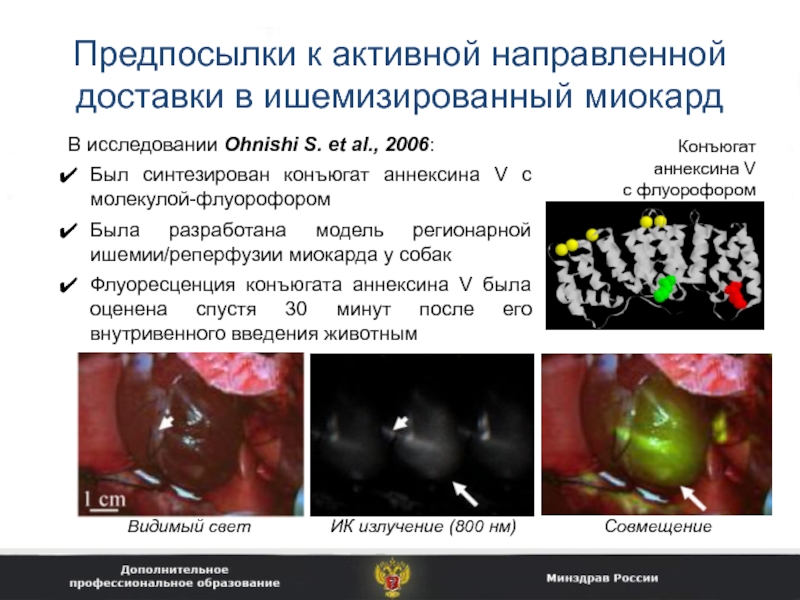
Слайд 17Предпосылки к активной направленной доставки в ишемизированный миокард
В исследовании Ohnishi
S. et al., 2006:
Был синтезирован конъюгат аннексина V с
молекулой-флуорофором
Была разработана модель регионарной ишемии/реперфузии миокарда у собак
Флуоресценция конъюгата аннексина V была оценена спустя 30 минут после его внутривенного введения животным
Конъюгат
аннексина V
с флуорофором
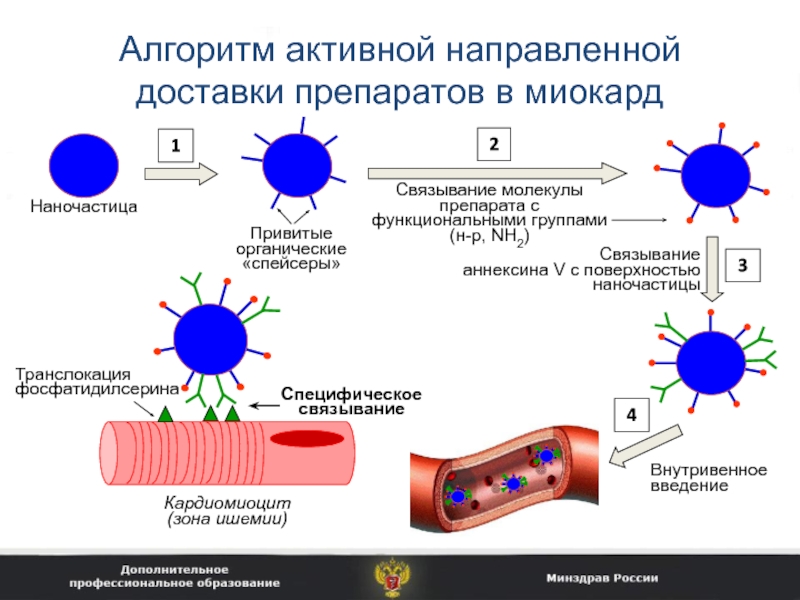
Слайд 18Алгоритм активной направленной доставки препаратов в миокард
Наночастица
Привитые органические «спейсеры»
Связывание молекулы
препарата с функциональными группами (н-р, NH2)
Связывание
аннексина V с поверхностью
наночастицы
Внутривенное введение
Кардиомиоцит
(зона ишемии)
Транслокация фосфатидилсерина
Специфическое связывание
Слайд 20Наночастицы кремнезема
Морфологию наночастиц кремнезема (НЧК) можно исследовать с помощью просвечивающей
электронной микроскопии:
удельная поверхность наночастиц кремнезема - 600-700 м2/г
диаметр наночастиц кремнезема
- 7-20 нм
Слайд 211. Влияние наночастиц кремнезема на гемодинамические и биохимические параметры
Слайд 22Влияние наночастиц кремнезема на артериальное давление
В исследовании Galagudza M. et
al., 2010 установлено, что внутривенное введение суспензий углеродных и кремнеземных
наночастиц животным не оказывает существенного влияния на гемодинамические показатели, что косвенно свидетельствует о хорошей биосовместимости использованных носителей.
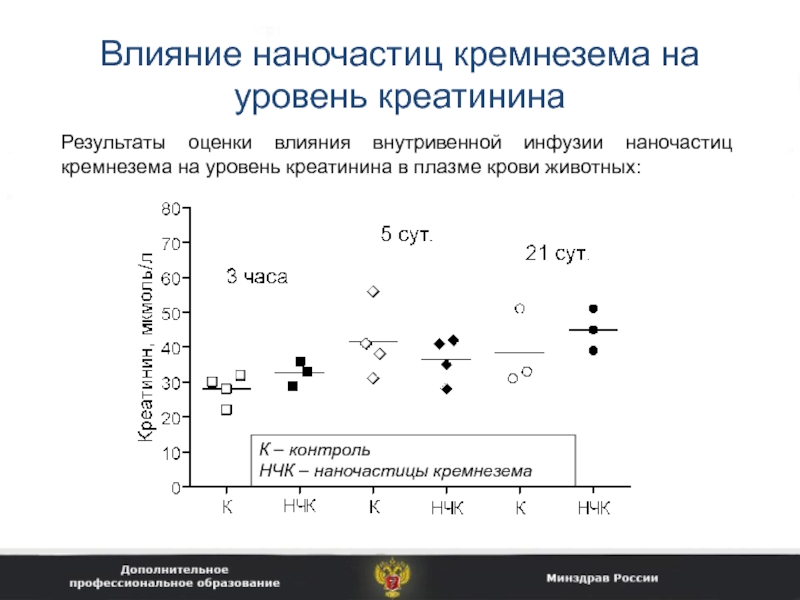
Слайд 23Влияние наночастиц кремнезема на уровень креатинина
Результаты оценки влияния внутривенной инфузии
наночастиц кремнезема на уровень креатинина в плазме крови животных:
К –
контроль
НЧК – наночастицы кремнезема
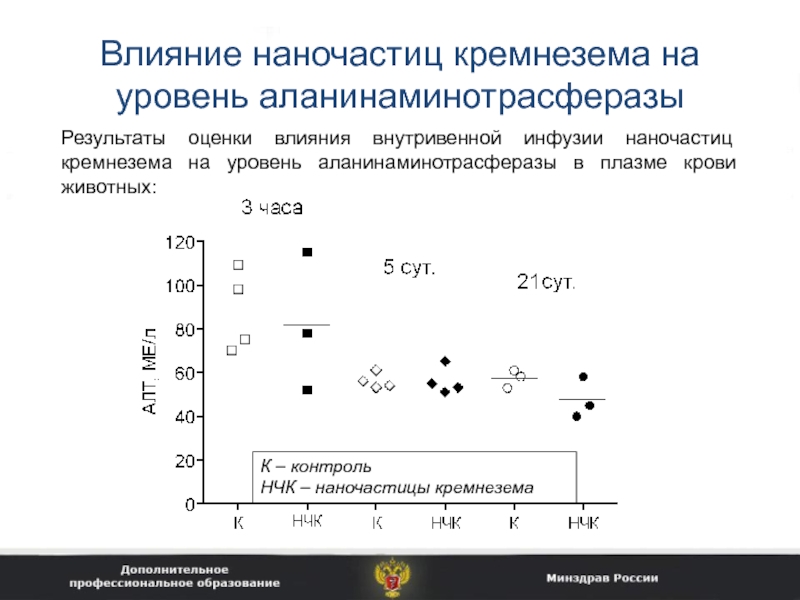
Слайд 24Влияние наночастиц кремнезема на уровень аланинаминотрасферазы
Результаты оценки влияния внутривенной
инфузии наночастиц кремнезема на уровень аланинаминотрасферазы в плазме крови животных:
К
– контроль
НЧК – наночастицы кремнезема
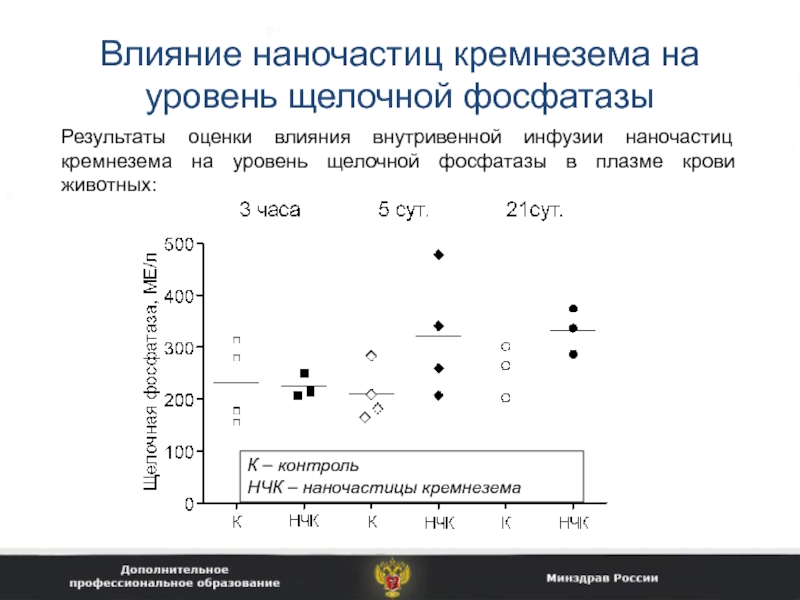
Слайд 25Влияние наночастиц кремнезема на уровень щелочной фосфатазы
Результаты оценки влияния внутривенной
инфузии наночастиц кремнезема на уровень щелочной фосфатазы в плазме крови
животных:
К – контроль
НЧК – наночастицы кремнезема
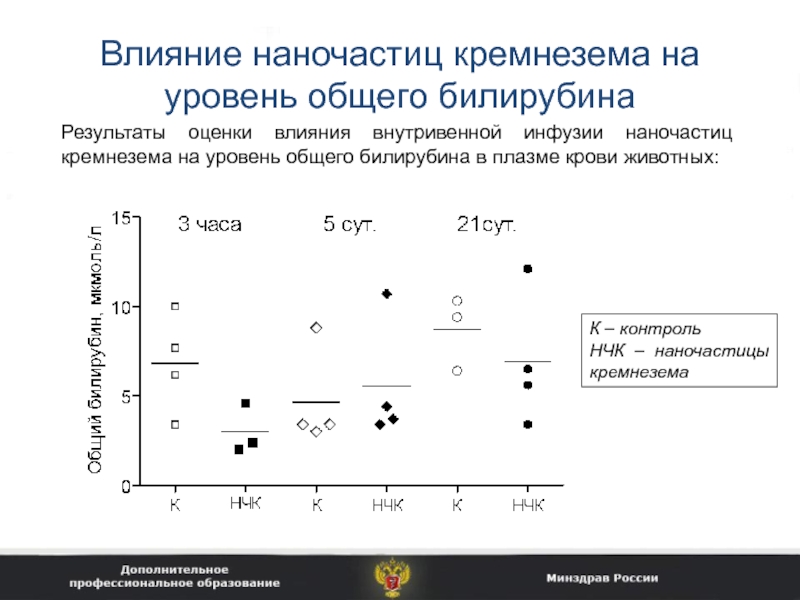
Слайд 26Влияние наночастиц кремнезема на уровень общего билирубина
Результаты оценки влияния внутривенной
инфузии наночастиц кремнезема на уровень общего билирубина в плазме крови
животных:
К – контроль
НЧК – наночастицы кремнезема
Слайд 272. Биораспределение наночастиц кремнезема
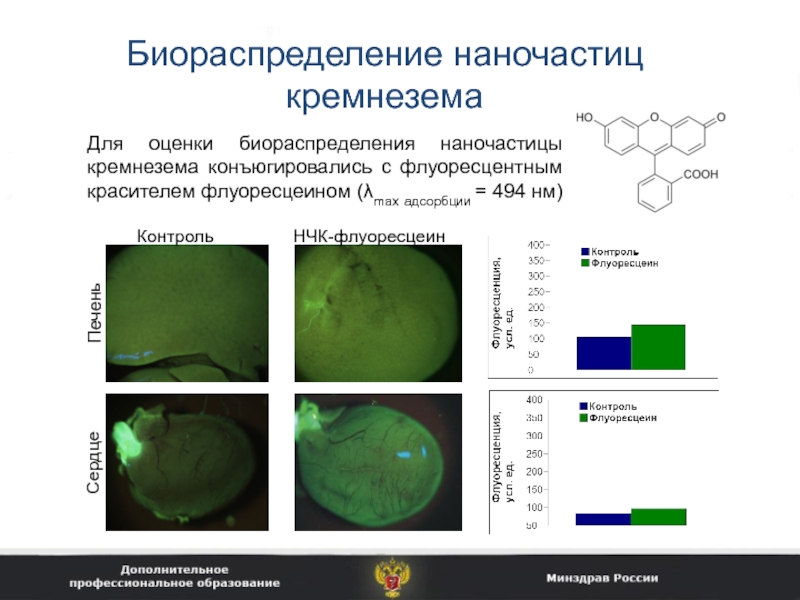
Слайд 28Биораспределение наночастиц кремнезема
Для оценки биораспределения наночастицы кремнезема конъюгировались с флуоресцентным
красителем флуоресцеином (λmax адсорбции = 494 нм)
Печень
Сердце
Контроль
НЧК-флуоресцеин
Слайд 29Биораспределение наночастиц кремнезема с флуоресцеином
Естественное биораспределение наночастиц кремнезема, модифицированных кремнеземом
через 30 минут после внутривенного введения оценивалось методом оптической флуоресценции:
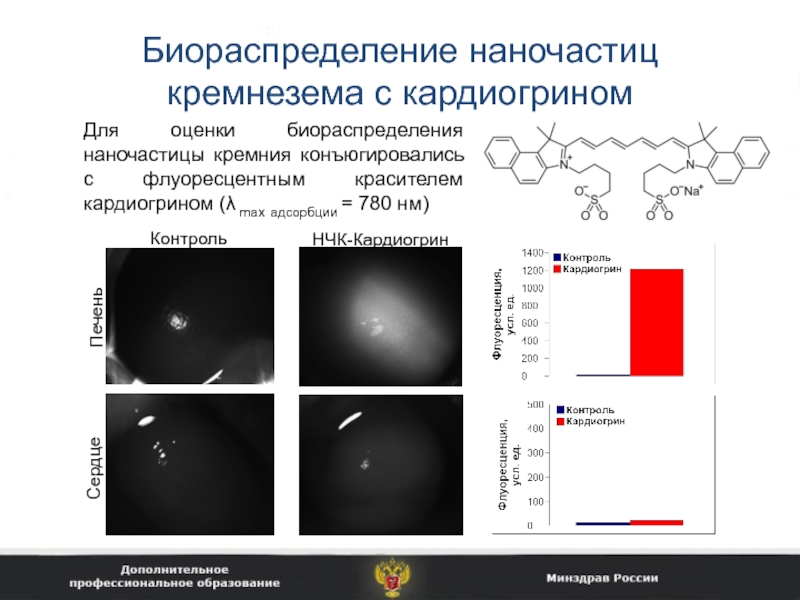
Слайд 30Биораспределение наночастиц кремнезема с кардиогрином
Для оценки биораспределения наночастицы кремния конъюгировались
с флуоресцентным красителем кардиогрином (λ max адсорбции = 780 нм)
Печень
Контроль
НЧК-Кардиогрин
Сердце
Слайд 313. Вопросы безопасности наночастиц кремнезема
Слайд 32Вопросы безопасности наночастиц кремнезема
Так как экспериментальные исследования показали, что наночастицы
кремнезема способны неселективно накапливаться в различных органах, необходимо было выяснить:
не
может ли накопление наночастиц кремнезема вызывать какие-либо побочные эффекты
способны ли наночастицы кремнезема деградировать в организме и выводиться из него
Иными словами был поставлен вопрос о биосовместимости и биодеградируемости наночастиц кремнезема.
Слайд 33Схема распада наночастиц кремнезема в организме
Кремниевые кислоты
H2SiO3
Наночастица SiO2
Эрозия поверхности
H2SiO4
Экскреция с
мочой
Циркуляция с кровью в растворенном виде
Слайд 34Биодеградация наночастиц кремнезема
Было определено содержание кремния в печени животных в
разные сроки после внутривенного введения наночастиц кремнезема
до введения наночастиц кремнезема
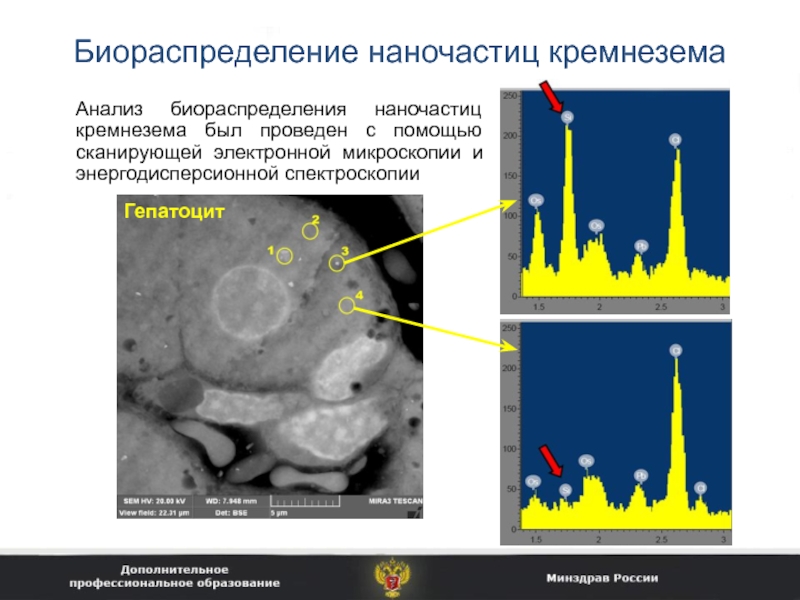
Слайд 35Биораспределение наночастиц кремнезема
Анализ биораспределения наночастиц кремнезема был проведен с помощью
сканирующей электронной микроскопии и энергодисперсионной спектроскопии
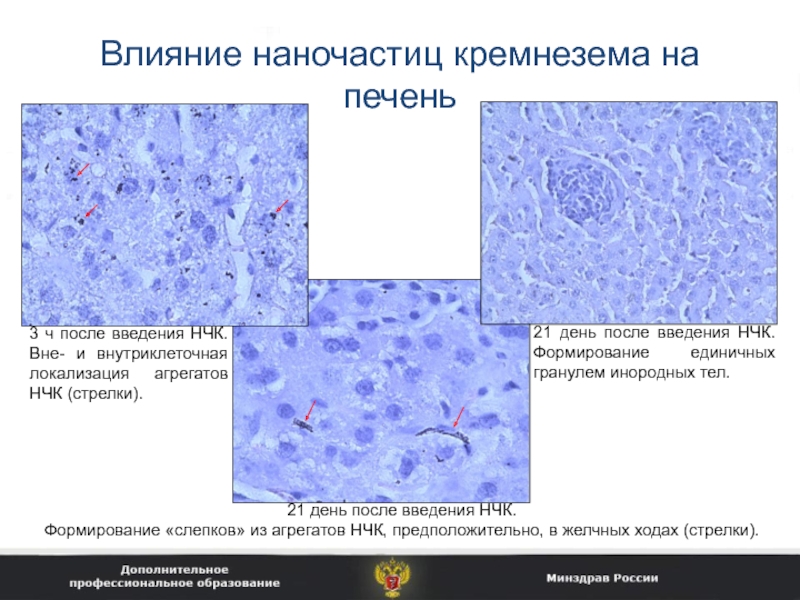
Слайд 36Влияние наночастиц кремнезема на печень
3 ч после введения НЧК. Вне-
и внутриклеточная локализация агрегатов НЧК (стрелки).
21 день после введения НЧК.
Формирование «слепков» из агрегатов НЧК, предположительно, в желчных ходах (стрелки).
21 день после введения НЧК. Формирование единичных гранулем инородных тел.
Слайд 37НАПРАВЛЕННАЯ ДОСТАВКА В МИОКАРД С ПОМОЩЬЮ НАНОЧАСТИЦ КРЕМНЕЗЕМА
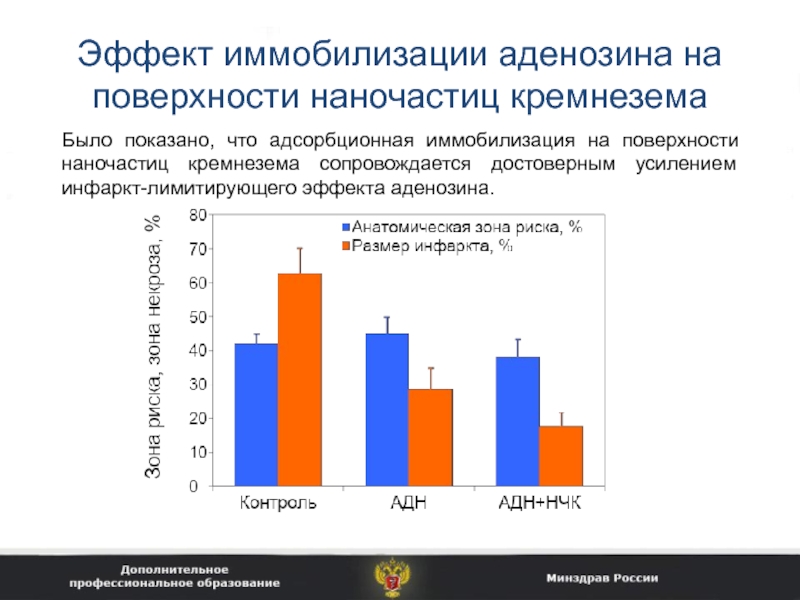
Слайд 38Эффект иммобилизации аденозина на поверхности наночастиц кремнезема
Было показано, что адсорбционная
иммобилизация на поверхности наночастиц кремнезема сопровождается достоверным усилением инфаркт-лимитирующего эффекта
аденозина.
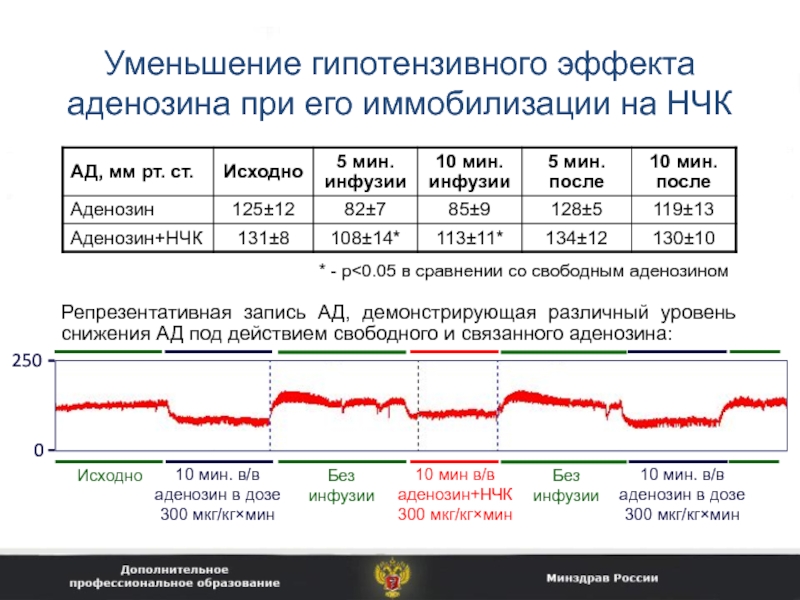
Слайд 39Уменьшение гипотензивного эффекта аденозина при его иммобилизации на НЧК
* -
p
уровень снижения АД под действием свободного и связанного аденозина:
Слайд 40Направленная доставка препаратов в миокард с помощью наночастиц кремнезема
Для проверки
гипотезы направленной доставки с помощью НЧК оценивалось биораспределение наночастиц у
интактных животных и животных с ишемией-реперфузией мио-карда.
Было показано, что содержание кремния в зоне повреждения миокарда сущест-венно выше, чем в неповреж-денном миокарде. Это позволяет говорить о том, что эффект пассивной направ-ленной доставки с помощью наночастиц может быть реализован при ишемии-реперфузии миокарда.
Слайд 41Препараты для доставки в обратимо поврежденный миокард
Для направленной доставки
в миокард могут использоваться различные кардиопротективные и ангиогенные препараты: «миметики»
прекондиционирования, активаторы тирозинкиназных рецепторов (факторы роста), влияние на сигнальный путь оксида азота.
Слайд 42НАПРАВЛЕННАЯ ДОСТАВКА С ПОМОЩЬЮ МАГНИТНЫХ НАНОЧАСТИЦ
Слайд 43Направленная доставка препаратов с помощью магнитных наночастиц
Проблема адресной доставки лекарственных
препаратов с противоишемическим и ангиогенным эффектами при хронической ишемии нижних
конечностей может быть решена путем аккумуляции в ишемизированной мышце нанодисперсных железосодержащих матриц под действием внешнего магнитного поля.
В результате применения такого подхода происходит:
накопление нагруженных препаратом наночастиц в зоне ишемии
высвобождение препарата в ходе биодеградации покрытия частицы
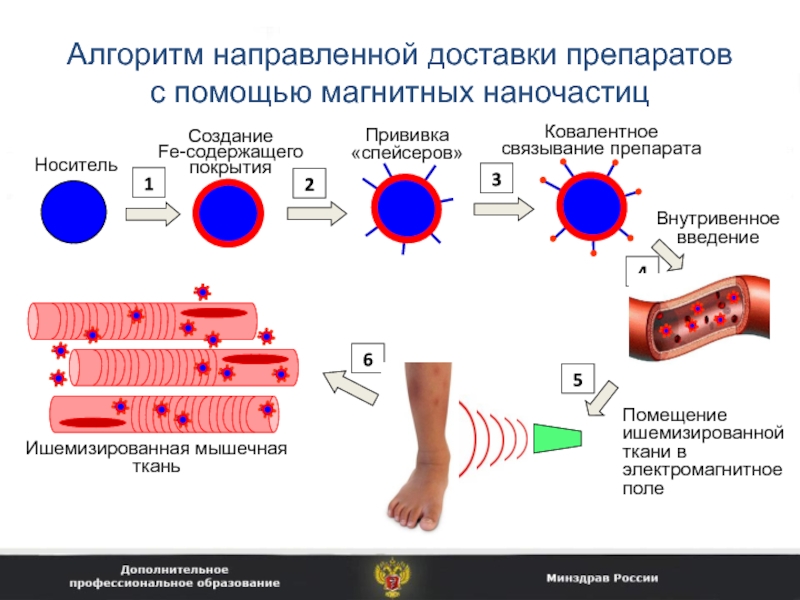
Слайд 44Алгоритм направленной доставки препаратов с помощью магнитных наночастиц
Носитель
Ковалентное связывание препарата
Внутривенное введение
Ишемизированная мышечная ткань
1
2
4
6
Создание
Fe-содержащего покрытия
Прививка «спейсеров»
3
Помещение ишемизированной ткани в
электромагнитное поле
5
Слайд 45Примеры структур магнитных наночастиц
Наночастицы магнетита (оксида железа) – простейший пример
из класса МНЧ. Возможно синтезировать биоксидные наночастицы, состоящие из ядра,
представленного оксидом циркония, и оболочки из магнетита. Дальнейшая адсорбция лекарственного препарата на поверхности такой частицы, и добавление поверхностно-активного вещества позволяют обеспечить направленную доставку лекарственных препаратов.
Слайд 46ДИЛЕММА НАПРАВЛЕННОЙ ДОСТАВКИ ПРЕПАРАТОВ
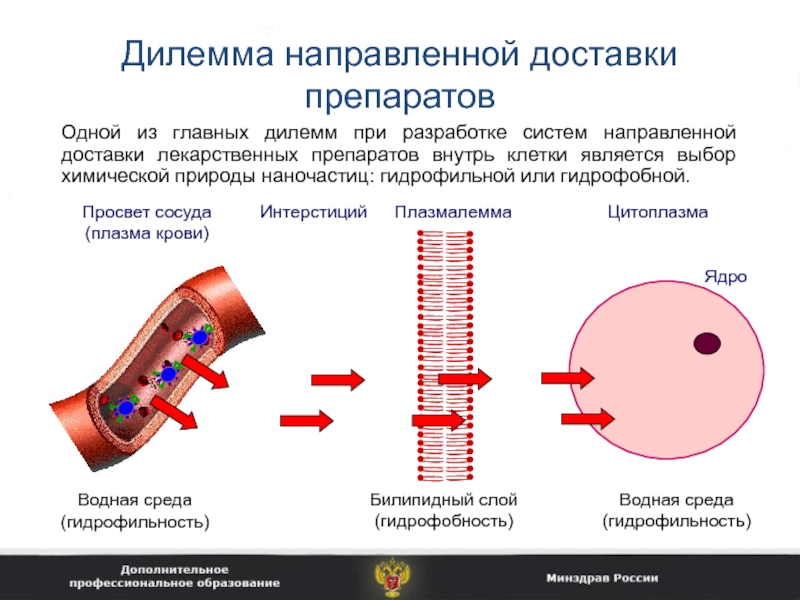
Слайд 47Дилемма направленной доставки препаратов
Одной из главных дилемм при разработке систем
направленной доставки лекарственных препаратов внутрь клетки является выбор химической природы
наночастиц: гидрофильной или гидрофобной.
Цитоплазма
Плазмалемма
Ядро
Интерстиций
Просвет сосуда (плазма крови)
Водная среда (гидрофильность)
Билипидный слой (гидрофобность)
Водная среда (гидрофильность)