Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Неотложные состояния в онкологии
Содержание
- 1. Неотложные состояния в онкологии
- 2. Неотложные состояния в онкологии: • компрессия спинного
- 3. Неотложные состояния в онкологии могут быть связаны:
- 4. Слайд 4
- 5. КОМПРЕССИЯ СПИННОГО МОЗГА Компрессия спинного мозга –
- 6. Причины КСМУ онкологических больных сдавление спинного мозга
- 7. Слайд 7
- 8. Слайд 8
- 9. Клиника КСМКлиника компрессии спинного мозга характеризуется тетрадой
- 10. Болевой синдром при КсмБоль локальная или по
- 11. Прогрессирующая мышечная слабость наблюдается у 76% больных
- 12. При поражениях спинного мозга выше уровня ThXII–
- 13. Потенциально смертельным осложнением метастатичесого поражения шейных позвонков является подвывих в атланто-аксилярном сочленении.
- 14. Метастазы во II шейный позвонок ведут к
- 15. Большинство больных с метастазами в верхние шейные
- 16. Диагностика КСМ• Неврологическое и физикальное обследование: перкуссия
- 17. • Радиоизотопное исследование костного мозга. • Компьютерная
- 18. Слайд 18
- 19. Слайд 19
- 20. Лечение КСМКак только диагноз ясен, необходимо начать
- 21. • Параллельно с дексаметазоном назначаются мочегонные, препараты
- 22. Лучевая терапия является одним из наиболее эффективных
- 23. Хирургическое лечение Стандартной операцией считается декомпрессионная ламинэктомия.
- 24. Химиотерапия• может быть проведена в качестве первой
- 25. СИНДРОМ ВЕРХНЕЙ ПОЛОЙ ВЕНЫ Синдром верхней полой
- 26. Причины СВПВК злокачественным опухолям, которые наиболее часто
- 27. Среди других причин, приводящих к СВПВ, следует
- 28. Клиника • Клиническое течение СВПВ может быть
- 29. Слайд 29
- 30. Диагностика • достаточно данных клиники и физикального
- 31. Слайд 31
- 32. Слайд 32
- 33. Слайд 33
- 34. Слайд 34
- 35. • Компьютерная томография с контрастированием позволяет уточнить
- 36. Лечение • Оптимальное лечение зависит от причин,
- 37. Лучевая терапия крупными фракциями является высокоэффективным методом
- 38. Химиотерапевтическое лечение • в качестве первой линии
- 39. Комбинированная терапия (химиотерапия и лучевая терапия) показана
- 40. ГИПЕРКАЛЬЦИЕМИЯГиперкальциемия у онкологических больных – наиболее частое
- 41. Гиперкальциемия с наибольшей частотой встречает ся при
- 42. Патогенез• локальная метастатическая деструкция кости,• генерализованный остеолиз,
- 43. Гуморальная гиперкальциемия наблюдается у больных раком легкого
- 44. Клиника• общие симптомы – обезвоживание, слабость, усталость,
- 45. Если не проводится коррекция гиперкальциемии, последовательно развивается
- 46. ЛечениеБольные с гиперкальциемией требуют постоянного мониторинга показателей:
- 47. • регидратация: введение изотонических растворов (3–6 л
- 48. • бисфосфонаты (клодронат, памидронат, ибандро. нат) –
- 49. • кальцитонин (миокальцик) – полипептидный гормон, секретируемый
- 50. Спасибо за внимание!
- 51. Скачать презентанцию
Неотложные состояния в онкологии: • компрессия спинного мозга • синдром верхней полой вены • гиперкальциемия • синдром распада опухоли
Слайды и текст этой презентации
Слайд 3Неотложные состояния в онкологии могут быть связаны:
• с проведением
инструментальной диагностики, особенно в поздних стадиях заболевания,
• лечением,
•
с наличием сопутствующей патологии, • с распространением опухолевого процесса.
Ургентная ситуация может возникнуть и как первое проявление злокачественной опухоли
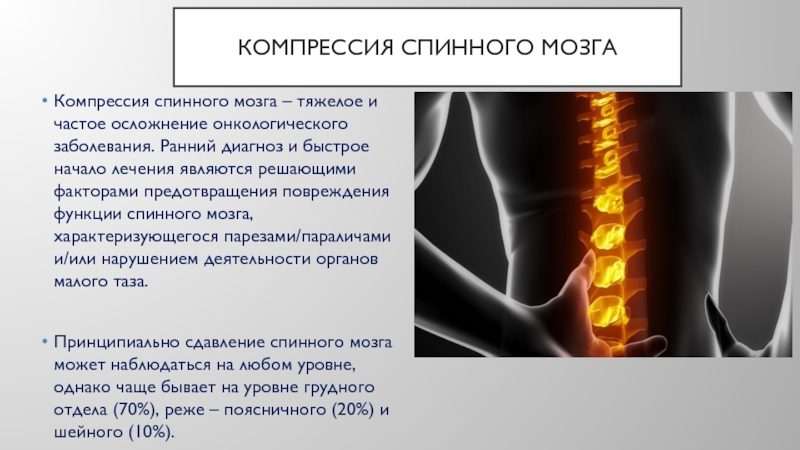
Слайд 5КОМПРЕССИЯ СПИННОГО МОЗГА
Компрессия спинного мозга – тяжелое и частое
осложнение онкологического заболевания. Ранний диагноз и быстрое начало лечения являются
решающими факторами предотвращения повреждения функции спинного мозга, характеризующегося парезами/параличами и/или нарушением деятельности органов малого таза.Принципиально сдавление спинного мозга может наблюдаться на любом уровне, однако чаще бывает на уровне грудного отдела (70%), реже – поясничного (20%) и шейного (10%).
Слайд 6Причины КСМ
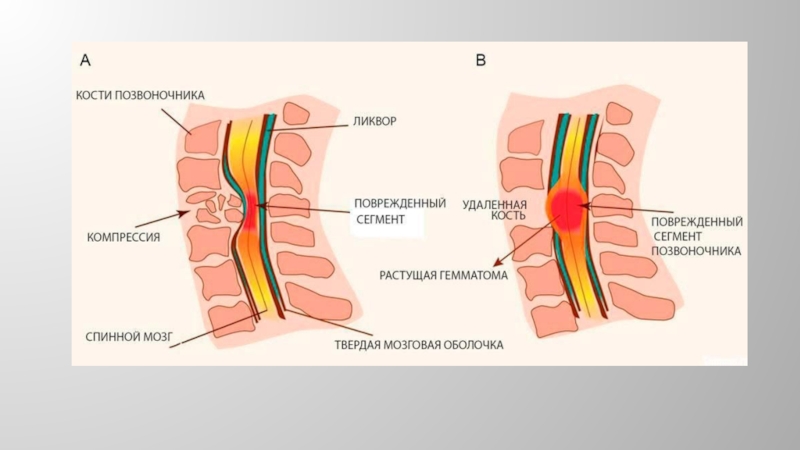
У онкологических больных сдавление спинного мозга может быть обусловлено:
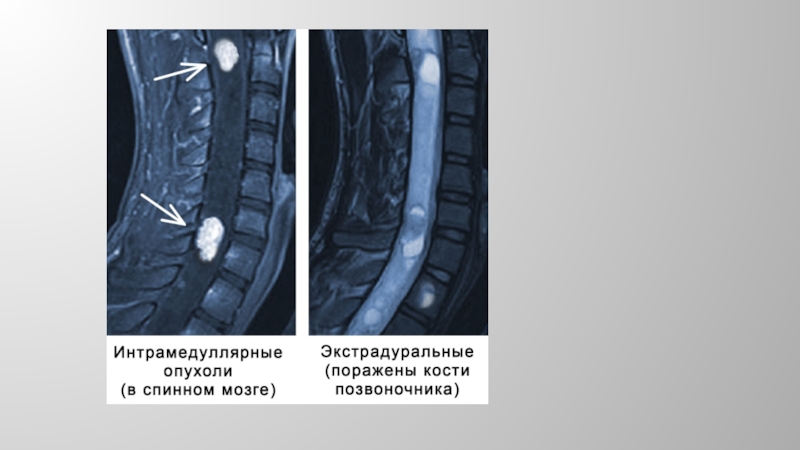
метастазами в эпидуральное пространство (метастаз в тело позвонка с последующей
инвазией переднего эпидурального про странства , при метастатическом раке молочной железы, раке легкого, предстательной железы, почки, опухолях ЖКТ);повреждающим действием костными фрагментами,
интрамедуллярными метастазами,
смещением позвонков,
гематомой в субдуральном пространстве спинного мозга
Слайд 9Клиника КСМ
Клиника компрессии спинного мозга характеризуется тетрадой клинических симптомов:
•
болями,
• дисфункцией вегетативной нервной системы (нарушением функции тазовых органов),
• нарушением чувствительности.
• слабостью,
Наличие любого из этих симптомов может свидетельствовать о компрессии спинного мозга
Слайд 10Болевой синдром при Ксм
Боль локальная или по типу радикулярного синдрома
является первым симптомом у 95% больных с опухолевым процессом в
эпидуральном пространстве.Болевой синдром опережает появление других симптомов на несколько недель или месяцев.
Локализация боли обычно соответствует уровню опухолевого поражения позвоночника. Иногда такового соответствия не наблюдается, и боль может отмечаться как выше, так и ниже области сдавления спинного мозга.
Болевой синдром обусловлен растяжением или сдавлением периостальных рецепторов или компрессией позвонка, а также растяжением нервов. Боли могут усиливаться при кашле, чиханьи, потягивании и в положении на спине, но могут быть отраженными, что существенно затрудняет диагностику.
Слайд 11Прогрессирующая мышечная слабость наблюдается у 76% больных с компрессией спинного
мозга и чаще проявляется жалобами на тяжесть и «одеревенение» нижних
конечностей, их «волочение» при ходьбе.Дисфункция вегетативной нервной системы отмечена у 57% больных в виде острых или постепенно нарастающих нарушений функции органов малого таза. Этот симптом является одним из наиболее тяжелых проявлений компрессии спинного мозга и является неблагоприятным фактором.
Нарушение чувствительности (парестезии, анестезии, ощущения холода) отмечают 51 % больных.
Слайд 12При поражениях спинного мозга выше уровня ThXII– LI , как
правило, развивается клиническая картина, которая включает мышечную слабость в нижних
конечностях, потерю чувствительности, нарушения функции тазовых органов и сексуальные расстройства.Сдавление спинного мозга каудальнее ThI сопровождается нижней параплегией или парапарезом с сохранением функции верхних конечностей. Если компрессия происходит выше СV, то развивается тетраплегия и тетрапарез.
При поражении дистальной части спинного мозга наблюдаются симметричные боли в перианальной области с ранней потерей чувствительности в области промежности. Компрессия в области cauda equina (между LI и SI,II), как правило, проявляется асимметричными, сегментарными нарушениями двигательного и чувствительного характера в нижних конечностях.
Слайд 13Потенциально смертельным осложнением метастатичесого поражения шейных позвонков является подвывих в
атланто-аксилярном сочленении.
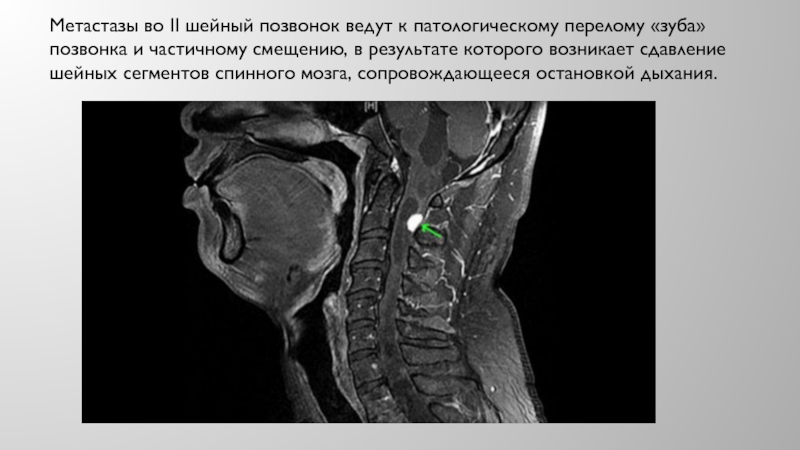
Слайд 14Метастазы во II шейный позвонок ведут к патологическому перелому «зуба»
позвонка и частичному смещению, в результате которого возникает сдавление шейных
сегментов спинного мозга, сопровождающееся остановкой дыхания.Слайд 15Большинство больных с метастазами в верхние шейные позвонки жалуются на
болевые ощущения в верхних отделах шеи, усиливающиеся при поворотах головы,
с возможной иррадиацией в плечо или лопатку. Боль в области шеи, спазм околопозвоночных мышц, ограничение движений в шейном отделе позвоночника – постоянные нарушения к моменту установления диагноза.При распространении процесса появляются слабость в нижних конечностях, потеря равновесия, несостоятельность сфинктеров прямой кишки и мочевого пузыря, головокружение, дизартрия, затруднения при глотании.
Слайд 16Диагностика КСМ
• Неврологическое и физикальное обследование: перкуссия позвоночника, оценка двигательной
и сенсорной слабости, пассивное сгибание шеи, подъем выпрямленной ноги, ректальное
обследование (оценка тонуса сфинктера), «булавочная» проба от пальцев стопы до головы для установления уровня чувствительности.• Рентгенографическое исследование. При рентгенографии в прямой проекции характерные изменения тел позвонков на уровне компрессии спинного мозга выявляются у 91% больных с эпидуральными метастазами.
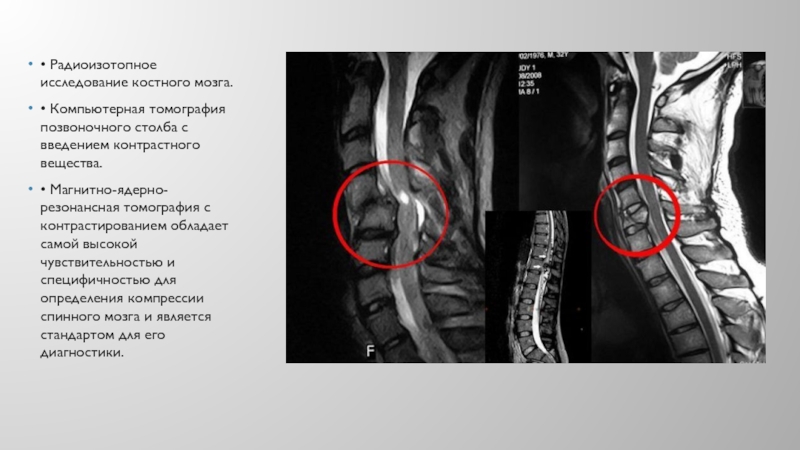
Слайд 17• Радиоизотопное исследование костного мозга.
• Компьютерная томография позвоночного столба
с введением контрастного вещества.
• Магнитно-ядерно-резонансная томография с контрастированием обладает
самой высокой чувствительностью и специфичностью для определения компрессии спинного мозга и является стандартом для его диагностики.Слайд 20Лечение КСМ
Как только диагноз ясен, необходимо начать лечение, так как
нередко выраженная слабость в течение нескольких часов может перейти в
необратимую параплегию.Неотложные мероприятия.
• Иммобилизация позвоночника, если таковой не было, с помощью жесткого щита, специальных ортопедических корсетов, воротников.
• Назначение кортикостероидных гормонов, способствующих уменьшению отека спинного мозга (высокие дозы дексаметазона по следующей схеме: однократное введение 20 мг дексаметазона внутривенно с последующим применением препарата перорально по 8 мг (16 таблеток) в сутки первые 10 дней, затем по 4 мг (8 таблеток) в сутки в течение 2 нед, затем – поддерживающая доза по 2 мг (4 таблетки) постоянно.
*Некоторыми авторами предлагается использовать следующий режим введения дексаметазона: 100 мг препарата внутривенно болюсно в первые сутки и в последующем – введение дексаметазона по 4 мг внутривенно через каждые 6 ч.
Слайд 21• Параллельно с дексаметазоном назначаются мочегонные, препараты калия, средства, улучшающие
мозговое кровообращение (кавинтон), сосудистые препараты (трентал).
За последние годы проведено
большое количество исследований с целью оптимизации лечения больных с синдромом компрессии спинного мозга. Однако вопрос лечебной тактики остается нерешенным, особенно в части, касаюшейся выбора между оперативным лечением и/или лучевой терапией.Слайд 22Лучевая терапия
является одним из наиболее эффективных методов лечения этого
осложнения и позволяет добиться положительного лечебного эффекта в 30–50% случаев.
Показания к лучевой терапии:
• наличие радиочувствительной опухоли (рак молочной железы, рак предстательной железы, множественная миелома, нейробластома),
• клинические признаки стабильности позвоночника,
• противопоказания к оперативному лечению.
Лучевая терапия может быть проведена больным с множественными очагами компрессии или медленным течением синдрома компрессии спинного мозга.
Слайд 23Хирургическое лечение
Стандартной операцией считается декомпрессионная ламинэктомия.
Некоторыми исследователями предлагаются
операции резекции тел позвонков с последующим их протезированием синтетическими тканями
или укреплением металлическими пластинками .Показания к хирургическому лечению
• клинические признаки нестабильности позвоночника,
• сдавление нервных стволов вследствие прямого распространения опухоли, расположенной паравертебрально, солитарный очаг поражения при отсутствии прогрессирования других очагов,
• непереносимые боли, требующие наркотических анальгетиков в больших дозах,
• нечувствительные к лучевой терапии опухоли,
• относительно удовлетворительное общее состояние больного и ожидаемая продолжительность жизни более 6 мес.
Слайд 24Химиотерапия
• может быть проведена в качестве первой линии для опухолей,
чувствительных к цитостатикам (лимфопролиферативные заболевания, миелома, рак молочной железы, рак
предстательной железы) и в случае, когда нельзя проводить ни лучевую терапию, ни оперативное лечение.Слайд 25СИНДРОМ ВЕРХНЕЙ ПОЛОЙ ВЕНЫ
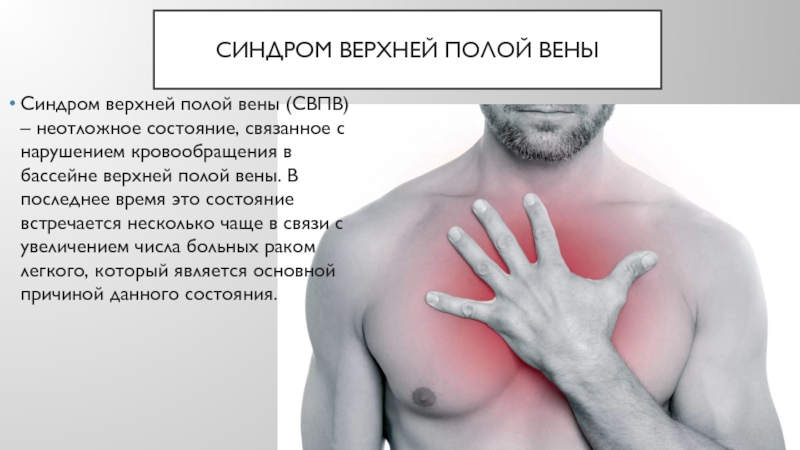
Синдром верхней полой вены (СВПВ) –
неотложное состояние, связанное с нарушением кровообращения в бассейне верхней полой
вены. В последнее время это состояние встречается несколько чаще в связи с увеличением числа больных раком легкого, который является основной причиной данного состояния.Слайд 26Причины СВПВ
К злокачественным опухолям, которые наиболее часто (80–90%) осложняются СВПВ,
относятся следующие:
• неходжкинские лимфомы, чаще диффузные крупноклеточные или лимфобластные
с локализацией в переднем средостении, • рак легкого, особенно правосторонний,
• метастатические формы рака молочной железы, яичка, ЖКТ
• саркома, особенно злокачественная фиброзная гистиоцитома,
• меланома.
Слайд 27Среди других причин, приводящих к СВПВ, следует отметить:
• инфекционные
заболевания: туберкулез, сифилис, гистиоплазмоз,
• тромбозы (травматические, спонтанные или вследствие
вторичного поражения сосудов средостения), • ятрогенные причины,
• идиопатический фиброзный медиастинит,
• сердечно-сосудистая недостаточность,
• загрудинный зоб.
Клиническая картина СВПВ связана с повышением внутрисосудистого венозного давления в зонах, венозный отток из которых в норме дренируется через верхнюю полую вену или образующие ее безымянные вены. Замедление скорости кровотока, развитие венозных коллатералей, симптомы, связанные с основным заболеванием, являются компонентами СВПВ. Выраженность различных признаков СВПВ зависит от скорости развития патологического процесса, уровня и степени сдавления просвета верхней полой вены и адекватности коллатерального кровообращения.
Слайд 28Клиника
• Клиническое течение СВПВ может быть острым или медленно прогрессирующим.
• Жалобы больного крайне разнообразны: головная боль, тошнота, головокружение, изменение
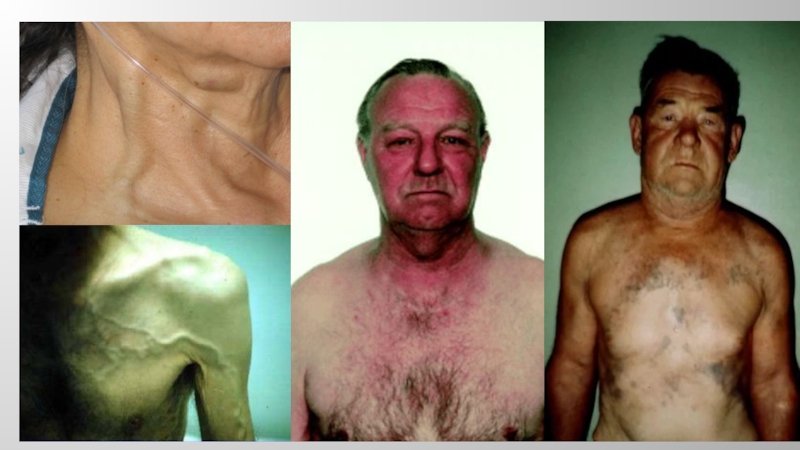
внешности, осиплость голоса, кашель, дисфагия, боли в грудной клетке, затрудненное дыхание, одышка, сонливость, обмороки, судороги.• При физикальном обследовании обнаруживаются наиболее характерные признаки СВПВ: расширение, набухание вен шеи, грудной стенки и верхних конечностей, отек лица, шеи или верхнего плечевого пояса, цианоз или полнокровие лица (плетора), тахипноэ
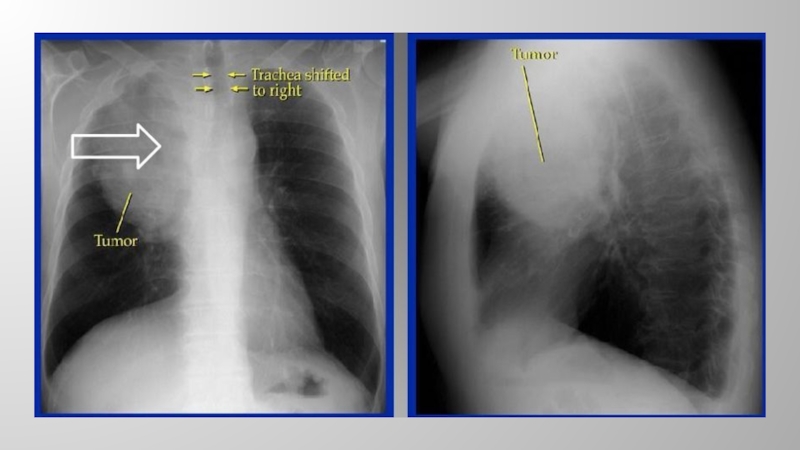
Слайд 30Диагностика
• достаточно данных клиники и физикального обследования.
• При отсутствии
морфологического диагноза необходимо проведение всех возможных исследований для верификации патологического
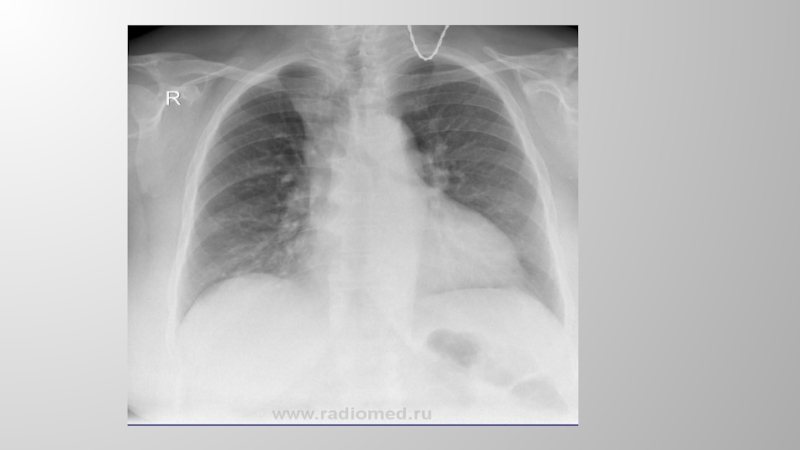
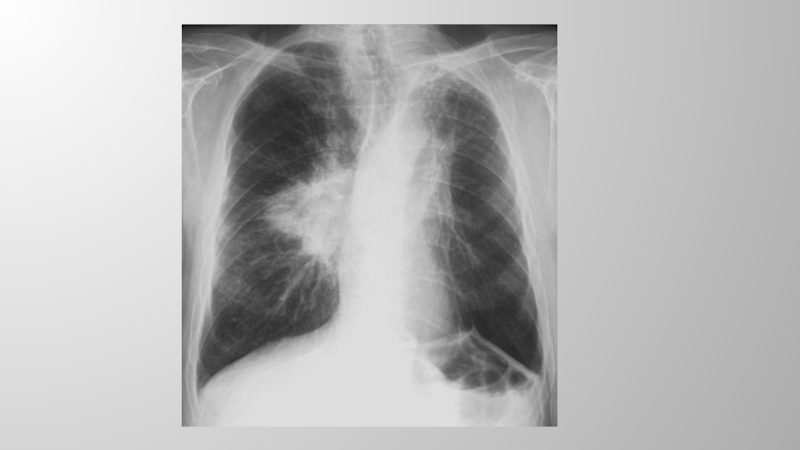
процесса: цитологическое исследование мокроты, бронхоскопия с биопсией и цитологическим исследованием смывов из бронхов, медиастиноскопия с биопсией, биопсия лимфатического узла, стернальная пункция• Рентгенография грудной клетки в прямой и боковых проекциях и томография показаны всем больным в случаях неотложных состояний или с подозрением на нарушение проходимости верхней полой вены. Рентгенологическое исследование позволяет выявить патологический процесс в средостении, степень его распространения и определить границы для последующей лучевой терапии.
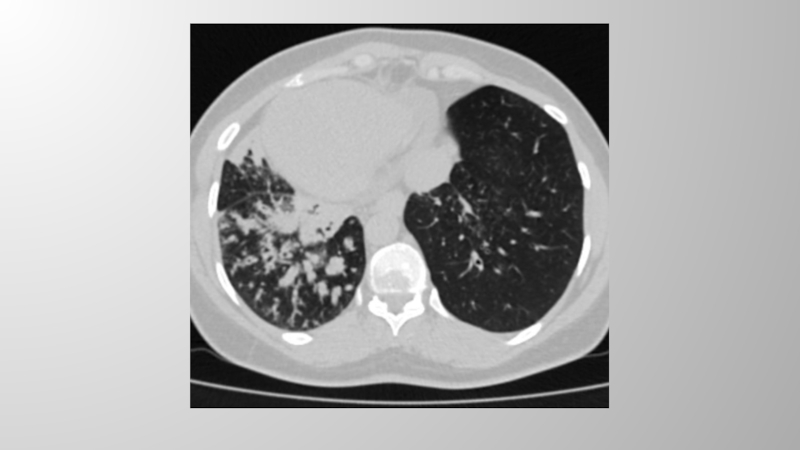
Слайд 35• Компьютерная томография с контрастированием позволяет уточнить контуры опухолевого процесса,
степень поражения лимфатических узлов средостения
• Доплеровское ультразвуковое исследование сонных
или надключичных вен может оказать помощь для дифференциальной диагностики между тромбозом и обструкцией извне • Не рекомендуется введение радиоконтрастных или других веществ в вену пораженной конечности ввиду высокого риска экстравазации. Однако в редких случаях проводят флебографию для выявления локализации и степени нарушения проходимости верхней полой вены.
Флебография оказывается полезной для дифференциальной диагностики сосудистого и внесосудистого характера поражения, решения вопроса об операбельности, определения протяженности пораженного сегмента.
Слайд 36Лечение
• Оптимальное лечение зависит от причин, вызвавших СВПВ, и
скорости развития симптомов прогрессии . В острой ситуации лечение можно
начинать, не имея точного морфологического диагноза.Экстренные симптоматические мероприятия направлены на спасение жизни больного, они необходимы, чтобы обеспечивать поступление воздуха в легкие, ликвидировать непроходимость верхней полой вены и сдавление органов средостения. Кроме покоя, возвышенного положения, кислородотерапии, иногда могут потребоваться трахеостомия, интубация, введение противосудорожных средств.
Показано применение диуретиков (фуросемид, маннитол),
ГКС. Рекомендуется введение гидрокортизона от 100 до 500 мг внутривенно с последующим снижением дозы каждые 6–8 ч с учетом клинической картины или назначение преднизолона 60– 90 мг внутривенно, затем по 40–60 мг в сутки перорально.
• Лечение антикоагулянтами или фибринолитическими препаратами показано при тромбозе вены. Но эти препараты не должны назначаться стандартно, за исключением тех случаев, когда на флебографии диагностируется тромбоз верхней полой вены или отсутствуют признаки улучшения при лечении другими методами.
Слайд 37Лучевая терапия
крупными фракциями является высокоэффективным методом лечения СВПВ, особенно
при немелкоклеточном раке легкого. Эффективность ее достигает 70–90%. Облучение грудной
клетки должно начинаться как можно раньше. Проведение неотложной лучевой терапии требуется при дыхательной недостаточности (в том числе стридорном дыхании) или при наличии симптомов со стороны ЦНС.Слайд 38Химиотерапевтическое лечение
• в качестве первой линии предпочтительнее проводить при
наличии опухолей, высокочувствительных к цитостатикам (лимфопролиферативные заболевания, миелома, герминогенные опухоли,
рак молочной и предстательной желез)Слайд 39Комбинированная терапия (химиотерапия и лучевая терапия)
показана при мелкоклеточном раке
легкого, лимфопролиферативных заболеваниях. Однако одновременное проведение химиотерапии и лучевой терапии
часто связано с увеличением числа осложнений (дисфагия, нейтропения) , поэтому предпочтительнее поэтапная комбинированная терапия (сначала лечение цитостатиками, а затем облучение или наоборот).Слайд 40ГИПЕРКАЛЬЦИЕМИЯ
Гиперкальциемия у онкологических больных – наиболее частое угрожающее жизни нарушение
метаболизма, как правило, обратимого характера, возникающее при распространенных злокачественных опухолях.
Слайд 41Гиперкальциемия с наибольшей частотой встречает ся при следующих опухолях :
• немелкоклеточный рак легкого (преимущественно плоскоклеточный с большими опухолевыми массами),
• рак молочной железы,
• рак почки,
• рак яичников,
• множественная миелома,
• опухоли головы, шеи,
• лимфопролиферативные заболевания (при лимфогранулематозе – у пожилых больных с большими очагами поражения или при Т-клеточной лимфоме высокой степени злокачественности),
• новообразования с неизвестной локализацией первичной опухоли,
• солидные опухоли с метастазами в кости, преимущественно литического характера
Слайд 42Патогенез
• локальная метастатическая деструкция кости,
• генерализованный остеолиз, обусловленный выделением опухолью
некоторых гуморальных факторов (парагормонподобный белок). В обоих случаях наблюдается усиление
костной резорбции.Непосредственная локальная инвазия костной тка. ни опухолевыми клетками, активированными остеокластами, стимулирует высвобождение кальция в кровь до уровня, который превышает экскреторные возможности почек. Костная резорбция усугубляется цитокинами и другими факторами, которые продуцируются инвазивными опухолевыми клетками. Наиболее часто этот механизм гиперкальциемии наблюдается при миеломной болезни, раке молочной железы
Слайд 43Гуморальная гиперкальциемия наблюдается у больных раком легкого и почки, у
которых могут отсутствовать метастазы в костях. В этом случае клиническая
картина соответствует гиперпаратиреоидизму, и удаление или регрессия первичной опухоли под действием цитостатической терапии приводит к исчезновению гиперкальциемии. Главной причиной развития этого состояния является остеолиз и усиленная почечная реабсорбция кальция вследствие продукции опухолевой тканью паратгормонподобного белка (РТНrР).Отмечено, что опухолевые клетки с экспрессией РТНrР, чаще метастазируют в кости, чем в другие органы и ткани.
Гиперкальциемия и гиперкальциурия приводят к нарушению реабсорбции натрия и воды, вызывая полиурию («кальциевый диурез»), соответственно снижается ОЦК и межтканевой жидкости. Возникает замкнутый круг: гиповолемия приводит к снижению почечного кровотока, что, в свою очередь, уменьшает степень клубочковой фильтрации, а это нарушение вызывает повышение реабсорбции кальция в проксимальных отделах почечных канальцев. Усугубляют состояние обезвоживание и частые рвоты.
Слайд 44Клиника
• общие симптомы – обезвоживание, слабость, усталость, снижение массы тела,
жажда;
• центральная нервная система – головная боль, гипофлексия, проксимальная
миопатия, апатия, заторможенность, психические нарушения, судороги, спутанность сознания, кома; • желудочно.кишечный тракт – анорексия, тошнота, рвота, запоры, кишечная непроходимость, панкреатит, метеоризм, увеличение желудочной секреции и секреции пепсина;
сердечно.сосудистая система – брадикардия, гипотония, короткий QT-интервал, широкий зубец Т, пролонгированный PR-интервал, аритмия, асистолия;
• мочевыделительная система – полиурия, азотемия, почечная недостаточность, кома.
Слайд 45Если не проводится коррекция гиперкальциемии, последовательно развивается дегидратация (уменьшение объема
внеклеточной жидкости), почечная недостаточность, кома и смерть. В случае адекватного
лечения этого осложнения и последующей профилактики рецидивов больные могут жить в течение многих месяцев и даже лет.В основном клинические симптомы появляются при уровне кальция в сыворотке крови выше 2,9–3,0 ммоль/л. Тяжелой принято считать гиперкальциемию 3,7 ммоль/л или выше. Это требует неотложного лечения. Когда уровень кальция становится равным 3,7–4,5 ммоль/л или выше, развивается кома и остановка сердца.
Слайд 46Лечение
Больные с гиперкальциемией требуют постоянного мониторинга показателей:
• гемодинамики,
•
диуреза,
• водного и электролитного баланса,
• центрального венозного давления,
• креатинина, мочевины крови.
Проводимая терапия включает восстановление объема циркулирующей крови (регидратация) и фармакологическую коррекцию гиперкальциемии путем повышения экскреции кальция и блокирования костной резорбци.
Слайд 47• регидратация: введение изотонических растворов (3–6 л 0,9% раствора натрия
хлорида в сутки или 300–400 мл в час каждые 3–4
ч).Желательно поддержание центрального венозного давления на уровне 10 см водн. ст.;
• мочегонные препараты на фоне проводимой регидратации при удовлетворительных гемодинамических показателях с поддержанием диуреза 150–200 мл/ч. Предпочтение отдается «петлевым диуретикам» – фуросемид по 20–40 мг внутривенно каждые 2–4 ч;
• кортикостероиды – преднизолон 40–100 мг внут ривенно каждые 8 ч (или эквивалентные дозы дексаме тазона, гидрокортизона) в зависимости от клиническо го течения с последующим применением препарата внутрь по 15–30 мг в сутки. При раке молочной железы не отменяется гормонотерапия антиэстрогенами.
Слайд 48• бисфосфонаты (клодронат, памидронат, ибандро. нат) – вводятся внутривенно капельно
после первых этапов регидратации. Эффективность бисфосфонатов, по данным разных авторов
, колеблется от 60 до 95 %.Клодронат (бонефос) вводится в дозе 1500 мг в сутки или по 300 мг в течение 4 ч с 1го по 5й день каждые 3 нед. Возможно последующее длительное применение препарата в дозе 1600 мг в сутки в капсулах.
Памидронат (аредия) используется в дозе 60–90 мг,
ибандронат (бон дранат) – по 2–4 мг в виде 4–6часовой внутривенной инфузии.
Доза препаратов определяется в зависимости от тяжести гиперкальциемии. Активность бисфосфонатов начинает определяться через 24–48 ч, а максимальный ответ регистрируется через 72 ч после введения. В обычной практике этот отсроченный эффект бисфосфонатов малозаметен, так как маскируется лечебным эффектом применяемой гидратации. Как правило, уровень кальция сыворотки начинает повышаться через4–5 нед, что требует повторного введения препарата;
Слайд 49• кальцитонин (миокальцик) – полипептидный гормон, секретируемый парафолликулярными клетками щитовидной
железы, способствует торможению резорбции кости остеокластами и увеличению почечного клиренса
кальция. По данным литературы, гиперкальциемия при злокачественных опухолях поддается временному контролю под действием кальцитонина у 75–90% больных .Активность кальцитонина начинает проявляться в первые часы после введения, что становится перспективным для достижения быстрого клинического эффекта. Однако активность кальцитонина непродолжительна, препарат вводится по 4– 8 МЕ/кг внутримышечно каждые 6–12 ч