Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Органическая химия. Введение
Содержание
- 1. Органическая химия. Введение
- 2. Слайд 2
- 3. Слайд 3
- 4. « Я не в силах больше молчать,
- 5. Слайд 5
- 6. Мы используем огромное количество синтетических органических веществ, которые в природе никогда не существовали (полиэтилен, капрон, лавсан и многие другие).
- 7. Слайд 7
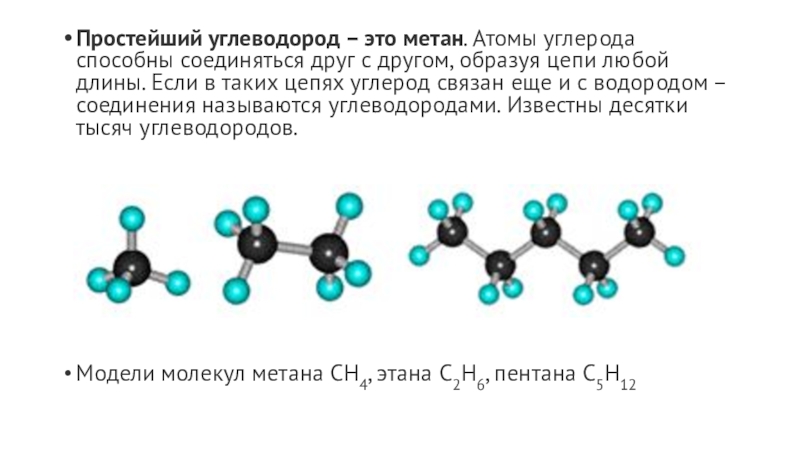
- 8. Простейший углеводород – это метан. Атомы углерода
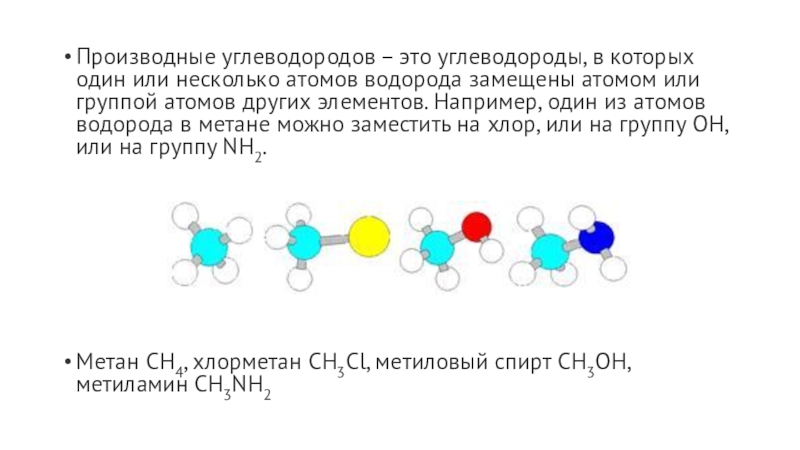
- 9. Производные углеводородов – это углеводороды, в которых
- 10. Слайд 10
- 11. Валентность – это способность атома образовывать химические
- 12. Основные положения теории А.М. Бутлерова.А. М.Бутлеров на
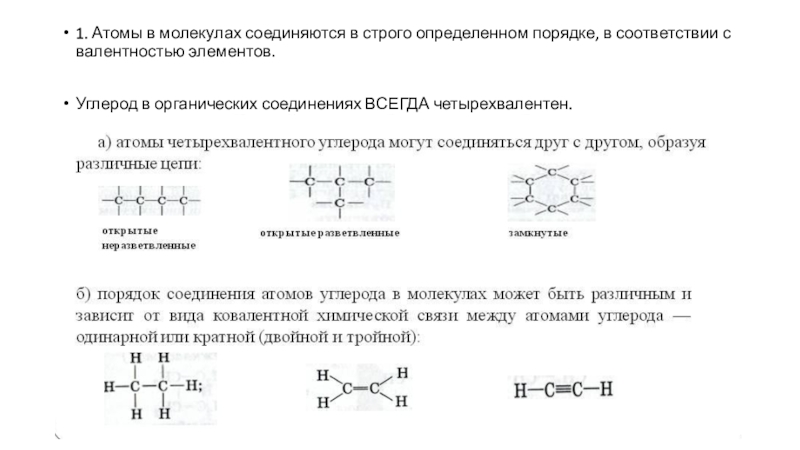
- 13. 1. Атомы в молекулах соединяются в строго
- 14. Свойства веществ зависят не только от качественного
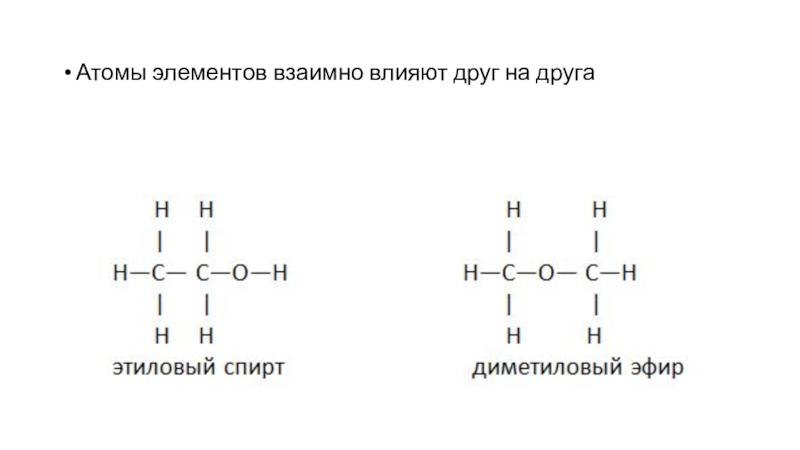
- 15. Атомы элементов взаимно влияют друг на друга
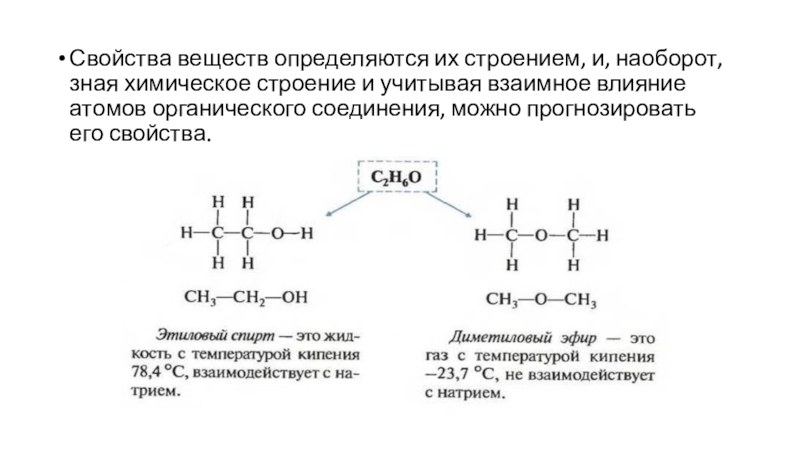
- 16. Свойства веществ определяются их строением, и, наоборот,
- 17. Скачать презентанцию
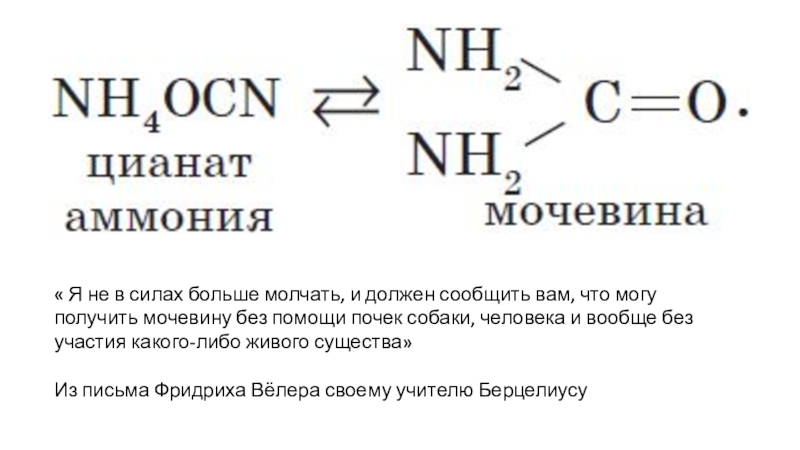
« Я не в силах больше молчать, и должен сообщить вам, что могу получить мочевину без помощи почек собаки, человека и вообще без участия какого-либо живого существа» Из письма Фридриха Вёлера
Слайды и текст этой презентации
Слайд 1Органическая химия. Введение.
Йенс Якоб Берцелиус
1808
« Органическими называются соединения, которые являются
продуктами жизнедеятельности растений и животных»
в природе больше прочих.Слайд 4« Я не в силах больше молчать, и должен сообщить
вам, что могу получить мочевину без помощи почек собаки, человека
и вообще без участия какого-либо живого существа»Из письма Фридриха Вёлера своему учителю Берцелиусу
Слайд 6Мы используем огромное количество синтетических органических веществ, которые в природе никогда не существовали (полиэтилен, капрон, лавсан и
многие другие).
Слайд 8Простейший углеводород – это метан. Атомы углерода способны соединяться друг
с другом, образуя цепи любой длины. Если в таких цепях
углерод связан еще и с водородом – соединения называются углеводородами. Известны десятки тысяч углеводородов.Модели молекул метана СН4, этана С2Н6, пентана С5Н12
Слайд 9Производные углеводородов – это углеводороды, в которых один или несколько
атомов водорода замещены атомом или группой атомов других элементов. Например,
один из атомов водорода в метане можно заместить на хлор, или на группу ОН, или на группу NH2.Метан CH4, хлорметан CH3Cl, метиловый спирт CH3OH, метиламин CH3NH2
Слайд 11Валентность – это способность атома образовывать химические связи.
Металлы основной подгруппы
первой группы всегда имеют валентность I. Это элементы Li, Na, K,
Rb, Cs, Fr.· Металлы основной подгруппы второй группы всегда имеют валентность II. Это элементы Be, Mg, Ca, Sr, Ba, Ra.
· Водород всегда имеет валентность I.
· Кислород всегда имеет валентность II.
· Элементы Al и В (основная группа третьей подгруппы) всегда имеют валентность III.
· Элементы основной подгруппы седьмой группы чаще (но не всегда!) имеют валентность I. Это элементы F, Cl, Br, I, At. Кстати, эти элементы носят название «галогены»
C (углерод), N (азот), P (фосфор), S (сера), Сr (хром), Fe (железо), Cu (медь).
Слайд 12Основные положения теории А.М. Бутлерова.
А. М.Бутлеров на основе анализа и
обобщения отдельных фактов и положений создал стройную научную теорию химического
строения органических соединений, которую можно сформулировать в виде следующих положений.Слайд 131. Атомы в молекулах соединяются в строго определенном порядке, в
соответствии с валентностью элементов.
Углерод в органических соединениях ВСЕГДА четырехвалентен.
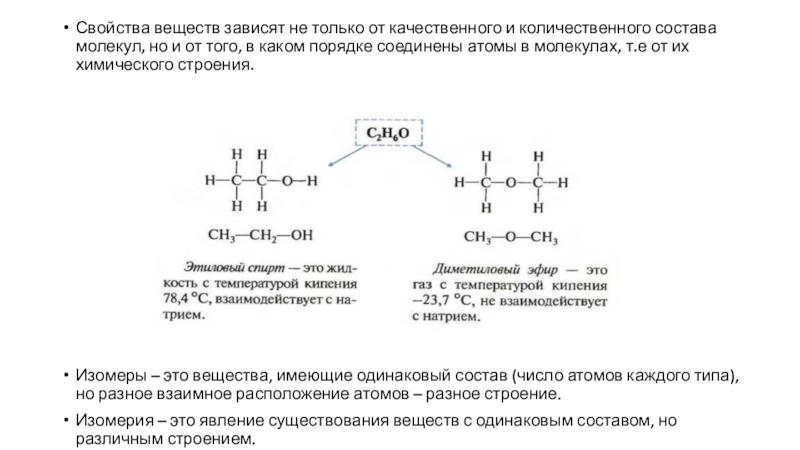
Слайд 14Свойства веществ зависят не только от качественного и количественного состава
молекул, но и от того, в каком порядке соединены атомы
в молекулах, т.е от их химического строения.Изомеры – это вещества, имеющие одинаковый состав (число атомов каждого типа), но разное взаимное расположение атомов – разное строение.
Изомерия – это явление существования веществ с одинаковым составом, но различным строением.