Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основные факторы устойчивости коллоидов. Коагуляция. Коллоидная защита и пептизация
Содержание
- 1. Основные факторы устойчивости коллоидов. Коагуляция. Коллоидная защита и пептизация
- 2. Виды устойчивости растворов (по Пескову)… устойчивость ДФ
- 3. Коагуляция ‒ …… процесс слипания частиц, образование
- 4. Факторы, вызывающие коагуляциюУвеличение концентрации золя приводит к
- 5. Факторы, вызывающие коагуляциюДобавление электролитов наиболее сильное по
- 6. При изучении влияния электролитов на коагуляцию следует
- 7. чем выше заряд коагулирующего иона, тем меньше
- 8. Правило Дерягина ‒ Ландау …… устанавливает связь
- 9. Способность ионов одного заряда к гидратации (лиотропные ряды)Факторы, вызывающие коагуляциюLi+Na+K+Rb+Cs+Li+Na+K+Rb+Cs+Коагулирующая способностьСтепень гидратации ионов
- 10. Факторы, вызывающие коагуляцию«Ионы-партнёры», идущие в паре с
- 11. Смесями электролитов;Многозарядными ионами‒коагуляторами (чередование зон коагуляции);При смешивании
- 12. Аддитивность(суммирование γ ионов одинакового q и близких
- 13. 2. Чередование зон коагуляции‒+++‒‒‒‒ ζ+ ζ0‒ 30
- 14. 3. Гетерокоагуляция+‒0Причина явления ‒ электростатическое притяжение частиц
- 15. … вызвана добавлением очень малых количеств ВМС
- 16. Вывод: адсорбционный слой является механическим препятствием для
- 17. Защитное число …… min масса ВМС (мг),
- 18. Процесс перехода свежевыпавшего при коагуляции осадка во
- 19. ---Теории коагуляцииАдсорбционная(Фрейндлих)Адсорбция ионов – коагулянтов на агрегате
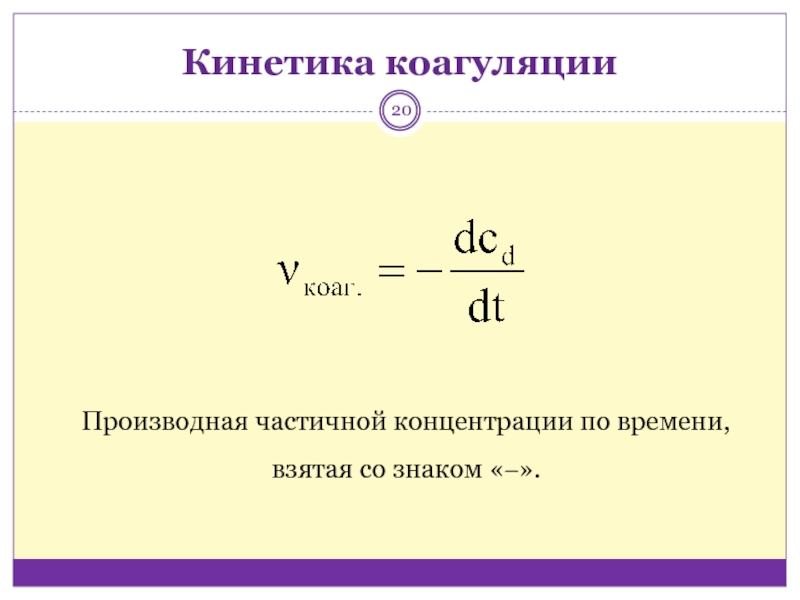
- 20. Кинетика коагуляцииПроизводная частичной концентрации по времени, взятая со знаком «‒».
- 21. Коагуляция по Смолуховскому М. (1906г.)При столкновении 2-х
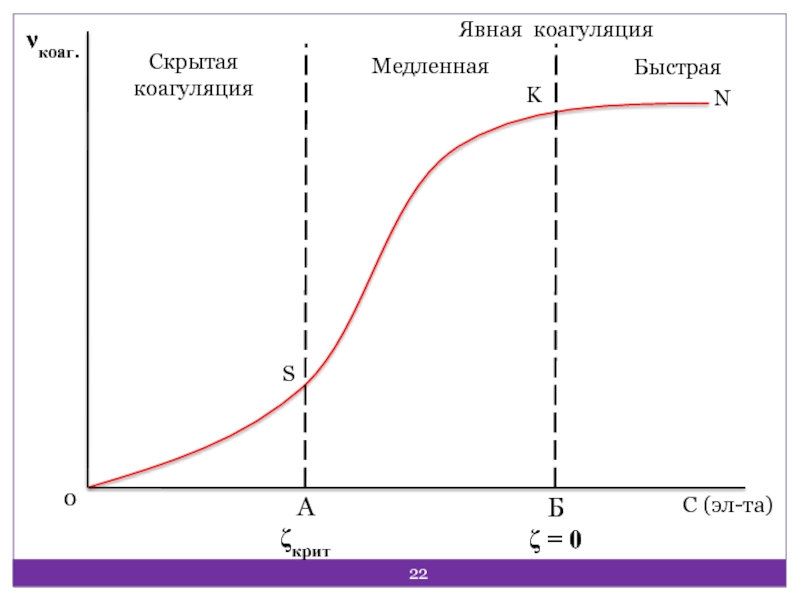
- 22. Скрытая коагуляцияМедленнаяБыстраяЯвная коагуляцияSA ζкритБ ζ = 0С (эл-та)0νкоаг.KN
- 23. КоагуляцияСкрытая включает образование вторичных, третичных и т.д.
- 24. Уравнение Смолуховского …… характеризует скорость быстрой коагуляции.nm
- 25. Спасибо за внимание!
- 26. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Лекции №24, 25 курса
«Общая химия»
Лектор: профессор Иванова Надежда Семёновна
Основные
факторы устойчивости коллоидов. Коагуляция. Коллоидная защита и пептизация
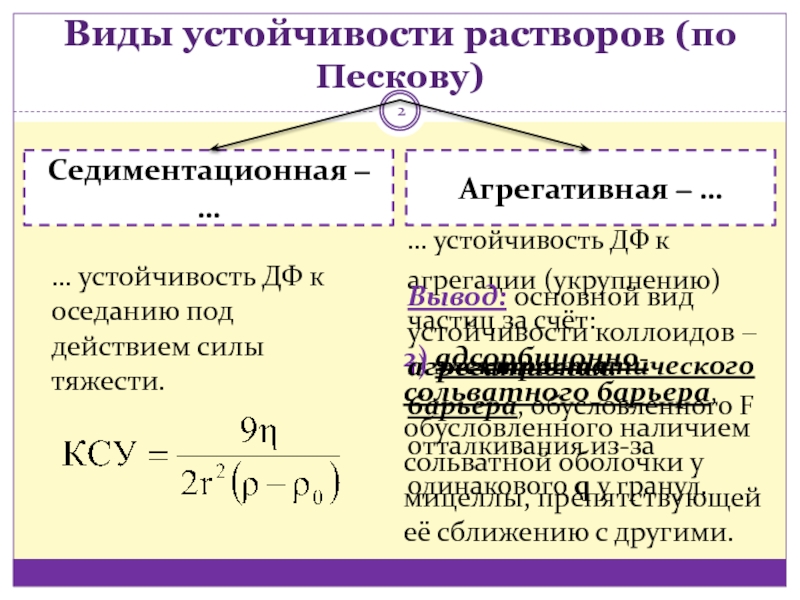
Слайд 2Виды устойчивости растворов (по Пескову)
… устойчивость ДФ к агрегации (укрупнению)
частиц за счёт:
1) электростатического барьера, обусловленного F отталкивания из-за
одинакового q у гранул.Седиментационная ‒ …
Агрегативная ‒ …
… устойчивость ДФ к оседанию под действием силы тяжести.
2) адсорбционно- сольватного барьера, обусловленного наличием сольватной оболочки у мицеллы, препятствующей её сближению с другими.
Вывод: основной вид устойчивости коллоидов ‒ агрегативная.
Слайд 3Коагуляция ‒ …
… процесс слипания частиц, образование крупных агрегатов с
потерей седиментационной и фазовой устойчивости и последующим разделением фаз.
… процесс
уменьшения степени дисперсности ДФ под действием тех или иных факторов.Стадии коагуляции
Вывод: для золей переход скрытой в явную происходит практически мгновенно!!!
явная
скрытая
Слайд 4Факторы, вызывающие коагуляцию
Увеличение концентрации золя приводит к уменьшению расстояния между
частицами, на котором начинают действовать силы притяжения.
Добавление неэлектролитов из-за способности
разрушения гидратной (сольватной) оболочки. Отсутствие оболочки позволяет частицам приблизиться на расстояние, на котором действуют силы притяжения.Слайд 5Факторы, вызывающие коагуляцию
Добавление электролитов наиболее сильное по 2-м причинам:
из-за адсорбции
ионов электролита на грануле и агрегате, снижении заряда гранулы и
ζ-потенциала;из-за уменьшения толщины диффузионного слоя, что приводит к уменьшению расстояния между частицами и возникновению сил притяжения.
Слайд 6При изучении влияния электролитов на коагуляцию следует учитывать:
коагуляция начинается при
достижении порога коагуляции (сп, ск)
Вывод: чем меньше сп, тем выше
γ электролита.коагулирующей частью электролита является ион, q которого противоположен q гранулы, а коагуляция наступает в ИЭТ золя.
Слайд 7чем выше заряд коагулирующего иона, тем меньше сп и выше
γ электролита.
Правило Шульце ‒ Гарди …
… коагулирующее действие оказывает противоион
и его γ возрастает пропорционально некоторой высокой степени его заряда.… γ электролита возрастает с увеличением заряда коагулирующего иона, противоположного по знаку заряду гранулы
Слайд 8
Правило Дерягина ‒ Ландау …
… устанавливает связь между сп и
зарядом коагулирующего иона.
Теор.:
Эксп.:
Дерягин
Борис Владимирович
(1902‒1994)
Ландау Лев Давидович (1908 —
1968)Слайд 9Способность ионов одного заряда к гидратации (лиотропные ряды)
Факторы, вызывающие коагуляцию
Li+
Na+
K+
Rb+
Cs+
Li+
Na+
K+
Rb+
Cs+
Коагулирующая
способность
Степень гидратации ионов
Слайд 10Факторы, вызывающие коагуляцию
«Ионы-партнёры», идущие в паре с коагулирующими ионами, уменьшают
их γ в случае адсорбции на поверхности коллоидной частицы.
Слайд 11Смесями электролитов;
Многозарядными ионами‒коагуляторами (чередование зон коагуляции);
При смешивании коллоидов с гранулами
разного по знаку заряда (взаимная коагуляция / гетерокоагуляция);
Добавлением очень малых
количеств ВМС (сенсибилизация).Особые случаи коагуляции
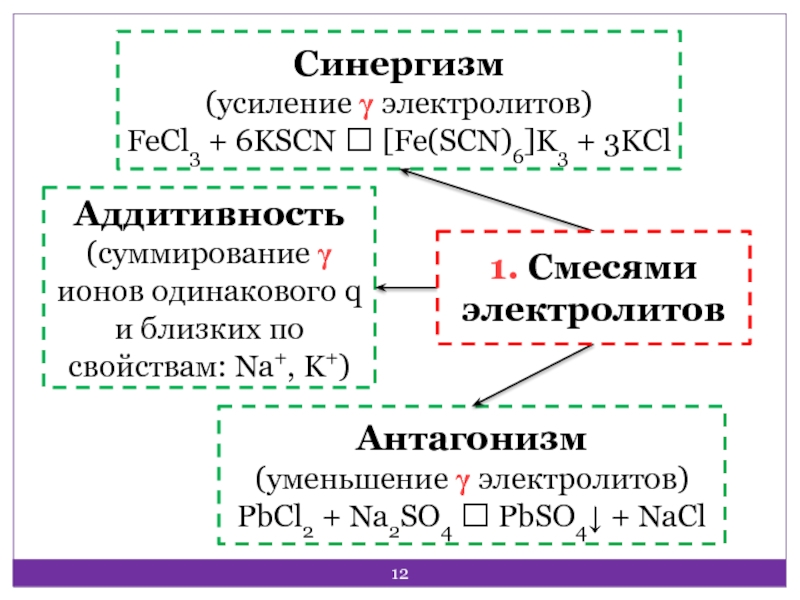
Слайд 12Аддитивность
(суммирование γ ионов одинакового q и близких по свойствам: Na+,
K+)
Антагонизм
(уменьшение γ электролитов)
PbCl2 + Na2SO4 ? PbSO4↓ + NaCl
Синергизм
(усиление γ
электролитов)FeCl3 + 6KSCN ? [Fe(SCN)6]K3 + 3KCl
1. Смесями электролитов
Слайд 13
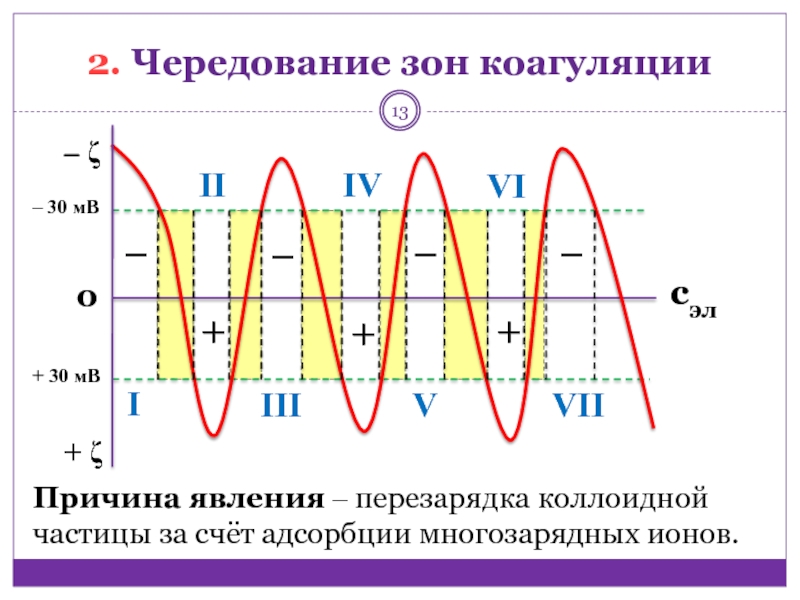
2. Чередование зон коагуляции
‒
+
+
+
‒
‒
‒
‒ ζ
+ ζ
0
‒ 30 мВ
+ 30 мВ
сэл
I
II
III
IV
V
VI
VII
Причина
явления ‒ перезарядка коллоидной частицы за счёт адсорбции многозарядных ионов.
Слайд 14
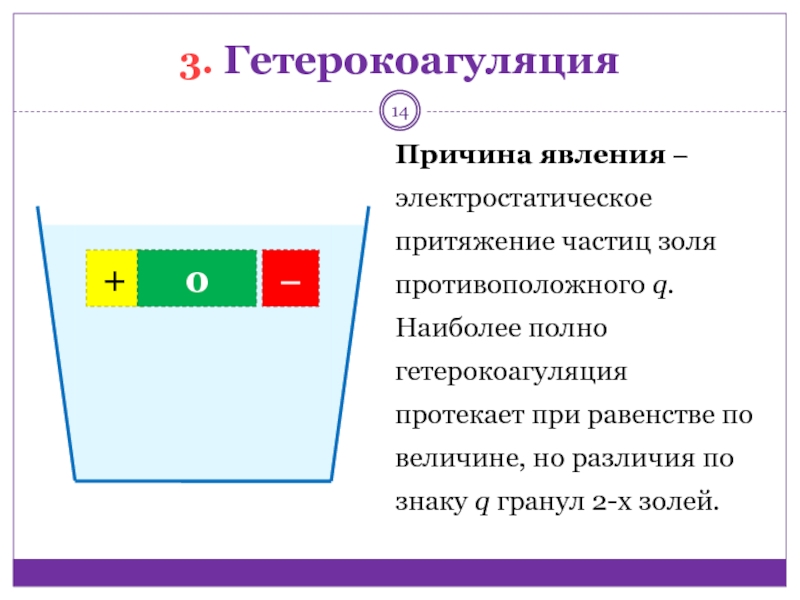
3. Гетерокоагуляция
+
‒
0
Причина явления ‒ электростатическое притяжение частиц золя противоположного q.
Наиболее полно гетерокоагуляция протекает при равенстве по величине, но различия
по знаку q гранул 2-х золей.Слайд 15… вызвана добавлением очень малых количеств ВМС и понижает устойчивость
коллоидов.
… связана с особенностями ВМС:
1. образование макроионов с большой адсорбционной
способностью;2. одновременная адсорбция макроионов на нескольких коллоидных частицах с образованием флокул (мостиковый механизм).
4. Сенсибилизация …
Слайд 16Вывод: адсорбционный слой является механическим препятствием для иона ‒ коагулянта.
…
повышение устойчивости коллоидов добавлением ВМС в концентрациях, достаточных для полного
адсорбционного насыщения поверхности мицелл защищаемого золя.Коллоидная защита …
+
‒
Слайд 17Защитное число …
… min масса ВМС (мг), достаточная для предотвращения
10 см3 гидрозоля от коагулирующего действия 1 см3 раствора NaCl
с ω=10% (массовая концентрация 100 г/л).
Слайд 18Процесс перехода свежевыпавшего при коагуляции осадка во взвешенное состояние (золь)
под влиянием пептизаторов ‒
б) адсорбция ионов пептизатора на поверхности
частиц осадка, появление у них одинакового q и за счёт электростатического отталкивания – переход в раствор.а) образование пептизатора за счёт хим. реакции;
пептизация
Адсорбционная
Диссолюционная
а) введение пептизатора;
Включают стадии:
↓Fe(OH)3 + FeCl3(пепт.) → {[Fe(OH)3]m·nFe3+·(3n‒x)Cl‒}x+ ·xCl‒
а) ↓Fe(OH)3 + HCl → FeOCl (пепт) + 2Н2О
б) ↓Fe(OH)3 + FeOCl (пепт) → {[Fe(OH)3]m·nFeО+·(n‒x)Cl‒}x+ ·xCl‒
Слайд 19-
-
-
Теории коагуляции
Адсорбционная
(Фрейндлих)
Адсорбция ионов – коагулянтов на агрегате и грануле, снижение
величины q и ζ – потенциала, коагуляция.
+
-
-
-
-
Физическая
(ДЛФО)
Уменьшение толщины диффузионного слоя
и гидратной оболочки, уменьшение расстояния между мицеллами, возникновение сил притяжения, коагуляция.На данном расстоянии действуют силы отталкивания
При действии ионов-коагулянтов происходит сжатие ионной атмосферы. Частицы сближаются на расстоянии, где действуют силы притяжения.
Слайд 21Коагуляция по Смолуховскому М. (1906г.)
При столкновении 2-х первичных частиц золя
появляются более крупные – вторичные и т.д.
Следовательно, коагуляция – реакция
II порядка и её ν можно описать кинетическим уравнением реакции II порядка.Недостаток схемы: 1) в дальнейшей хим. реакции продукты не участвуют, а коллоидные частицы, участвуют, увеличивая свой размер; 2) все частицы сферической формы и одного радиуса.
Слайд 23Коагуляция
Скрытая включает образование вторичных, третичных и т.д. частиц. Протекает незаметно
и медленно.
Явная заметна и протекает с разной скоростью в зависимости
от концентрации Э.Отрезок OS – период скрытой коагуляции. В точке А достигается сn электролита и ζкрит..
Отрезок SK – медленная явная коагуляция. В точке Б ζ = 0.
Отрезок KN – быстрая явная коагуляция. νкоаг. не зависит от сэлектролита.
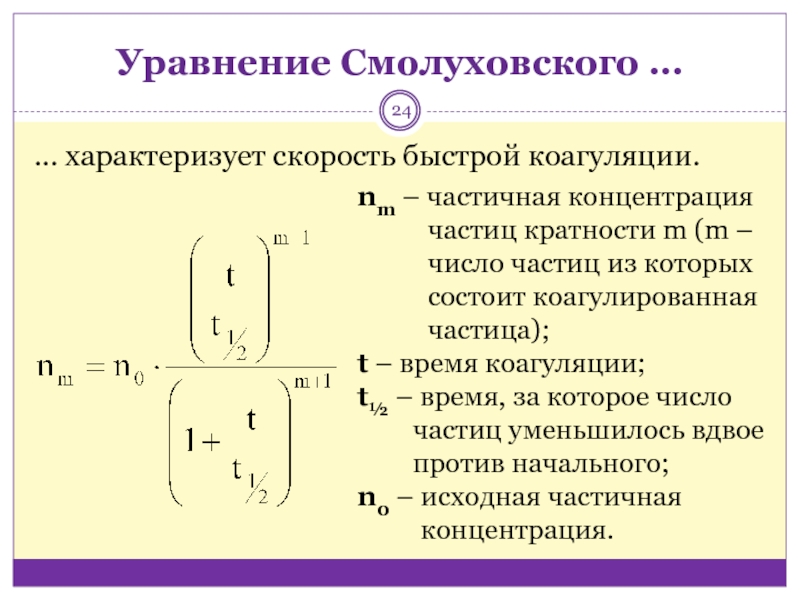
Слайд 24Уравнение Смолуховского …
… характеризует скорость быстрой коагуляции.
nm – частичная концентрация
частиц кратности m (m – число частиц из которых состоит
коагулированная частица);t – время коагуляции;
t½ – время, за которое число частиц уменьшилось вдвое против начального;
n0 – исходная частичная концентрация.