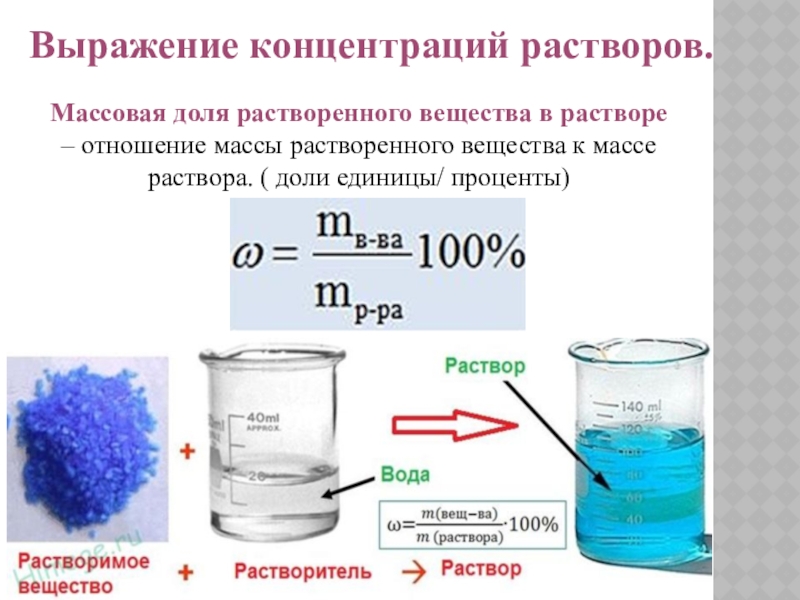
более компонентов: растворитель и растворенное вещество (вещества).
Точное определение раствора
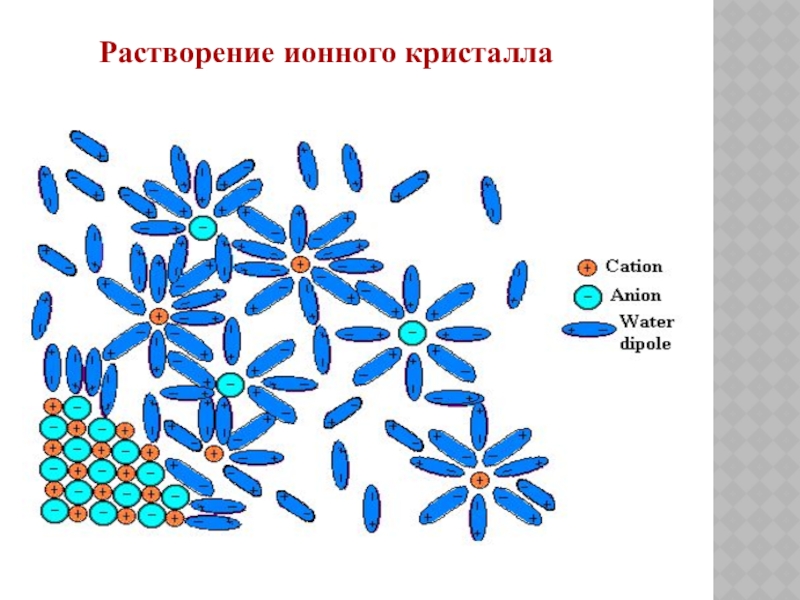
( 1887 год Д.И. Менделеев):Раствор – гомогенная (однородная) система, состоящая из
частиц растворенного
вещества, растворителя
и продуктов
их взаимодействия.
.