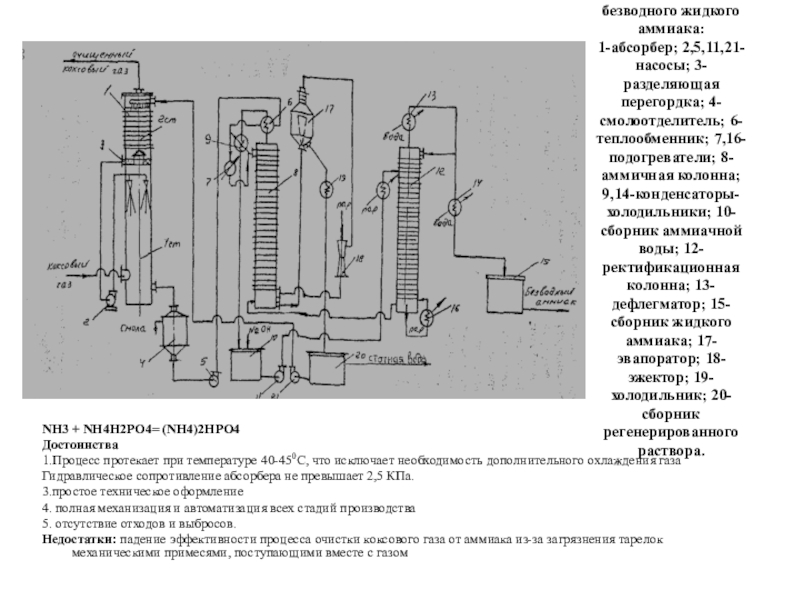
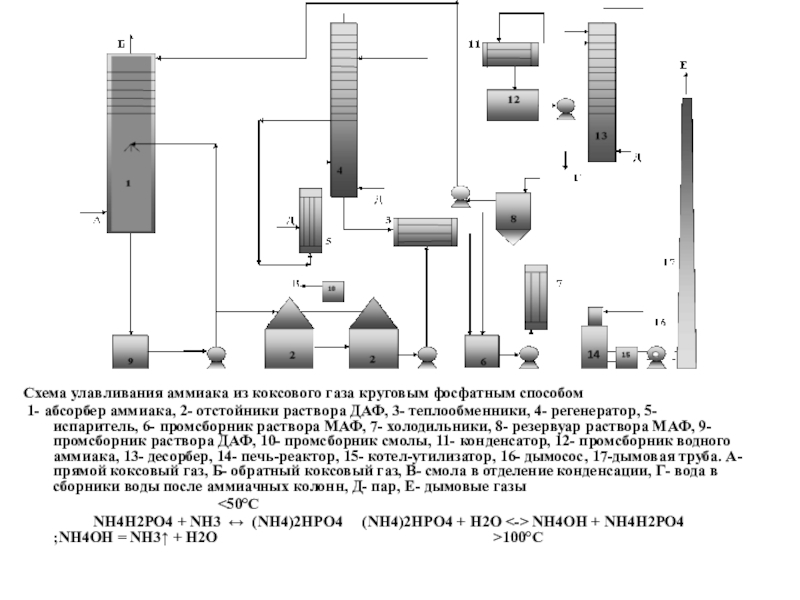
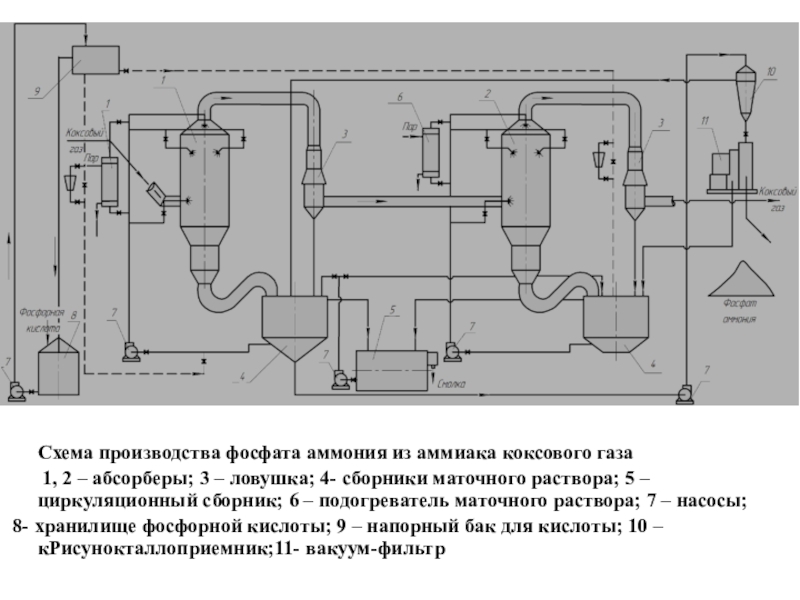
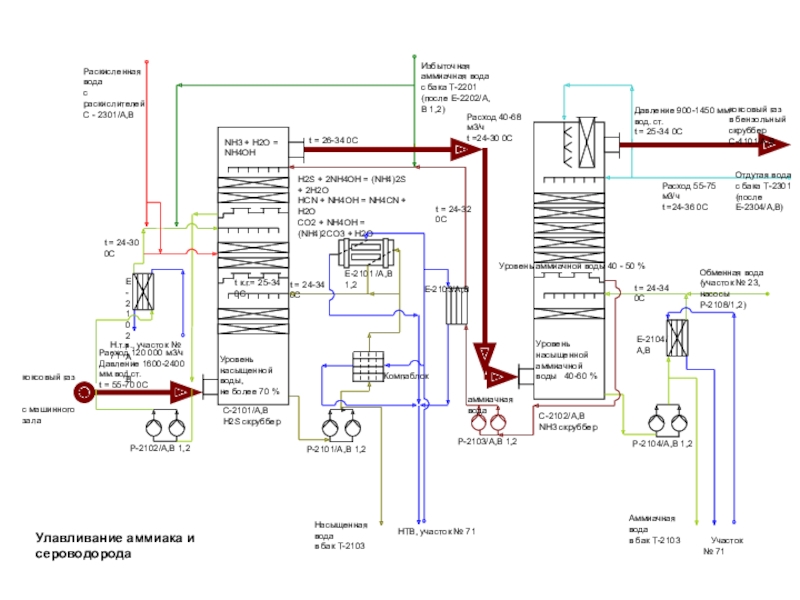
(NH4)2СО3 → 2 NH3 + СО2 + H2О,
(NH4)2S → 2NH3
+ H2S,NH4CN → NH3 + HCN
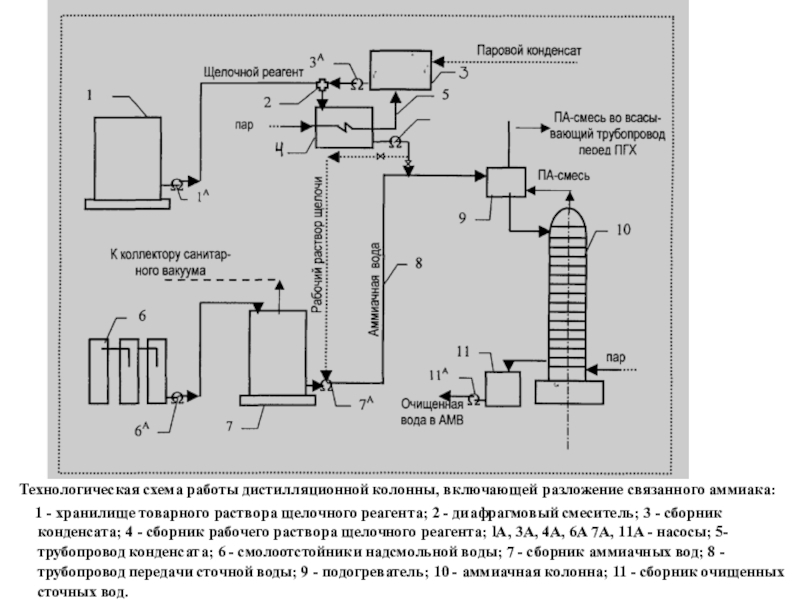
Реакции разложения основных аммонийных солей (связанного аммиака) сточных вод КХП каустической содой:
NH4CI + NaOH → NH3 + NaCI + Н2О
NH4CNS +NaOH → NНз + NaCNS + H20
(NH4)2S04 + 2NaOH → 2NНз + Na2S04+ 2Н20
Реакции разложения основных аммонийных солей (связанного аммиака) сточных вод КХП кальцинированной содой:
NH4CI +1/2Na2СОз → NНз + NaCI +1/2 H2COз
NH4CNS +l/2Na2COз → NНз + NaCNS +1/2 Н2СОз
(NH4)2S04 + Na2C03 → 2 NНз + Na2S04+ Н2СОз