Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Респираторные вирусы
Содержание
- 1. Респираторные вирусы
- 2. Классификация I. Orthomyxoviridae Inluenzavirus (Alphainfluenzavirus, Betainfluenzavirus, Gammainfluenzavirus,
- 3. Классификация II. Paramyxoviridae / ParamyxovirinaeРод Morbillivirus (7 видов)Measles morbillivirus [syn. Measles
- 4. КЛАССИФИКАЦИЯIII. Coronaviridae (HCoV, SARS-CoV, MERS-CoV, SARS-CoV-2 - COVID-19
- 5. Эпидемиология ОРВИ Источник инфекции Больной человекПути передачи инфекции: Воздушно-капельный Воздушно-пылевой Контактный (адено-, рино-, RS-вирусы)
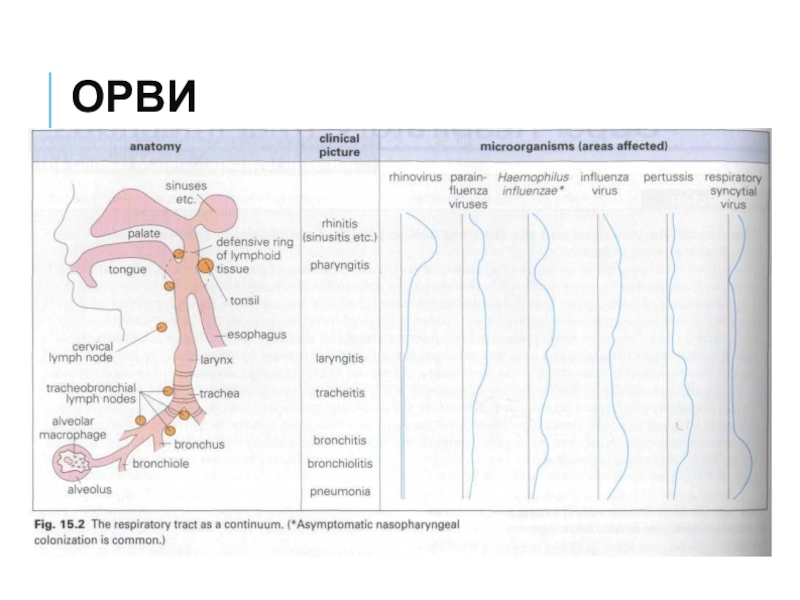
- 6. ОРВИ
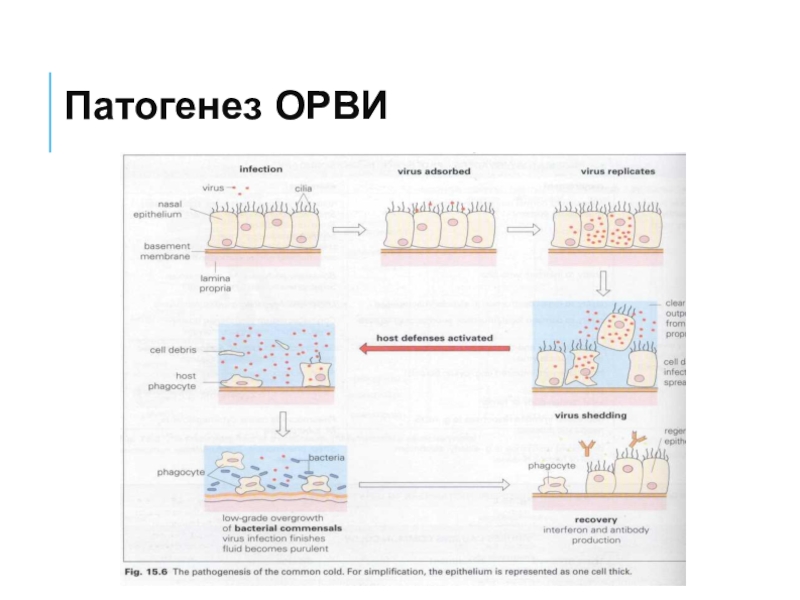
- 7. Патогенез ОРВИ
- 8. Вирус гриппаВирион (инфекционная частица) гриппа имеет форму сферы или
- 9. Внедрение в клетку, репликация и выход вируса
- 10. ПатогенезИнкубационный период развития гриппа составляет от 3 до
- 11. патогенез1. Вирусные частицы проникают к клеткам эпителия дыхательных путей,
- 12. Клинические признакираздражение верхних дыхательных путей: сильный кашель;заторможенность нервных
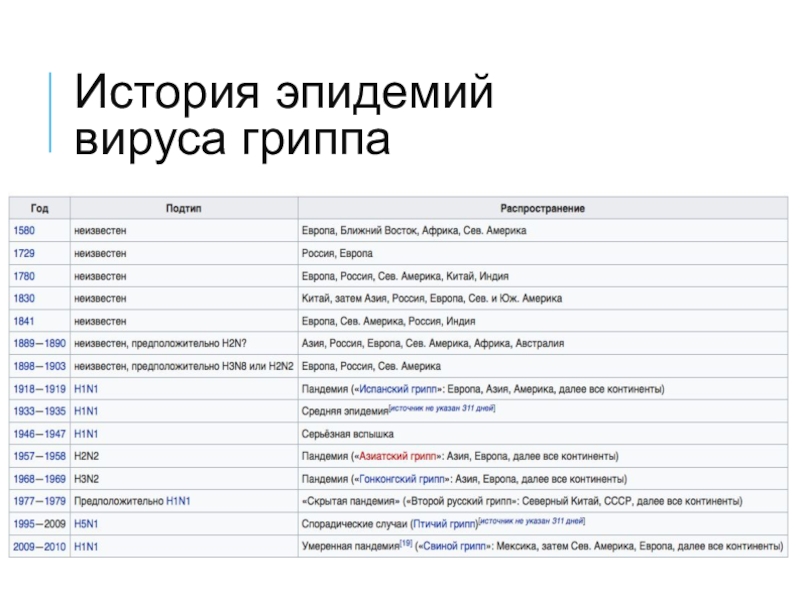
- 13. История эпидемий вируса гриппа
- 14. Вирус гриппа
- 15. Вирус гриппа
- 16. специфическая профилактика
- 17. ПарамиксовирусыПАРАГРИПППАРОТИТКОРЬРЕСПИРАТОРНО-СИНЦИТИАЛЬНЫЙ ВИРУС
- 18. ПарамиксовирусыВирионы имеют сферическую форму, диаметр 150—200 нм.Геном
- 19. Схема репродукции парамиксовирусовВирус связывается гликопротеинами оболочки с
- 20. Парамиксовирусы
- 21. Слайд 21
- 22. Вирус кориКорь (Measles morbillivirus) — острое инфекционное вирусное заболевание с очень
- 23. Вирус кориCферическая форма и диаметр 120—230 нм. Вирус
- 24. Вирус кори
- 25. патогенез кори1. Проникновение вируса в организм человека
- 26. Клиническая картина Инкубационный период 8—14 дней (редко до
- 27. Эпидемический паротит Вирионы полиморфны, округлые вирионы имеют диаметр
- 28. патогенез паротитаВходные ворота инфекции – верхние дыхательные
- 29. Слайд 29
- 30. Специфическая профилактикаВ соответствии с российским национальным календарём
- 31. КоронавирусыСемейство коронавирусов (лат. Coronaviridae)РНК - содержащие вирусы46 видов
- 32. КоронавирусыHCoV-229E — Alphacoronavirus, впервые выявлен в середине 1960-х годов;HCoV-NL63 — Alphacoronavirus,
- 33. COVID-19 (SARS-CoV-2)COVID-19 (аббревиатура от англ. COronaVIrus Disease 2019), ранее коронавирусная инфекция
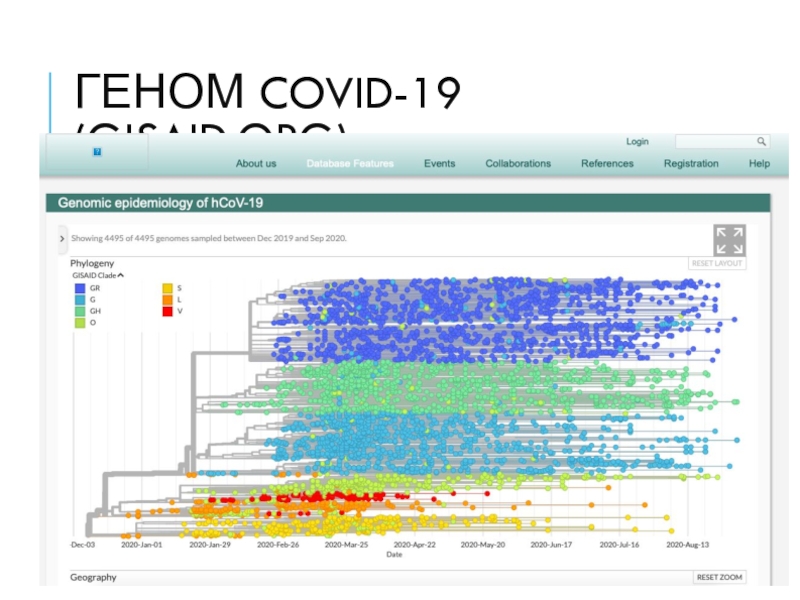
- 34. Геном COVID-19 (gisaid.org)
- 35. SARS-CoV-2Размер вириона порядка 50-200 нанометров. Белковое моделирование, осуществлённое на основе
- 36. SARS-CoV-2 Модель поперечного сечения большинства представителей группы
- 37. SARS-CoV-2SARS-CoV-2 является вирусом с оболочкой. Липидный бислой оболочки таких
- 38. Передача инфекции Вирус передаётся воздушно-капельным путём через
- 39. Клиническая картина Инфекция, вызывается вирусом SARS-CoV-2, инкубационный период составляет
- 40. Возможные осложнения COVID-19: острый респираторный дистресс-синдром, от
- 41. Лабораторная диагностика Диагностировать вирус возможно при помощи полимеразной
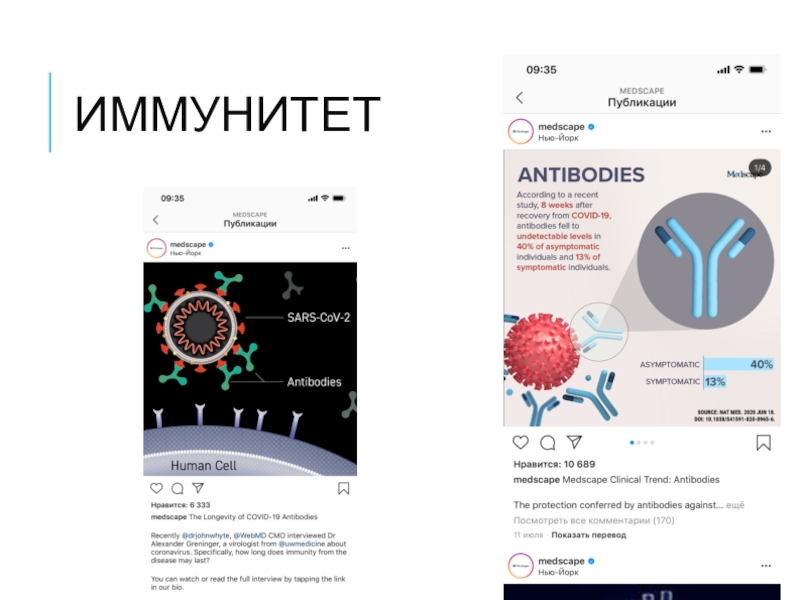
- 42. Иммунитет
- 43. ВакцинаВ работе принимают участие около 35 компаний и академических учрежденийШесть вакцин проходят клинические исследования на людях
- 44. Слайд 44
- 45. Слайд 45
- 46. Аденовирусная инфекция Вирус рода Mastadenovirus семейства AdenoviridaeДиаметр 70—90 нм, содержат единичную двухцепочечную молекулу ДНК, ассоциированную с двумя основными ядерными белками
- 47. ПатогенезВ организм инфекция попадает через слизистые оболочки
- 48. Клиническая картинаИнкубационный период от 1 дня до 2
- 49. Эта биопсия аллотрансплантата показывает характерные признаки аденовирусной
- 50. У больного А. 38 лет, внезапно поднялась
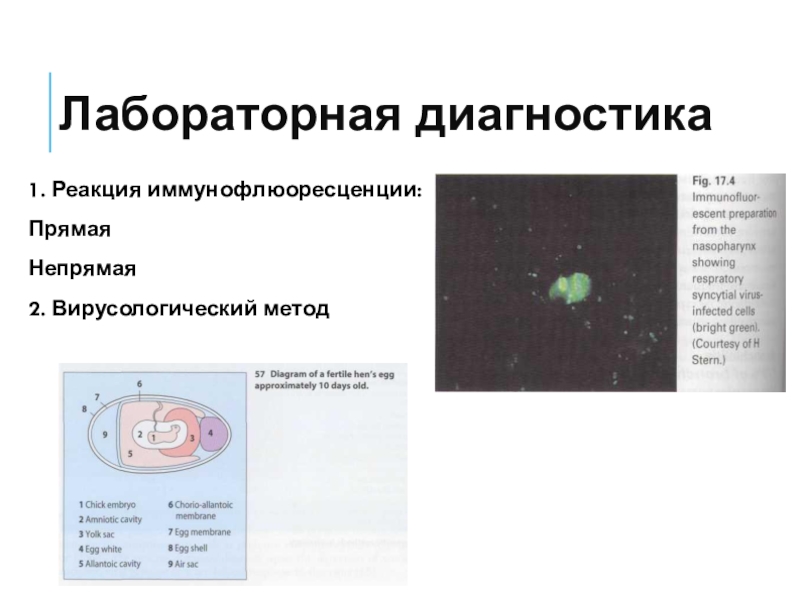
- 51. Лабораторная диагностика1. Реакция иммунофлюоресценции:Прямая Непрямая 2. Вирусологический метод
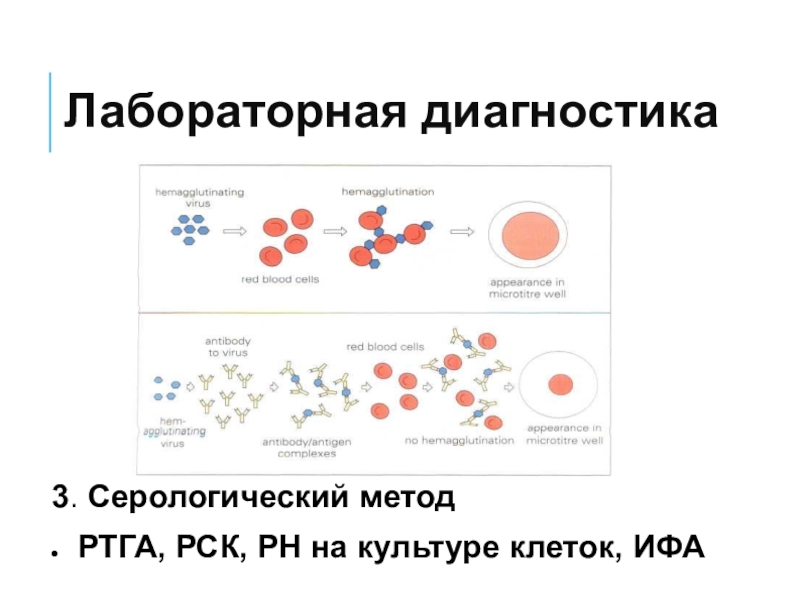
- 52. Лабораторная диагностика3. Серологический методРТГА, РСК, РН на культуре клеток, ИФА
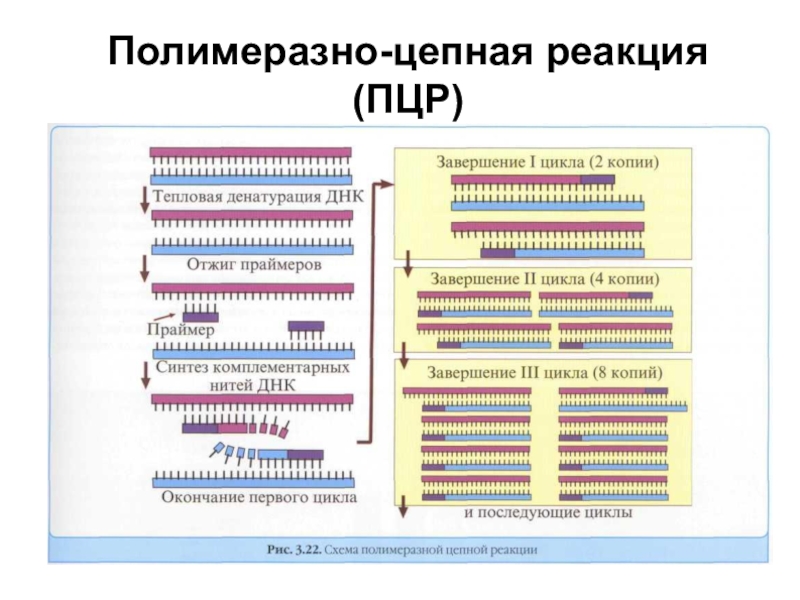
- 53. Стадии постановки ПЦРПодготовка пробы биологического материалаАмплификацияДетекция в агарозном геле
- 54. ПЦРГ.-Р.Бурместер, А.Пецутто/ Наглядная иммунология.М.2009
- 55. Полимеразно-цепная реакция (ПЦР)
- 56. благодарю за внимание!
- 57. Скачать презентанцию
Классификация I. Orthomyxoviridae Inluenzavirus (Alphainfluenzavirus, Betainfluenzavirus, Gammainfluenzavirus, Deltainfluenzavirus)В обозначение штаммов вирусов гриппа включают:1. тип;2. место выделения (географическое происхождение штамма);3. индекс, присвоенный в лаборатории (порядковый номер штамма);4. год выделения;5. индекс поверхностных белков,
Слайды и текст этой презентации
Слайд 1Респираторные вирусы
к.м.н. Давидович Наталия Валерьевна
доцент кафедры клинической биохимии,
микробиологии и
лабораторной диагностики
Слайд 2Классификация
I. Orthomyxoviridae
Inluenzavirus (Alphainfluenzavirus, Betainfluenzavirus, Gammainfluenzavirus, Deltainfluenzavirus)
В обозначение штаммов
вирусов гриппа включают:
1. тип;
2. место выделения (географическое происхождение штамма);
3. индекс,
присвоенный в лаборатории (порядковый номер штамма);4. год выделения;
5. индекс поверхностных белков, ставится последним и заключается в скобки, имеет смысл только для вируса типа «A»;
Примеры: «А (Бразилия) 11/78 (H1N1)» (вирус гриппа «A» человека с гемагглютинином H1, нейраминидазой N1, выделенный в Бразилии в 1978 г.), «A/Moscow/10/99 (H3N2)», «A/New Caledonia/120/99 (H1N1)», «B/Hong Kong/330/2001», «A/Fujian/411/2002 (H3N2)»
Слайд 3Классификация
II. Paramyxoviridae / Paramyxovirinae
Род Morbillivirus (7 видов)
Measles morbillivirus [syn. Measles virus] — Вирус кори
Род Respirovirus (5
видов)
Human respirovirus 1 [Human parainfluenza virus 1] — Вирус парагриппа человека 1
тип; Human respirovirus 3 [Human parainfluenza virus 3] — Вирус парагриппа человека 3 типаMurine respirovirus [Sendai virus] — Вирус Сендай
Род Rubulavirus (17 видов)
Human rubulavirus 2 [Human parainfluenza virus 2] — Вирус парагриппа человека 2 типа
Human rubulavirus 4 [Human parainfluenza virus 4] — Вирус парагриппа человека 4 типа
Mumps rubulavirus [Mumps virus] — Вирус эпидемического паротита
Слайд 4КЛАССИФИКАЦИЯ
III. Coronaviridae (HCoV, SARS-CoV, MERS-CoV, SARS-CoV-2 - COVID-19 )
IV.
Picornaviridae
Rhinovirus — 113
Parechovirus (1,2)
V. Reoviridae
Orthoreovirus -3
VI.
AdenoviridaeMastadenovirus — 42 (3,4,7,12,21)
VII.Parvoviridae (Bocavirus (HBoV -2005))
VIII. Mimiviridae (Mimivirus)
Слайд 5Эпидемиология ОРВИ
Источник инфекции
Больной человек
Пути передачи инфекции:
Воздушно-капельный
Воздушно-пылевой
Контактный (адено-, рино-, RS-вирусы)
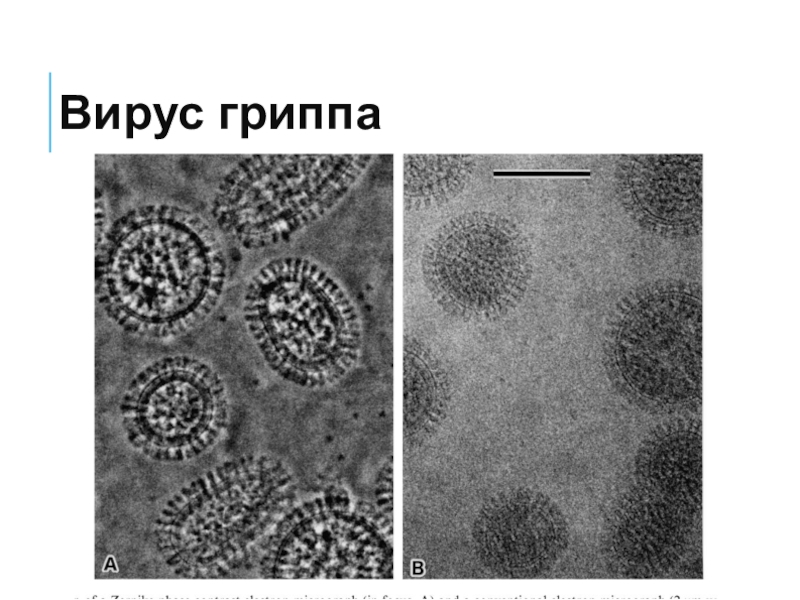
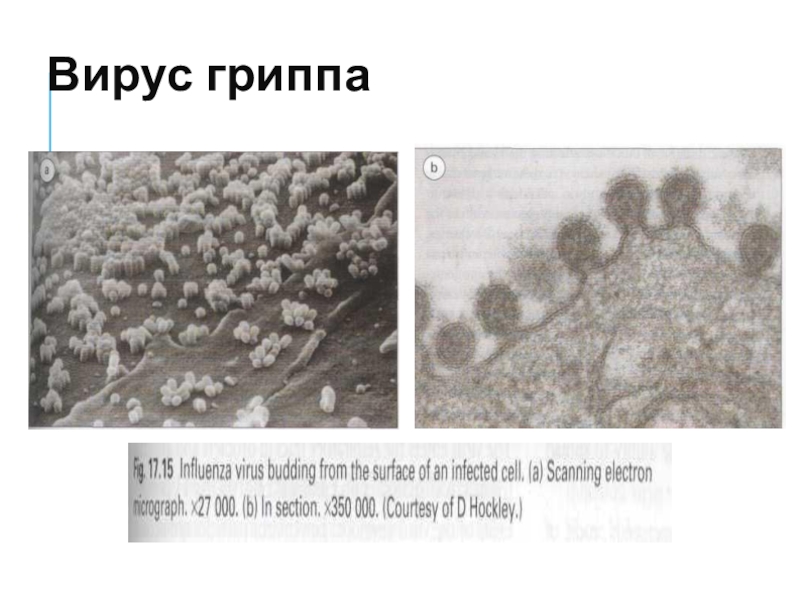
Слайд 8Вирус гриппа
Вирион (инфекционная частица) гриппа имеет форму сферы или приближающуюся к шарообразной,
его диаметр 100−120 нм.
Вирус гриппа представляет собой оболочечный вирус: внешний
слой — липидная мембрана, в которую вставлены «шипы»: гликопротеины и матриксный белок M2, формирующий ионные каналы. Под липидной мембраной расположен матричный (матриксный) белок M1, он формирует внутренний слой оболочки вируса, придает устойчивость и жесткость внешней липидной оболочке.Гликопротеины гемагглютинин и нейраминидаза — ключевые белки для размножения вируса типов «A» и «B». Гемагглютинин используется для проникновения в клетку, нейраминидаза — для выхода из неё.
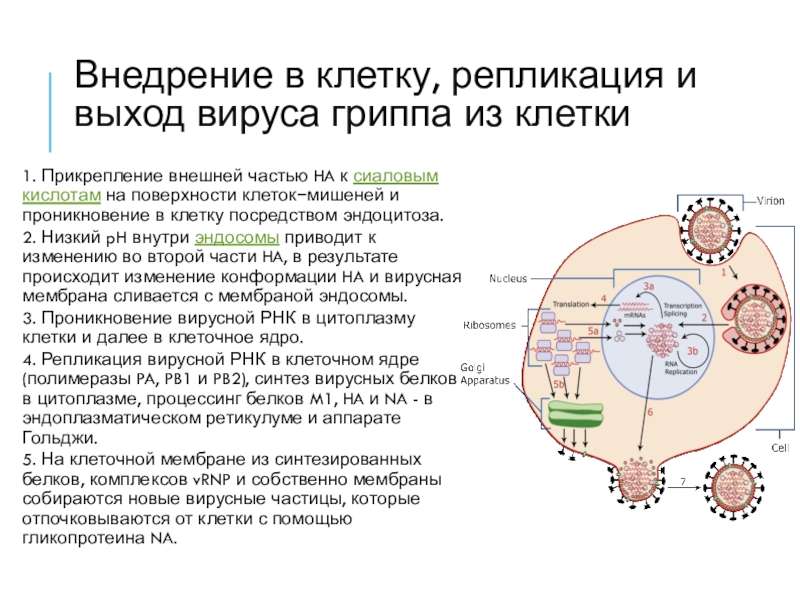
Слайд 9Внедрение в клетку, репликация и выход вируса гриппа из клетки
1.
Прикрепление внешней частью HA к сиаловым кислотам на поверхности клеток−мишеней и проникновение
в клетку посредством эндоцитоза.2. Низкий pH внутри эндосомы приводит к изменению во второй части HA, в результате происходит изменение конформации HA и вирусная мембрана сливается с мембраной эндосомы.
3. Проникновение вирусной РНК в цитоплазму клетки и далее в клеточное ядро.
4. Репликация вирусной РНК в клеточном ядре (полимеразы PA, PB1 и PB2), синтез вирусных белков в цитоплазме, процессинг белков M1, HA и NA - в эндоплазматическом ретикулуме и аппарате Гольджи.
5. На клеточной мембране из синтезированных белков, комплексов vRNP и собственно мембраны собираются новые вирусные частицы, которые отпочковываются от клетки с помощью гликопротеина NA.
Слайд 10Патогенез
Инкубационный период развития гриппа составляет от 3 до 24 часов с
момента заражения.
Вирус гриппа имеет сродство к эпителию трахеи и верхней части
бронхов, некоторые штаммы — к эпителию кишечника.Слайд 11патогенез
1. Вирусные частицы проникают к клеткам эпителия дыхательных путей, преимущественно цилиндрического эпителия трахеи и бронхов,
прикрепляются к ним и с помощью гемагглютинина «впрыскивают» фрагменты РНК и белки через клеточную мембрану внутрь клетки.
2.
РНК вируса синтезирует белки и РНК для новых вирусов, и белки собирают их в новые вирусные частицы.3. Вирусные частицы выходят из клетки с помощью нейраминидазы, либо, реже, вызывают апоптоз клетки.
4. Развивается иммунный ответ организма на клетки с остатками гемагглютинина на поверхности мембраны — высвобождается большое количество цитокинов.
5. В кровеносной системе нарастает повреждение эпителия и базальной мембраны, увеличение проницаемости капилляров.
6. В лёгких вирусный белок PB1-F2 уничтожает тканевые макрофаги, образуя брешь в защите лёгких от инфекций.
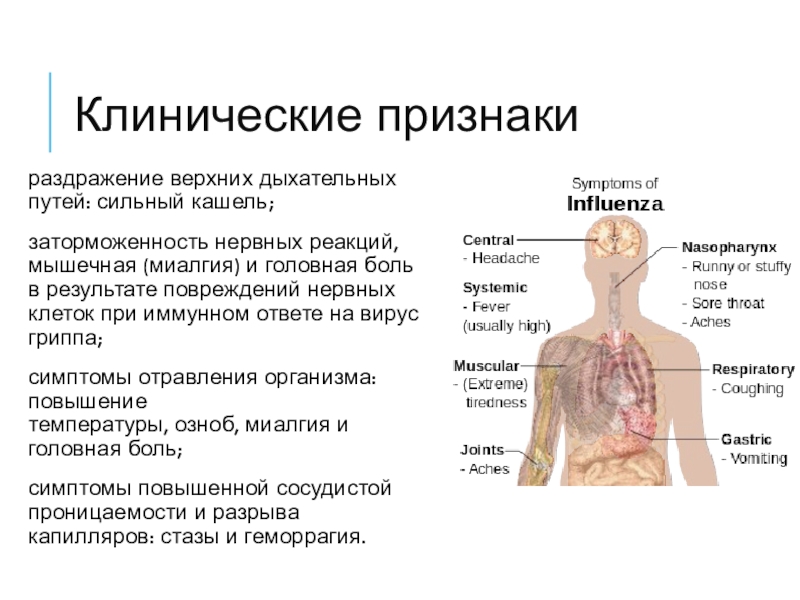
Слайд 12Клинические признаки
раздражение верхних дыхательных путей: сильный кашель;
заторможенность нервных реакций, мышечная (миалгия)
и головная боль в результате повреждений нервных клеток при иммунном
ответе на вирус гриппа;симптомы отравления организма: повышение температуры, озноб, миалгия и головная боль;
симптомы повышенной сосудистой проницаемости и разрыва капилляров: стазы и геморрагия.
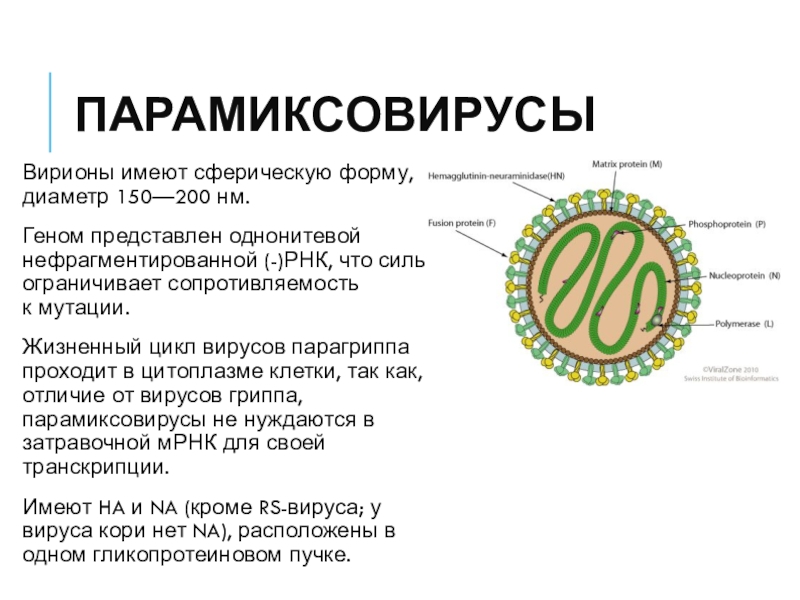
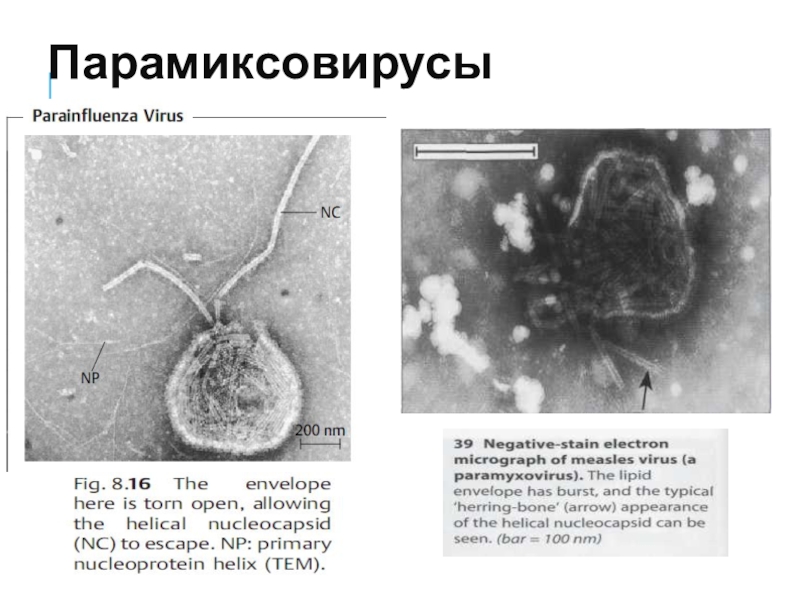
Слайд 18Парамиксовирусы
Вирионы имеют сферическую форму, диаметр 150—200 нм.
Геном представлен однонитевой нефрагментированной
(-)РНК, что сильно ограничивает сопротивляемость к мутации.
Жизненный цикл вирусов парагриппа
проходит в цитоплазме клетки, так как, в отличие от вирусов гриппа, парамиксовирусы не нуждаются в затравочной мРНК для своей транскрипции.Имеют HA и NA (кроме RS-вируса; у вируса кори нет NA), расположены в одном гликопротеиновом пучке.
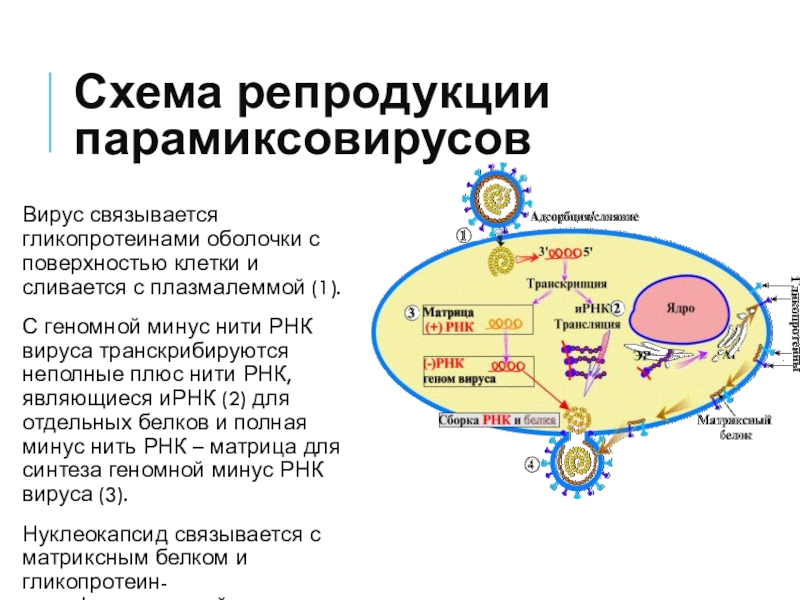
Слайд 19Схема репродукции
парамиксовирусов
Вирус связывается гликопротеинами оболочки с поверхностью клетки и сливается
с плазмалеммой (1).
С геномной минус нити РНК вируса транскрибируются
неполные плюс нити РНК, являющиеся иРНК (2) для отдельных белков и полная минус нить РНК – матрица для синтеза геномной минус РНК вируса (3). Нуклеокапсид связывается с матриксным белком и гликопротеин-модифицированной плазмалеммой. Выход вирионов – почкованием (4).
Слайд 22Вирус кори
Корь (Measles morbillivirus) — острое инфекционное вирусное заболевание с очень высоким уровнем контагиозности (90 %),
которое характеризуется высокой температурой (до 40,5 °C), воспалением слизистых оболочек полости рта и
верхних дыхательных путей, конъюнктивитом и характерной пятнисто-папулёзной сыпью кожных покровов, общей интоксикацией.По оценкам ВОЗ, в 2017 году в мире от кори погибло около 110 тысяч человек, 92 тысячи из них — дети в возрасте до пяти лет.
Корь остается одной из заметных причин детской смертности в развивающихся странах (1.3 % детской смертности на 2016 год).
В России заболеваемость корью в 2018 году составила 1,7 случаев на 100 000 человек - ?
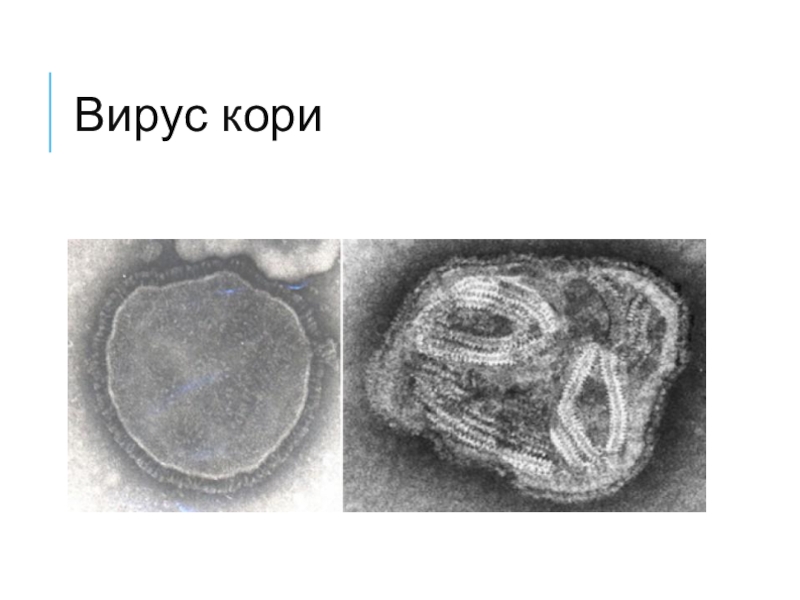
Слайд 23Вирус кори
Cферическая форма и диаметр 120—230 нм.
Вирус состоит из нуклеокапсида
— минус-нити РНК, трёх белков и внешней оболочки, образованной матричным
белком и двумя поверхностными гликопротеинами: один из них — гемагглютинин, другой — «фьюжен» белок.Слайд 25патогенез кори
1. Проникновение вируса в организм человека происходит через слизистую
оболочку верхних дыхательных путей и далее с током крови (первичная виремия) вирус
попадает в ретикулоэндотелиальную систему (лимфатические узлы) и поражает все виды белых кровяных клеток.2. С 3-го дня инкубационного периода в лимфоузлах, миндалинах, селезёнкеможно обнаружить типичные гигантские многоядерные клетки Warthin-Finkeldey с включениями в цитоплазме.
3. После размножения в лимфатических узлах вирус снова попадает в кровь, развивается повторная (вторичная) вирусемия, с которой связано начало клинических проявлений болезни.
4. Вирус кори подавляет деятельность иммунной системы (возможно непосредственное поражение Т-лимфоцитов), происходит снижение иммунитета и, как следствие, развитие тяжёлых вторичных, бактериальных осложнений с преимущественной локализацией процессов в органах дыхания.
Слайд 26Клиническая картина
Инкубационный период 8—14 дней (редко до 17 дней).
Острое начало — подъём
температуры до 38-40 °C, сухой кашель, насморк, светобоязнь, чихание, осиплость голоса, головная боль, отёк
век и покраснение конъюнктивы, гиперемия зева и коревая энантема — красные пятна на твёрдом и мягком нёбе.На 2-й день болезни на слизистой щёк в области моляров появляются мелкие белёсые пятнышки, окружённые узкой красной каймой: это так называемые пятна Бельского — Филатова — Коплика, представляющие собой патогномоничный симптом кори.
Коревая сыпь (экзантема) появляется на 4—5-й день болезни, сначала на лице, шее, за ушами, на следующий день на туловище и на 3-й день высыпания покрывают разгибательные поверхности рук и ног, включая пальцы. Сыпь состоит из мелких папул, окружённых пятном и склонных к слиянию (в этом её характерное отличие от краснухи, сыпь при которой не сливается).
Обратное развитие элементов сыпи начинается с 4-го дня высыпаний: температура нормализуется, сыпь темнеет, буреет, пигментируется, шелушится (в той же последовательности, что и высыпания).
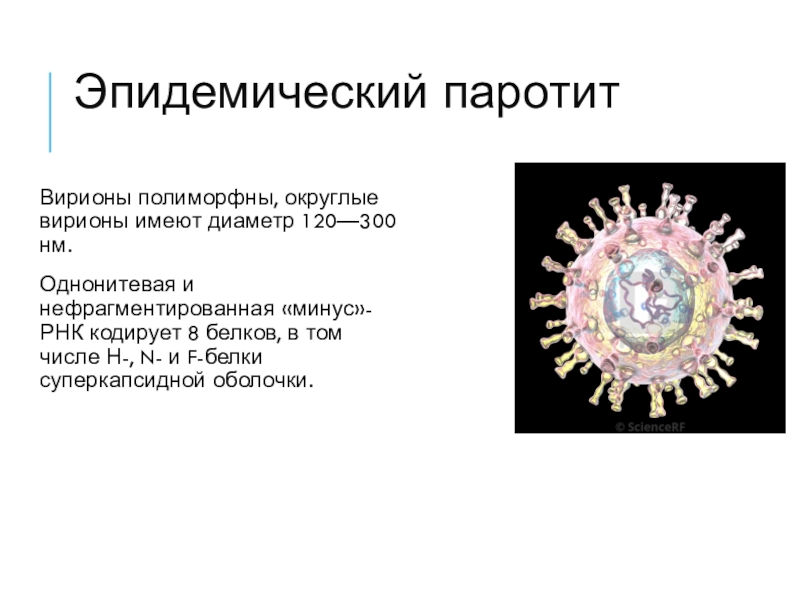
Слайд 27Эпидемический паротит
Вирионы полиморфны, округлые вирионы имеют диаметр 120—300 нм.
Однонитевая и
нефрагментированная «минус»-РНК кодирует 8 белков, в том числе Н-, N-
и F-белки суперкапсидной оболочки.Слайд 28патогенез паротита
Входные ворота инфекции – верхние дыхательные пути
Размножение вируса в
слизистых оболочках полости рта
Проникновение вируса по стенонову протоку в околоушную
железуПоступление в кровь и диссеминация по организму
Поражение внутренних органов: яичек, яичников, щитовидной и поджелудочной желез, почек и ГМ
Развитие осложнений: орхит, оофорит, менингит, менингоэнцефалит, тиреоидит ит.д.
Последствие перенесенного двустороннего орхита – половая стерильность (бесплодие)
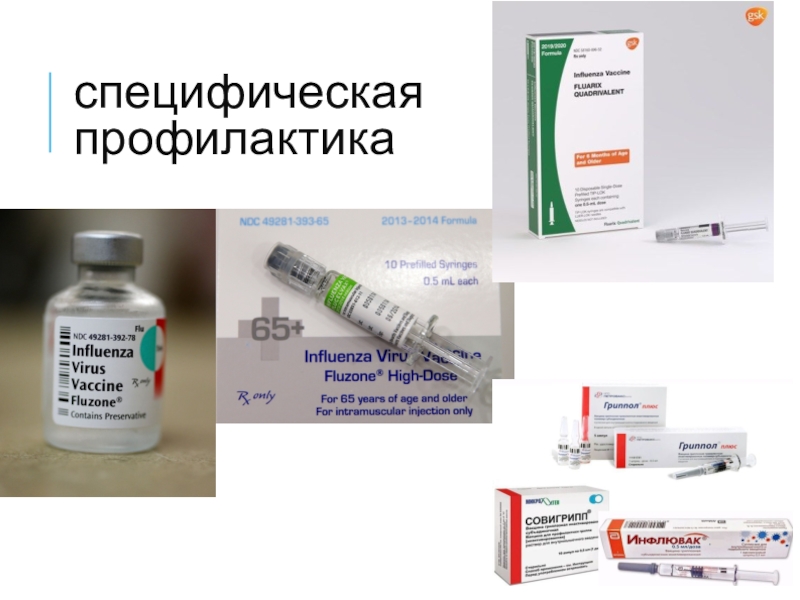
Слайд 30Специфическая профилактика
В соответствии с российским национальным календарём прививок, который утверждён
приказом Министерства здравоохранения РФ № 125н от 21 марта 2014 г., вакцинация против
кори проводится комбинированной живой вакциной от кори, краснухи и паротита одновременно в возрасте 12 месяцев, ревакцинация — в 6 лет.Слайд 32Коронавирусы
HCoV-229E — Alphacoronavirus, впервые выявлен в середине 1960-х годов;
HCoV-NL63 — Alphacoronavirus, возбудитель был выявлен
в Нидерландах в 2004 году;
HCoV-OC43 — Betacoronavirus A, возбудитель выявлен в 1967 году;
HCoV-HKU1 — Betacoronavirus A,
возбудитель обнаружен в Гонконге в 2005 году;SARS-CoV — Betacoronavirus B, возбудитель тяжёлого острого респираторного синдрома, первый случай заболевания которым был зарегистрирован в 2002 году;
MERS-CoV — Betacoronavirus C, возбудитель ближневосточного респираторного синдрома, вспышка которого произошла в 2015 году;
SARS-CoV-2 — Betacoronavirus B, выявленный во второй половине 2019, вызвавший пандемию пневмонии нового типа COVID-19
Слайд 33COVID-19 (SARS-CoV-2)
COVID-19 (аббревиатура от англ. COronaVIrus Disease 2019), ранее коронавирусная инфекция 2019-nCoV
SARS-CoV-2 (Severe acute respiratory
syndrome-related coronavirus 2)
SARS-CoV-2 был обнаружен в образцах жидкости, взятой из лёгких
в группе пациентов с пневмонией в китайском городе Ухань в декабре 2019 года. SARS-CoV-2 относится к подроду Sarbecovirus и является седьмым по счёту известным коронавирусом, способным заражать человека
Вирус является результатом рекомбинации
коронавируса летучих мышей с другим,
пока ещё не известным, коронавирусом
Предполагается, что человеку вирус передался
от панголина
Слайд 35SARS-CoV-2
Размер вириона порядка 50-200 нанометров.
Белковое моделирование, осуществлённое на основе расшифрованного генома вируса,
показало, что рецептор-связывающий S-белок вируса может иметь достаточно высокую аффинность к белку
человека ангиотензинпревращающий фермент 2 (АПФ2, англ. ACE2) и использовать его как точку входа в клеткуВ конце января 2020 года две группы в Китае и США независимо друг от друга экспериментально показали, что именно АПФ2 является рецептором для вируса SARS-CoV-2, так же как и для вируса SARS-CoV.
В марте 2020 в препринте статьи было выдвинуто предположение, что вирус для проникновения в клетки человека использует белок SP, с помощью которого взаимодействует с белком басигином (CD147) заражаемой клетки человека
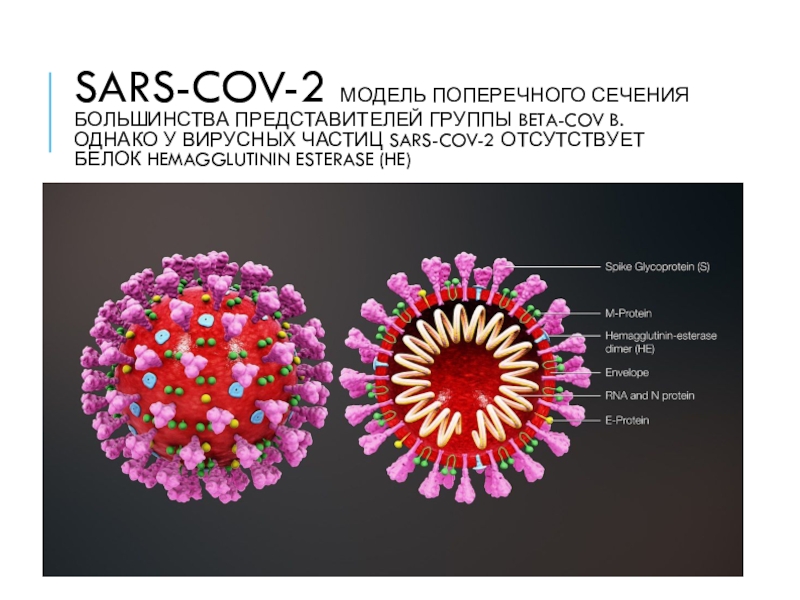
Слайд 36SARS-CoV-2 Модель поперечного сечения большинства представителей группы Beta-CoV B. Однако
у вирусных частиц SARS-CoV-2 отсутствует белок Hemagglutinin esterase (HE)
Слайд 37SARS-CoV-2
SARS-CoV-2 является вирусом с оболочкой. Липидный бислой оболочки таких вирусов довольно чувствителен
к высыханию, повышенной температуре и дезинфицирующим агентам, поэтому такие вирусы легче поддаются стерилизации,
чем непокрытые вирусы, хуже выживают вне хозяйской клетки и обычно передаются от хозяина к хозяину.Вирус держится на большинстве поверхностей около 72 часов и лучше сохраняет жизнеспособность на пластике и нержавеющей стали, чем, например, на меди и картоне; в воздухе возбудители заболевания держатся до трёх часов (что подтверждает воздушно-капельный путь заражения)
К настоящему времени не существует достаточно полных и достоверных оценок жизнестойкости и сохранения активности вируса вне организма, из-за большого количества влияющих факторов, относительно незначительного времени наблюдения и небольшого количества полученных данных.
Слайд 38Передача инфекции
Вирус передаётся воздушно-капельным путём через вдыхание мелких капель, распылённых
в воздухе при кашле, чихании или разговоре.
Капли с вирусом
могут попадать на поверхности и предметы, а затем инфицировать прикоснувшегося к ним человека через последующие прикосновения к глазам, носу или рту. Вирус может оставаться жизнеспособным в течение нескольких часов, попадая на поверхности предметов.
По данным Китайского центра по контролю и профилактике заболеваний жизнеспособный вирус был обнаружен в фекалиях больных COVID-19, что означает возможность фекально-оральной передачи инфекции, например, через контаминированные руки, пищу и воду, однако данный механизм передачи не является основным в случае COVID-19
Слайд 39Клиническая картина
Инфекция, вызывается вирусом SARS-CoV-2, инкубационный период составляет 1—14 дней, может протекать
бессимптомно, в лёгкой форме и в тяжёлой форме, с риском
смерти, но полная клиническая картина пока ещё не ясна. Симптомы развиваются в среднем на 5—6 день с момента заражения. Пациенты с лёгкими симптомами обычно выздоравливают в течение недели.Проявляется в трёх основных клинических формах:
острая респираторная вирусная инфекция лёгкого течения с наличием симптомов инфекции верхних дыхательных путей (в большинстве случаев);
пневмония без угрозы для жизни;
тяжёлая пневмония с острым респираторным дистресс-синдромом.
Слайд 40Возможные осложнения COVID-19:
острый респираторный дистресс-синдром, от 15 % до 33 %;
острая дыхательная
недостаточность, 8 %;
острая сердечная недостаточность, от 7 % до 20 %;
вторичная инфекция, от
6 % до 10 %;острая почечная недостаточность, от 14 % до 53 %;
септический шок, от 4 % до 8 %;
кардиомиопатии, у 33 % критических;
диссеминированное внутрисосудистое свёртывание, у 71 % погибших;
осложнения беременности, не исключаются.
Слайд 41Лабораторная диагностика
Диагностировать вирус возможно при помощи полимеразной цепной реакции с обратной
транскрипцией в реальном времени (материал - мокрота, но можно использовать
и слизь из верхних дыхательных путей)Серодиагностика - В отличие от ПЦР, тесты на антитела не определяют наличие активного вируса в организме, но определяют наличие иммунитета к нему, то есть наличие IgM- и IgG-антител в крови
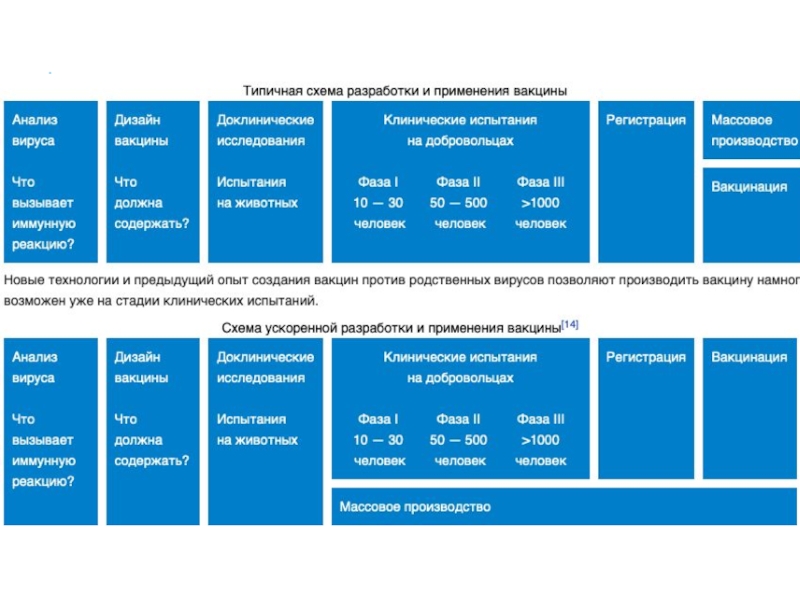
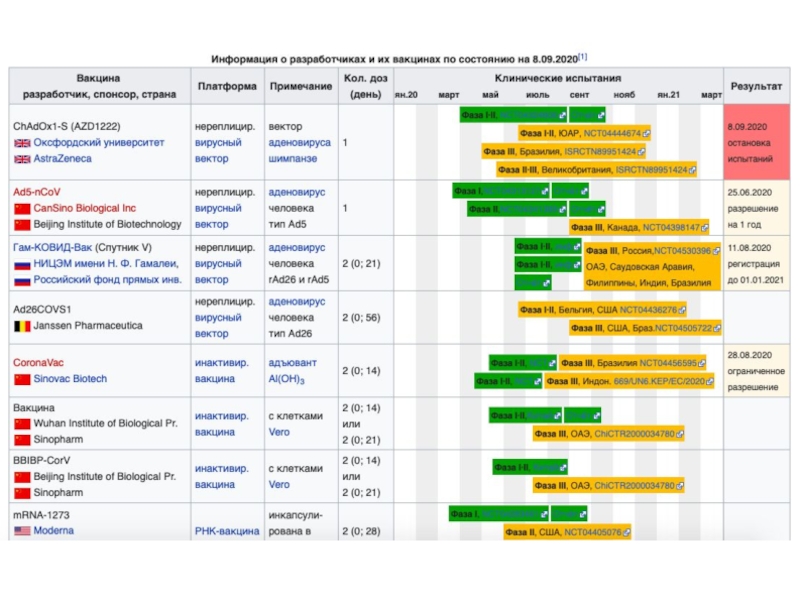
Слайд 43Вакцина
В работе принимают участие около 35 компаний и академических учреждений
Шесть
вакцин проходят клинические исследования на людях
Слайд 46Аденовирусная инфекция
Вирус рода Mastadenovirus семейства Adenoviridae
Диаметр 70—90 нм, содержат единичную двухцепочечную молекулу ДНК, ассоциированную с
двумя основными ядерными белками
Слайд 47Патогенез
В организм инфекция попадает через слизистые оболочки верхних дыхательных путей,
реже — кишечник либо конъюнктиву. Вирус попадает в эпителиальные клетки
и клетки лимфоидной ткани, поражает цитоплазму и ядро, где происходит репликация вирусной ДНК.Поражённые клетки прекращают деление и погибают.
Вирусы проникают в другие клетки слизистых оболочек и лимфатических узлов, а также в кровь.
Это сопровождается массивным экссудативным воспалением со стороны слизистых, т.е. накоплением в них жидкости.
Появляется конъюнктивит. Далее в патологический процесс вовлекаются внутренние органы (лёгкие, бронхи, кишечник, почки, печень, селезёнка), а также головной мозг, мезентериальные лимфоузлы.

![Респираторные вирусы Классификация II. Paramyxoviridae / ParamyxovirinaeРод Morbillivirus (7 видов)Measles morbillivirus [syn. Measles virus] — Вирус кориРод Respirovirus (5 видов)Human Классификация II. Paramyxoviridae / ParamyxovirinaeРод Morbillivirus (7 видов)Measles morbillivirus [syn. Measles virus] — Вирус кориРод Respirovirus (5 видов)Human respirovirus 1 [Human parainfluenza virus 1] — Вирус](/img/tmb/7/637922/308c422df3882e1c6379bb57dde446ab-800x.jpg)