Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Соединения алюминия
Содержание
- 1. Соединения алюминия
- 2. Соединения алюминияОксид алюминия (AL2O3)Гидроксид алюминияAL(OH)3
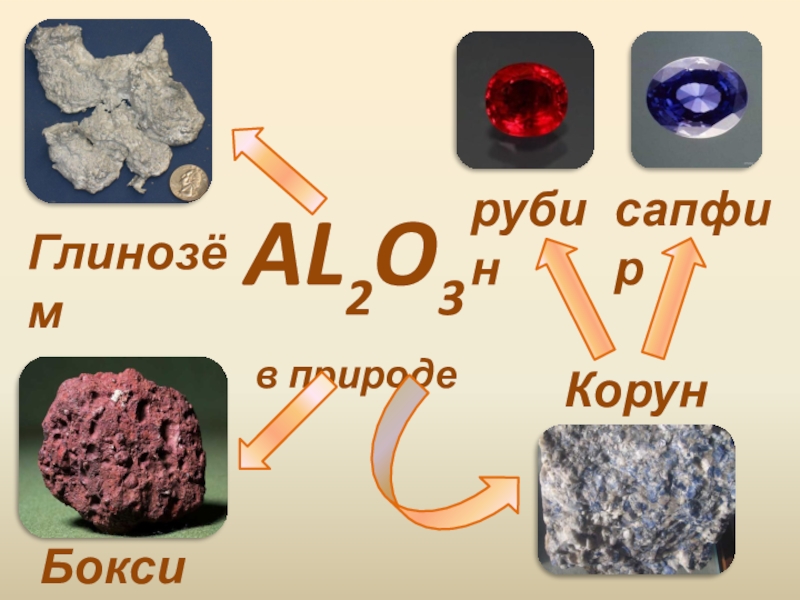
- 3. AL2O3 в природеГлинозёмКорундсапфиррубинБоксит
- 4. Применение сапфировзнаменитые сапфиры английской королевской семьи
- 5. Применение рубинов
- 6. Химические свойства оксида алюминияАмфотерный оксидРеагирует с кислотамиРеагирует с щелочамиAL2O3 + 6HCL=2ALCL3 + 3H2OAL2O3+ 2NaOH +3H2O=2Na[AL(OH)4]
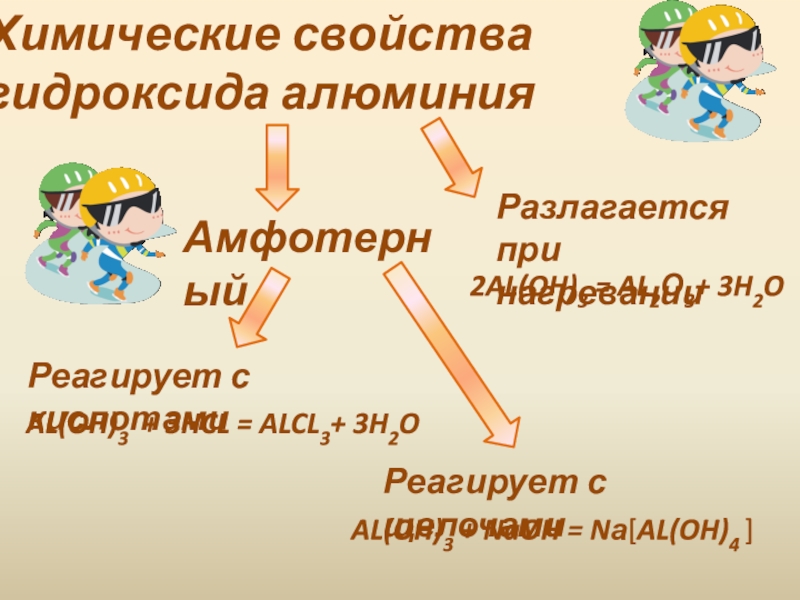
- 7. Химические свойства гидроксида алюминияАмфотерныйРеагирует с кислотамиРеагирует с
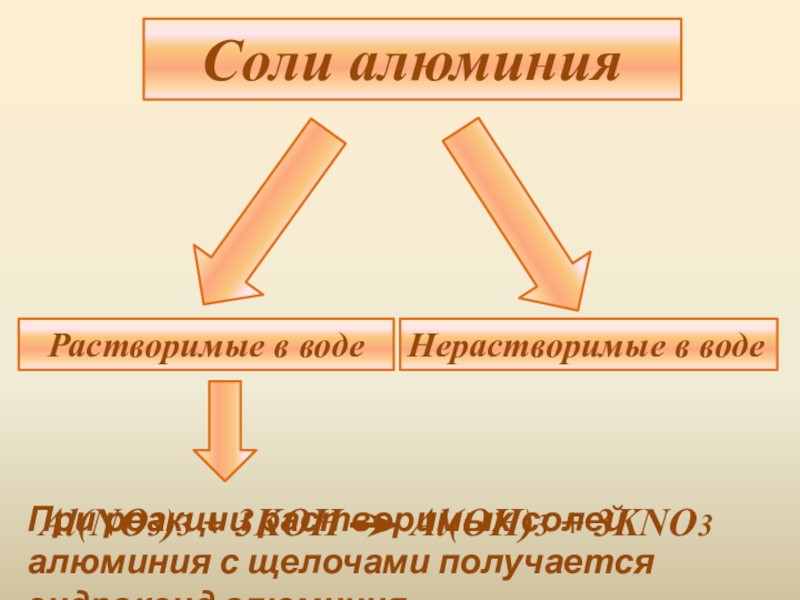
- 8. Соли алюминияРастворимые в водеНерастворимые в водеПри реакции
- 9. Скачать презентанцию
Соединения алюминияОксид алюминия (AL2O3)Гидроксид алюминияAL(OH)3




![Соединения алюминия Химические свойства оксида алюминияАмфотерный оксидРеагирует с кислотамиРеагирует с щелочамиAL2O3 + 6HCL=2ALCL3 + 3H2OAL2O3+ 2NaOH +3H2O=2Na[AL(OH)4] Химические свойства оксида алюминияАмфотерный оксидРеагирует с кислотамиРеагирует с щелочамиAL2O3 + 6HCL=2ALCL3 + 3H2OAL2O3+ 2NaOH +3H2O=2Na[AL(OH)4]](/img/tmb/6/596115/d23a87f1b60058019349c053a6a00d28-800x.jpg)