Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Современные подходы к лечению нейроэндокринных опухолей
Содержание
- 1. Современные подходы к лечению нейроэндокринных опухолей
- 2. Цели лечения Излечение Продление жизниУлучшение качества жизни
- 3. Слайд 3
- 4. Около в 2/3 случаев НЭО являются функционирующими
- 5. Основные прогностические признаки НЭОЛокализация опухоли Стадия, распространённость
- 6. Хирургическое лечение Лучевая терапия Лекарственное лечение Локальный
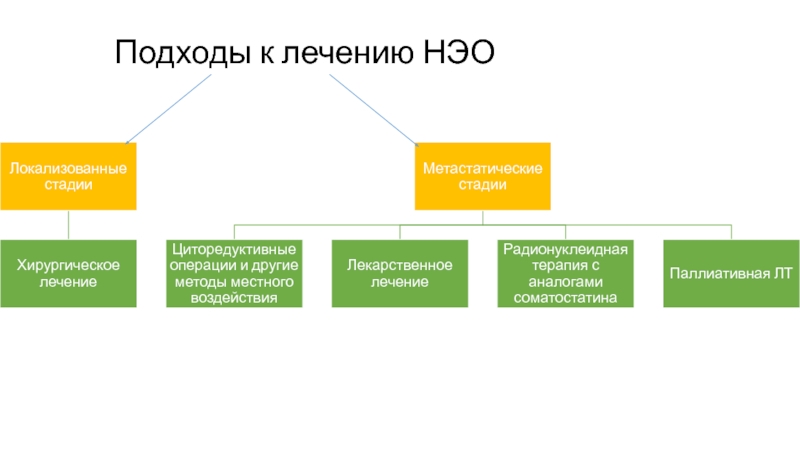
- 7. Подходы к лечению НЭО
- 8. Слайд 8
- 9. Радикальные операцииДля НЭО бронхолёгочной системы операции выбора
- 10. Циторедуктивные операцииПолное удаление опухоли и метастазов в
- 11. Другие методы местного воздействия Радиочастотная абляция (РЧА,
- 12. G3G1-2
- 13. Химиотерапия
- 14. Основные понятия и принципы Режим ХТ -
- 15. Химиотерапия Показания: G3 (низкодифференцированные опухоли)Схемы леченияНЭО бронхолёгочной
- 16. Слайд 16
- 17. Гормональная терапия - аналоги соматостатина Октреотид, Ланреотид,
- 18. Показания: G1-2 опухолиПри функционирующих опухолях для контроля
- 19. Таргетная терапияmTOR ингибиторы (эверолимус)СунитинибПазопаниб Ленватиниб Кабозантиниб
- 20. mTOR ингибиторы mTOR является центральным фактором, регулирующим
- 21. Показания для таргетной терапии: Эверолимус - G1-2
- 22. Неспецифическая иммунотерапия ИФНαНизкая эффективность, плохая переносимостьНо имеется
- 23. Иммунотерапия чекпоинт-ингибиторами PD-1Ниволумаб (Опдиво)Пембролизумаб (Кейтруда)PD-L1Атезолизумаб (Тецентрик)Дурвулумаб (Имфинзи) CTLA-4Ипилимумаб (Ервой)
- 24. Радионуклидная терапия с аналогами соматостатина Пептид-рецепторная (радиолигандная, радиотаргетная,
- 25. 177Lu-DOTATATE (Lutathera) состоит из Пептида – аналог
- 26. Показания к терапии177LU-DOTATATE Нерезектабельная местнораспространенная и/или
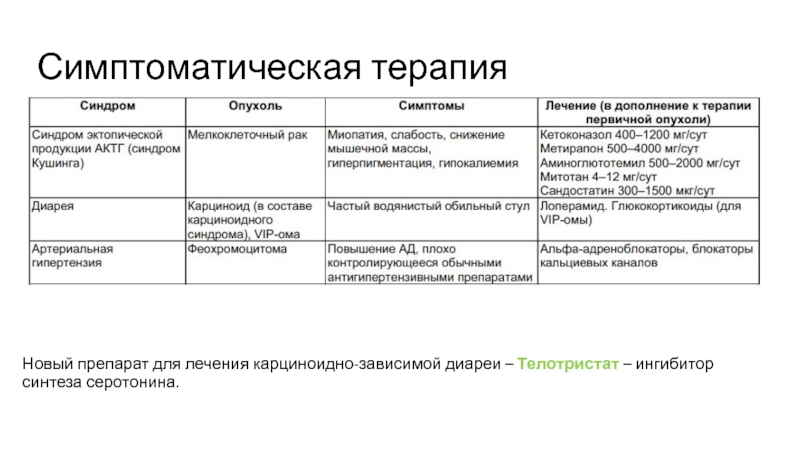
- 27. Симптоматическая терапия Новый препарат для лечения карциноидно-зависимой диареи – Телотристат – ингибитор синтеза серотонина.
- 28. Благодарю за внимание!
- 29. Скачать презентанцию
Цели лечения Излечение Продление жизниУлучшение качества жизни Цели лечения нейроэндокринных опухолей (НЭО): Излечение (на I и II стадии 5-я выживаемость 100%)Продление жизни (метастатическая стадия)Контроль симптомов -> улучшение качества жизни
Слайды и текст этой презентации
Слайд 1Современные подходы к лечению нейроэндокринных опухолей
САНКТ-ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
МЕДИЦИНСКИЙ ФАКУЛЬТЕТ
КАФЕДРА ОНКОЛОГИИ
Подготовила
студентка 5 курса
г.Слайд 2Цели лечения
Излечение
Продление жизни
Улучшение качества жизни
Цели лечения нейроэндокринных
опухолей (НЭО):
Излечение (на I и II стадии 5-я выживаемость
100%)Продление жизни (метастатическая стадия)
Контроль симптомов -> улучшение качества жизни
Слайд 4Около в 2/3 случаев НЭО являются функционирующими и приводят к
возникновению у пациента тягостного симптомокомплекса, обусловленного гиперпродукцией характерного активного гормона
или пептидаЧасто причиной смерти является не прогрессия опухоли, а осложнения, возникшие в результате гормональной гиперпродукции
Радикальное удаление первичной опухоли при НЭО является наиболее эффективным методом лечения
Однако в 65-70% случаев больные со злокачественными формами НЭО на момент первичного обращения уже имеют отдалённые метастазы (в печень и др. органы), что требует комплексного подхода для получения максимального клинического результата
Подбор лечения и прогноз зависят от стадии, дифференцировки и степени злокачественности, локализации опухоли, продукции гормонов, общего состояния больного
Особенности лечения
Слайд 5Основные прогностические признаки НЭО
Локализация опухоли
Стадия, распространённость процесса
Дифференцировка и
степень злокачественности (низкодифференцированные опухоли – G3, умереннодифференцированные – G2, высокодифференцированные
–G1)Функциональный статус опухоли
Общее состояние и возраст больного
Слайд 6Хирургическое лечение
Лучевая терапия
Лекарственное лечение
Локальный метод 1 +
локальный метод 2
Локальный метод + системный метод лечения
Слайд 9Радикальные операции
Для НЭО бронхолёгочной системы операции выбора – лобэктомия или
циркулярная резекция бронха
+ лимфодиссекция
2. Для НЭО тимуса –
радикальная хирургическая резекция3. Для НЭО ЖКТ:
Резекция тонкой кишки
Правосторонняя гемиколэктомия
+ лимфодиссекция мезентериальных и ретроперитонеальных ЛУ
Панкреатодуоденальная резекция, дистальная резекция ПЖ, энуклеация
опухоли с резекцией + лимфодиссекция
G3 опухоли ПЖ не оперируются
Слайд 10Циторедуктивные операции
Полное удаление опухоли и метастазов в печень дает возможность
добиться 80% 5-летней выживаемости
Особенно важно при наличии гормонактивной опухоли и
облегчения симптомов, вызванных выработкой БАВ Слайд 11Другие методы местного воздействия
Радиочастотная абляция (РЧА, Radiofrequence ablation, RFA)
Лазериндуцированная термотерапия (ЛИТТ, laserinduced thermotherapy, LITT)
Транскатетерная селективная эмболизация печёночных артерий
(transcatheter arterial embolization, TAE) Транскатетерная селективная химиоэмболизация печёночных артерий (transcatheter arterial chemoembolization, TACE)
Селективная внутренняя радиотерапия (selective internal radiotherapy, SIRT)
Слайд 14Основные понятия и принципы
Режим ХТ - адекватность дозы химиопрепарата
и способа его введения, соблюдение сроков введения противоопухолевого вещества, интервалов
между циклами, последовательности применения химиопрепаратов.Курс лечения состоит из циклов, во время которого пациент получает лечение, после цикла следует период «отдыха»
Линия - последовательности использования химиопрепаратов (I, II, III линия)
Виды:
Неоадъювантная ХТ (предоперационная) – проводится перед операцией с целью уменьшения объёма опухоли
Адъювантная ХТ (послеоперационная) – профилактическая, после радикальной операции с целью предотвращения рецидива
Паллиативная ХТ – для контроля симптомов и продления жизни
И др.
Принципы:
Использование ЛС с разным механизмами действия
Использование ЛС с разным механизмами резистентности
Использование ЛС с разным профилем токсичности
Слайд 15Химиотерапия
Показания: G3 (низкодифференцированные опухоли)
Схемы лечения
НЭО бронхолёгочной системы
Этопозид (ингибитор
топоизомеразы II)+ Цисплатин (алкилирующий агент)
Иринотекан (ингибитор топоизомеразы I) + Цисплатин
Паклитаксел (ингибитор клеточного веретена деления) + Карбоплатин (алкилирующий агент)
НЭО ЖКТ
Стрептозоцин (алкилирующий агент) + Доксорубицин (противоопухолевый антибиотик)
Стрептозоцин + 5-Фторурацил (антиметаболит)
Темозоломид (алкилирующий агент) + капецитабин (антиметаболит)
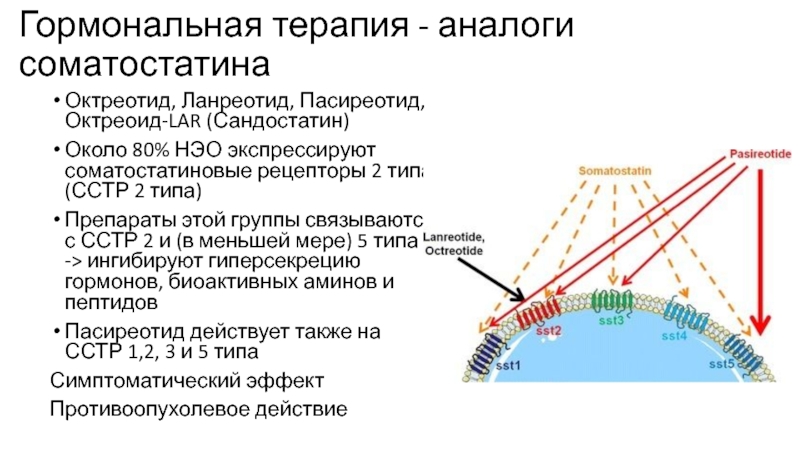
Слайд 17Гормональная терапия - аналоги соматостатина
Октреотид, Ланреотид, Пасиреотид, Октреоид-LAR (Сандостатин)
Около
80% НЭО экспрессируют соматостатиновые рецепторы 2 типа (ССТР 2 типа)
Препараты
этой группы связываются с ССТР 2 и (в меньшей мере) 5 типа -> ингибируют гиперсекрецию гормонов, биоактивных аминов и пептидовПасиреотид действует также на ССТР 1,2, 3 и 5 типа
Симптоматический эффект
Противоопухолевое действие
Слайд 18
Показания: G1-2 опухоли
При функционирующих опухолях для контроля карциноидного и других
синдромов
При нефункционирующих опухолях с антипролиферативной целью и профилактикой развития карциноидного
синдрома Применение аналогов соматостатина снижает риск возникновения карциноидной болезни сердца на 20%
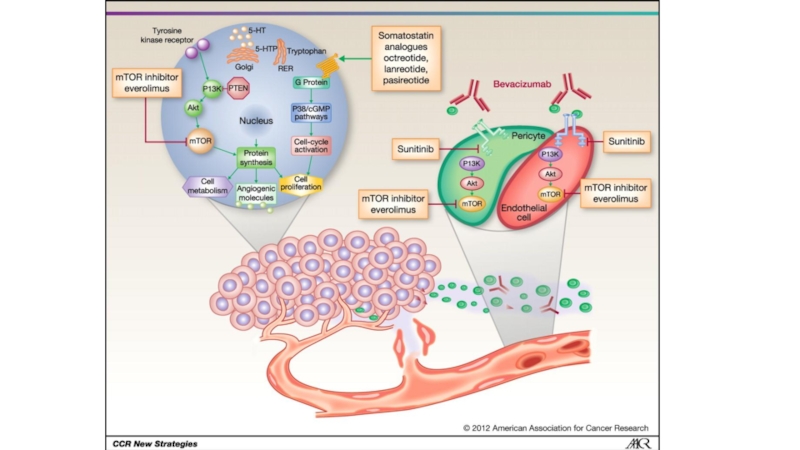
Слайд 20mTOR ингибиторы
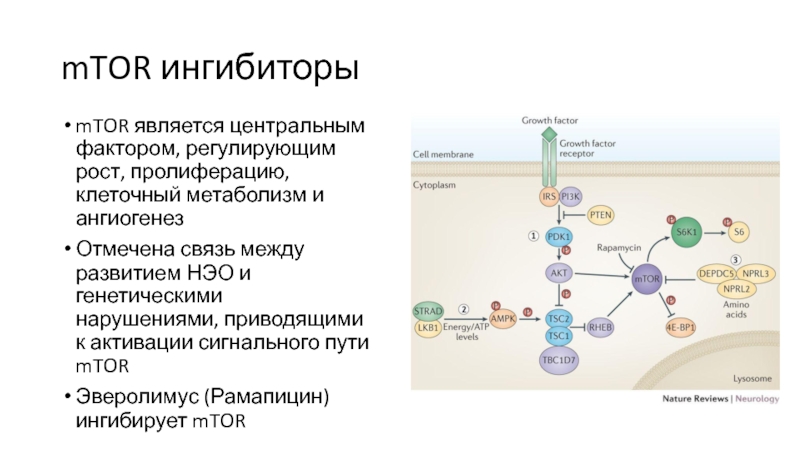
mTOR является центральным фактором, регулирующим рост, пролиферацию, клеточный
метаболизм и ангиогенез
Отмечена связь между развитием НЭО и генетическими
нарушениями, приводящими к активации сигнального пути mTORЭверолимус (Рамапицин) ингибирует mTOR
Слайд 21Показания для таргетной терапии:
Эверолимус
- G1-2 опухоли,
- в качестве
антипролиферативной терапии во II–III линии после лечения аналогами соматостатина у больных
с диссеминированным процессом,- в I линии — при отсутствии рецепторов к соматостатину
- Комбинированное применение аналогов соматостатина и эверолимуса
Сунитиниб
- G1-2 опухоли,
- зарегистрирован только для лечения НЭО ПЖ
- во II линии после лечения аналогами соматостатина
- в I линии лечения при отсутствии рецепторов к соматостатину
Слайд 22Неспецифическая иммунотерапия
ИФНα
Низкая эффективность, плохая переносимость
Но имеется биохимический и симптоматический
ответ
Показания: G1-3 опухоли
1) вторая линия терапии 2) в
сочетании с аналогами соматостатина, если последние не обеспечивают контроль симптомов 3) может использоваться в качестве терапии I линии при отсутствии экспрессии рецепторов соматостатинаСлайд 23Иммунотерапия чекпоинт-ингибиторами
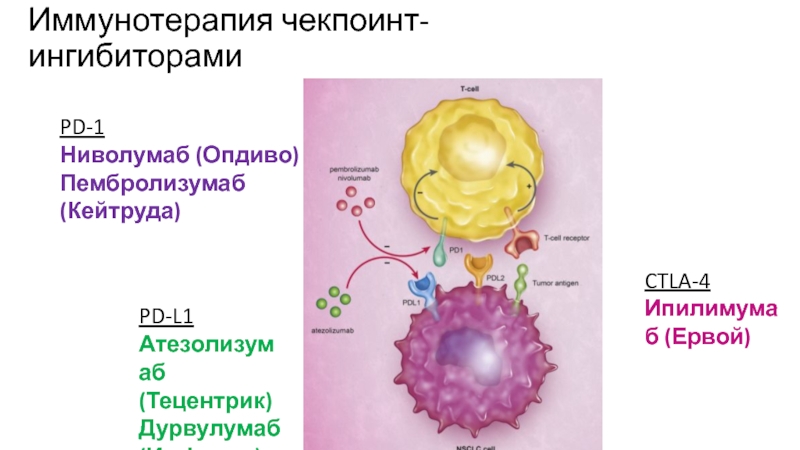
PD-1
Ниволумаб (Опдиво)
Пембролизумаб (Кейтруда)
PD-L1
Атезолизумаб (Тецентрик)
Дурвулумаб (Имфинзи)
CTLA-4
Ипилимумаб (Ервой)
Слайд 24Радионуклидная терапия с аналогами соматостатина
Пептид-рецепторная (радиолигандная, радиотаргетная, радиопептидная) радионуклидая терапия (ПРРТ, англ. PRRT)
– вариант таргетной лучевой терапии путем селективной доставки радиофармпрепарата (РФП)
в виде открытого источника излучения (бета, альфа-излучатель) к клеткам опухоли с целью цитотоксического радиационного противоопухолевого эффекта.FDA по результатам 3-й фазы международного рандомизированного клинического исследования NETTER-12 одобрил РФП 177Lu-DOTATATE (Lutathera) для ПРРТ НЭО ЖКТ, имеющих положительный соматостатин-рецепторный статус (STTR+).
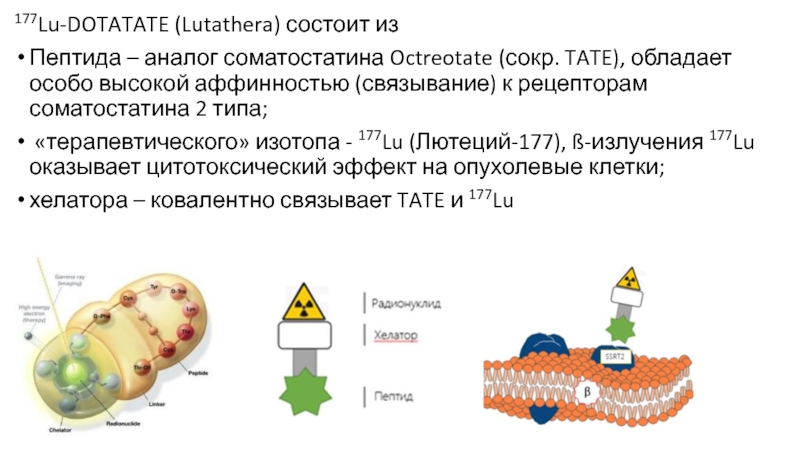
Слайд 25177Lu-DOTATATE (Lutathera) состоит из
Пептида – аналог соматостатина Octreotate (сокр.
TATE), обладает особо высокой аффинностью (связывание) к рецепторам соматостатина 2
типа;«терапевтического» изотопа - 177Lu (Лютеций-177), ß-излучения 177Lu оказывает цитотоксический эффект на опухолевые клетки;
хелатора – ковалентно связывает TATE и 177Lu
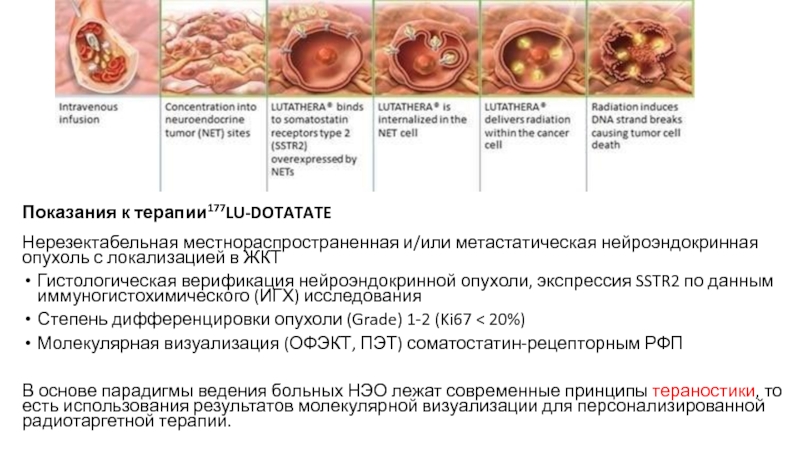
Слайд 26Показания к терапии177LU-DOTATATE Нерезектабельная местнораспространенная и/или метастатическая нейроэндокринная опухоль с локализацией
в ЖКТ
Гистологическая верификация нейроэндокринной опухоли, экспрессия SSTR2 по данным иммуногистохимического
(ИГХ) исследования Степень дифференцировки опухоли (Grade) 1-2 (Ki67 < 20%)
Молекулярная визуализация (ОФЭКТ, ПЭТ) соматостатин-рецепторным РФП
В основе парадигмы ведения больных НЭО лежат современные принципы тераностики, то есть использования результатов молекулярной визуализации для персонализированной радиотаргетной терапии.