Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Белки
Содержание
- 1. Белки
- 2. «Урок — это солнце, вокруг которого, как
- 3. Рождение урока начинается: с осознания и четкого
- 4. Задачи урока:Сформировать знания о составе и строении
- 5. Цели урока:Обучающая: познакомить учащихся со структурой и
- 6. План урокаВид урока: лекция с элементами беседы.Метод
- 7. Ход урокаОрганизационный момент.
- 8. Актуализация опорных знаний, умений и навыков.
- 9. Вопросы на повторение:Какие вещества называют аминокислотами? Какие
- 10. Формирование новых понятий на уроке
- 11. ЗакреплениеТестовый контроль учащихся по изученной темеДомашнее задание§
- 12. Конспект урока1. Строение белков и история их
- 13. Белки обладают рядом особенностей, прежде всего громадной
- 14. АминокислотыЗаменимыеНезаменимыеВалинИзолейцинЛейцинЛизинМетионинТреонинТриптофанФенилаланин
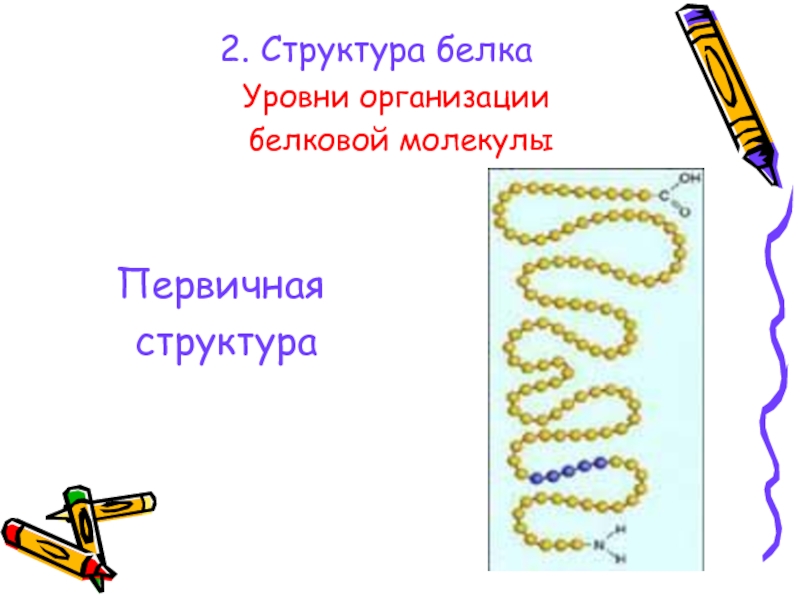
- 15. 2. Структура белкаУровни организации белковой молекулыПервичная структура
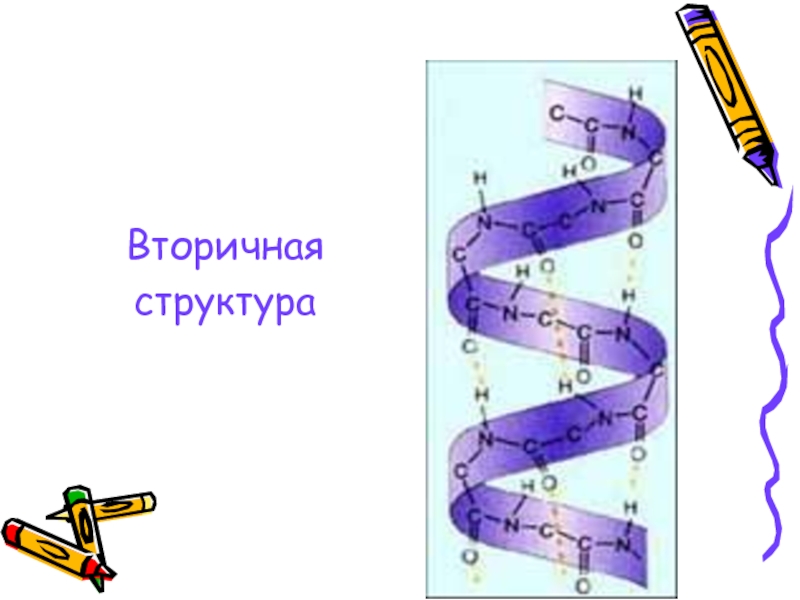
- 16. Вторичная структура
- 17. Третичная структура
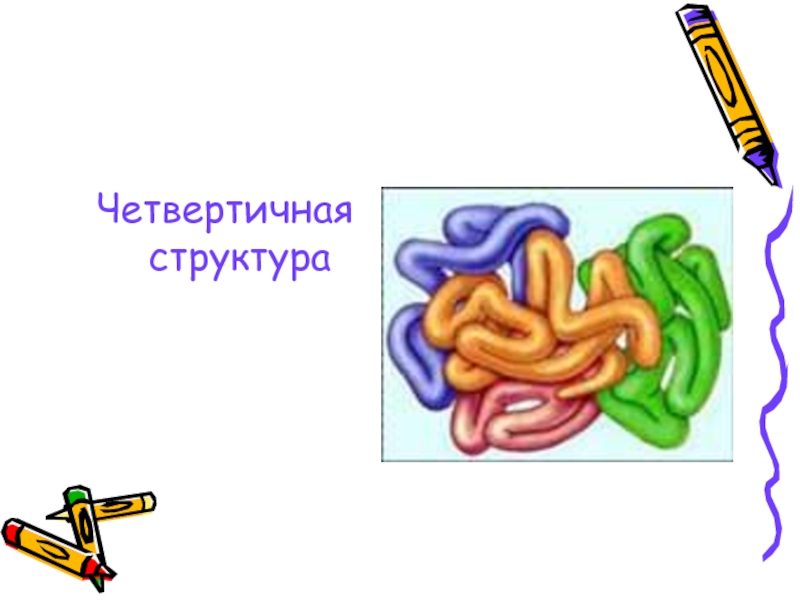
- 18. Четвертичная структура
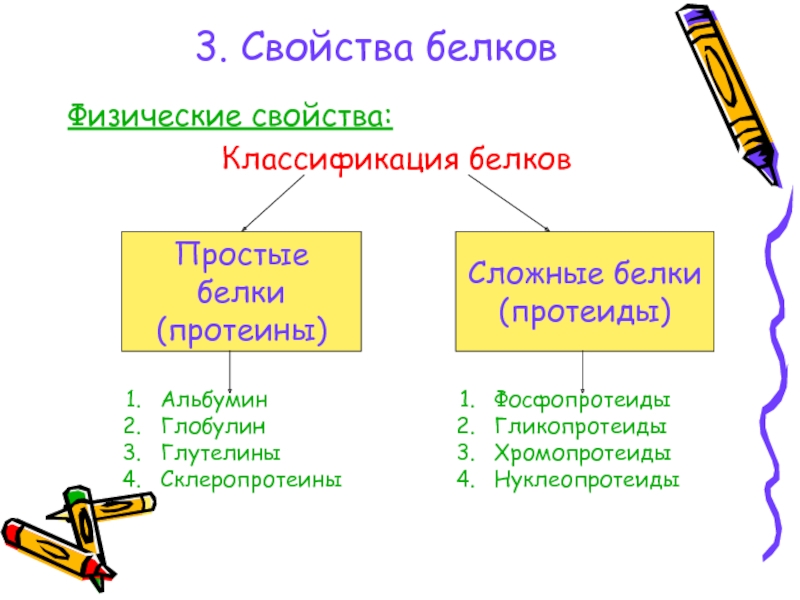
- 19. 3. Свойства белковФизические свойства:Классификация белковПростые белки(протеины)Сложные белки(протеиды)АльбуминГлобулинГлутелиныСклеропротеиныФосфопротеидыГликопротеидыХромопротеидыНуклеопротеиды
- 20. Химические свойства:Денатурация – процесс нарушения естественной структуры
- 21. 4. Биологические функции белковБелокэнергетическаязащитнаядвигательнаястроительнаякаталитическаясигнальнаярегуляторная
- 22. Список использованной литературыБаранова Т.А. Правильное питание. –
- 23. Скачать презентанцию
«Урок — это солнце, вокруг которого, как планеты, вращаются все формы учебных занятий» Н.М. Верзилин
Слайды и текст этой презентации
Слайд 2«Урок — это солнце, вокруг которого, как планеты, вращаются все
формы учебных занятий»
Н.М. Верзилин
Слайд 3Рождение урока начинается:
с осознания и четкого определения его конечной цели
— «Чего преподаватель хочет добиться?»
установления средства — «Что поможет преподавателю
в достижении цели?»определения способа — «Как преподаватель будет действовать, чтобы цель была достигнута?»
Слайд 4Задачи урока:
Сформировать знания о составе и строении белков как высшей
ступени развития вещества.
Сформировать знания о химических свойствах белков.
Научиться
подтверждать химические свойства белков экспериментально.Слайд 5Цели урока:
Обучающая:
познакомить учащихся со структурой и свойствами белков;
способствовать овладению
методами анализа аминокислотного состава белков с помощью цветных реакций.
Развивающая:
развитие умения
анализировать, сравнивать, делать выводы о свойствах белков.Воспитывающая:
формирование интереса у учащихся к данной теме;
развитие памяти, коммуникативных качеств.
Слайд 6План урока
Вид урока: лекция с элементами беседы.
Метод урока: объяснительно-стимулирующий.
Тип урока:
урок усвоения новых знаний на основе уже имеющихся.
Межпредметные связи: биология,
физиология питания.Материально-техническое обеспечение урока:
Диск CD «Структура белков».
Яичный белок, NaOH, CuSO4, HNO3, шерстяная нить, пробирки, держатель, спички, спиртовка.
Учебник химии 11 класс (Г.Е. Рудзитис, Ф.Г. Фельдман)
Слайд 9Вопросы на повторение:
Какие вещества называют аминокислотами? Какие функциональные группы содержатся
в их молекулах?
Почему молекулы аминокислот могут взаимодействовать между собой?
Какая существует
связь между белками и аминокислотами?Слайд 11Закрепление
Тестовый контроль учащихся по изученной теме
Домашнее задание
§ 1, стр. 18
– 24.
Как можно доказать наличие белков в пищевых продуктов?
Слайд 12Конспект урока
1. Строение белков и история их открытия
В состав белков
входят химические элементы C, H, O, N, S. Ферментные белки
часто содержат P (казеин молока), Fe (гемоглобин), Cu, Zn.Слайд 13Белки обладают рядом особенностей, прежде всего громадной молекулярной массой: альбумин
– 36 000, гемоглобин – 152 000, миозин (белок мышц) – 500 000.
Молекулы
белков – это молекулы-великаны, их называют макромолекулами. Белки или протеины - природные соединения, построенные из аминокислот, их всего в природе 20.
Слайд 14
Аминокислоты
Заменимые
Незаменимые
Валин
Изолейцин
Лейцин
Лизин
Метионин
Треонин
Триптофан
Фенилаланин
Слайд 193. Свойства белков
Физические свойства:
Классификация белков
Простые белки
(протеины)
Сложные белки
(протеиды)
Альбумин
Глобулин
Глутелины
Склеропротеины
Фосфопротеиды
Гликопротеиды
Хромопротеиды
Нуклеопротеиды
Слайд 20Химические свойства:
Денатурация – процесс нарушения естественной структуры белка (разрушение вторичной,
третичной, четвертичной структуры).
Гидролиз - разрушение первичной структуры в кислом или
щелочном растворе с образованием аминокислот.
Качественные реакции белков:
биуретовая;
ксантопротеиновая;
реакция определения серы в белках.
Слайд 214. Биологические
функции белков
Белок
энергетическая
защитная
двигательная
строительная
каталитическая
сигнальная
регуляторная
Слайд 22Список использованной литературы
Баранова Т.А. Правильное питание. – М.: Интербук, 1991.
– С. 78 – 80.
Беляев Д.К. Общая биология. – М.:
Просвещение, 2002. – С. 132 – 140.Габриелян О.С., И.Г. Остроумов. Органическая химия. – 2006. – С. 125 – 130.
Рудзитис Г.Е. Химия: Органич. химия.Учеб. для 11 кл. общеобразоват. учреждений. – М.: Просвещение, 2001. – С. 18 – 24.
Химия в школе. – 2006. - №7. – С. 69 – 73.
Хомченко Г.П. Химия для поступающих в вузы. – М.: Высшая школа, 1985. – С. 45 – 50.
Теги