Слайд 1Зымыран сұрақтар:
1)Азотты кім, қашан ашты
2)Азоттың табиғатта қандай күйде кездеседі?
3)Ауа құрамындағы азоттың мөлшері?
4)Азоттың физикалық қасиетін
сипаттаңдар.
5)Азот қышқылының тұздары қалай аталады?
6)Азот (ІІ) оксиді атмосферада қалай түзіледі?
7)Аммиактың судағы ерітіндісі қалай аталады?
8)Азот молекуласында неше байланыс бар?
9) Концентрациялы HNO3–пен әрекеттеспейтін металл
10) Азот қышқылының қолданылуы?
Слайд 2CAБАҚТЫҢ МАҚСАТЫ:
Фосфордың қасиеттері,оның аллотропиялық түр өзгерісі және қосылыстары мен қасиеттерімен
таныстыру;
Слайд 3
Сабақтың көрнекілігі:Слайд, интернет тақта, Д.И. Менделеев
периодтық жүйесі.
Сабақтың әдісі: Пән
аралық байланыс.
Сабақтың барысы:
I. Ұйымдастыру кезеңі.
II. Үйге тапсырма сұрау.
III. Жаңа сабақты түсіндіру.
IV.Бекіту.
V.Бағалау
VI.Үйге тапсырма беру
I.Ұйымдастыру кезеңі:
1. Good morning, children! 1. Доброе утра, дети!
2. What is the date today? 2. Какая сегодня дата?
3. Who is the absent today? 3. Кто сегодня отсутствует?
4. What was your home work? 4. Какова была ваша домашняя раб-а?
Слайд 4
Химиялық элементтердің периодтық жүйесінде фосфор III
периодта, V топтың негізгі топшасында орналасқан.
Химиялық таңбасы: Р
Реттік нөмірі:15
Салыстырмалы
атомдық массасы: 31
Электрондық формуласы: 1s22s22р63s23р3
Слайд 5Алынуы
Бос күйіндегі фосфорды алу үшін табиғи фосфатты электр пеште кремний
(IV) оксиді мен көмірді косып қыздырады. Бөлінген фосфордың буын су
астында ақ фосфор Р түрінде бөліп алады. Реакция теңдеуі:
Са3(РО4)2+ 3SiО2 + 5С = 3CaSiО3+ 5CО↑ + 2Р
Слайд 6Ендігі кезекте күнделікті қолданылып жүрген сіріңкенің қалай пайда болғанына тоқталсақ:
Ізденуші:
Сіріңкені 1831 жылы 19 жасар Шарл Сориа алғаш ойлап
тапқан. Бірақ ол сірңкеге патент ала алмаған, себебі ол қымбат болатын. 1832 жылы неміс мұғалмі Камерер сіріңкеге патент алып, оны өндіре бастад. Бірақ оның сіріңкесі ақ фосфордан жасалғандықтан өте қауіпті болды. Қауіпсіз сіріңкені1848 жылы швед химигі Бетгер алды. Бұл өзіміздің кәдімгі сіріңкеміз, ол қызыл фосфордан жасалады.
Слайд 7Шырпының басын қорапқа үйкегенде қызыл фосфор бертолле тұзынан от алып
тез тұтанады.
Қалыпты жағдайда қызыл фосфор тұрақты
6P + 5KCLO3
= 5KCL + 3P2O5
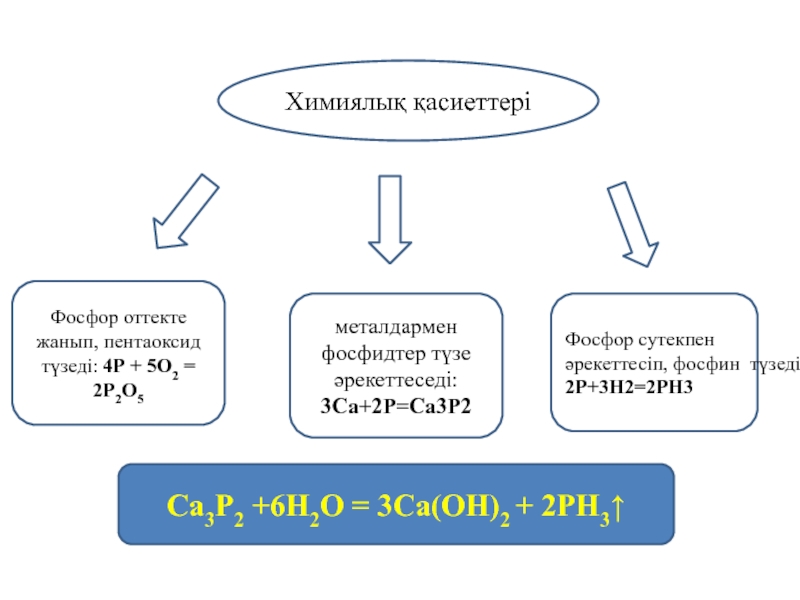
Слайд 8Химиялық қасиеттері
Фосфор оттекте жанып, пентаоксид түзеді: 4Р + 5O2 = 2Р2O5
металдармен
фосфидтер түзе әрекеттеседі: 3Са+2P=Са3P2
Фосфор сутекпен әрекеттесіп, фосфин түзеді: 2P+3H2=2PH3
Ca3P2 +6H2O
= 3Ca(OH)2 + 2PH3↑
Слайд 9Фосфор (V) оксиді P2O5- ақ түсті ұнтақ зат. Кәдімгі жағдайда
ылғал тарататын қасиетіне сәйкес оны газдар мен сұйықтарды ылғалдан құрғату
үшін қолданылады.
Слайд 10Физикалық қасиеттері:
Фосфор қышқылы- Ақ түсті кристалды,
улы емес зат. Суда жақсы ериді, орташа қышқыл қатарына жатады.
Слайд 11
Фосфор қышқылы суда ерігенде, сатылап диссоциацияланады:
Н3PO4↔ Н++ Н2PO4-
дигидрофосфат ион
Н2PO4- ↔ Н++ НPO42-
гидрофосфат ион
НPO42- ↔ Н++ PO43-
фосфат ион
Слайд 12 Ерітіндідегі фосфор қышқылы сілтімен сатылап әрекеттескенде, бір орта және
екі қышқыл тұз түзеді:
NaOH+H3PO4=NaH2PO4+H2O
натрий
дигидрофосфаты
2NaOH+H3PO4=Na2HPO4+2H2O
натрий
гидрофосфаты
3NaOH+H3PO4=Na3PO4+3H2O
натрий
фосфаты
Слайд 13 Фосфат ионға PO43- сапалық реакция:
Күміс нитратының 3-4 мл ерітіндісін Н3PO4, Na3PO4 тамызса, сары
түсті күміс (І) фосфаты тұнбаға түседі:
H3PO4+3AgNO3=3HNO3+Ag3PO4↓
PO43-+3Ag+=Ag3PO4↓
Слайд 14Фосфор
кездеседі
Сүт тағам-
дарында
Асбұр-
шақта
Ірімшікте
Балықта
Нанда
Слайд 16Химиялық диктант
1. Фосфорды ............жылы .................. ашты.
2. Фосфор қосылыстарда ............................ тотығу
дәрежелерін көрсетеді.
3. Фосфор ядросында ....... протон, .......нейтрон болады.
4. Фосордың металдармен
қосылысы ........................... деп аталады.
5. Фосфор элементі жай зат ретінде бірнеше аллотропия түзеді: ......................... , ........................... және ......................... .
6. Фосфордың жер қыртысындағы массалық үлесі ..........%
7. Фосфор ......................... .........................................
.....................................................................кездеседі.
8. Ауасыз ортада қыздырғанда ақ фосфор ......................... айналады, ал жоғарғы
қысымда .................... айналады.
Слайд 17Химиялық диктант
1. Фосфорды 1669 жылы Бранд ашты.
2. Фосфор қосылыстарда -3,
0, +3, +5 тотығу дәрежелерін көрсетеді.
3. Фосфор ядросында 15 протон,
16 нейтрон болады.
4. Фосордың металдармен қосылысы фосфидтер деп аталады.
5. Фосфор элементі жай зат ретінде бірнеше аллотропия түзеді: ақ фосфор, қызыл фосфор және қара фосфор.
6. Фосфордың жер қыртысындағы массалық үлесі 0,12%
7. Фосфор нанда, сүт тағамдарында, ірімшікте, балықта, асбұршақта кездеседі.
8. Ауасыз ортада қыздырғанда ақ фосфор қызыл фосфорға айналады, ал жоғарғы
қысымда қара фосфорға айналады.
Слайд 18Есептей білсең- есебің түгенделеді
№ 1. Сіріңке шаққанда 1,86 г
фосфор қанша бертолле
тұзымен әрекеттеседі?
№ 2. 19,6 гфосфор қышқылын алу үшін неше грамм фосфор
(V) оксидін суда еріту қажет?
№ 3. 62 т кальций ортафосфатынан қанша фосфор қышқылы
алынады?
№ 4. Массасы 34,5 г бертолле тұзы фосфордың қанша зат мөлшерімен әрекеттесе алады?
Слайд 19Үйге тапсырма
§19. Фосфор
№10. 114-бет
№ 20. 115 - бет