Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Галлий
Содержание
- 1. Галлий
- 2. Галлий – это химический
- 3. Существование галлия («экаалюминия») и основные
- 4. Среднее содержание галлия в
- 5. Единственным производителем металлического
- 6. Получение галлия. Основной источник получения галлия
- 7. При содово-известковом способе переработки бокситовой или нефелиновой
- 8. Широкого промышленного применения галлий
- 9. Скачать презентанцию
Галлий – это химический элемент с атомным номером 31. Относится к группе легких металлов и обозначается символом “Ga”. Галлий в чистом виде не встречается в природе, однако его
Слайды и текст этой презентации
Слайд 3 Существование галлия («экаалюминия») и основные его свойства были
предсказаны в 1870 Д. И. Менделеевым. Элемент был открыт спектральным
анализом в пиренейской цинковой обманке и выделен в 1875 французским химиком П. Э. Лекоком де Буабодраном; назван в честь Франции (лат. gallia). Точное совпадение свойств галлия с предсказанными было первым триумфом периодической системы.Поль Эмиль Лекок де Буабодран
Слайд 4 Среднее содержание галлия в земной коре относительно
высокое, 1,5-10 -30 % по массе, что равно содержанию свинца
и молибдена. Галлий — типичный рассеянный элемент. Единственный минерал галлия — галлит CuGaS2 очень редок. Геохимия галлия тесно связана с геохимией алюминия , что обусловлено сходством их физико-химических свойств. Основная часть галлия в литосфере заключена в минералах алюминия. Содержание галлия в бокситах и нефелинах колеблется от 0,002 до 0,01%. Повышенные концентрации галлия наблюдаются также в сфалеритах (0,01—0,02% ), в каменных углях (вместе с германием), а также в некоторых железных рудах.Слайд 5 Единственным производителем металлического галлия в Казахстане
является АО "Алюминий Казахстана". Предприятие имеет мощность по его выпуску
25 т в год и является по этому показателю лидером в СНГ. Согласно отчету АО "Алюминий Казахстана", в структуре производства (2003 г.) доля галлия составила 1,2% (369 млн. тенге), в 2001 г. - 3,2% (922 млн. тенге). По данным предприятия, выпуск галлия в 2004 и 2005 гг. составил соответственно 8,2 и 6,2 т. Предприятие выпускает чистый галлий (99,9999% - 6N), весь объем производства поставляется на экспорт (в основном в Японию).09.03.04 - Единственный производитель глинозема в Центральной Азии - ОАО Алюминий Казахстана - прекратил производство первичного металлического галлия из-за резкого снижения цен на мировом рынке, сообщила пресс-служба Евразийской промышленной ассоциации.
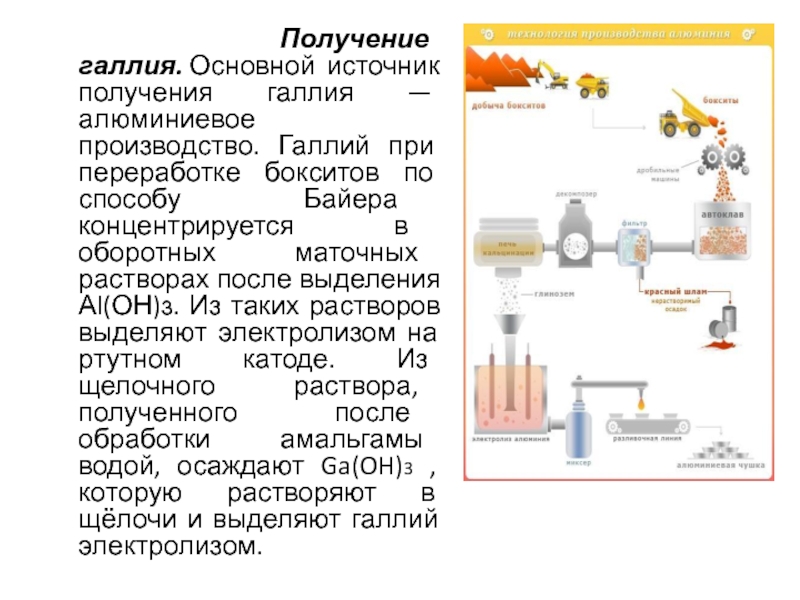
Слайд 6 Получение галлия. Основной источник получения галлия — алюминиевое производство.
Галлий при переработке бокситов по способу Байера концентрируется в оборотных
маточных растворах после выделения Аl(ОН)з. Из таких растворов выделяют электролизом на ртутном катоде. Из щелочного раствора, полученного после обработки амальгамы водой, осаждают Ga(OH)3 , которую растворяют в щёлочи и выделяют галлий электролизом.Слайд 7При содово-известковом способе переработки бокситовой или нефелиновой руды галлия концентрируется
в последних фракциях осадков, выделяемых в процессе карбонизации. Для дополнительного
обогащения осадок гидроокисей обрабатывают известковым молоком. При этом большая часть Al остаётся в осадке, а галлий переходит в раствор, из которого пропусканием CO2 выделяют галлиевый концентрат (6—8% Ga2O3); последний растворяют в щёлочи и выделяют галлий электролитически.Источником галлия может служить также остаточный анодный сплав процесса рафинирования Al по методу трёхслойного электролиза. В производстве цинка источниками галлия являются возгоны(вельц-окислы), образующиеся при переработке хвостов выщелачивания цинковых огарков.
Полученный электролизом щелочного раствора жидкий галлий, промытый водой и кислотами (HCl, HNOз), содержит 99,9—99,95% Ga. Более чистый металл получают плавкой в вакууме, зонной плавкой или вытягиванием монокристалла из расплава.