Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Галогены
Содержание
- 1. Галогены
- 2. Сафиканов А.Ф.1. История открытия галогенов2. Положение в Периодической системе3. Химические свойства4. Применение5.Проверка знанийГлавнаяГалогены6.Домашнее задание. Итоги урока.*
- 3. ФторИстория открытия галогеновСафиканов А.Ф.ХлорБромЙодАстат*
- 4. Слайд 4
- 5. В 1774
- 6. В 1825
- 7. В 1811
- 8. В
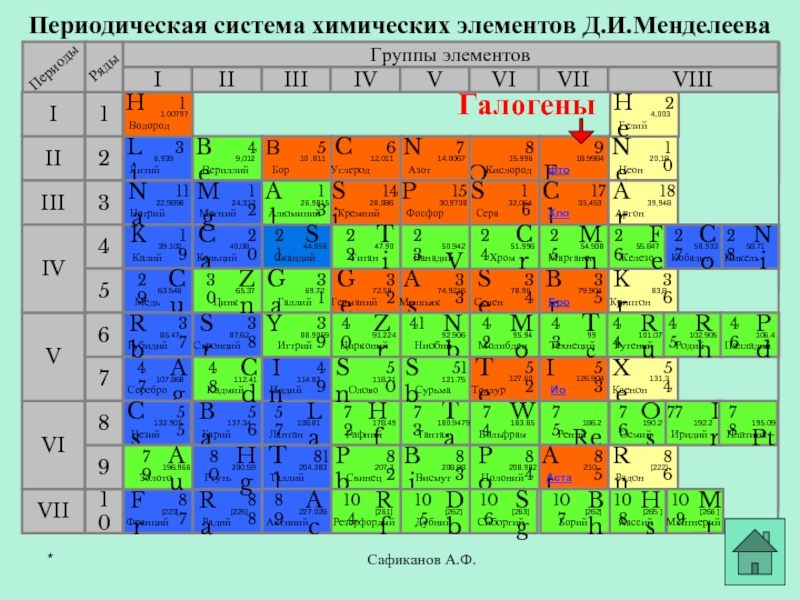
- 9. Сафиканов А.Ф.Периодическая система химических элементов Д.И.МенделееваГруппы элементовIIIIIIVIIIIVVVIVIIIIIIIIVIIVIVIV213456710 Fфтор918.9984BrБром3579.904IИод53126.904ClХлор1735,453AtАстат8521098Галогены*
- 10. Сафиканов А.Ф.Периодическая система химических элементов Д.И.МенделееваГруппы элементовIIIIIIVIIIIVVVIVIIIIIIIIVIIVIVIV213456798F 19 9 0 10*
- 11. Сафиканов А.Ф.Периодическая система химических элементов Д.И.МенделееваГруппы элементовIIIIIIVIIIIVVVIVIIIIIIIIVIIVIVIV213456798Cl 35 17 0 10*
- 12. Сафиканов А.Ф.Периодическая система химических элементов Д.И.МенделееваГруппы элементовIIIIIIVIIIIVVVIVIIIIIIIIVIIVIVIV213456798Br 80 35 0 10*
- 13. Сафиканов А.Ф.Периодическая система химических элементов Д.И.МенделееваГруппы элементовIIIIIIVIIIIVVVIVIIIIIIIIVIIVIVIV213456798I 127 53 0 10*
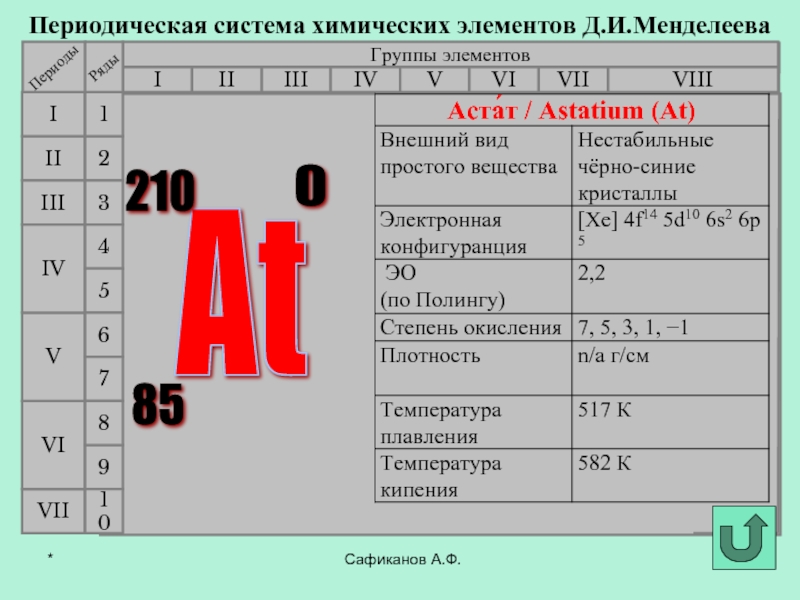
- 14. Сафиканов А.Ф.Периодическая система химических элементов Д.И.МенделееваГруппы элементовIIIIIIVIIIIVVVIVIIIIIIIIVIIVIVIV213456798At 210 85 0 10*
- 15. Химические свойства 45 F2 -наиболее реакционноспособен
- 16. Химические свойства 45 F2 -наиболее реакционноспособен
- 17. Химические свойства Cl2 - сильно реакционноспособен
- 18. Химические свойства Cl2 - сильно реакционноспособен
- 19. Химические свойства Br2 - реакционноспособен
- 20. Химические свойства Br2 - реакционноспособен
- 21. Химические свойства I2 - химически наименее
- 22. Химические свойства I2 - химически наименее
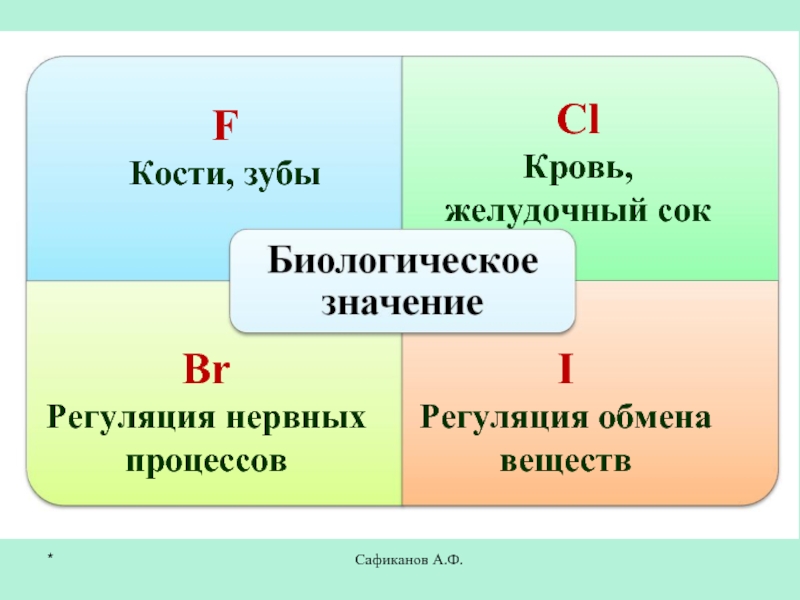
- 23. Сафиканов А.Ф.F Кости, зубыСlКровь, желудочный сокBrРегуляция нервных процессовIРегуляция обмена веществ*
- 24. Сафиканов А.Ф.Применение фтораТефлон ФреонОкислитель ракетного топливаЗаменитель кровиФториды
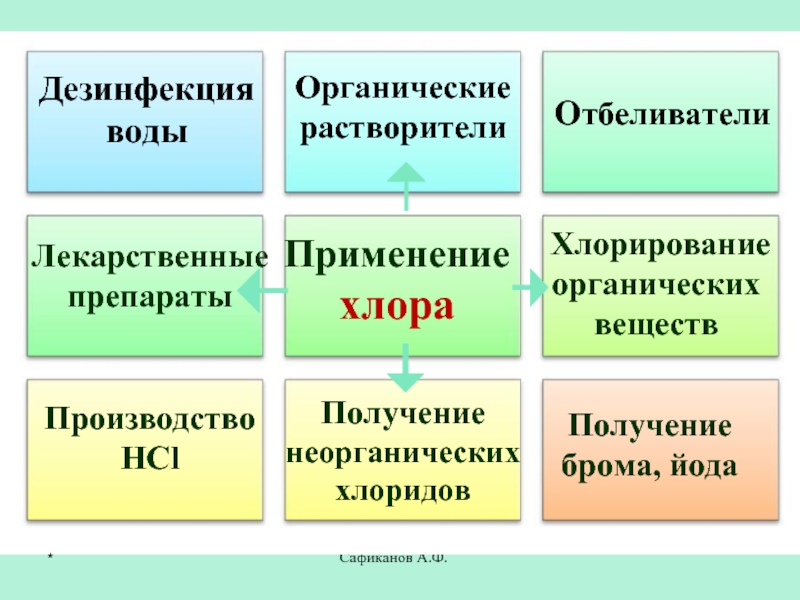
- 25. Сафиканов А.Ф.Применение хлораОтбеливателиПроизводство HClПолучение
- 26. Сафиканов А.Ф.Применение бромаЛекарственные препаратыКрасители ФотографияВетеренарные препаратыИнгибиторыПрисадки
- 27. Сафиканов А.Ф.Применение йодаЛекарственные препаратыФотографияКрасителиДезинфекция одеждыЭлектролампы*
- 28. Физические свойства галогенов Заполни пропускиФтор -
- 29. Химические свойства галогенов Поставь коэффициентыСафиканов А.Ф.
- 30. Химические свойства галогенов Найди соответствие между исходными
- 31. Сафиканов А.Ф.§ 17, упр.5, 8 стр 63.
- 32. Сафиканов А.Ф.Спасибо за урок!Благодарю за сотрудничество.*
- 33. Сафиканов А.Ф.«Химия-9», О.С.Габриелян, М, Дрофа,2005г, стр 78-90
- 34. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Сафиканов А.Ф.
Выполнил:
учитель химии
первой квалификационной категории
Сафиканов Ахат Файзрахманович
МБОУ «Школа-интернат №1 среднего
(полного) общего образования» городского округа город Стерлитамак Республики Башкортостан
Слайд 2Сафиканов А.Ф.
1. История открытия галогенов
2. Положение в Периодической системе
3. Химические
свойства
4. Применение
5.Проверка знаний
Главная
Галогены
6.Домашнее задание. Итоги урока.
*
Слайд 4 В 1886 году
французский химик А. Муассан, используя электролиз жидкого фтороводорода, охлажденного до
температуры –23°C (в жидкости должно содержаться немного фторида калия, который обеспечивает ее электропроводимость), смог на аноде получить первую порцию нового, газа. В первых опытах для получения фтора Муассан использовал очень дорогой электролизер, изготовленный из платины и иридия. При этом каждый грамм полученного фтора «съедал» до 6 г платины.Сафиканов А.Ф.
История открытия фтора
Анри Муассан
(1852 – 1907)
*
Слайд 5 В 1774 году шведский ученый
К. Шееле открыл хлор, который принял за сложное вещество и
назвал "дефлогистированной соляной кислотой".В 1807 году английский химик Гемфри Дэви получил тот же газ. Он пришел к выводу, что получил новый элемент и назвал его "хлорин" (от "хлорос" - желто-зеленый).
В 1812 году Гей-Люсеок дал газу название хлор.
Сафиканов А.Ф.
История открытия хлора
Карл Вильгельм Шееле
(1742 – 1786)
*
Слайд 6 В 1825 году французский химик
А.Ж.Балар при изучении маточных рассолов выделил темно-бурую жидкость, который он
назвал - "мурид" (от латинского слова muria, означающего "рассол"). Комиссия Академии, проверив это сообщение, подтвердила открытие Балара и предложила назвать элемент бромом (от "бромос", с греческого "зловонный").История открытия брома
Антуан Жером Балар
(1802 – 1876)
Сафиканов А.Ф.
*
Слайд 7 В 1811 году французский химик
Бернар Куртуа открыл иод путём перегонки маточных растворов от
своего азотнокислого кальция с серной кислотой Чтобы другие химики могли изучать новое вещество, Б. Куртуа подарил его (правда, очень небольшое количество) фармацевтической фирме в Дижоне.В 1813 году Ж.-Л.Гей-Люссак подробно изучил этот элемент и дал ему современное название. Название "иод" происходит от греческого слова "иодэс" - "фиолетовый" (по цвету паров).
Сафиканов А.Ф.
История открытия йода
Бернар Куртуа (1777 – 1838 )
*
Слайд 8 В 1869 г Д.И.Мендеелеев
предсказал его существование и возможность открытия в будущем (как «эка-иод»).
Впервые астат был получен искусственно в 1940 г открыт Д.Корсоном, К.Маккензи и Э.Сегре (Калифорнийский университет в Беркли) . Для синтеза изотопа 211At они облучали висмут альфа-частицами. В 1943-1946 годах изотопы астата были обнаружены в составе природных радиоактивных рядов. Астат является наиболее редким элементом среди всех, обнаруженных в природе. В поверхностном слое земной коры толщиной 1,6 км содержится всего 70 мг астата.
Сафиканов А.Ф.
История открытия астата
*
Слайд 9Сафиканов А.Ф.
Периодическая система химических элементов Д.И.Менделеева
Группы элементов
I
III
II
VIII
IV
V
VI
VII
II
I
III
VII
VI
V
IV
2
1
3
4
5
6
7
10
F
фтор
9
18.9984
Br
Бром
35
79.904
I
Иод
53
126.904
Cl
Хлор
17
35,453
At
Астат
85
210
9
8
Галогены
*
Слайд 10Сафиканов А.Ф.
Периодическая система химических элементов Д.И.Менделеева
Группы элементов
I
III
II
VIII
IV
V
VI
VII
II
I
III
VII
VI
V
IV
2
1
3
4
5
6
7
9
8
F
19
9
0
10
*
Слайд 11Сафиканов А.Ф.
Периодическая система химических элементов Д.И.Менделеева
Группы элементов
I
III
II
VIII
IV
V
VI
VII
II
I
III
VII
VI
V
IV
2
1
3
4
5
6
7
9
8
Cl
35
17
0
10
*
Слайд 12Сафиканов А.Ф.
Периодическая система химических элементов Д.И.Менделеева
Группы элементов
I
III
II
VIII
IV
V
VI
VII
II
I
III
VII
VI
V
IV
2
1
3
4
5
6
7
9
8
Br
80
35
0
10
*
Слайд 13Сафиканов А.Ф.
Периодическая система химических элементов Д.И.Менделеева
Группы элементов
I
III
II
VIII
IV
V
VI
VII
II
I
III
VII
VI
V
IV
2
1
3
4
5
6
7
9
8
I
127
53
0
10
*
Слайд 14Сафиканов А.Ф.
Периодическая система химических элементов Д.И.Менделеева
Группы элементов
I
III
II
VIII
IV
V
VI
VII
II
I
III
VII
VI
V
IV
2
1
3
4
5
6
7
9
8
At
210
85
0
10
*
Слайд 15Химические свойства 45 F2 -наиболее реакционноспособен , реакции идут на холоду,
при нагревании – даже с участием Au, Pt.
С простыми веществами:
С металлами С неметаллами
Na + F2 → H2 + F2 →
Mo + F2 → Xe + F2 →
Со сложными веществами:
H2O + F2 →
KCl + F2 →
KBr + F2 →
KI + F2 →
Сафиканов А.Ф.
Проверить
*
Слайд 16Химические свойства 45 F2 -наиболее реакционноспособен , реакции идут на холоду,
при нагревании – даже с участием Au, Pt.
С простыми веществами:
С металлами С неметаллами
2Na + F2 → 2NaF H2 + F2 → 2HF
Mo + 3F2 → MoF6 Xe + 2F2 → XeF4
Со сложными веществами:
2H2O + F2 → 4HF + O2
2KCl + F2 → Cl2 + 2NaF
2KBr + F2 → Br2 + 2КF
2KI + F2 → I2 + 2КF
Сафиканов А.Ф.
*
Слайд 17Химические свойства Cl2 - сильно реакционноспособен (искл. C, O2, N2
и некот. др.)
С простыми веществами:
С металлами С неметаллами
Fe + Cl2 → H2 + Cl2 →
Cu + Cl2 → P + Cl2 →
Со сложными веществами:
H2O + Cl2 →
NaOH + Cl2 →
KBr + Cl2 →
KI + Cl2 →
Сафиканов А.Ф.
Проверить
Горение железа в хлоре
*
Слайд 18Химические свойства Cl2 - сильно реакционноспособен (искл. C, O2, N2
и некот. др.)
С простыми веществами:
С металлами С неметаллами
2Fe + 3Cl2 → 2FeCl3 H2 + Cl2 → 2HCl (tº, hυ)
Cu + Cl2 → Cu Cl2 2P + 5Cl2 → 2PCl5 ( tº, в изб. Сl2)
Со сложными веществами:
H2O + Cl2 → HCl+HClO хлорная вода
2NaOH + Cl2 → NaOCl + NaCl + H2O жавелевая вода
2KBr + Cl2 → Br2 + 2КCl
2KI + Cl2 → I2 + 2КCl
Сафиканов А.Ф.
*
Слайд 19Химические свойства
Br2 - реакционноспособен
С простыми веществами:
С металлами С неметаллами
Al + Br2 → H2 + Br2 →
Cu + Br2 → P + Br2 →
Со сложными веществами:
Br2 + H2O →
KI + Br2 →
Сафиканов А.Ф.
Проверить
*
Слайд 20Химические свойства
Br2 - реакционноспособен
С простыми веществами:
С металлами С неметаллами
2Al + 3Br2 → 2AlBr3 H2 + Br2 → 2HCl
Cu + Br2 → Cu Br2 2P + 5Br2 → 2PBr5
Со сложными веществами:
Br2 + H2O → HBr + HBrO бромная вода
2KI + Br2 → I2 + 2КCl
Сафиканов А.Ф.
*
Слайд 21Химические свойства
I2 - химически наименее активен
С простыми веществами:
С металлами С неметаллами
Hg + I2 → H2 + I2 →
Al + I2 → P + Br2 →
Со сложными веществами:
I2 + H2O →
I2 + р-р крахмала →
Сафиканов А.Ф.
Проверить
Действие крахмала на йод
*
Слайд 22Химические свойства
I2 - химически наименее активен
С простыми веществами:
С металлами С неметаллами
Hg + I2 → HgI2 H2 + I2 → 2HCl (tº)
2Al + 3I2 → 2AlI3 2P + 3Br2 → 2PI3
Со сложными веществами:
I2 + H2O → HI + HIO
I2 + р-р крахмала → темно-синее окрашивание
Сафиканов А.Ф.
*
Слайд 23Сафиканов А.Ф.
F
Кости, зубы
Сl
Кровь, желудочный сок
Br
Регуляция нервных процессов
I
Регуляция обмена веществ
*
Слайд 24Сафиканов А.Ф.
Применение фтора
Тефлон
Фреон
Окислитель ракетного топлива
Заменитель крови
Фториды
в зубных пастах
*
Слайд 25
Сафиканов А.Ф.
Применение хлора
Отбеливатели
Производство
HCl
Получение
брома, йода
Дезинфекция воды
Органические растворители
Лекарственные препараты
Хлорирование органических веществ
Получение
неорганических хлоридов*
Слайд 26Сафиканов А.Ф.
Применение брома
Лекарственные препараты
Красители
Фотография
Ветеренарные препараты
Ингибиторы
Присадки
к бензину
*
Слайд 27Сафиканов А.Ф.
Применение йода
Лекарственные препараты
Фотография
Красители
Дезинфекция одежды
Электролампы
*
Слайд 28Физические свойства галогенов
Заполни пропуски
Фтор -
, в воде , так как интенсивно с ней взаимодействует. Хлор - , раствор хлора в воде практически бесцветен - . Бром - . Йод - с с металлическим блеском. Кристаллический йод легко - переходит из твердого в газообразное состояние. Астат похож на , но имеет более ярко выраженный металлический характер. Все галогены обладают запахом, вдыхание их вызывает сильнейшее раздражение дыхательных путей и тяжелые .
Сафиканов А.Ф.
черно-фиолетовые кристаллы
не растворим
светло-желтый газ
хлорная вода
желто-зеленый газ
бурая жидкость
йод
резким
отравления
*
Слайд 29Химические свойства галогенов
Поставь коэффициенты
Сафиканов А.Ф.
Na + Cl2
= NaCl S + F2 =
SF6 Fe + Br2= FeBr3 P + Cl2 = PCl5 NaI + Cl2 = NaCl + I2 F2 + H2O = HF + O2 NaBr + Cl2 = NaCl + Br2 KOH + Cl2 = KCl + KClO3 + H2O2
2
2
4
2
3
5
3
2
2
2
2
2
2
3
2
3
5
2
6
*
Слайд 30
Химические свойства галогенов
Найди соответствие между исходными веществами и продуктами реакций
Сафиканов
А.Ф.
Xe + 2F2 =
H2 + F2 =
2Au +
3Cl2 = 2NaCl + 2H2 O =
2NaI + Cl2 =
2H2 O + 2F2 =
2NaOH + H2 +Cl2
2NaCl + I2
XeF4
4 HF + O2
2HF
2AuCl3
*
Слайд 31Сафиканов А.Ф.
§ 17, упр.5, 8 стр 63.
Дополнительно: ссылка на сайт учителя химии Сафиканова А.Ф. http://int-46.ucoz.ru/load/13-1-0-155 , где размещен комплект интерактивных заданий на закрепление и проверку знаний по теме «Галогены» в программе Hot Potatoes.
Домашнее задание
*
Слайд 33Сафиканов А.Ф.
«Химия-9», О.С.Габриелян, М, Дрофа,2005г, стр 78-90
«Химия в действии»,
М.Фримантл, М, «Мир»,1991г, стр 269-286.
«Неорганическая химия в таблицах»,Н.В.Манцевич, Минск, Современная
школа,2008г, стр 275-280http://www.chem100.ru/
http://rrc.dgu.ru/res/n-t.ru/ri/ps/index.htm
http://www.periodictable.ru/
http://sevchem.info/?go=galeri&act=show_photo&idr=17&id_f=35
http://sevchem.info/?go=galeri&act=show_photo&idr=17&id_f=23
http://sevchem.info/?go=galeri&act=show_photo&idr=17&id_f=72
http://ru.wikipedia.org/wiki/%D0%A4%D1%80%D1%8D%D0%B4_%D0%90%D0%BB%D0%BB%D0%B8%D1%81%D0%BE%D0%BD
Использованная литература, интернет-ресурсы
*