реакций.
3. Зависимость скорости реакции от концентрации реагирующих веществ.
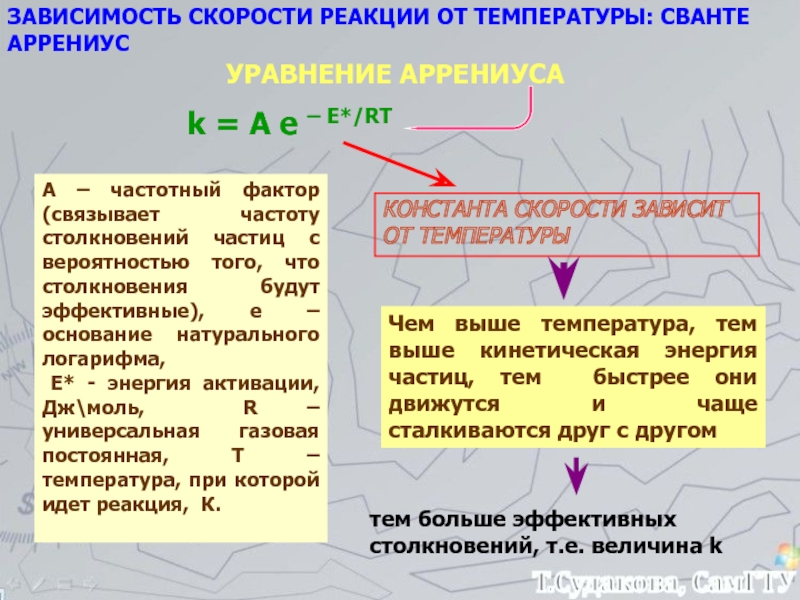
4. Зависимость скорости
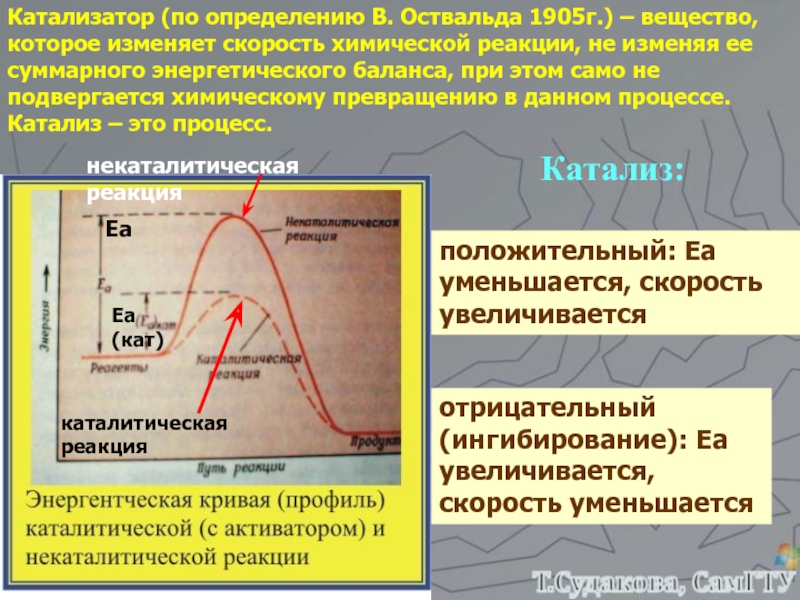
реакции от температуры.5. Катализ.
6. Химическое равновесие.
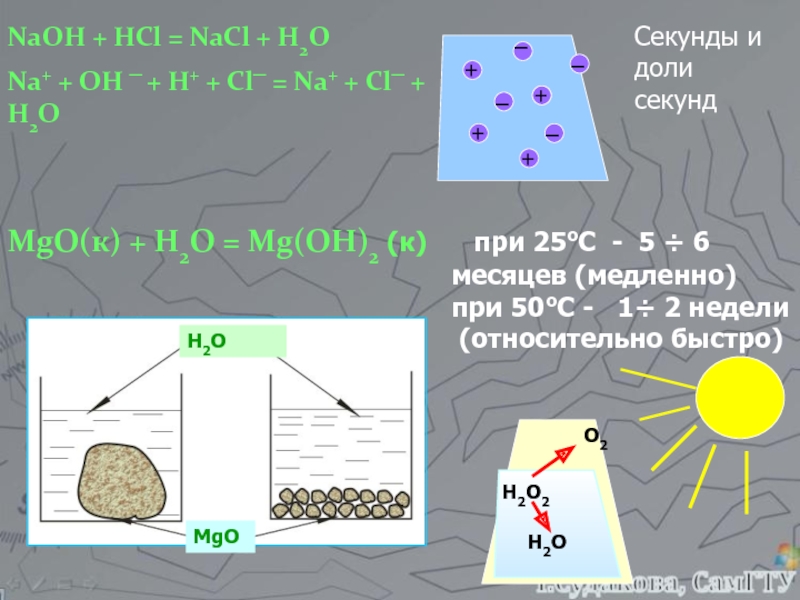
Кинетика химических реакций.
Химическое равновесие.
План.