Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Классы неорганических соединений
Содержание
- 1. Классы неорганических соединений
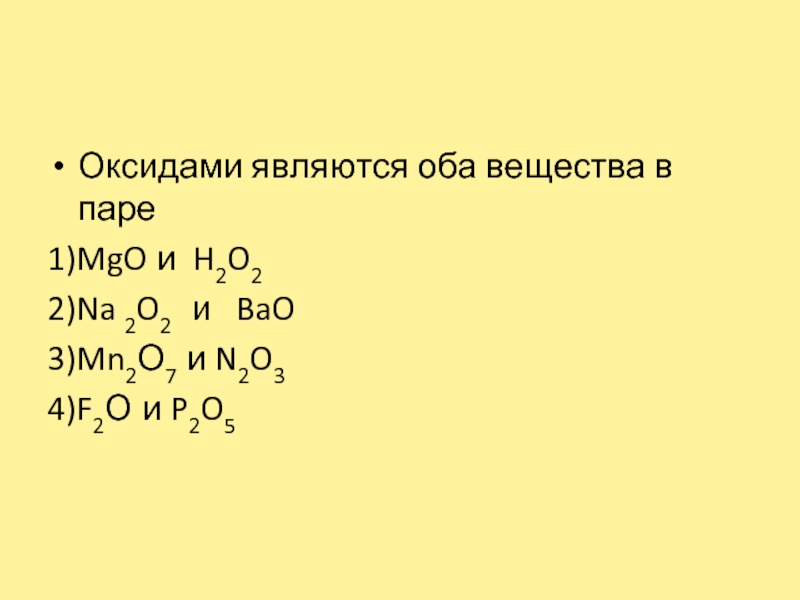
- 2. Оксиды Образованы двумя химическими элементами Один из элементов кислород, имеющий степень окисления -2Примеры: MgO, H2O
- 3. Оксидами являются оба вещества в паре1)MgO и
- 4. Классификация оксидовНесолеобразующие (безразличные)NOCON2OСолеобразующиеОсновныеКислотныеАмфотерные
- 5. Основные оксидыОксиды металлов, в которых металл имеет
- 6. Свойства основных оксидов Реагируют с кислотами:
- 7. Кислотные оксиды Оксиды неметаллов и металлов, в
- 8. Свойства кислотных оксидов Реагируют со щелочами (растворимыми
- 9. Амфотерные оксиды Оксиды металлов, в которых металл
- 10. Свойства амфотерных оксидов Амфотерность – двойственность свойствРеагируют
- 11. С водой реагируют оксиды: 1)BaO и SiO22)СuO и SO33)BaO и SO34)FeO и СО2
- 12. Оксид серы (IV) взаимодействует с каждым из
- 13. С соляной кислотой реагируют каждый из двух
- 14. И с раствором гидроксида натрия и с
- 15. Гидроксиды Основные – основания (щелочи и нерастворимые в воде) Кислотные – кислоты кислородсодержащие Амфотерные
- 16. Только кислоты расположены в ряду1)HNO3, Ca(NO3)2, NO22)KHCO3, Ba(HSO4)2, Zn(OH)Cl3)HNO2, HNO3, CH3COONa4)H2S, Н2SO3, CH3COOH
- 17. Оцените правильность следующих суждений:А) Гидроксиды по свойствам
- 18. Щелочи – растворимые в воде основанияЩелочи образуют
- 19. Свойства щелочейРеагируют с кислотами: 2NaOH + H2SO4
- 20. Нерастворимые в воде основанияРеагируют с кислотами: Mg(OH)2 + 2HNO3 = Mg(NO3)2 +2H2OРазлагаются при нагревании: Mg(OH)2 = MgO +H2O
- 21. Кислотные гидроксиды – кислородсодержащие кислотыРеагируют с основаниями: KOH
- 22. Амфотерные гидроксидыРеагируют с кислотами, проявляя свойства оснований: Al(OH)3
- 23. Гидроксид натрия не взаимодействует с 1)CuCl22)SO23)PbS4)HNO3
- 24. Гидроксид натрия реагирует со всеми веществами ряда:1)Zn,
- 25. Гидроксид калия реагирует со всеми веществами группы1)Zn, SiO2, H2O2)HNO3, Na2CO3, Mg3)CuSO4, SO3, H3PO44)CuO, Cа(OH)2, N2O5
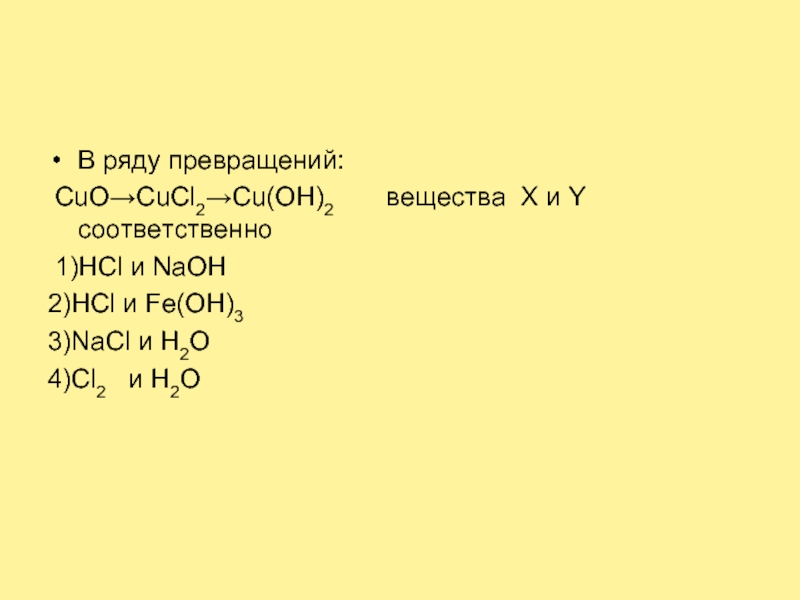
- 26. В ряду превращений: CuO→CuCl2→Cu(OH)2
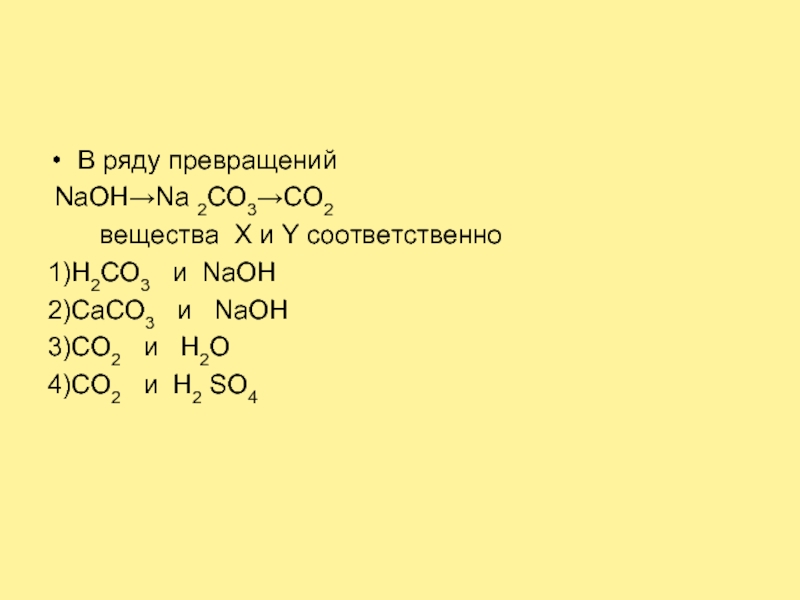
- 27. В ряду превращений NaOH→Na 2CO3→CO2
- 28. Каждое из перечисленных веществ: CuCl2, SO3, H3PO4,
- 29. При действии избытка раствора гидроксида натрия на
- 30. 6) NaAlO2+ H2Исходные веществаА) Al + NaOH
- 31. Скачать презентанцию
Оксиды Образованы двумя химическими элементами Один из элементов кислород, имеющий степень окисления -2Примеры: MgO, H2O
Слайды и текст этой презентации
Слайд 2Оксиды
Образованы двумя химическими элементами
Один из элементов кислород, имеющий
степень окисления -2
Слайд 4Классификация оксидов
Несолеобразующие (безразличные)
NO
CO
N2O
Солеобразующие
Основные
Кислотные
Амфотерные
Слайд 5Основные оксиды
Оксиды металлов, в которых металл имеет степень окисления +1
или +2 как правило
Основным оксидам соответствуют основания (основные гидроксиды):
Na2O – NaOHMgO – Mg(OH)2
Слайд 6Свойства основных оксидов
Реагируют с кислотами:
MgO + H2SO4 = MgSO4 + H2O
Некоторые реагируют с водой
(оксиды щелочных и щелочно-земельных металлов):Na2O + H2O = 2NaOH
Реагируют с кислотными оксидами:
CaO + CO2 = CaCO3
Слайд 7Кислотные оксиды
Оксиды неметаллов и металлов, в которых элемент имеет
степень окисления +4 и выше как правило
Кислотным оксидам соответствуют
кислоты (кислотные гидроксиды):CO2 – H2CO3 Mn2O7 – HMnO4
SO3 – H2SO4 CrO3 – H2CrO4, H2Cr2O7
Слайд 8Свойства кислотных оксидов
Реагируют со щелочами (растворимыми в воде основаниями):
CO2
+ 2NaOH = Na2CO3 + H2O
Большинство реагирует с водой:
SO3 +
H2O = H2SO4Реагируют с основными оксидами:
P2O5 + 3CaO = Ca3(PO4)2
Слайд 9Амфотерные оксиды
Оксиды металлов, в которых металл проявляет степень окисления
+3 или +4 как правило
Амфотерным оксидам соответствуют амфотерные гидроксиды:
Al2O3
– Al(OH)3 ZnO – Zn(OH)2Cr2O3 – Cr(OH)3 BeO – Be(OH)2
MnO2 – Mn(OH)4
Слайд 10Свойства амфотерных оксидов
Амфотерность – двойственность свойств
Реагируют с кислотами, проявляя
свойства основных оксидов:
Al2O3 + 6HCl = 2AlCl3 + 3H2O
Реагируют со
щелочами, проявляя свойства кислотных оксидов:Al2O3 + 2NaOH + 3H2O= 2Na[Al(OH)4]
Al2O3 + 2NaOH = 2NaAlO2 + H2O (при сплавлении)
Слайд 12
Оксид серы (IV) взаимодействует с каждым из двух веществ:
1)H2O и
KCl
2)Ba(OH)2 и CaO
3)CaCO3 и ZnSO3
4)Ca(OH)2 и N2
Слайд 13
С соляной кислотой реагируют каждый из двух оксидов
1)K2O и SO3
2)Al2O3
и CaO
3)CO2 и ZnO
4)CrO3 и Na2O
Слайд 15Гидроксиды
Основные – основания (щелочи и нерастворимые в воде)
Кислотные – кислоты
кислородсодержащие
Амфотерные
Слайд 16
Только кислоты расположены в ряду
1)HNO3, Ca(NO3)2, NO2
2)KHCO3, Ba(HSO4)2, Zn(OH)Cl
3)HNO2, HNO3,
CH3COONa
4)H2S, Н2SO3, CH3COOH
Слайд 17
Оцените правильность следующих суждений:
А) Гидроксиды по свойствам делятся на кислоты,
основания и амфотерные гидроксиды.
Б) Гидроксиды элементов главных подгрупп
первой и второй групп Периодической системы – растворимые основания (щелочи).1)верно только А
2)верно только Б
3)верны оба суждения
4)оба суждения неверны
Слайд 18Щелочи – растворимые в воде основания
Щелочи образуют металлы 1 группы
главной подгруппы (щелочные металлы) и щелочноземельные металлы (Ca, Sr, Ba)
Примеры:
NaOH, Ca(OH)2Слайд 19Свойства щелочей
Реагируют с кислотами:
2NaOH + H2SO4 = Na2SO4 +
2H2O
Реагируют с кислотными оксидами:
2NaOH + CO2 = Na2CO3 + H2O
Реагируют
с растворами солей, если выпадает осадок:2NaOH+ CuSO4 = Cu(OH)2↓ + Na2SO4
Реагируют с металлами, образующими амфотерные оксиды и гидроксиды:
2NaOH + Zn +2H2O = Na2[Zn(OH)4] + Н2
Слайд 20Нерастворимые в воде основания
Реагируют с кислотами:
Mg(OH)2 + 2HNO3 = Mg(NO3)2
+2H2O
Разлагаются при нагревании:
Mg(OH)2 = MgO +H2O
Слайд 21Кислотные гидроксиды – кислородсодержащие кислоты
Реагируют с основаниями:
KOH + HNO3 =
KNO3 + H2O
Реагируют с основными оксидами:
MgO + H2SO4 = MgSO4
+ H2OРеагируют с металлами, стоящими в ряду напряжений до водорода:
Mg + H2SO4 = MgSO4 + H2
Реагируют с солями:
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2
Слайд 22Амфотерные гидроксиды
Реагируют с кислотами, проявляя свойства оснований:
Al(OH)3 + 3HCl =
AlCl3 + 3H2O
Реагируют со щелочами, проявляя свойства кислот:
Al(OH)3 + NaOH
= Na[Al(OH)4]Слайд 24
Гидроксид натрия реагирует со всеми веществами ряда:
1)Zn, Na 2CO3, CuO
2)CO2,
H3 PO4 CuO
3)S O3, H3PO 4, AI2O3
4)SO3, MgO, H3PO4,
Слайд 25
Гидроксид калия реагирует со всеми веществами группы
1)Zn, SiO2, H2O
2)HNO3, Na2CO3,
Mg
3)CuSO4, SO3, H3PO4
4)CuO, Cа(OH)2, N2O5
Слайд 26
В ряду превращений:
CuO→CuCl2→Cu(OH)2 вещества X и
Y соответственно
1)НСl и NaOH
2)HCl и Fe(OH)3
3)NaCl и Н2O
4)Cl2
и H2O Слайд 27
В ряду превращений
NaOH→Na 2CO3→CO2
веществa
X и Y соответственно
1)Н2CO3 и NaOH
2)CaCO3
и NaOH3)CO2 и H2O
4)CO2 и H2 SO4
Слайд 28
Каждое из перечисленных веществ: CuCl2, SO3, H3PO4, Zn(OH)2
реагирует с
1)серной
кислотой
2)водой3)гидроксидом натрия 4)оксидом углерода(VI)
Слайд 29
При действии избытка раствора гидроксида натрия на раствор сульфата цинка
образуется
1) ZnO
2)
Zn(OH)2 3) Na2ZnO2
4)Na2[Zn(OH)4]
Слайд 306) NaAlO2+ H2
Исходные вещества
А) Al + NaOH + H2O
Б) Al2O3+
NaOH ( плавление)
В) Al2O3+ NaOH+ H2O
Г) Al(OH)3+ NaOH
Теги