Слайд 1Проект по химии
Лешковой Ирины
10 «Б»
Полисахариды
Слайд 2Углеводы
Углеводы широко распространены в природе и играют большую
роль в биологических процессах живых организмов и человека. К ним
относятся, например, виноградный сахар, или глюкоза свекловичный ( тростниковый ) сахар, или сахароза, крахмал и клетчатка. Название «углеводы» возникло в связи с тем, что химический состав большинство соединений этого класса выражается общей формулой Cn(H4O)m. Дальнейшее исследование углеводов показало, что такое название является ниточным. Во-первых, найдены углеводы, состав которых не отвечает этой формуле. Во-вторых, известны соединения (формальдегид СН2О, уксусная кислота С2Н4О2 ), состав которых хотя и соответствует общей формуле Сn(Н2О)m, но по свойствам они отличаются от углеводов.
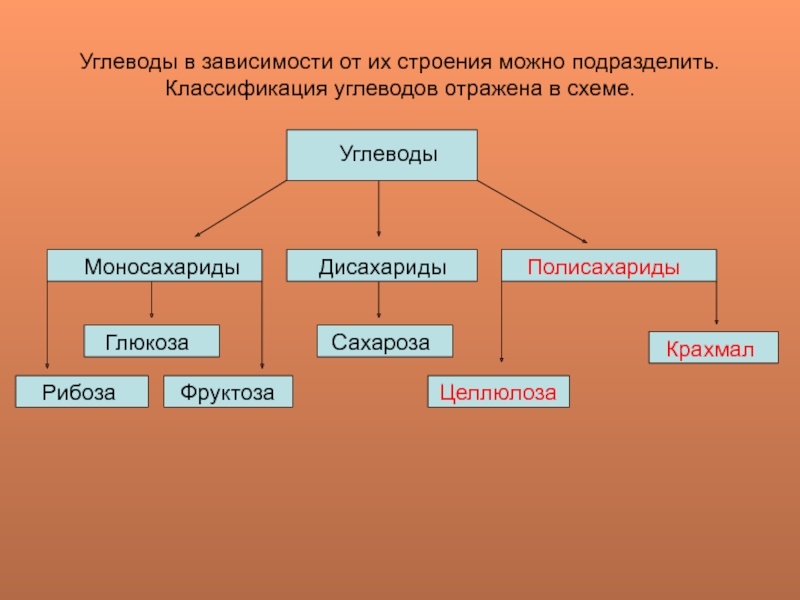
Слайд 3Углеводы в зависимости от их строения можно подразделить.
Классификация углеводов отражена
в схеме.
Углеводы
Моносахариды
Дисахариды
Полисахариды
Глюкоза
Рибоза
Фруктоза
Сахароза
Целлюлоза
Крахмал
Слайд 4Что такое полисахариды?
Полисахариды являются высокомолекулярными соединениями, содержащими сотни и остатков
моносахаридов. Общим для строения полисахаридов является то, что остатки моносахаридов
связываются за счет полуацетального гидроксила одной молекулы и спиртового гидроксила другой и т.д. Каждый остаток моносахарида связан с соседними остатками гликозидными связями. Полигликозиды могут содержать разветвленные и неразветвленные цепи. Остатки моносахаридов, входящие в состав молекулы, могут быть одинаковыми или разными. Наибольшее значение из высших полисахаридов имеют крахмал, гликоген (животный крахмал), клетчатка (или целлюлоза). Все эти три полисахарида состоят из молекул глюкозы, по-разному соединенных друг с другом. Состав всех трех соединений можно выразить общей (С6Н10О5)п
Слайд 5Крахмал
Крахмал относится к полисахаридам. Молекулярная масса этого вещества точно не
установлена, но известно, что очень велика (порядка 100000) и для
разных образцов может быть различна. Поэтому формулу крахмала, как и других полисахаридов, изображают в виде (С6Н10О5)п. Для каждого полисахарида п имеет различные значения.
Слайд 6Физические свойства
Крахмал представляет собой безвкусный порошок, нерастворимый в холодной воде.
В горячей воде набухает, образуя клейстер. Крахмал широко распространен в
природе. Он является для различных растений запасным питательным материалом и содержится в них в виде крахмальных зерен. Наиболее богато крахмалом зерно злаков: риса (до 86%), пшеницы (до 75%), кукурузы (до 72%), а также клубни картофеля (до 24%). В клубнях картофеля крахмальные зерна плавают в клеточном соке, а в злаках они плотно склеены белковым веществом клейковиной. Крахмал является одним из растений извлекают крахмал, разрушая клетки и отмывая его водой. В масштабе его получают главным образом из клубней картофеля (в виде картофельной муки), а также из кукурузы.
Слайд 8Химические свойства
1) При действии ферментов или при нагревании с кислотами
(ионы водорода служат катализатором) крахмал, как и все сложные углеводы,
подвергается гидролизу. При этом образуется растворимый крахмал, затем менее сложные вещества — декстрины. Конечным продуктом гидролиза является глюкоза. Можно выразить суммарное уравнение реакции следующим образом:
Слайд 9Происходит постепенное расщепление макромолекул. Гидролиз крахмала — его важное химическое
свойство.
крахмал декстрины
мальтоза глюкоза
Слайд 102) Крахмал не дает реакции «серебряного зеркала», но ее дают
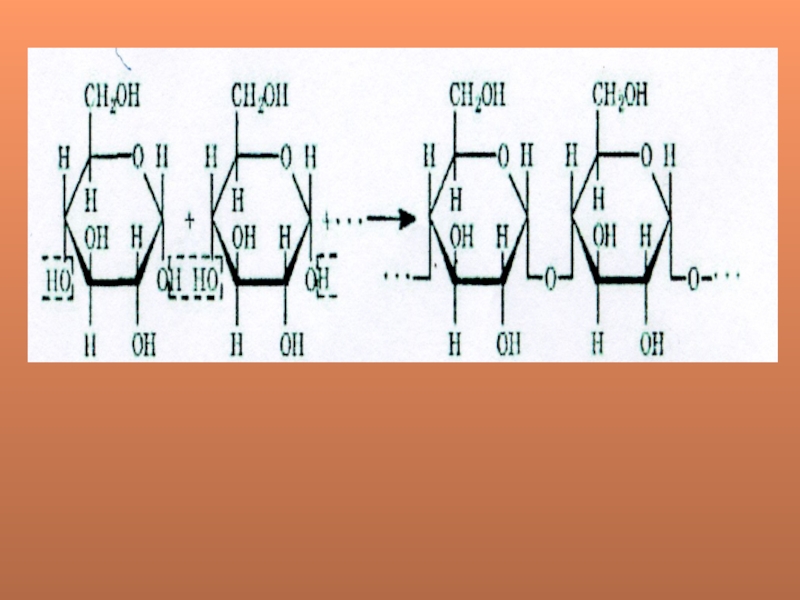
продукты его гидролиза. Макромолекулы крахмала состоят из многих молекул циклической
П-глюкозы. Процесс образования крахмала можно выразить так (реакция поликонденсации):
Слайд 123) Характерной реакцией является взаимодействие крахмала с растворами иода. Если
к охлажденному крахмальному клейстеру добавить раствор иода, то появляется синее
окрашивание. При нагревании клейстера оно исчезает, а при охлаждении появляется вновь. Этим свойством пользуются при определении крахмала в пищевых продуктах. Так, например, если каплю иода нанести на срез картофеля или ломтик белого хлеба, то появляется синее окрашивание
Слайд 13Применение
Крахмал является основным углеводом пищи человека, он в больших количествах
содержится в хлебе, крупах, картофеле, овощах. В значительных количествах крахмал
перерабатывается на декстрины, патоку, глюкозу, которые используются в кондитерской промышленности. Крахмал используется как клеящее средство, применяется для отделки тканей, на крахмаливания белья. В медицине на основе крахмала готовят мази, присыпки и т.д.
Слайд 14Целлюлоза
Целлюлоза — еще более распространенный углевод, чем крахмал. Из него
состоят в основном стенки растительных клеток. В древесине содержится до
60%, в вате и фильтровальной бумаге — до 90% целлюлозы.
Слайд 15Физические свойства
Чистая целлюлоза — белое твердое вещество, нерастворимое в воде
и в обычных органических растворителях, хорошо растворимо в концентрированном аммиачном
растворе гидроксида меди (II) (реактив Швейцера). Из этого раствора кислоты осаждают целлюлозу в виде волокон (гидратцеллюлоза). Клетчатка обладает довольно большой механической прочностью.
Слайд 16Состав и строение
Состав целлюлозы, так же как и крахмала, выражают
формулой (С6Н10О5)п. Значение п в некоторых видах целлюлозы достигает 10-12
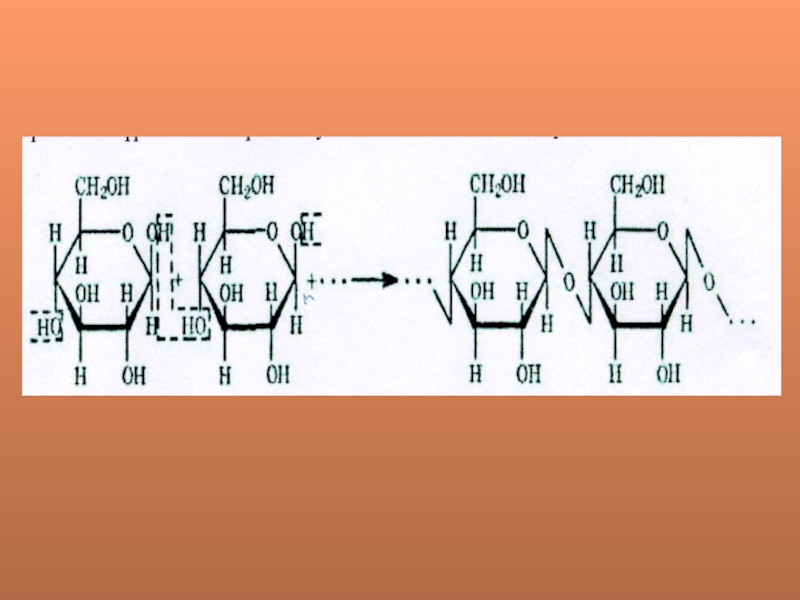
тыс., а молекулярная масса доходит до нескольких миллионов. Молекулы ее имеют линейное (неразветвленное) строение, вследствие чего целлюлоза легко образует волокна. Молекулы же крахмала имеют как линейную, так и разветвленную структуру. В этом основное отличие крахмала от целлюлозы. Имеются различия и в строении этих веществ: макромолекулы крахмала состоят из остатков молекул П-глюкозы, а макромолекулы целлюлозы — из остатков П-глюкозы. Процесс образования фрагмента макромолекулы целлюлозы можно изобразить схемой:
Слайд 18Химические свойства.
Применение целлюлозы.
Небольшие различия в строении молекул обуславливают значительные различия
в свойствах полимеров: крахмал — продукт питания, целлюлоза для этой
цели непригодна.
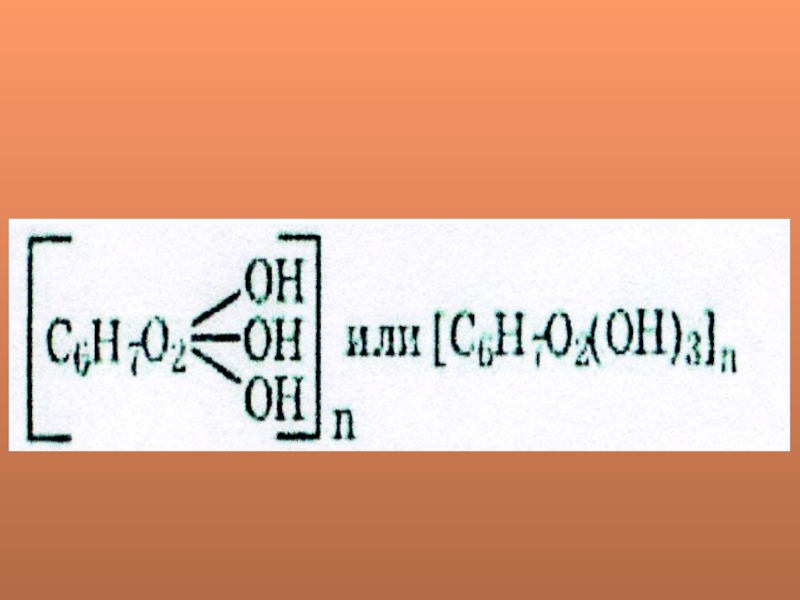
Слайд 191) Целлюлоза не дает реакции «серебряного зеркала» (нет альдегидной группы).
Это позволяет рассматривать каждое звено С6Н10О5 как остаток глюкозы, содержащий
три гидроксильные группы. Последние в формуле целлюлозы часто выделяют:
Слайд 21За счет гидроксильных групп целлюлоза может образовывать простые и сложные
эфиры.
Например, реакция образования сложного эфира с уксусной кислотой имеет вид:
[С6Н7О2(ОН)3]п+ЗпСНЗСООНа[С6Н7О2(ОСОСНЗ)3]п+ЗпН2О
При
взаимодействии целлюлозы с концентрированной азотной кислотой в присутствии
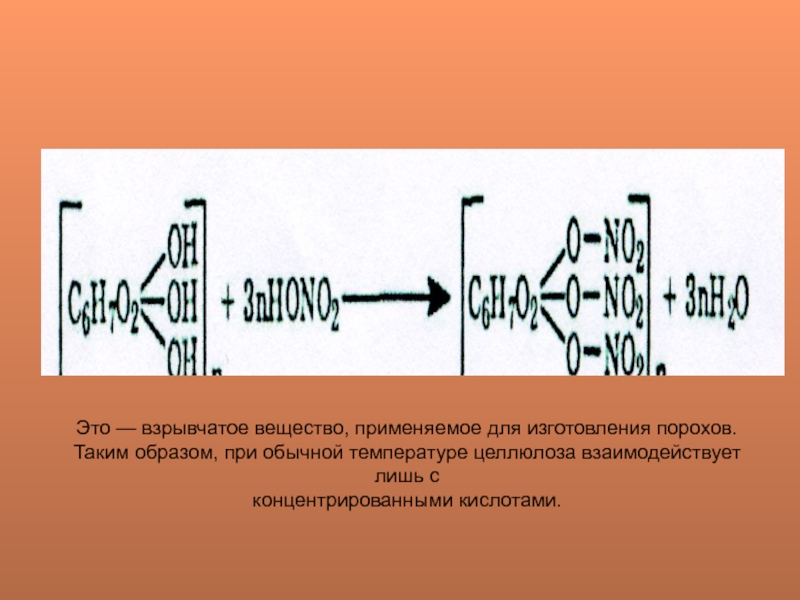
концентрированной серной кислоты в качестве водоотнимающего средства образуется сложны эфир — тринитрат целлюлозы:
Слайд 22Это — взрывчатое вещество, применяемое для изготовления порохов.
Таким образом, при
обычной температуре целлюлоза взаимодействует лишь с
концентрированными кислотами.
Слайд 232) Подобно крахмалу, при нагревании с разбавленными кислотами целлюлоза подвергается
гидролизу
с образованием глюкозы:
(С6Н1006)п+пН2ОПпСбН12О6
Гидролиз целлюлозы, иначе называемый осахариванием, — очень важное
свойство целлюлозы,
он позволяет получить из древесных опилок и стружек целлюлозу, а сбраживанием последней —
этиловый спирт. Этиловый спирт, полученный из древесины, называется гидролизным.
На гидролизных заводах из 1 т древесины получают до 200 л этилового спирта, что позволяет
заменить 1,5 т картофеля или 0,7 т зерна