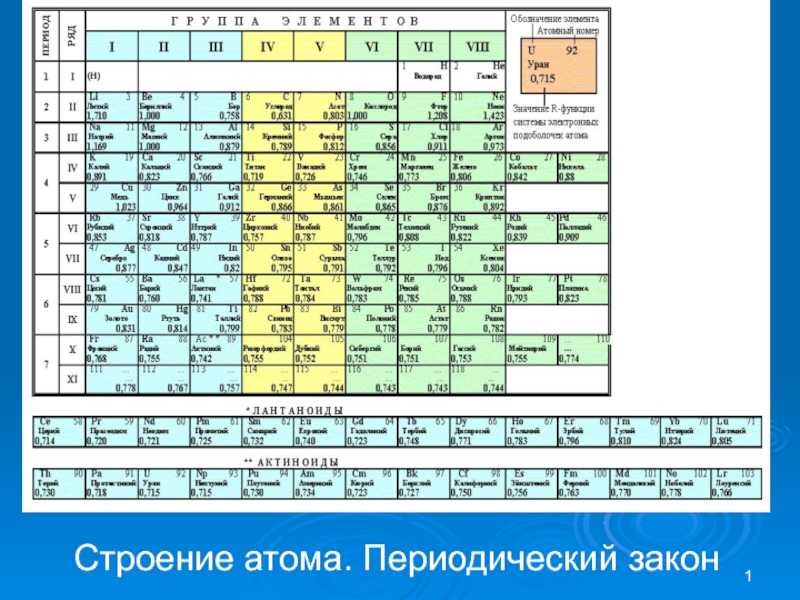
Слайд 1Строение атома. Периодический закон
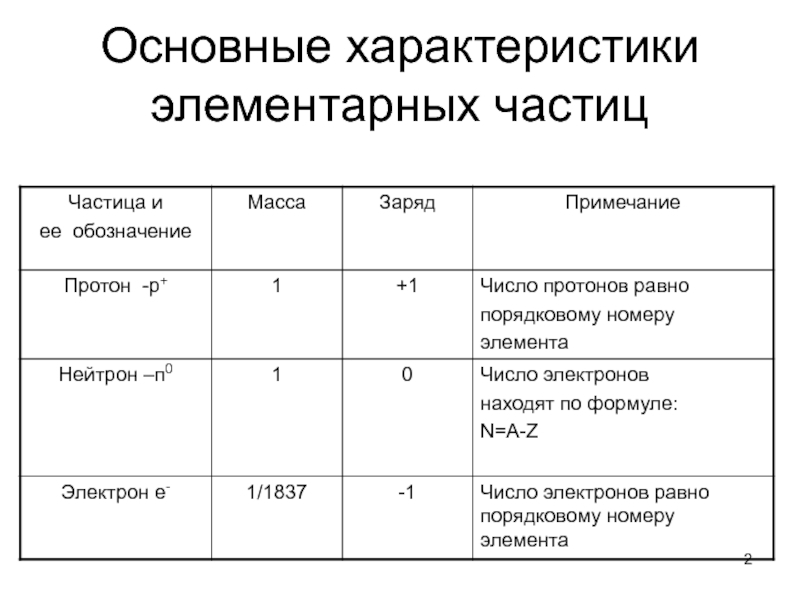
Слайд 2Основные характеристики элементарных частиц
Слайд 3Главное квантовое число(n)
n - 1, 2, 3,…, определяет энергию электрона
в атоме
Энергетический уровень - состояние электронов в атоме с тем
или иным значением n
Основное состояние атома - min энергия электронов
Возбужденное состояние – более высокие значения энергии электронов
Слайд 4 Орбитальное квантовое число (l) харак-ет форму электронного облака l
= 0, 1, 2, 3….n-1
Подуровень: s, p, d,
f, g, h
Т.е. энерг-кий уровень (n) содержит совокупность энерг-ких подуровней, отличающихся по энергиям (в многоэлектронном атоме)
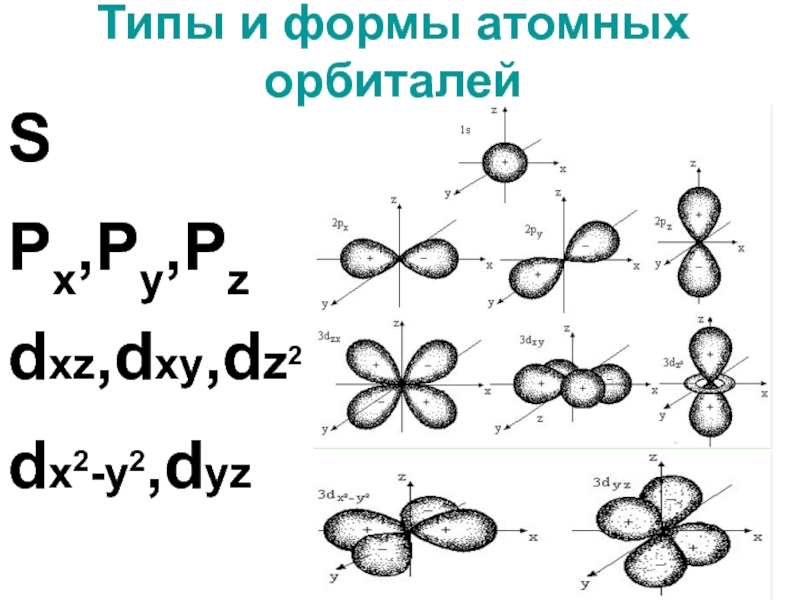
Слайд 5Типы и формы атомных орбиталей
S
Px,Py,Pz
dxz,dxy,dz2
dx2-y2,dyz
Слайд 6Магнитное квантовое число (ml) характеризует
ориентацию электронных облаков в пространстве
ml
меняется от –l до +l,
а всего = 2l + 1 значений
Например:
l = 0 (s); ml = 0
l = 1 (p); ml = 0, +1, -1
Слайд 7Спиновое квантовое число (ms) характеризует собственный магнитный момент электрона, который
или совпадает с ориентацией орбитального момента, или направлен в противоположную
сторону.
ms имеет значения: +1/2 или -1/2
Слайд 8Атомная орбиталь (АО)
это состояние электрона в атоме, которое описывается волновой
функцией с набором из трех квантовых чисел n,
l, ml
Условное изображение АО
АО обозначают с помощью кв. чисел
Например:
1s (n = 1, l = 0, ml = 0)
2p (n = 2, l = 1, ml = -1, 0, +1)
Слайд 9Закономерности формирования электронных структур
Принцип наименьшей энергии: электрон размещается на
АО c min энергией
Принцип Паули: в
атоме не может быть двух электронов с одинаковым набором 4-х кв.чисел
Правила Гунда: (1) на одном подуровне сумма спинов электронов максимальна, (2) сумма магнитных кв-х чисел максимальна.
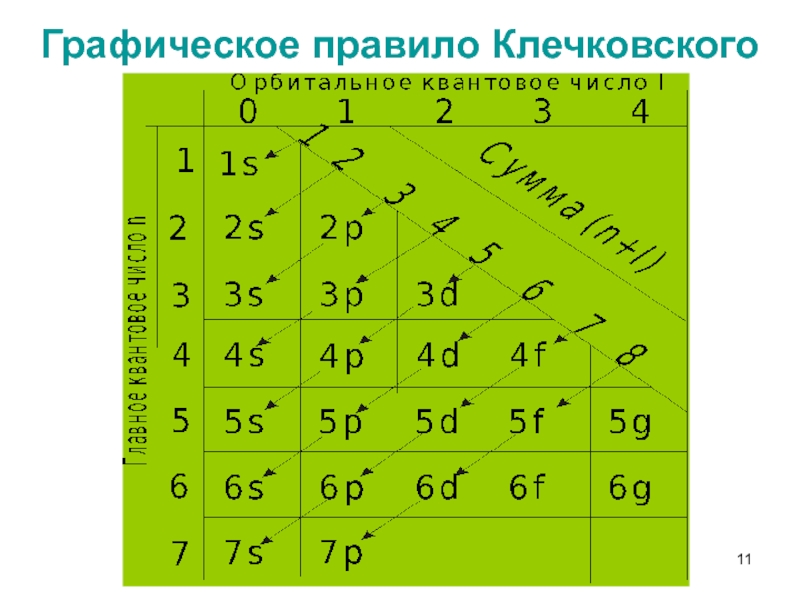
Слайд 10Правила Клечковского
Ниже по энергии находится та орбиталь для которой сумма
(n + l) минимальна
Если сумма (n + l) для двух
подуровней одинакова , то сначала эл-ны заполняют АО с меньшим значением n
Слайд 11Графическое правило Клечковского
Слайд 12Последовательность заполнения АО по правилам Клечковского
1sι 2s2pι 3s3pι 4s3d4pι 5s4d5pι
6s4f5d6pι 7s5f6d7p
Слайд 13Способы изображения электронных структур
Электронная формула
Графическая структура
Энергетическая диаграмма
Слайд 14Примеры электронных структур
Полная электронная формула
Se - 1s22s22p63s23p64s23d104p4
Краткая формула Se - 4s24p4
Электроно-графическая формула
Ti
p d
S
4
3
2
1
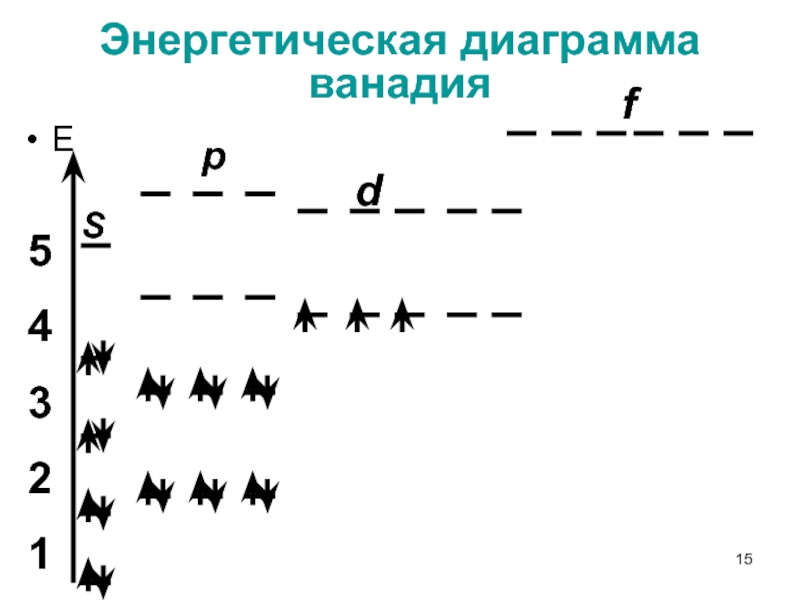
Слайд 15Энергетическая диаграмма ванадия
Е
5
4
3
2
1
S
p
d
f
Слайд 16Maксимальная емкость подуровня:
2(2l+1)e
Максимальная емкость уровня: 2n2е
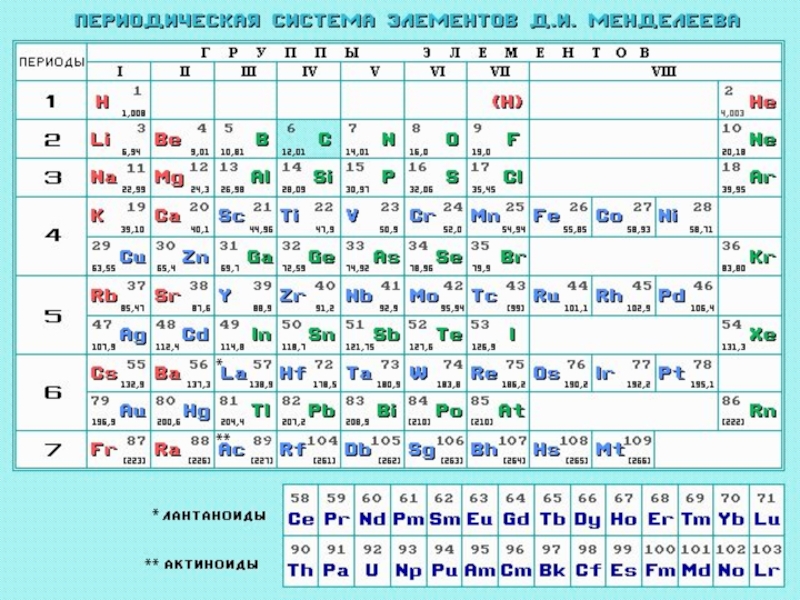
Слайд 17Периодическая система элементов
Д.И. Менделеева (1869г.)
Свойства элементов, а также
формы и свойства их соединений находятся в периодической зависимости от
их атомных весов
Слайд 18Неясные моменты
В чем причина периодичности?
Почему элементы одной группы имеют
одинаковую валентность и образуют одинаковые соединения?
Почему число элементов в периодах
не одинаковое?
Почему в ПС расположение элементов не всегда соответствует возрастанию атомной массы (Аr – К, Co – Ni, Te – I)?
Слайд 19Периодический закон
Свойства элементов, а также формы и свойства их
соединений находятся в периодической зависимости от заряда ядер их атомов
Слайд 20Причина периодичности
Определенная последовательность формирования электронных оболочек (принципы и правила Паули,
Хунда, Клечковского)
Периодическое повторение сходных электронных слоёв и их усложнение
при увеличении гл. кв. числа: периоды начинаются s-элементами, а заканчиваются р-элементами
Слайд 21Короткие периоды
1 период (n=1): (2n2)
2 элемента (1s2)
2 период (n=2): (2n2)
8
элементов (2s22p6)
3 период (n=3): (2n2 – 2*5)
8 элементов (3s23p6)
Слайд 22Длинные периоды
4 период (n=4): (2n2 -2*7)
18 элементов (4s23d104p6)
5 период (n=5):
(2n2 -2(7 + 9) )
18 элементов (5s24d105p6)
6 период (n=6):
(2n2 -2(9 + 11) )
32 элемента (6s24f145d106p6)
7 период (n=7): (2n2 -2(9 + 11 + 13) )
32 элемента (7s25f146d107p6), незавершенный
Слайд 23Период - горизонтальная последовательность эл-тов, атомы которых имеют равное число
энергетических уровней, частично или полностью заполненных электронами
Слайд 24Группа - вертикальная последовательность элементов с однотипной электроной конфигурацией атомов,
равным числом внешних эл-нов, одинаковой max валентностью и похожими химическими
свойствами
Слайд 26Периодичность свойств элементов
атомные и ионные радиусы
энергия ионизации
сродство к электрону
электроотрицательность
валентность
элементов
Слайд 27 Валентность
Валентность определяется электронами внешнего уровня, поэтому высшая валентность элементов
главных подгрупп равна номеру группы
Слайд 28Периодичность свойств простых веществ и соединений
температура плавления и кипения
длина
химической связи
энергия химической связи
электродные потенциалы
стандартные энтальпии образования веществ
энтропии
веществ и т.д.
Слайд 29Атомные и ионные радиусы химических элементов
Орбитальный радиус атома (иона) –
это расстояние от ядра до максимума электронной плотности наиболее удаленной
орбитали этого атома
Слайд 31Эффективные радиусы
атомов и ионов определяют
по межъядерным расст-ям
в молекулах и кристаллах,
предполагая,
что атомы –
несжимаемые шары
Слайд 32Ковалентные радиусы - это эффективные радиусы, определяемые по межъядерным расстояниям
в ковалентных молекулах
Металлические радиусы - это эффективные радиусы в металлах
Ионные
радиусы – это эффективные радиусы в ионах
Слайд 33 Энергия
и потенциал ионизации атомов
Энергия ионизации – это энергия,
необходимая для отрыва электро-на от атома и превращение атома в
положительно заряженный ион
Э – е = Э+, Еион [кДж/моль]
Ионизационный потенциал – это разность потенциалов, при которой происходит ионизация
J [эВ/атом]; Еион= 96,5•J
Слайд 34Сродство к электрону
это энергия, выделяющаяся или поглощающаяся при захвате электрона
атомом или энергия, необходимая для присоединения электрона к атому:
Э
+ е = Э- , F [кДж/моль]
Слайд 35Периодические свойства соединений
основно-кислотные свойства оксидов и гидроксидов:
в периодах ум-ся
основные свойства, но ув-ся кислотные свойства этих соединений
в группах
основные свойства ув-ся, а кислотные ум-ся