Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Алканы - Алкены - Алкины
Содержание
- 1. Алканы - Алкены - Алкины
- 2. АЛКАНЫПолучение, нахождение в природе и применение алкановВПЕРЕДНАЗАД
- 3. ВПЕРЕДГазообразные алканы получают из природного и попутного
- 4. ВПЕРЕДРудничный газ состоит из МЕТАНАПриродный газ на
- 5. ВПЕРЕД3. Изомеризация алканов:4. Гидрирование непредельных углеводородов:ВПЕРЕДНАЗАД
- 6. ВПЕРЕД5. Синтез на основе водяного газа:ВПЕРЕДНАЗАД
- 7. Если в реакцию вступают различные галогеналканы, то
- 8. ВПЕРЕД2. Реакция Дюма - сплавление солей карбоновых кислот со щелочью.
- 9. 3. Синтез Кольбе - электролиз солей карбоновых
- 10. Применение АЛКАНОВВПЕРЕДНАЗАД
- 11. Применение алкановГазообразные АЛКАНЫ (метан и пpопан-бутановая смесь)
- 12. тетрахлорметан – растворитель, для гашения пламени;фтор-, хлор-
- 13. ВПЕРЕД Метан– получение сажи для типографской краски, резины, синтез водорода, производство ацетилена, формальдегида.Применение алкановВПЕРЕДНАЗАД
- 14. ВПЕРЕДНахождение в природе АЛКАНОВ ВПЕРЕДНАЗАД
- 15. ВПЕРЕДНахождение в природеОсновные источники алканов – нефть
- 16. ВПЕРЕДВПЕРЕДНАЗАД
- 17. В природе широко распространены также газовые гидраты
- 18. Твердые алканы встречаются
- 19. АЛКЕНЫПолучение и применение алкановВПЕРЕДНАЗАД
- 20. ПРОМЫШЛЕННЫЕСПОСОБЫПОЛУЧЕНИЯ АЛКЕНОВЛАБОРАТОРНЫЕКРЕКИНГ АЛКАНОВДЕГИДРИРОВАНИЕАЛКАНОВДЕГИДРАТАЦИЯСПИРТОВДЕГАЛОГЕНИРОВАНИЕДЕГИДРО-ГАЛОГЕНИРОВАНИЕВПЕРЕДНАЗАД
- 21. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯКРЕКИНГ АЛКАНОВАЛКАН →
- 22. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН →
- 23. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯДЕГИДРАТАЦИЯ СПИРТОВСПИРТ → АЛКЕН +
- 24. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯДЕГАЛОГЕНИРОВАНИЕПРИМЕР:
- 25. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯДЕГИДРОГАЛОГЕНИРОВАНИЕ
- 26. ПрименениеВПЕРЕДНАЗАД
- 27. Применение алкеновВПЕРЕДНАЗАД
- 28. АЛКИНЫПолучение и применение алкановВПЕРЕДНАЗАД
- 29. Получение АЛКИНОВ1) В промышленности ацетилен получают высокотемпературным пиролизом
- 30. 4) Алкины можно получить дегидрогалогенированием дигалогенопроизводных парафинов. Атомыгалогена
- 31. Применение алкиновВПЕРЕДНАЗАД
- 32. Ранее ацетилен широко применялся для создания высокотемпературного
- 33. Применение алкиновВПЕРЕДНАЗАД
- 34. Ссылки:http://www.chemistry.ssu.samara.ru/chem2/u4.htmhttp://www.chemistry.ssu.samara.ru/chem2/u44.htmАлканыАлкеныАлкиныhttp://alhimikov.net/organikbook/alcan.htmlhttp://school-sector.relarn.ru/nsm/chemistry/Rus/Data/Text/Ch3_2-23.htmlhttp://organichimik.blogspot.ru/2012/06/blog-post_7218.htmlhttp://www.trotted.narod.ru/organic/lec-15/15.htmlhttp://organichimik.blogspot.ru/2012/06/cc.htmlНАЗАД
- 35. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3ВПЕРЕД
Газообразные алканы получают из природного и попутного нефтяных газов;
Жидкие и
твердые – из нефти.
Промышленные способы
получения алканов.
2. КРЕКИНГ
НЕФТИ: 1. ВЫДЕЛЕНИЕ УГЛЕВОДОРОДОВ ИЗ
ПРИРОДНОГО СЫРЬЯ:
ВПЕРЕД
НАЗАД
Слайд 4ВПЕРЕД
Рудничный газ состоит из МЕТАНА
Природный газ на 95% состоит из
метана
МЕТАН называют ещё и болотным газом. Образуется в результате ГНИЕНИЯ
ВПЕРЕД
НАЗАД
Слайд 7Если в реакцию вступают различные галогеналканы, то образуется смесь алканов.
ВПЕРЕД
II.
Лабораторные способы получения алканов.
1. Реакция Вюрца- взаимодействие натрия с галогенпроизводными
алканов:ШАРЛЬ ВЮРЦ
Приводит к увеличению углеводородной цепи.
ВПЕРЕД
НАЗАД
Слайд 93. Синтез Кольбе - электролиз солей карбоновых кислот.
4. Гидролиз карбидов
металлов.
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4↑
карбид
алюминия
ВПЕРЕД
ВПЕРЕД
НАЗАД
Слайд 11Применение алканов
Газообразные АЛКАНЫ (метан и пpопан-бутановая смесь) используются в качестве
ценного ТОПЛИВА.
Жидкие УГЛЕВОДОPОДЫ составляют значительную долю в моторных и ракетных
топливах и используются в качестве РАСТВОРИТЕЛЕЙ. ВПЕРЕД
ВПЕРЕД
НАЗАД
Слайд 12
тетрахлорметан – растворитель, для гашения пламени;
фтор-, хлор- углеводороды (фреоны) –
хладагенты, производство аэрозолей, производство тефлона.
Применение алканов
Галогенпроизводные:
ВПЕРЕД
Слайд 13ВПЕРЕД
Метан– получение сажи для типографской краски, резины, синтез водорода,
производство ацетилена, формальдегида.
Применение алканов
ВПЕРЕД
НАЗАД
Слайд 15ВПЕРЕД
Нахождение в природе
Основные источники алканов – нефть и природный газ.
Метан составляет основную массу природного газа, в нем присутствуют также
в небольших количествах этан, пропан и бутан. Метан содержится в выделениях болот и угольных пластов. Наряду с легкими гомологами метан присутствует в попутных нефтяных газах. Эти газы растворены в нефти под давлением и находятся также над ней. Алканы составляют значительную часть продуктов переработки нефти.
Содержатся в нефти и циклоалканы
– они называются нафтенами
(от греч. naphtha – нефть).
ВПЕРЕД
НАЗАД
Слайд 17В природе широко распространены также газовые гидраты алканов, в основном
метана, они залегают в осадочных породах на материках и на
дне океанов. Их запасы, вероятно, превышают известные запасы природного газа и в будущем могут случить источником метана и его ближайших гомологов.Нахождение в природе
ВПЕРЕД
НАЗАД
Слайд 18 Твердые алканы встречаются в природе в
виде залежей горного воска – озокерита, в восковых покрытиях листьев,
цветов и семян растений, входят в состав пчелиного воска.Нахождение в природе
ВПЕРЕД
НАЗАД
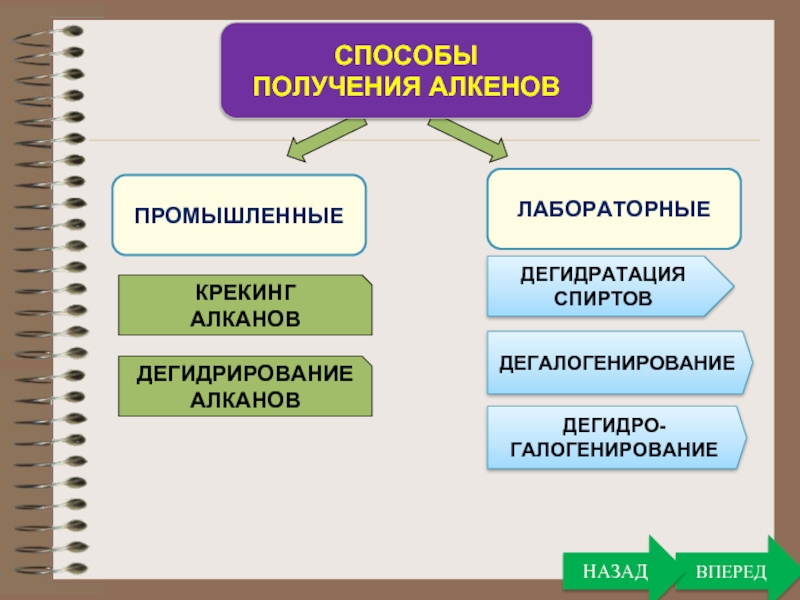
Слайд 20
ПРОМЫШЛЕННЫЕ
СПОСОБЫ
ПОЛУЧЕНИЯ АЛКЕНОВ
ЛАБОРАТОРНЫЕ
КРЕКИНГ
АЛКАНОВ
ДЕГИДРИРОВАНИЕ
АЛКАНОВ
ДЕГИДРАТАЦИЯ
СПИРТОВ
ДЕГАЛОГЕНИРОВАНИЕ
ДЕГИДРО-
ГАЛОГЕНИРОВАНИЕ
ВПЕРЕД
НАЗАД
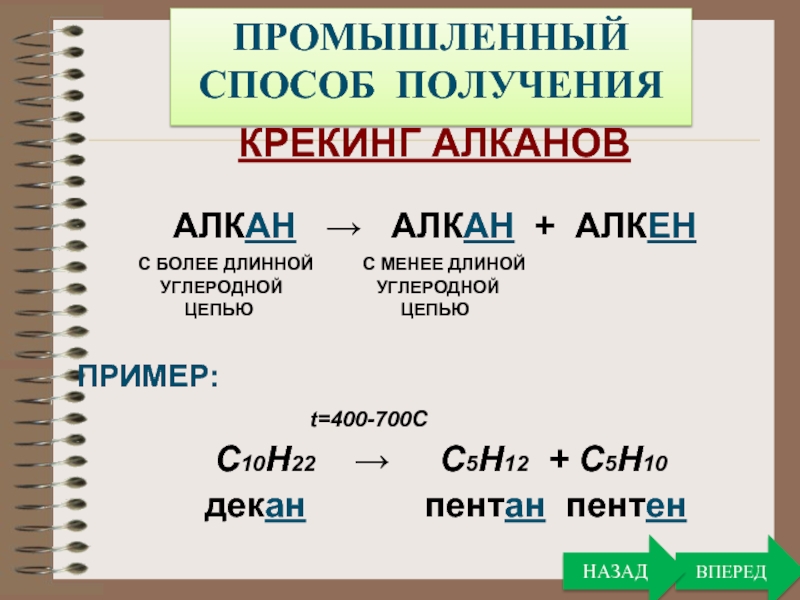
Слайд 21ПРОМЫШЛЕННЫЙ
СПОСОБ ПОЛУЧЕНИЯ
КРЕКИНГ АЛКАНОВ
АЛКАН → АЛКАН + АЛКЕН
С БОЛЕЕ ДЛИННОЙ
С МЕНЕЕ ДЛИНОЙУГЛЕРОДНОЙ УГЛЕРОДНОЙ
ЦЕПЬЮ ЦЕПЬЮ
ПРИМЕР:
t=400-700C
С10Н22 → C5H12 + C5H10
декан пентан пентен
ВПЕРЕД
НАЗАД
Слайд 22ПРОМЫШЛЕННЫЙ
СПОСОБ ПОЛУЧЕНИЯ
ДЕГИДРИРОВАНИЕ АЛКАНОВ
АЛКАН → АЛКЕН + ВОДОРОД
ПРИМЕР:
Н3С - СН3 → Н2С = СН2 + Н2
этан этен
(этилен)
ВПЕРЕД
НАЗАД
Слайд 23ЛАБОРАТОРНЫЙ
СПОСОБ ПОЛУЧЕНИЯ
ДЕГИДРАТАЦИЯ СПИРТОВ
СПИРТ → АЛКЕН + ВОДА
ПРИМЕР:
t≥140C,
Н Н Н2SO4(конц.)Н-С – С-Н → Н2С = СН2 + Н2О
Н ОН этен
(этилен)
ВПЕРЕД
НАЗАД
Слайд 24ЛАБОРАТОРНЫЙ
СПОСОБ ПОЛУЧЕНИЯ
ДЕГАЛОГЕНИРОВАНИЕ
ПРИМЕР:
t
Н2С – СН2 + Zn → Н2С = СН2 + ZnBr2
Br Br этен
1,2-дибромэтан (этилен)
ВПЕРЕД
НАЗАД
Слайд 25ЛАБОРАТОРНЫЙ
СПОСОБ ПОЛУЧЕНИЯ
ДЕГИДРОГАЛОГЕНИРОВАНИЕ
УДАЛИТЬ ВОДОРОД
ГАЛОГЕН ДЕЙСТВИЕ
ПРИМЕР:
спиртовойH H раствор
Н-С–С-Н+KOH→Н2С=СН2+KCl+H2O
Н Cl этен
хлорэтан (этилен)
ВПЕРЕД
НАЗАД
Слайд 29Получение АЛКИНОВ
1) В промышленности ацетилен получают высокотемпературным пиролизом метана.
1500ºС
2CH4 → HC≡CH + 3H2
2) Дегидрирование алканов
CH3 – CH3 (Ni, t)↔ 2H2 + CH ≡ CH
3) Ацетилен получают карбидным способом при разложении карбида кальция водой.
CaC2 + 2H2O → Ca(OH)2 + HC≡CH
ВПЕРЕД
НАЗАД
Слайд 304) Алкины можно получить дегидрогалогенированием
дигалогенопроизводных парафинов. Атомы
галогена при этом могут
быть расположены как у соседних атомов углерода, так и у
одного углеродного атома.СH3–CH(Br)–CH2(Br) + 2 KOH→CH3–C≡CH +
+ 2KBr + 2H2O спирт. р-р
CH3–C(Br2)–CH2–CH3+2KOH→CH3–C≡C–CH3+ 2KBr + 2H2O спирт. р-р
Получение АЛКИНОВ
ВПЕРЕД
НАЗАД
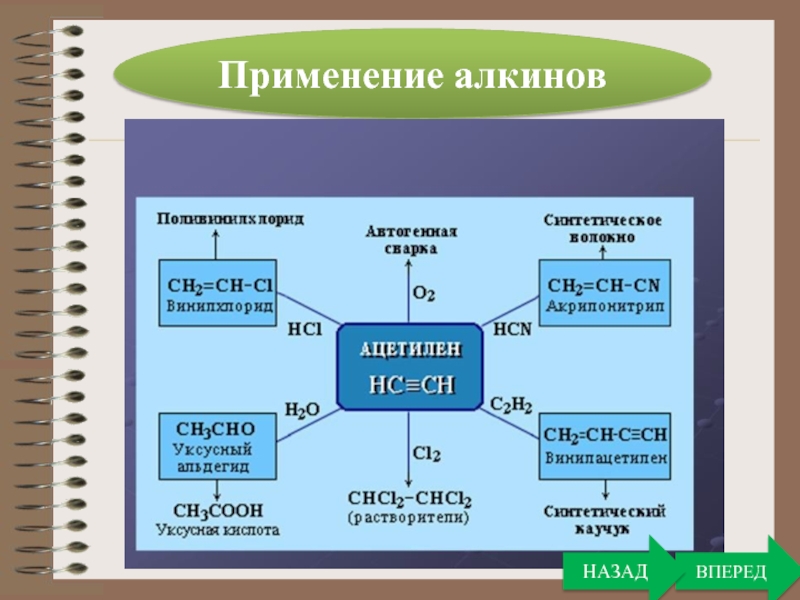
Слайд 32Ранее ацетилен широко применялся для создания высокотемпературного пламени при газовой
сварке. Сейчас на первый план вышло его применение для целей
органического синтеза.Получение растворителей. При присоединении хлора к ацетилену получается тетрахлорэтан а отщеплением от последнего молекулы хлороводорода — 1,1,2-трихлорэтен. Оба этих вещества являются весьма ценными и широко применяемыми растворителями.
Полимеры. Из ацетилена получают, в частности, поливинил-хлорид.
Поливинил-хлорид очень широко применяется в промышленности и в быту.
Применение алкинов
ВПЕРЕД
НАЗАД