оболочки
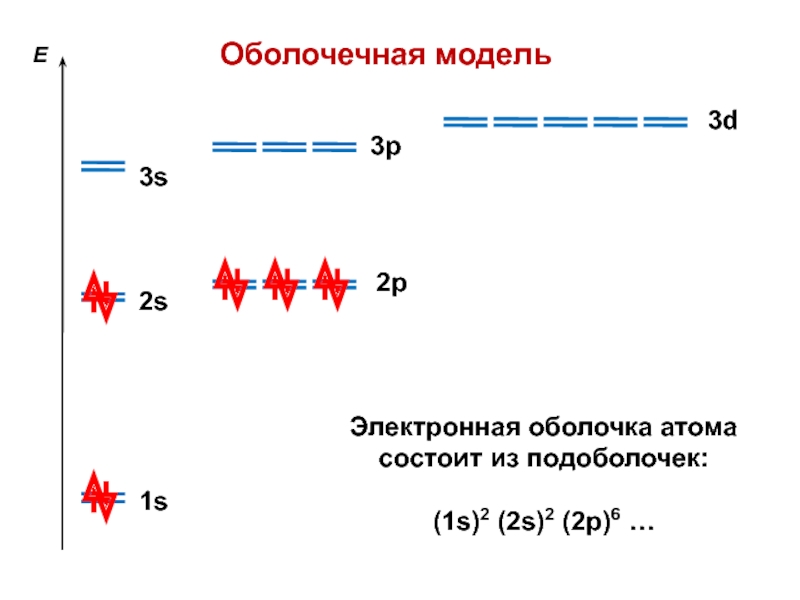
( n, )ν, где ν — заселенность
(число электронов) 1s-оболочка ( νмакс. = 2 )
2s-оболочка ( νмакс. = 2 )
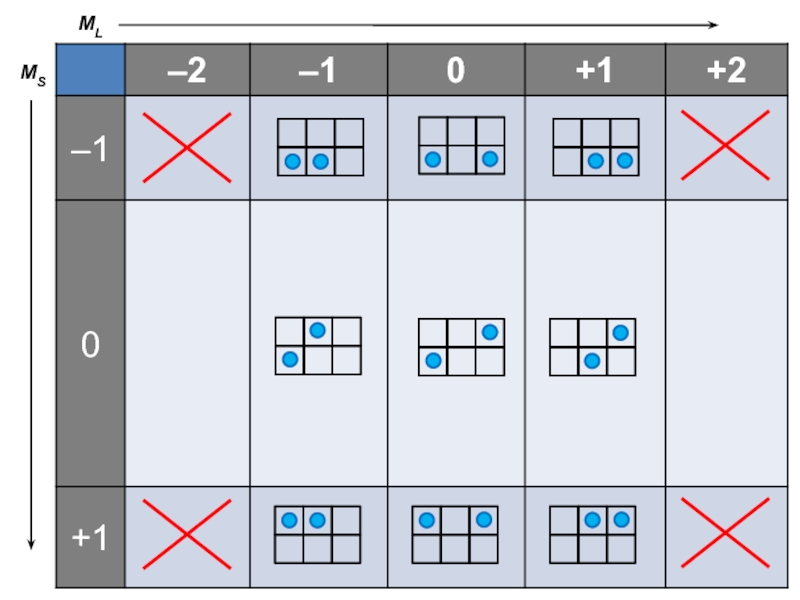
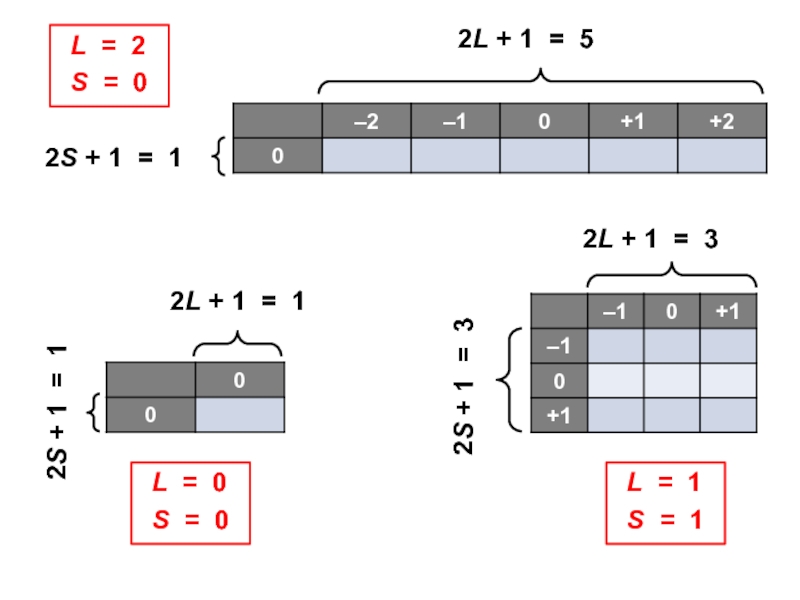
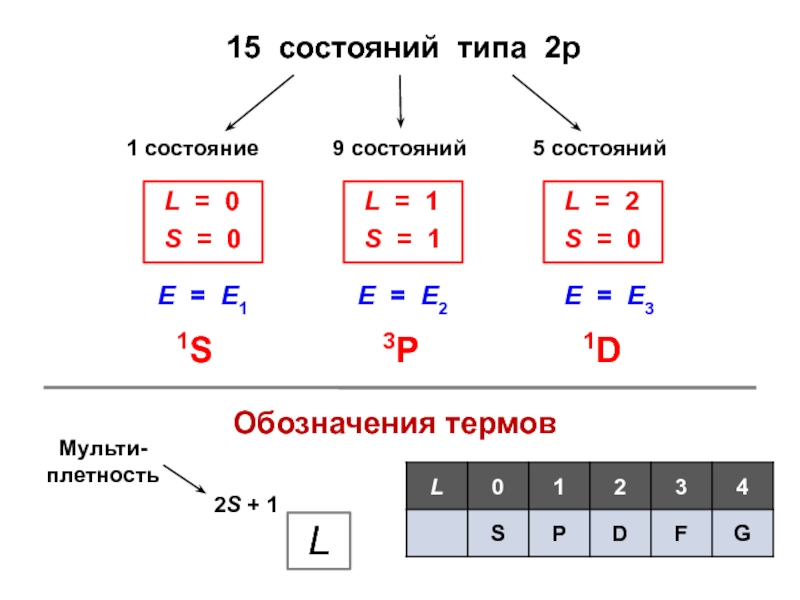
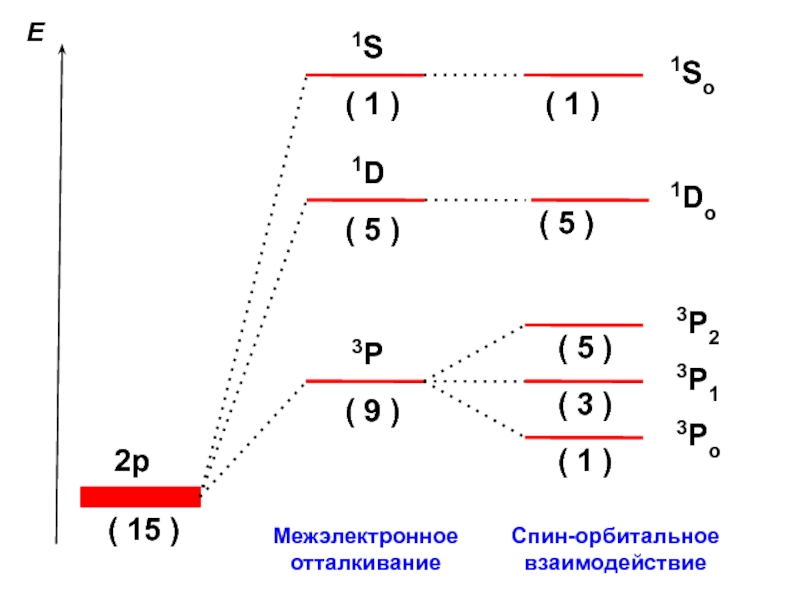
2p-оболочка ( νмакс. = 6 )
3p-оболочка ( νмакс. = 6 )
3s-оболочка ( νмакс. = 2 )
3d-оболочка ( νмакс. = 10 )