Слайд 1 Биологическое Окисление -2
лекция
Слайд 2Содержание:
1.Пути утилизации килорода в организме.
2. Структура и функции
дыхательной цепи (ДЦ) митохондрий.
3.Окислительное фосфорилирование(ОФ)
4.Значение тканевого обмена в биоэнергетике
5.Микросомальное
окисление
6.Понятие о перекисных процессах.
Слайд 3Пути утилизации кислорода в организме
В организме существуют три пути потребления
и утилизации кислорода.
1 путь: 90-95% О2 идет на митохондриальное окисление
2
путь: 5-10% О2 идет на микросомальное окисление( в печени при поступлении токсинов)
3 путь: перекисное окисление 2-5%
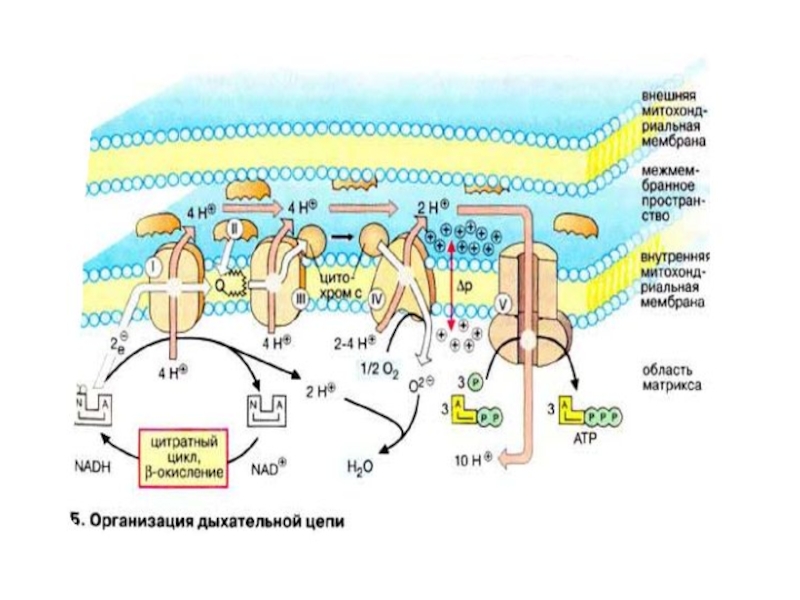
Слайд 4 В процессе окисления СН3-СО-SКоА в ЦТК, восстановленные формы NADH2
и FADH2, поступают в ДЦ, где энергия электронов и
Н+, трансформируется в энергию макроэргических связей АТФ.
ДЦ - это совокупность дегирогеназ (ДГ), которые транспортируют электроны и Н+. c S( субстратов) на О2.
Слайд 7 Принципы функционирования ДЦ основаны на I и
II законах термодинамики.
1 закон- сохранения энергии
2 закон –▲G = ▲ H- Т▲S,
где G-энергия Гиббса
Слайд 8
Все системы стремятся к состоянию с
минимумом энергии ( Е), выделяющаяся энергия приводит к энтропии.
Движущей силой ДЦ является разность ОВП. Суммарная разность всей ДЦ составляет 1.1 вольта
Слайд 9
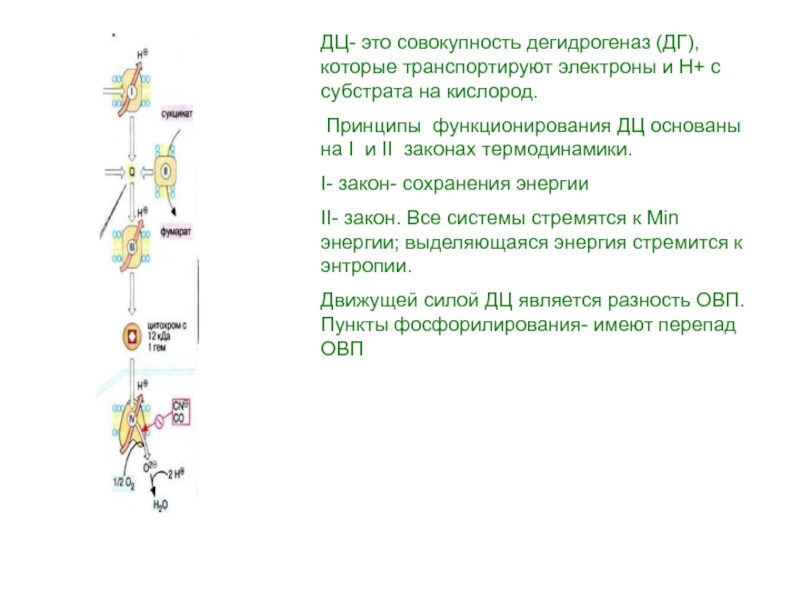
ДЦ- это совокупность дегидрогеназ (ДГ), которые транспортируют электроны и Н+
с субстрата на кислород.
Принципы функционирования ДЦ основаны на I
и II законах термодинамики.
I- закон- сохранения энергии
II- закон. Все системы стремятся к Min энергии; выделяющаяся энергия стремится к энтропии.
Движущей силой ДЦ является разность ОВП. Пункты фосфорилирования- имеют перепад ОВП
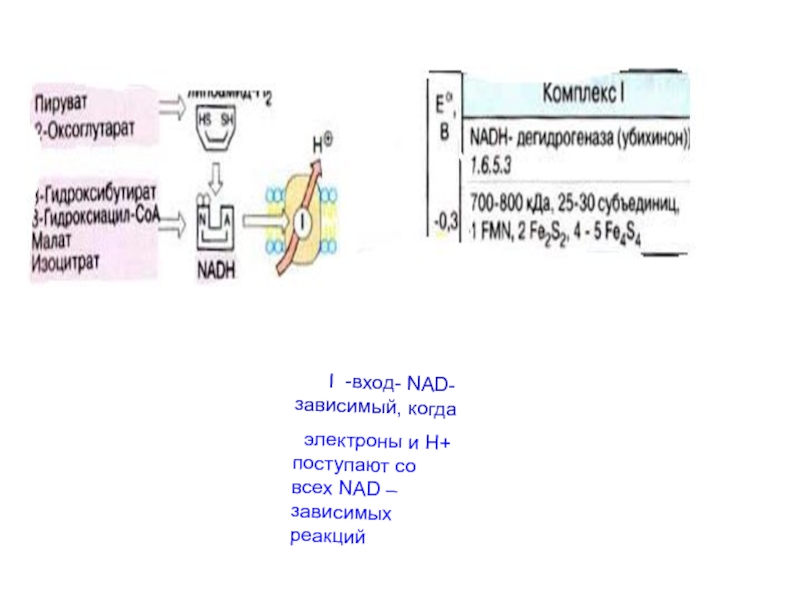
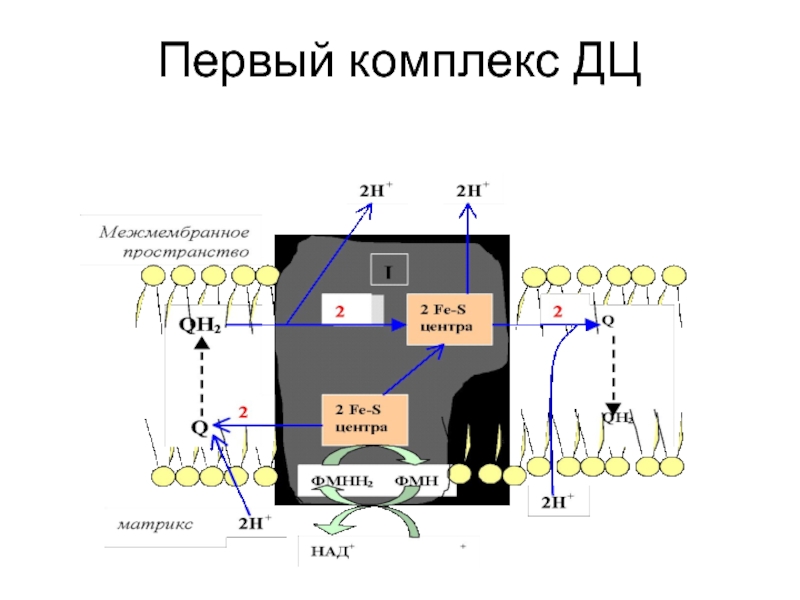
Слайд 10 I -вход- NAD- зависимый, когда
электроны и
Н+ поступают со всех NAD –зависимых реакций
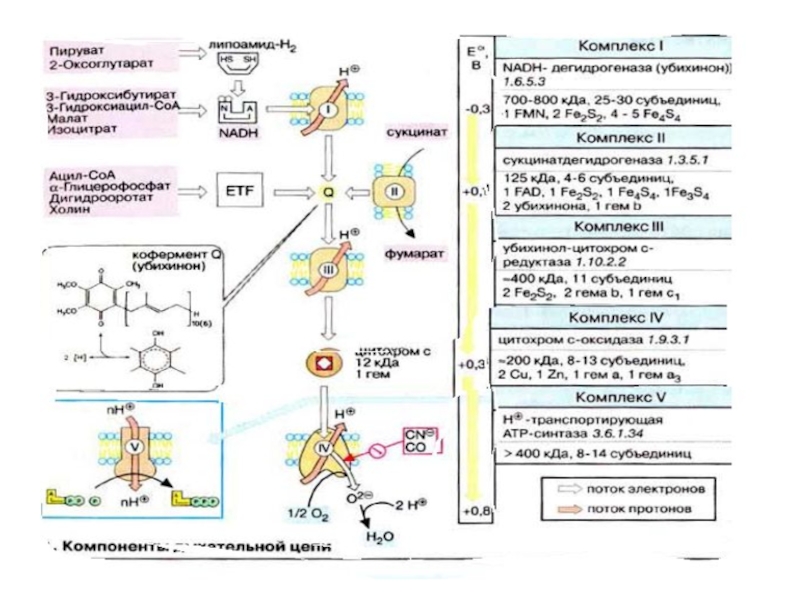
Слайд 11 Электроны, передаваемые НАДН (NADH), не переносятся прямо на
кислород.
Они проходят по меньшей мере десять промежуточных
окислительно-восстановительных систем, большинство из которых это связанные простетические группы в комплексах I, III и IV.
Прежде всего поражает большое число коферментов, принимающих участие в переносе электронов.
Слайд 12 Изменение свободной энергии ΔG в реакциях
восстановления зависит только от разности окислительно-восстановительных потенциалов донора и акцептора.
Наличие дополнительных окислительно-восстановительных систем между НАДН и О2 не приводит к изменению свободной энергии реакции
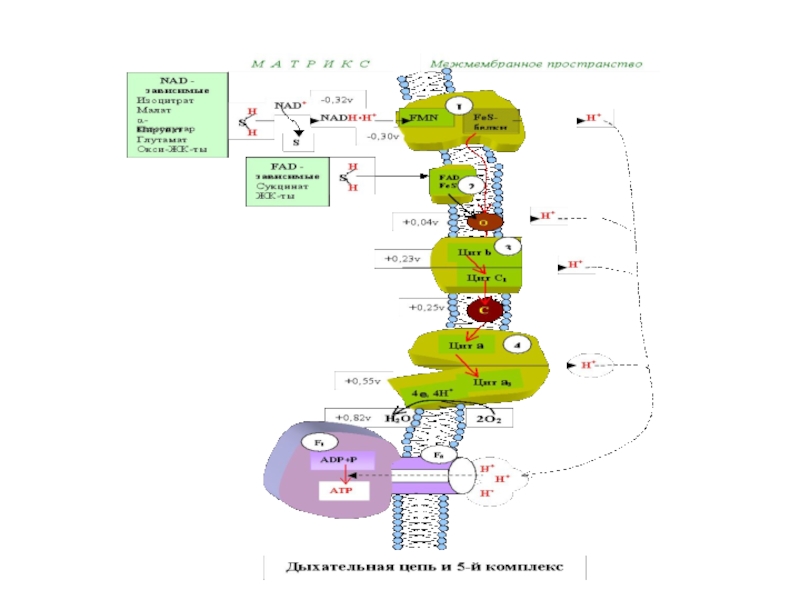
Слайд 13 В дыхательной цепи электроны переносятся
от НАДН или убихинона (QH2) на О2. Выделяющаяся энергия используется
для создания протонного градиента на внутренней митохондриальной мембране. Синтез АТФ сопряжен с обратным потоком протонов из межмембранного пространства в матрикс.
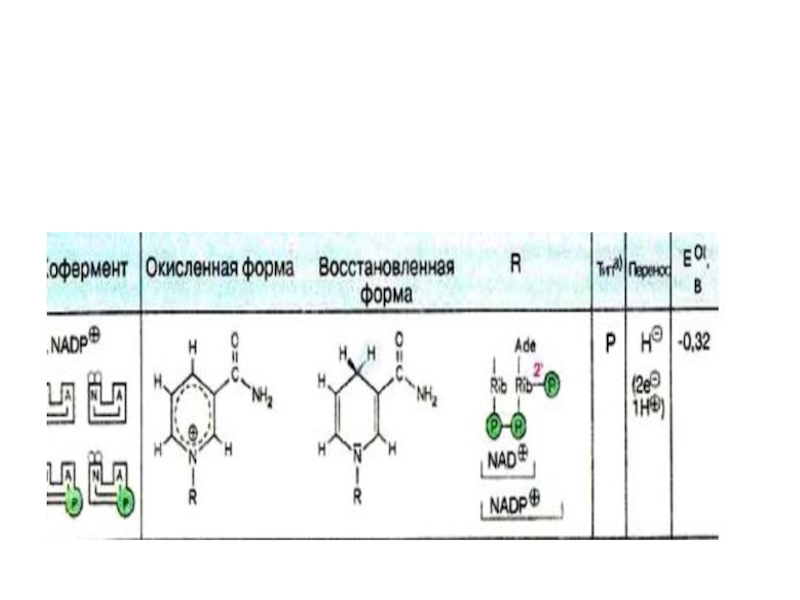
Слайд 15
H+ + 2e-
Ribose
Adenine
Nicotinamide
Ribose
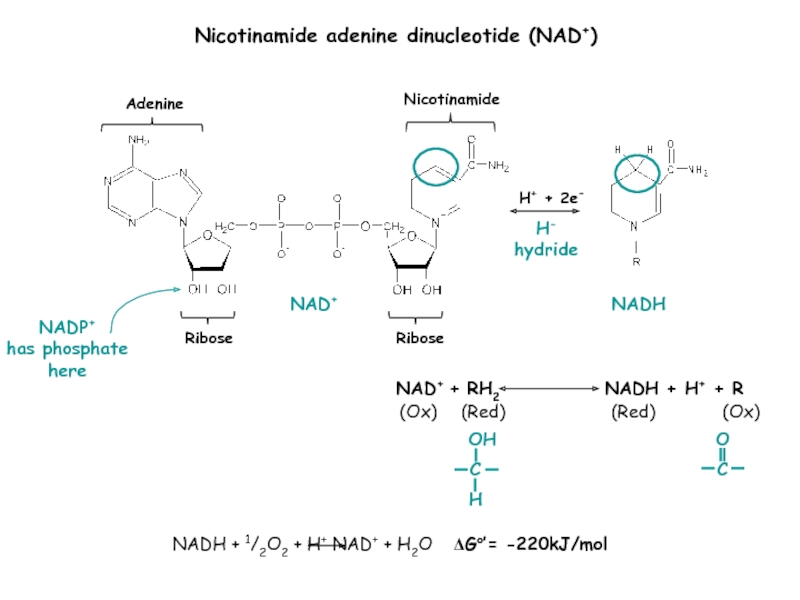
Nicotinamide adenine dinucleotide (NAD+)
NAD+ + RH2
NADH +
H+ + R
(Ox)
(Red)
(Ox)
(Red)
NADP+
has phosphate
here
NADH + 1/2O2 + H+ NAD+ +
H2O ΔGo’= -220kJ/mol
NAD+
H-
hydride
NADH
OH
C
C
O
H
Слайд 16
Окисление НАДН (NADH) комплексом I
происходит на внутренней стороне мембраны, а также в матриксе, где
протекает также цитратный цикл и β-окисление — самые важные источники НАДН.
Слайд 17 В матриксе митохондрий протекают, кроме того, восстановление
O2 и образование АТФ.
Полученный АТФ переносится
по механизму антипорта (против АДФ) в межмембранное пространство откуда через порины проникает в цитоплазму
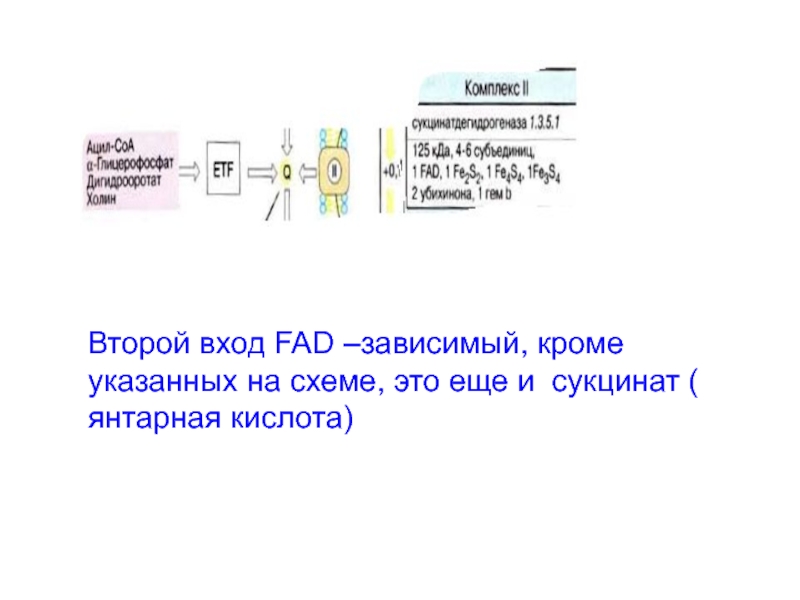
Слайд 18Второй вход FAD –зависимый, кроме указанных на схеме, это еще
и сукцинат ( янтарная кислота)
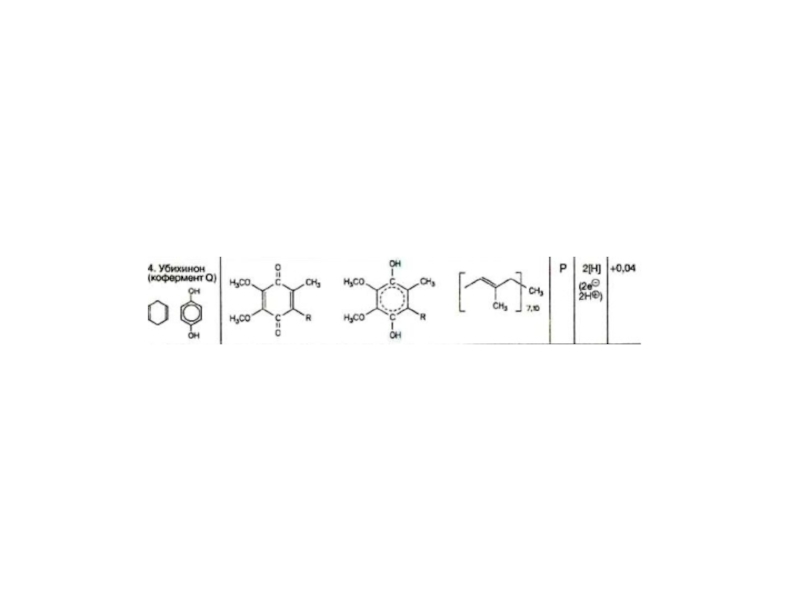
Слайд 19
Кофермент Q или убихинон гидрофобное соединение, является компонентом клеточных мембран.
Содержится в большой концентрации на наружной поверхности мембран.
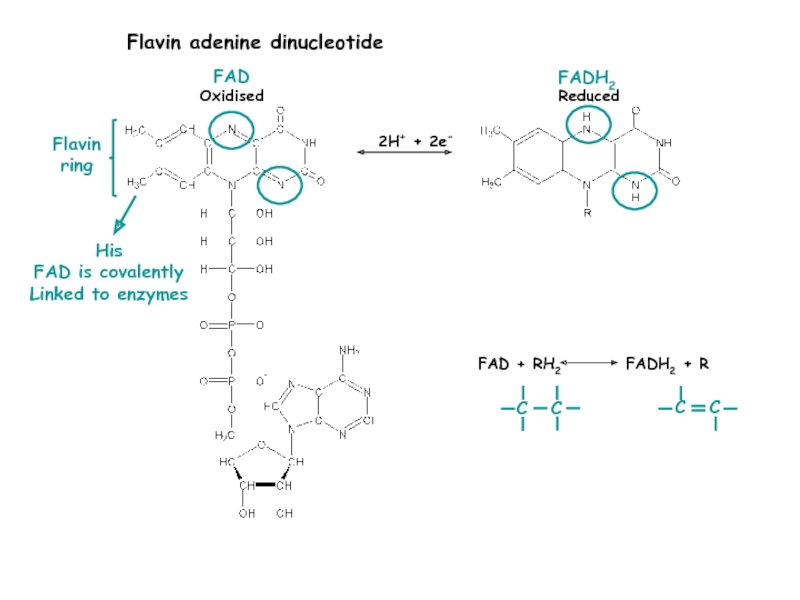
Слайд 212H+ + 2e-
Flavin adenine dinucleotide
Oxidised
Reduced
FAD
FADH2
Flavin
ring
His
FAD is covalently
Linked to enzymes
FAD +
RH2
FADH2 + R
Слайд 23
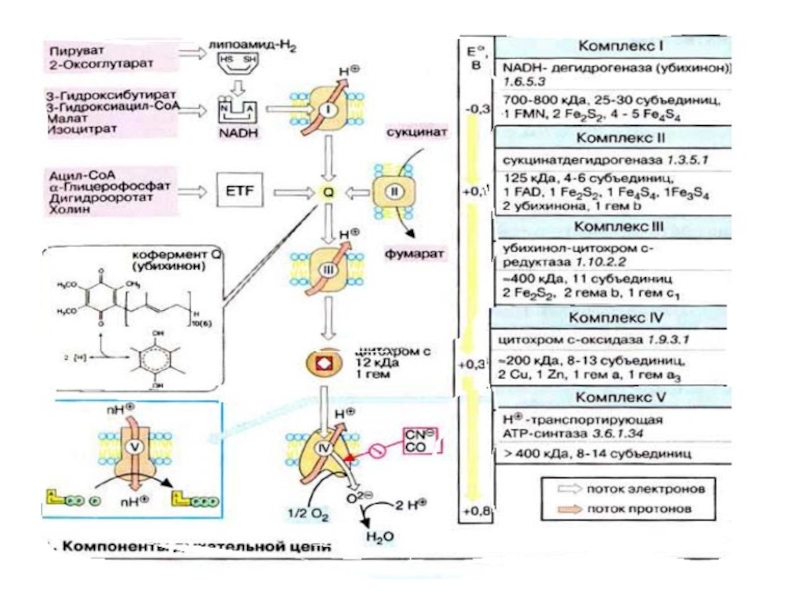
В комплексе I электроны переносятся от
НАДН на ФМН (FMN), а затем на железосодержащие белки (Fe/S-центры).
Эти окислительно-восстановительные системы стабильны только в составе молекул белков. Они могут содержать от 2 до 6 ионов железа, образующих комплексы различного состава с неорганическим сульфидом и SH-группами остатков цистеина.
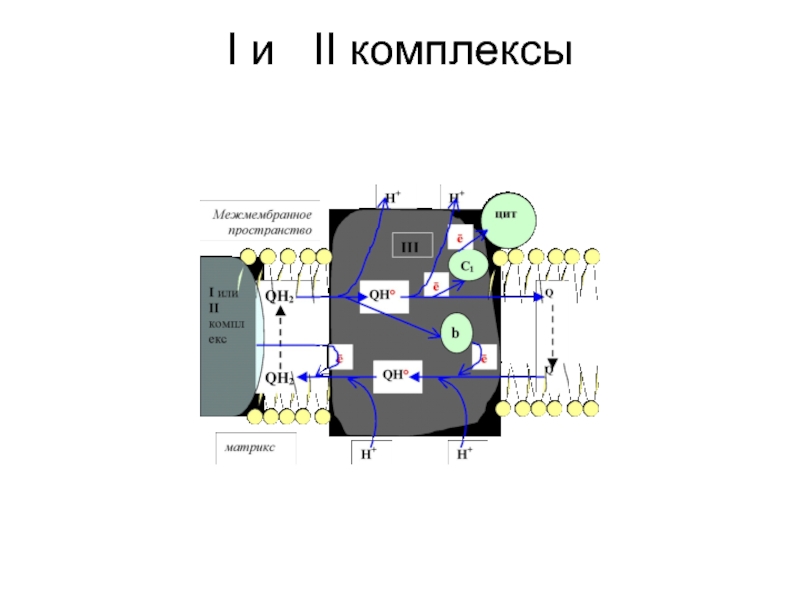
Слайд 24
Как уже упоминалось, все комплексы с I
по V интегрированы во внутренней мембране митохондрий, тем не менее
обычно они не контактируют друг с другом, так как электроны переносятся убихиноном и цитохромом с.
Слайд 25
Убихинон благодаря неполярной боковой цепи свободно перемещается в
мембране. Водорастворимый цитохром с находится на внешней стороне внутренней мембраны.
Слайд 27
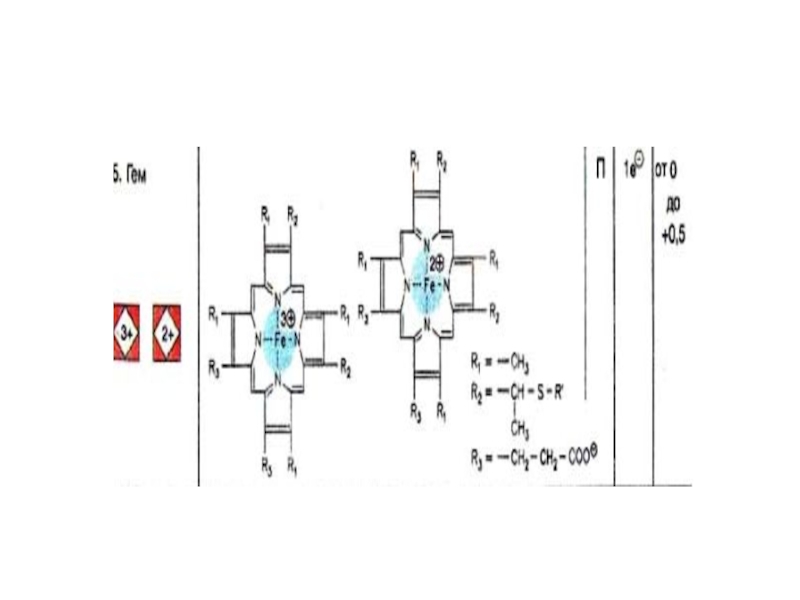
В переносе электронов принимают участие различные типы гемов. Гемы
типа b соответствуют гемоглобинам.
Слайд 28
Гем с ковалентно связан с белком, в
то время как тетрапиррольное кольцо гема а изопренилировано и несет
формильную группу. В комплексе IV непосредственно с кислородом взаимодействуют ион меди (CuB) и гем а3.
Слайд 31
Перенос протонов комплексами I, III и IV протекает
векторно из матрикса в межмембранное пространство. При переносе электронов в
дыхательной цепи повышается концентрация ионов H+, т. е. понижается значение рН.
Слайд 32 В интактных митохондриях по существу только АТФ-синтаза позволяет
осуществить обратное движение протонов в матрикс. На этом основано важное
в регуляторном отношении сопряжение электронного переноса с образованием АТФ.
Слайд 33
Общая величина энергии реакции (более 200
кДж/моль) разбивается на небольшие и более удобные комплексы, величина которых
определяется разностью окислительно-восстановительных потенциалов соответствующих промежуточных продуктов.
Слайд 34
Предполагается, что это разделение на комплексы обеспечивает
дыхательной цепи удивительно высокий выход энергии, составляющий примерно 60%.
Слайд 36 На схеме представлены основные окислительно-восстановительные системы митохондриального
электронного транспорта и их приблизительные окислительно-восстановительные потенциалы
Слайд 37
Эти потенциалы важны для переноса электронов, так
как для обеспечения спонтанного переноса члены окислительно-восстановительного ряда должны располагаться
в порядке возрастания потенциалов
Слайд 38 Т.о. работа ДЦ состоит в том,
что молекулы NAD.H и FAD.H переносят е от S
на О2. Причем эта реакция равноценна сгоранию Н2 на воздухе с образованием воды.
Объектом переноса являются не Н+, а е,т.к. протоны остаются в водном растворе и могут акцептироваться из него по мере необходимости. Перенос е сопровождается умножением Е, на каждой ступени, вплоть до конца,
Слайд 39 е соединятся с О2, диффундирующим через мембрану
МХ.
Связываясь с О2, который имеет мах. сродство к
е, сам е оказывается на самом низком энергетическом уровне. А энергия,выделившаяся при этом, идет на перекачку Н+ из матрикса на наружную поверхность внутренней мембраны Мх. Так создается ▲µН+ , энергия которого трансформируется в макроэргическую связь АТФ.
Слайд 40 Основная масса Е, образующаяся в организме, формируется
в реакциях О/Ф. В сутки образуется около 30-70кг АТФ. Перенос
е возможен только в случае снятия Все системы стремятся к состоянию с минимумом энергии ( Е), выделяющаяся энергия приводит к энтропии.
Движущей силой ДЦ является разность ОВП. Суммарная разность всей ДЦ составляет 1.1 вольта ▲µН+, поскольку его накопление блокирует транспорт е по ДЦ., а значит блокирует синтез АТФ.
Слайд 41 В 1939г введен коэффициент Р/О как мера
количественной оценки работы ДЦ.
Р/О- отношение количества, поглощенных молекул
фосфата( в процесе реакции АДФ+Фн) к количеству, поглощенных атомов О2.
Слайд 42 Так при окислении NAD- зависимых субстратов-(
альфа-кетоглутарата,) е, в этом случае проходят все три пункта фосфорилирования
и на образование АТФ уходит 3 молекулы Фн на 1 атом О2, поэтому Р/О =3.
Слайд 43
Если окисляются FAD, зависимые субстраты( сукцинат,
ацил-КоА), то е, проходят всего 2 пункта фосфорилирования(3 и4) ,
и тратиться 2 молекулы Фн на 1 атом О2, поэтому Р/О= 2.
Vit C и адреналина, е поставляется прямо на цитохром с,
поэтому они проходят только один путь фосфорилирования(4), и Р/О =1.
Слайд 45 Работа всей ДЦ состоит из 2х составляющих:
1.Образование
АТФ( 50% энергии депонируется в виде АТФ).
2.Генерация тепла (остальные 50%
энергии рассеивается в виде тепла).
Для синтез АТФ требуется разница ОВП между переносчиками е и Н+ примерно 0.25V.
Слайд 46 Основная масса Е, образующаяся в организме, формируется
в реакциях О/Ф. В сутки образуется около 30-70кг АТФ. Перенос
е возможен только в случае снятия ▲µН+, поскольку его накопление блокирует транспорт е по ДЦ., а значит блокирует синтез АТФ.
Слайд 47Теория П.Митчелла
В 1961г. П.Митчелл предположил, что митохондрия работает как протонная
помпа, откачивая Н+ на наружную сторону ввнутренней мембраны митохондрий. При
этом на внутренней мембране митохондрий создается электрохимический потенциал-
▲ µН+.
Энергия этого потенциала трансформируется в энергию макроэргической связи АТФ.
Слайд 48 Дельта- ^µН+ имеет две составляющие:1.электрическую ^φ( создается за
счет движения е по ДЦ);
2. Осмотическоую- ^РН.
▲µН+ возникает
за счет «+» заряда на внешней поверхности внутренней мембраны митохондрии, а на внутренней поверхности –»-». За счет откачки Н+ из матрикса, последний защелачивается.
Слайд 49
В живых системах ▲µН+
= 180 мВольт.В пересчете на 1 см2 приходится 250 киловольт.
В гепатоците около 1000 митохондрий, в кардиоците 5000, Таким образом живая материя обладает огромным энергетическим запасом.
Слайд 50
В возбудимых тканях( миокард,
нервная) ▲µН+ представлена в виде ^φ, а в эпителии почечных
канальцев в виде ▲рН.
Слайд 51 Процесс фосфорилирования мембранного потенциала осуществляется с помощью
протонной АТФ-азы, т.е. фермента, способного трансформировать Е ^ ▲µН+ в
энергию АТФ. Однако этот процесс обратим:
▲ µН+ = АТФ.
Т.е. эта АТФ-аза может быть первичным протонным генератором.
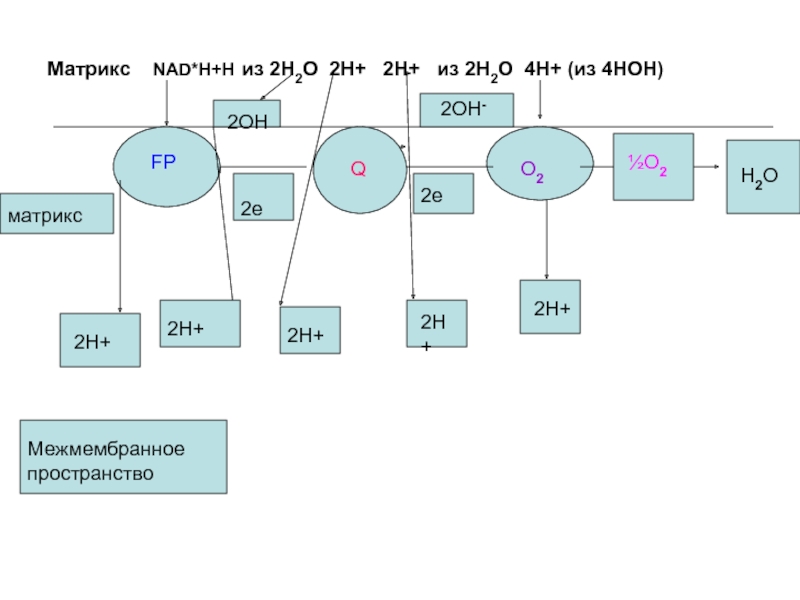
Слайд 52Матрикс NAD*H+H из 2Н2О 2Н+ 2Н+ из
2Н2О 4Н+ (из 4НОН)
½О2
Н2О
2е
2е
FP
Q
O2
2OH
2OH-
2H+
2H+
2H+
2H+
2H+
матрикс
Межмембранное пространство
Слайд 53Таким образом , мы видим три цикла:
флавиновый
убихиноновый
Кислородный
За пределы внутренней мембраны
выбрасывается 10Н+.
Для образования АТФ необходимы 6Н+(по 2на каждый шунт
фосфорилирования). Остальные протоны нужны для совершения осмотической работы митохондрий, для транспорта внутрь митохондрий ПВК, Фн, АДФ.
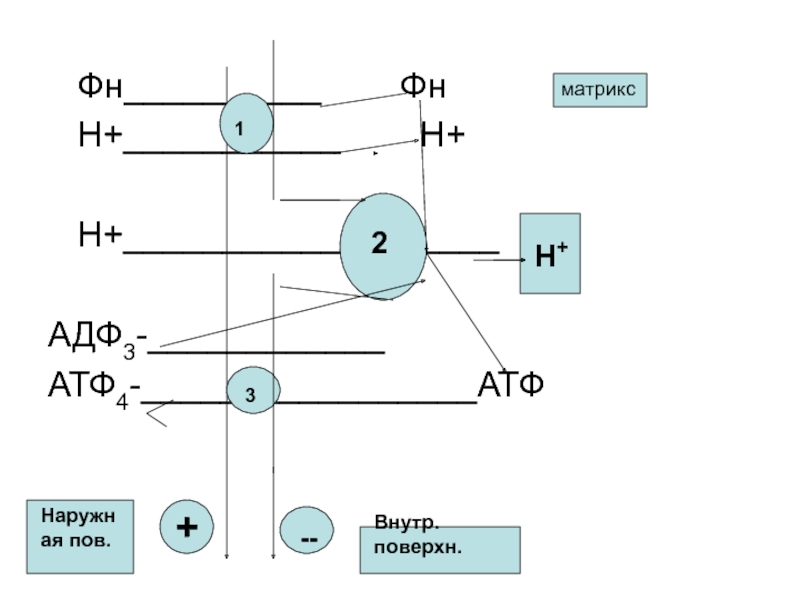
Слайд 54 Фн__________ Фн
Н+___________
Н+
Н+___________________
АДФ3-____________
АТФ4-_________________АТФ
1
3
H+
2
матрикс
+
--
Внутр. поверхн.
Наружная пов.
Слайд 55Протонная АТФ-аза видна как морфологическое образование в виде грибовидных выростов
на внутренней мембране митохондрий. Часть ▲µН+,
( т.е. часть Н+), выброшенных
за пределы митохондриального матрикса используется для обеспечения транспорта Фн, субстратов ЦТК, ЖК, аденилаттранслоказы. Другая часть расходуется на синтез АТФ.:
Слайд 56 Другая часть ^µН+ расходуется на синтез АТФ в
реакции:
АДФ 3- + Фн2- + Н+ ----? АТФ4-.
В цитоплазме происходит противоположная реакция:
АТФ4- ----? АДФ 3- + Фн2- + Н+.
Митохондрии работают путем связывания Н+ и снижения [Н+], - при этом происходит ощелачивание матрикса
Слайд 57 Всякая работа сопровождается гидролизом АТФ, что
ведет к образованию Н+ и закислению среды.
В большинстве случает метаболические нарушения связаны с нарушением реакций:
АТФ-синтетазной- поглощение Н+, и АТФ-азной( выделение Н+).
При окислении мембрана митохондрий заряжается, а при синтезе АТФ- разражатеся
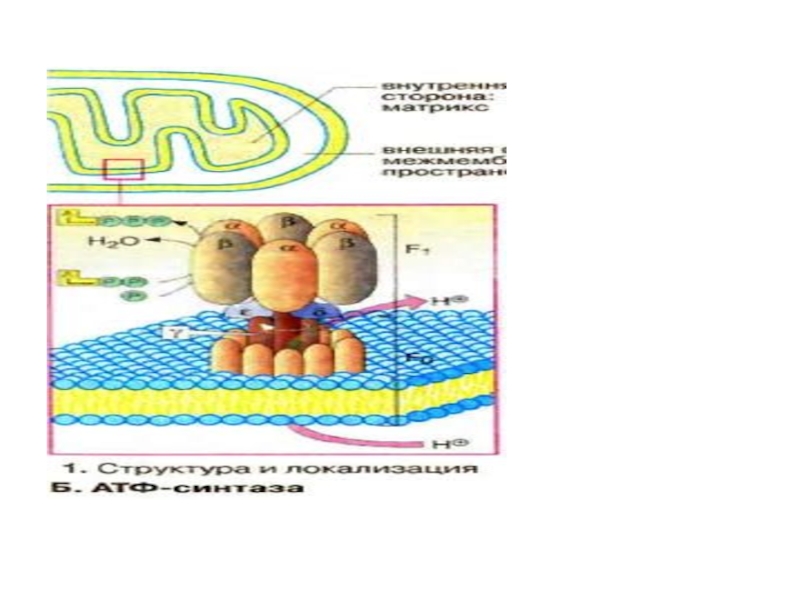
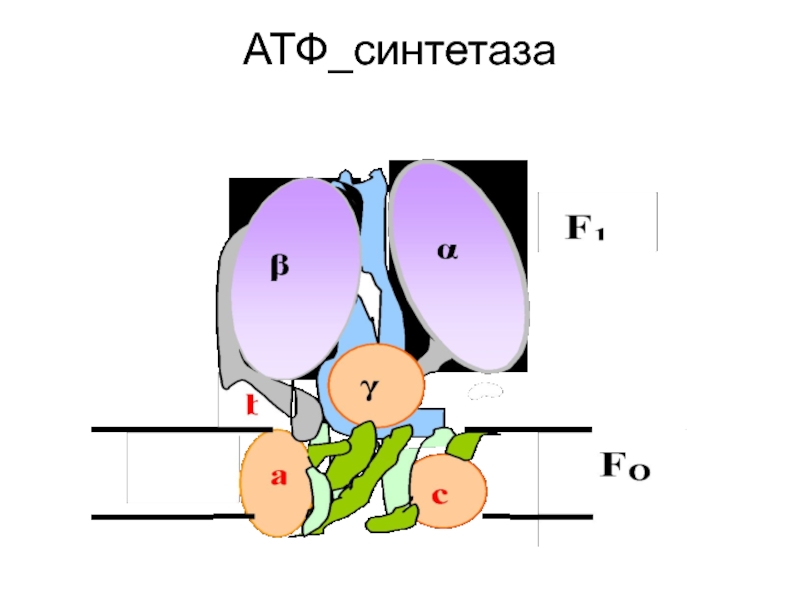
Слайд 60Н+-транслоцирующая АТФ-синтаза состоит из двух частей: встроенного в мембрану протонного
канала (F0) из по меньшей мере 13 субъединиц и каталитической
субъединицы (F1), выступающей в матрикс. «Головка» каталитической части образована тремя α- и тремя β-субъединицами, между которыми расположены три активных центра. "Ствол" структуры образуют полипептиды F0-части и γ-, δ- и ε-субъединиц головки.
Слайд 61 Дельта- ^µН+ имеет две составляющие:1.электрическую ^φ( создается за
счет движения е по ДЦ);
2. Осмотическоую- ^pН.
^µН+ возникает за
счет «+» заряда на внешней поверхности внутренней мембраны митохондрии, а на внутренней поверхности «–-». За счет откачки Н+ из матрикса, последний защелачивается.
Слайд 62
Если клетка не расходует
АТФ, едва ли в митохондриях имеется АДФ. В отсутствие АДФ,
АТФ-синтаза (3) не в состоянии использовать протонный градиент на внутренней митохондриальной мембране
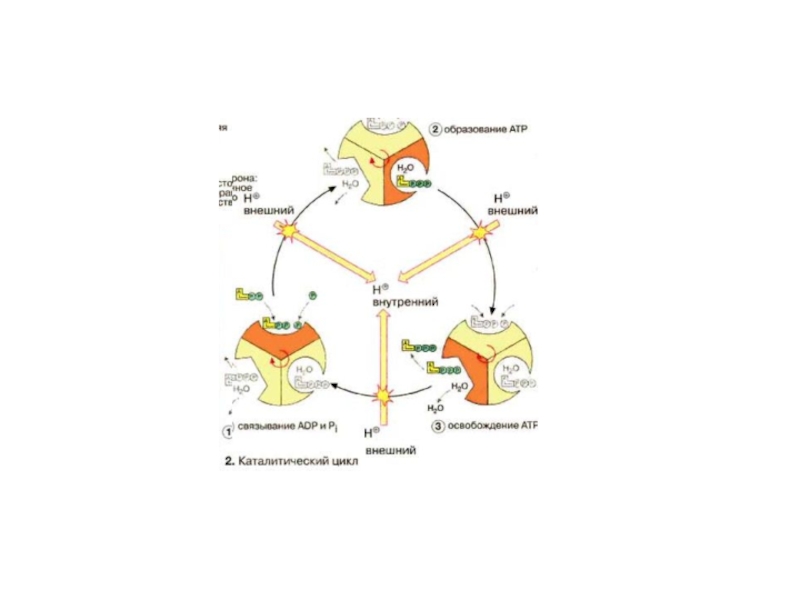
Слайд 63 Каталитический цикл подразделяется на три фазы, каждая из которых
проходит поочередно в трех активных центрах. Вначале идет связывание АДФ
(ADP) и Ρi (1), затем образуется фосфоангидридная связь (2) и, наконец, освобождается конечный продукт реакции (3). При каждом переносе протона через белковый канал F0 в матрикс все три активных центра катализируют очередную стадию реакции. Предполагается, что энергия протонного транспорта прежде всего расходуется на поворот γ-субъединицы, в результате которого циклически изменяются конформации α- и β-субъединиц.
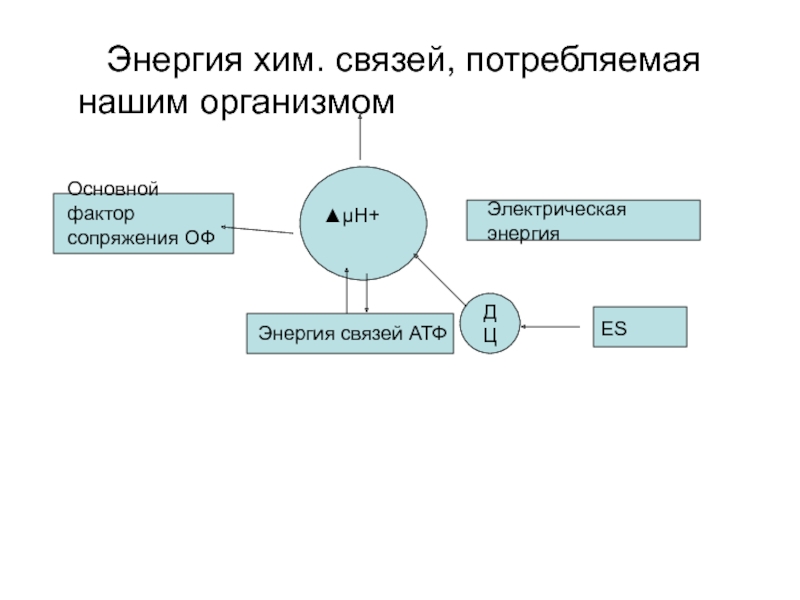
Слайд 66 Энергия хим. cвязей, потребляемая нашим организмом
▲μΗ+
Электрическая энергия
Основной фактор сопряжения ОФ
ДЦ
ЕS
Энергия связей АТФ
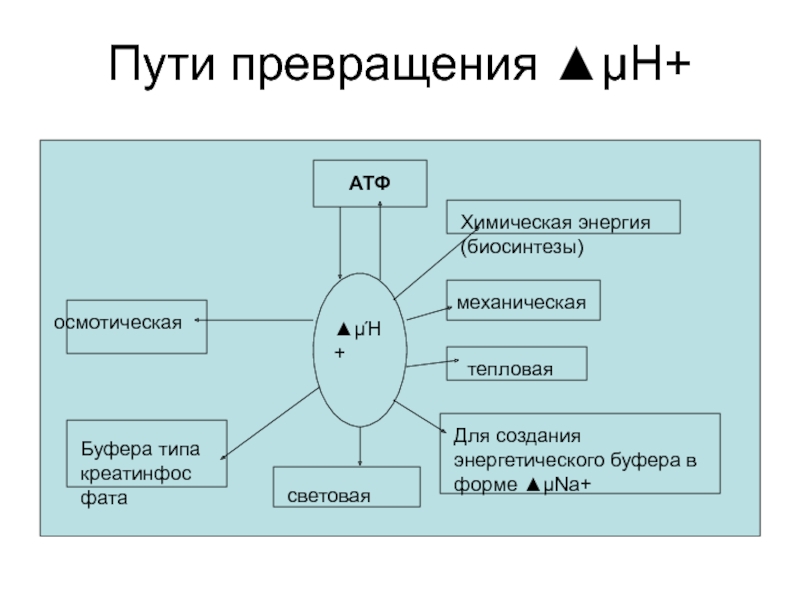
Слайд 67Пути превращения ▲μΗ+
АТФ
▲μΉ+
Химическая энергия (биосинтезы)
механическая
тепловая
Для создания энергетического буфера
в форме ▲μNa+
световая
Буфера типа креатинфосфата
осмотическая
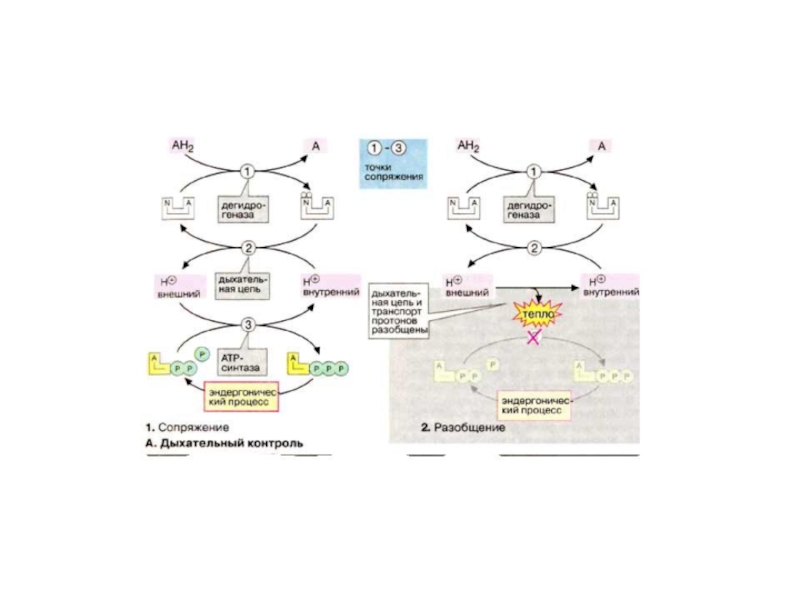
Слайд 68 Дыхательный контроль
Простой механизм
регуляции образования и потребления АТФ (АТР) называется дыхательным контролем. Он
основан на сопряжении упомянутых процессов с общими коферментами и другими факторами.
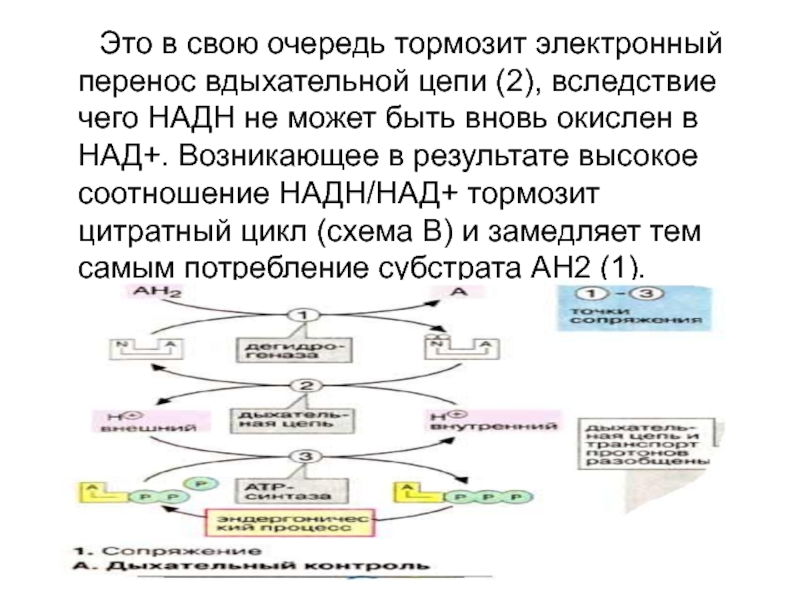
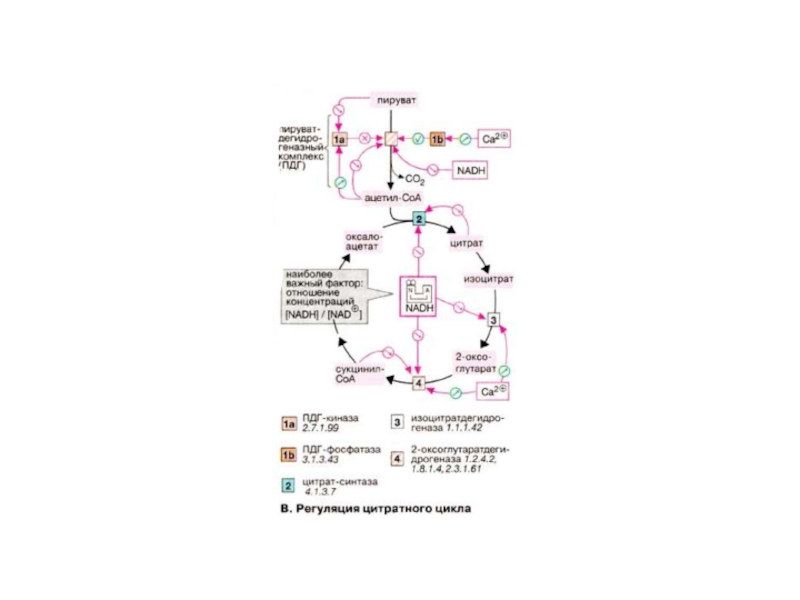
Слайд 69 Это в свою очередь тормозит электронный перенос
в ДЦ (2), вследствие чего НАДН не может быть вновь
окислен в НАД+. Возникающее в результате высокое соотношение НАДН/НАД+ тормозит цитратный цикл (схема В) и замедляет тем самым потребление субстрата АН2 (1). И наоборот, высокие скорости потребления АТФ стимулируют усвоение пищи и дыхательную цепь по тому же механизму.
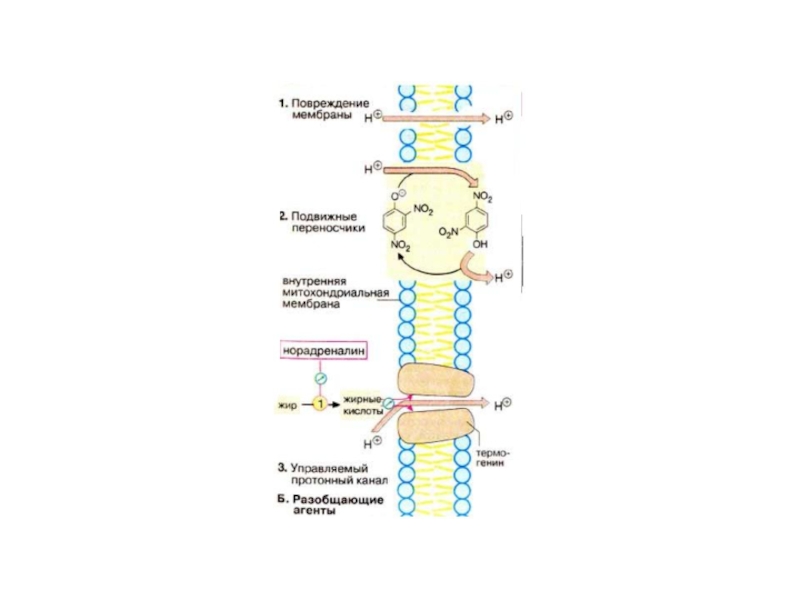
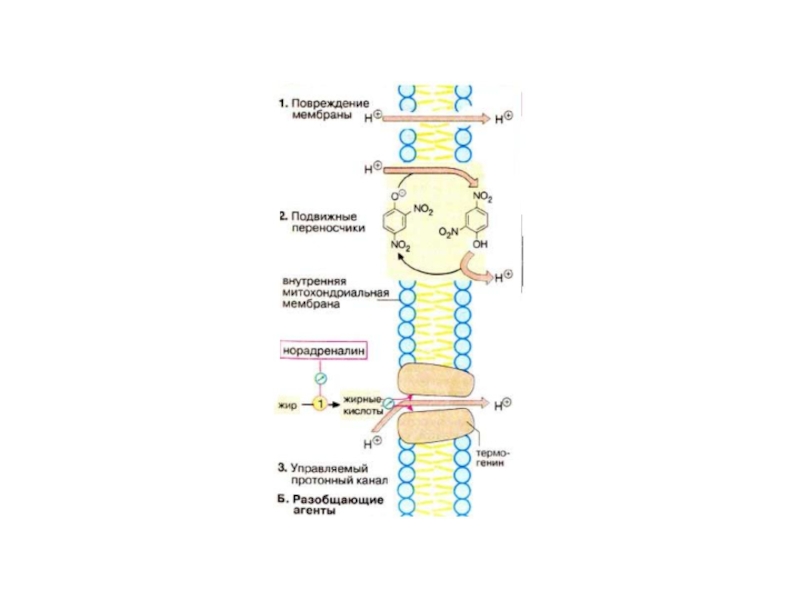
Слайд 70 Эффект разобщения О/Ф связан с тем, что,
Разобщители, являясь слабыми кислотами( следовательно хорошими акцепторами Н+), связывают протоны,
и увлекают их из митохондриального матрикса. Возникает дефицит Н+ на АТФ-азе и синтез АТФ блокируется.
Слайд 73
ДЦ активно реагирует
на чрезмерные нагрузки, яды. Так например барбитураты ингибируют пренос е
и Н+ в первом комплексе (I) ДЦ, в ответ на это возникает энергетический голод , т.к. происходит
недогрузка ДЦ.
Слайд 74
В результате снижается
синтез АТФ, и в тканях активируется производство и окисление эндогенной
янтарной кислоты( побочные продукты ГАМК и ГОМК- тормозные медиаторы для ЦНС).
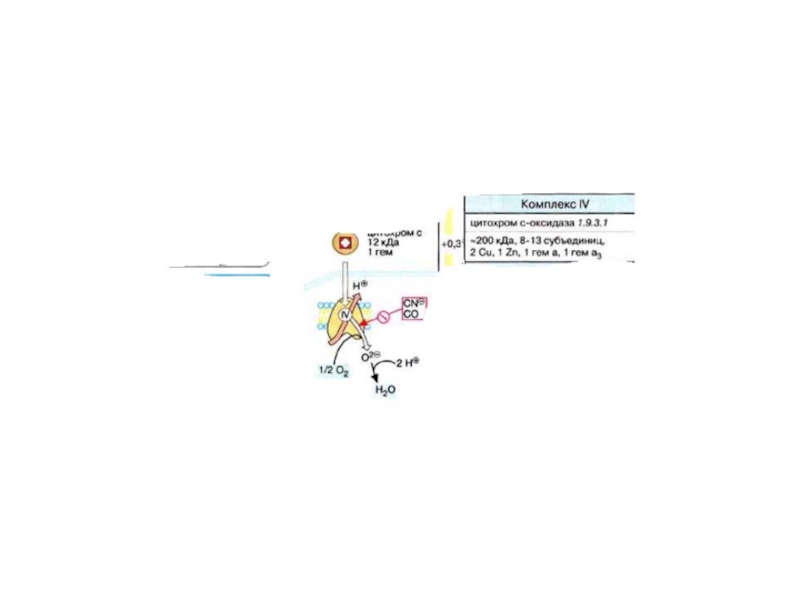
Слайд 75 Такие яды как цианиды, СО, Н2S,-SNC блокируют 4-комплекс
ДЦ. Если ингибирование 1 комплекса ДЦ приводит к активации 3-х
оставшихся, и за счет этого работа ДЦ компенсируется, то при блокировании 4-го комплекса работа ДЦ не состоится, что приводит к смерти.
Слайд 76 Аналогичным эффектом обладает алкоголь, который является NAD-
зависимым субстратом. Этанол монополизирует основной фонд NAD+, переводя его в
восстановленную форму. ДЦ перезагружается избытком восстановленной формы NADH2, и ткани не получают энергию за счет окисления естественных субстратов.
Слайд 77
Если ингибирование 1 комплекса ДЦ приводит
к активации 3х оставшихся,и за счет этого работа ДЦ компенсируется,
то при блокаде 4-го комплекса, работа ДЦ вообще не состоится, что приводит к смерти.
Слайд 78 Регуляция энергетического обмена
Биохимический
процесс усвоения пищи и образования АТФ должны постоянно приспосабливаться к
изменению энергетических потребностей клеток. Необходимость согласования производства и потребления АТФ следует уже из того факта, что суммарное содержание коферментов в организме незначительно.
Слайд 79
Калорийность суточного рациона человека составляет
примерно 12000 кДж .При к.п.д. 50% такая энергия достаточна для
образования 120 молей АТФ, т. е. примерно 65 кг.
Слайд 80 Однако в организме человека содержится всего 3-4
г свободных адениновых нуклеотидов (АМФ, АДФ и АТФ). Следовательно, каждая
молекула АДФ должна ежедневно тысячекратно фосфорилироваться в АТФ и вновь дефосфорилироваться
Слайд 81 Это в свою очередь тормозит электронный перенос
вдыхательной цепи (2), вследствие чего НАДН не может быть вновь
окислен в НАД+. Возникающее в результате высокое соотношение НАДН/НАД+ тормозит цитратный цикл (схема В) и замедляет тем самым потребление субстрата АН2 (1).
некоторые пункты фосфорилирования могут « выключаться» такое состояние называется «разобщением»
окислительного фосфорилирования, и в этом случае Р/О снижается.
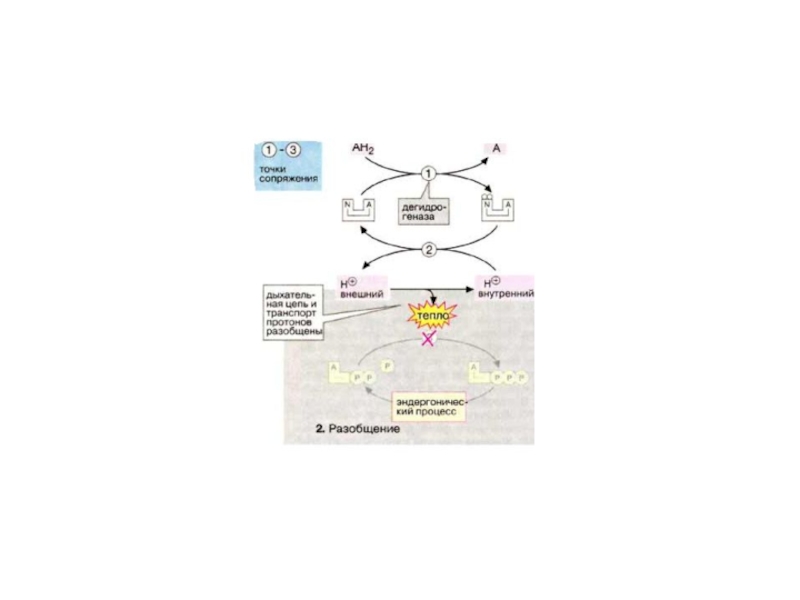
Слайд 84В «разобщенных» митохондриях, согласно I закону термодинамики, увеличивается теплообразование. Это
происходит за счет того, что энергия переноса е, которая должна
быть использована для синтеза АТФ, в выключенном пункте фофорилирования, рассеивается в виде тепла.
Слайд 85
В качестве разобщителей О/Ф выступают слабые гидрофобные кислоты(
ЖК ), тиреоидные гормоны, лекарства, дикумарин, динитрофенол, валимицин.
Слайд 86Процесс разобщения О/Ф лежит в основе лихорадки, вызванной бактериями, вирусами
и другими агентами.
Разобщение резко усиливается при охлаждении организма.
Работа митохондрий
при всех включенных пунктах фосфорилирования называется сопряженной.
В противном, выше описанном случае- разобщения., дыхание при этом будет
С В О Б О Д Н Ы М.
Слайд 87ДЦ имеет механизм шунтирования: сброс е и Н+ с NAD
на цитохромы, или с NAD на цитохромы, или с NAD
на межмембранные дегидрогеназы, на наружную мембрану и гладкую ЭПС( микросомальное окисление).
Такой перенос характерен для гепатоцитов, При воздействии какого -либо блокатора, возникает блок в I комплексе ДЦ, увеличивается NADH2, и становится реальной угроза гипоксии.
Чтобы этого не произошло происходит сброс
NADH2 с митохондриальной ДЦ на микросомальную.
Слайд 88 Эффект разобщения О/Ф связан с тем, что,
Разобщители, являясь слабыми кислотами( следовательно хорошими акцепторами Н+), связывают протоны,
и увлекают их из митохондриального матрикса. Возникает дефицит Н+ на АТФ-азе и синтез АТФ блокируется.
Слайд 91Итак -типы клеточного дыхания
1.Энергетически сопряженное дыхание, имеющее мак.
Р/О, поскольку при этом образуется ^µН+, энергия которого используется для
выполнения полезной работы.
Слайд 92
2.Несопряженнное дыхание, свойственное буровой жировой ткани. В
этом случае при дыхании энергия не депонируется в форме ▲
µН+, а диссипируется в виде тепла.
Слайд 93
3. Разобщенное дыхание, при котором часть энергии
▲ µН+ рассеивается в виде тепла из-за высокой ионной проводимости
мембран митохондрий.
Слайд 94 В процессе разобщения О/Ф возрастает протонная проницаемость
внутренней мембраны митохондрий и происходит рассеивание энергии трансмембранного потенциала ▲
µН+, при участии АТФ/АДФ антипортера ( аденилаттранслоказы), а также других переносчиков- глутамт-аспартатного и глутаматного.
наряду с регуляторной функцией играет важную адаптивную роль, препятствуя повышенному
образованию АФК (активных форм кислорода).
Слайд 96 В этом случае происходит снижение локальной концентрации кислорода
в клетке и уровня восстановленности убихинона (Q) ДЦ митохондрий. Это
предотращает обратному транспорту электронов по ДЦ, который сопровождается образованием О2.-.
Слайд 97
Разобщенное и несопряженное дыхания,
отличаются по механизмам, являются энергодиссипирующими и по существу представляют собой
варианты» свободного дыхания».
Слайд 98Значение тканевого дыхания
Энергетический обмен играет ведущую роль в жизнедеятельности организмов,
т. к. все функции организма энергозависимы. Систему механизмов, обеспечивающих стабильный
уровень субстратов энергообмена называют энергетическим гомеостазом.
Слайд 99Одним из механизмов поддержания постоянного уровня АТФ в клетке, является
наличие мегамитохондрий, которое дает большое преимущество.
Если один участок клетки плохо
снабжается кислородом, то при помощи мегамитохондрий энергия ▲μН+ транспортируется в этот участок и восполняет недостаток АТФ.
Слайд 100Микросомальное окисление
Микросомы (микрочастицы) - это замкнутые мембранные пузырьки (везикулы), образуемые
из гладкой ЭПС при гомогенизации клетки. Как таковых микросом не
существует.
Микросомальное окисление - это окисление, протекающее на гладкой ЭПС нормальной неразрушенной клетки.
Слайд 101
Наиболее интенсивно микросомальное окисление протекает в
печени и надпочечниках, а также в местах контакта с внешней
средой, в коже, почках, легких, селезенке.
Слайд 102ЭПС - 2-й слой мембран, ассоциированных с 3-мя основными классами
ферментов:
1) оксидоредуктазы;
2) трансферазы;
3) гидролазы.
Слайд 103 Главная функция этих ферментов - реакции детоксикации.
Микросомальное окисление осуществляется с помощью одноименной ДЦ, которая представляет собой
систему переносчиков протонов и электронов с НАД или НАДФ на кислород.
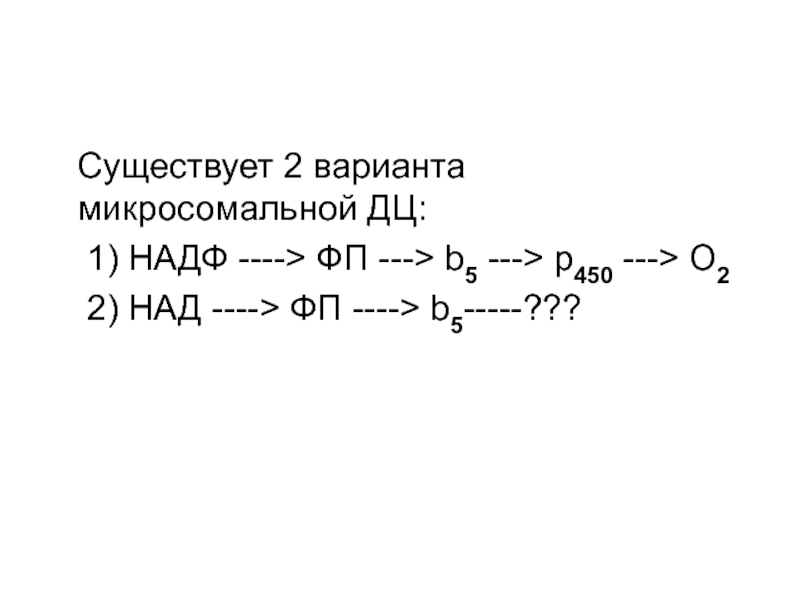
Слайд 104 Существует 2 варианта микросомальной ДЦ:
1) НАДФ ---->
ФП ---> b5 ---> p450 ---> O2
2) НАД ---->
ФП ----> b5-----???
Слайд 105 Цитохром b5 одной цепи может передавать свои электроны
на цитохром b5 другой цепи, а также на цитохром P450.
Микросомальное окисление можно записать и так:
RH + НАД (НАДФ).H2 + O2 ---> ROH + НАД (НАДФ) + HOH
Слайд 106 FP - флавопротеид, включающий ФАД и Fe-белок, содержащий
негеминовое железо.
P450 - восстановленный CO-комплекс, который имеет max
поглощения при длине волны = 450 нм.
Слайд 107
Многие гидрофобные вещества организма обладают токсичностью, за счет того, что
растворяются в клеточных мембранах и тем самым разрушают их.
Слайд 108Задачей организма является перевод этих гидрофобных соединений в гидрофильные, которые
легче выводятся почками. Это осуществляется микросомальным окислением
Слайд 109
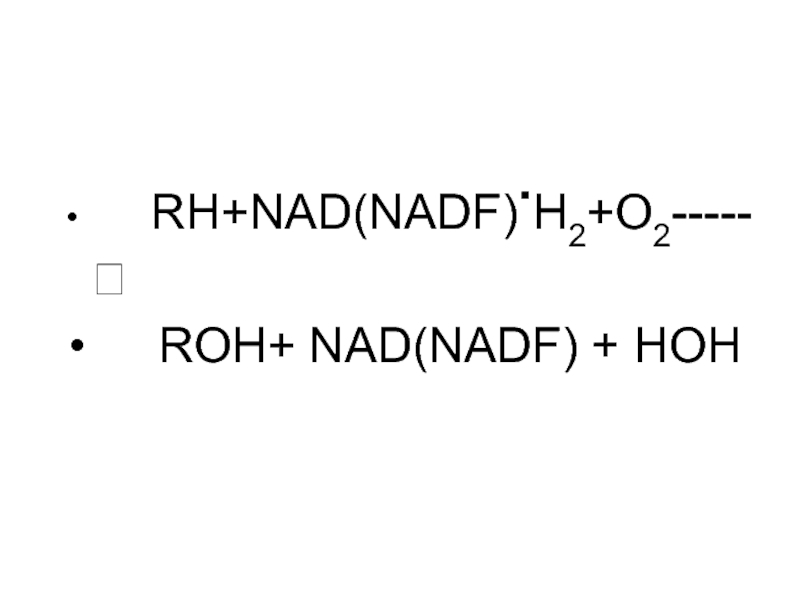
RH+NAD(NADF).H2+O2-----?
ROH+ NAD(NADF) +
HOH
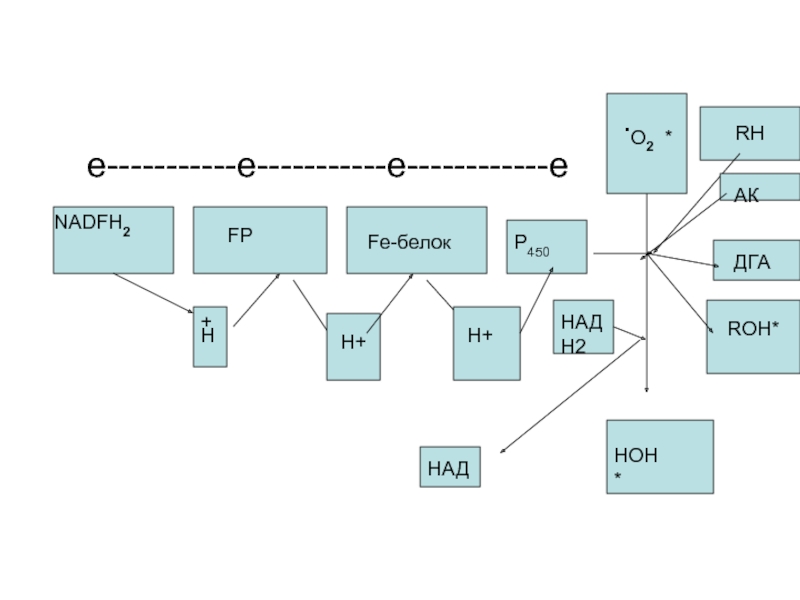
Слайд 110
e-----------e-----------e------------e
RH
NADFH2
FP
Fe-белок
Р450
+
Н
Н+
Н+
НАДН2
НАД
НОН*
ROH*
.O2 *
АК
ДГА
Слайд 111Таким образом, основная роль микросомальной ДЦ заключается в осуществлении реакций
синтеза с участием кислорода (в схеме видно образование фенола из
бензола (гидроксилирование
Слайд 112Для связывания второго атома кислорода необходим косубстрат, каковым является аскорбат
(Vit C), который также отдает 2H+ на синтез H2O. Для
обеспечения реакций детоксикации необходимо большое количество Vit C в составе косубстрата:
Слайд 113Реакции детоксикации протекают по механизму гидроксилирования гетероциклических и алифатических соединений
(ксенобиотики), которые поступают из внешней среды.
Реакции детоксикации могут привести к
снижению концентрации токсических веществ, но может возникнуть летальный синтез.
Слайд 114 Роль микросомального окисления состоит в биосинтезе Vit D,
кортикостероидов, коллагена, тирозина, катехоламинов.
- Реакции деалкилирования - отщепление
алкильной группы;
- реакции окисления спиртов, альдегидов, кетонов, нитросоединений;
Слайд 115 - реакции разрыва кольца
ароматических соединений;
-
реакции восстановления, когда идет
сброс протонов;
-
реакции десатурации (перевод
насыщенных ЖК в ненасыщенные
Слайд 116 Микросомальная и митохондриальная дыхательные цепи взаимодействуют друг с
другом через цитохром b5.
В условиях интоксикации (этанол, барбитураты)
происходит ингибирование 1 комплекса митохондриальной ДЦ.
НАД -**--> ФП --> Q ---> b ---> c1 ---> c--?a1------?a3-------1/2O2
****-- какой- либо ингибитор
Слайд 117 Несмотря на то, что окисление НАД.Н2 не происходит,
он не накапливается.
В межмембранном пространстве имеется цитохром b5,
который принимает электроны с НАД.Н2 митохондриальной ДЦ, и перебрасывает их на микросомальную ДЦ, и тем самым угроза энергетического голода устраняется.
Слайд 118Таким образом цитохром. b5 - фермент, компонент микросомальной ДЦ, который
обеспечивает межмембранный митохондриально-микросомальный перенос электронов.
Слайд 119 Различиямитохондриальной и микросомальной ДЦ:
а) по локализации;
б)
микросомальная ДЦ короче и электроны на последнем переносчике МС цепи
более энергизированы и способны активировать кислород;
Слайд 120 в) будучи активным кислород способен внедряться в структуру
многих молекул, т. е. используется с «пластическими» целями (ФЕН---> ТИР).
В то время как в Митохондриальной ДЦ кислород - всего лишь конечный акцептор электронов, и используется в энергетических целях;
Слайд 121 г) в процессе переноса электронов в Мтх. ДЦ
их энергия депонируется в форме АТФ.
В Микросомальной ДЦ
- депонирование энергии ни в каком виде не происходит;
Слайд 122
д) Микросомальное окисление – это современная
интерпретация теории Баха Энглера. Митохондриальное окисление - современный вариант теории
Палладина-Виланда
Слайд 123Перекисное окисление
1.Механизм образования активных форм кислорода.
2.Роль перекисных процессов в
норме и при патологии. Общее представление о ПОЛ (НЭЖК →
R∙ → диеновые коньюгаты → гидроперекиси → МДА).
3.Способы оценки активности ПОЛ
Слайд 124Еще Мечников, изучая фагацитоз утверждал, что фагоцитарное действие лейкоцитов осуществляется
за счет перекисных процессов.
Перекисное окисление - это третий путь утилизации
вдыхаемого кислорода (от 2 до 5%).
Слайд 125Кислород сам по себе является парамагнитным элементом (это было установлено
методом молекулярных орбиталей) т. к. имеет на внешнем слое 2
неспаренных электрона.
O2 + e ---> O2-, т. е. в реакциях перекисного
окисления происходит одноэлектронное восстановление кислорода.
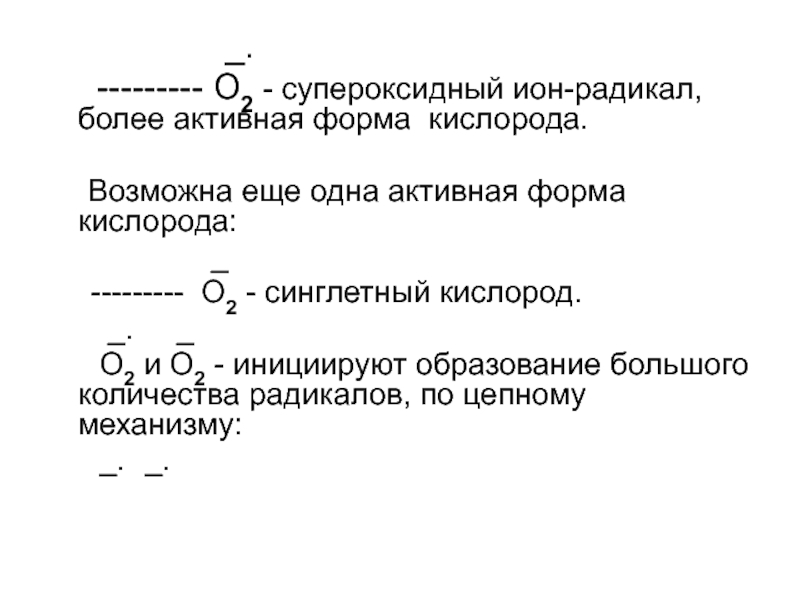
--------- O2 - супероксидный ион-радикал, более активная форма
кислорода.
Возможна еще одна активная форма кислорода:
_
--------- O2 - синглетный кислород.
_. _
O2 и O2 - инициируют образование большого количества радикалов, по цепному механизму:
_. _.
_.
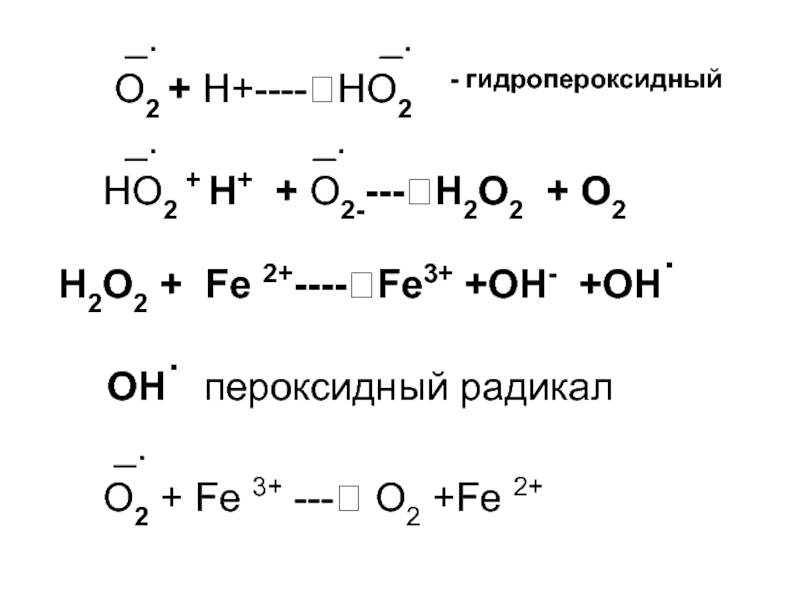
O2 + Н+----?НО2
- гидропероксидный
_. _.
НО2 + Н+ + O2----?Н2О2 + О2
Н2О2 + Fe 2+----?Fe3+ +ОН- +OH.
OH. пероксидный радикал
_.
O2 + Fe 3+ ---? O2 +Fe 2+
Слайд 128В процессе взаимодействия этих радикалов с веществом поражаются наиболее уязвимые
места клеток: ненасыщенные ЖК фосфолипидов мембран, они «выжигаются» в результате
чего мембрана делается более ригидной и следовательно изменяется ответная реакция клетки.
Слайд 129В нормальных условиях перекисное окисление регулирует агрегатное состояние мембран, и
лежит в основе тканевой адаптации. (Это играет роль в стрессовых
ситуациях, когда клетка т. о. защищается от избытка гормонов).
При всех видах патологии активность перекисных процессов возрастает, и является инструментом повреждения мембраны.
Слайд 130В мембране образуются мощные ионные каналы через которые входят ионы
Na+, K+ и другие. Это нарушает клеточный гомостаз, ее содержимое
теряется и клетка гибнет.
Слайд 131 Клетки имеют мощную антиоксидантную систему защиты клеток
(АОЗ), состоящую из двух уровней:ферментативную и неферментативную.
1.
ферментативная – благодаря ей, происходит восстановление продуктов перекисного окисления и их ликвидация с помощью ферментов :
Слайд 132
а) супероксиддисмутаза – сложный фермент. При
этом встречаются Mg, Zn, Fe, Cu – содержащие формы в
разных тканях. Его активность повышается при любых формах активации перекисных процессов.
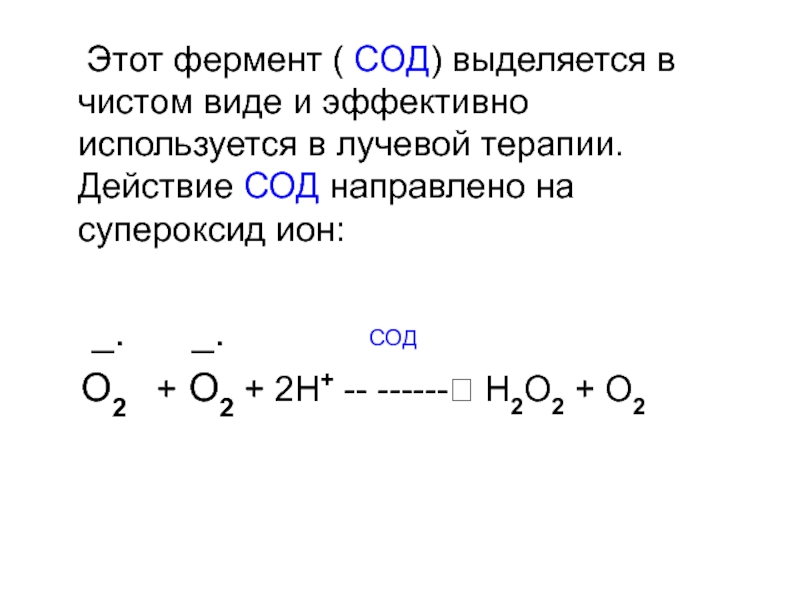
Слайд 133 Этот фермент ( СОД) выделяется в чистом виде
и эффективно используется в лучевой терапии. Действие СОД направлено на
супероксид ион:
_. _. СОД
O2 + O2 + 2Н+ -- ------? Н2О2 + О2
Слайд 134
б) каталаза (её субстратом является
Н2О2) особенно активна в эритроцитах, которые специализируются на переносе кислорода:
2Н2О2 ------? 2Н2О + О2
Слайд 135в) пероксидаза – наиболее активна глутатионпероксидаза
г) глутатионредуктаза – является непосредственным
защитником эритроцитов, в частности предохраняют от образования МеHb, который не
способен к транспорту кислорода, что ведёт к гипоксии. МеHb образуется при приёме избытка нитратов, аспирина, сульфаниламидов.
Слайд 136
К системе ферментативной АОЗ относятся ферменты, генерирующие восстановительную форму НАД
.Н и НАДF.Н. Такую систему имеют все клетки, но особенно
клетки мозга и миокарда.
Слайд 1372. Неферментативная система: сюда относится ряд легко окисляющихся веществ, обладающих
меньшей активностью, чем естественные метаболиты:
хинон
убихинон (Ко – Q)
витамины Е и
А (являются компонентами мембран и блокируют перекисные процессы)
витамин С
Слайд 138Между этими тремя витаминами существует взаимосвязь: витамин С обеспечивает восстановительную
форму витамина Е, а для поддержания восстановительной формы витамина С
нужен витамин А. В настоящее время существует мощный препарат антиоксидантной защиты, представляющий собой комплекс трёх витаминов (Vit C = 2 г, Vit E = 500000 E, Vit A + 140000 – 170000 Е).
Слайд 139
В настоящее время существует мощный препарат антиоксидантной защиты, представляющий собой
комплекс трёх витаминов (Vit C = 2 г, Vit E
= 500000 E, Vit A + 140000 – 170000 Е). Это Антиоксикапс, содержащий Se.
Слайд 140Витамин А довольно токсичен, поэтому в качестве замены используется В
– каротин.
Также к антиоксидантам относятся Vit F, кортикостероиды, гистидин,
аргинин, билирубин и растительные пигменты.