клетках, основная функция которых - энергетическое обеспечение метаболизма.
Биологическое окисление:
Окисление,
сопряженное с фосфорилированием АДФ.1.1. Окислительное фосфорилирование (ЭТЦ митохондрий);
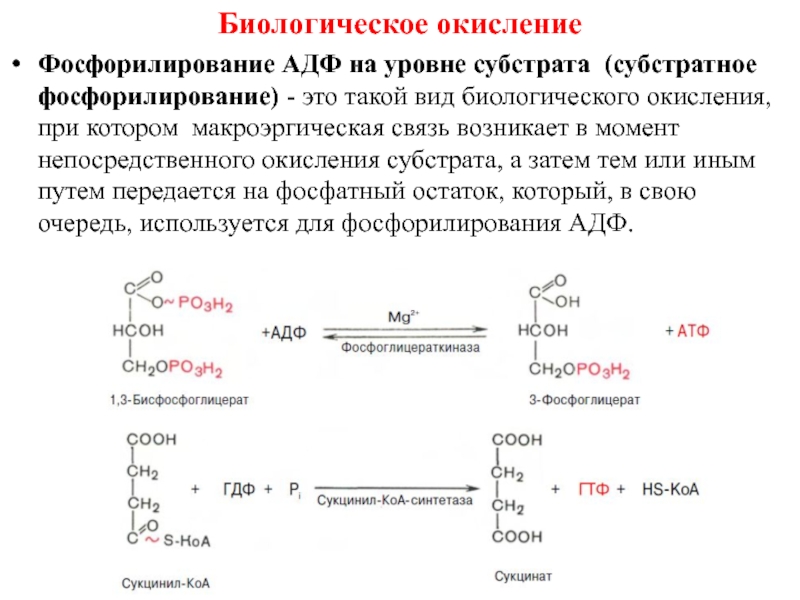
1.2. Субстратное фосфорилирование;
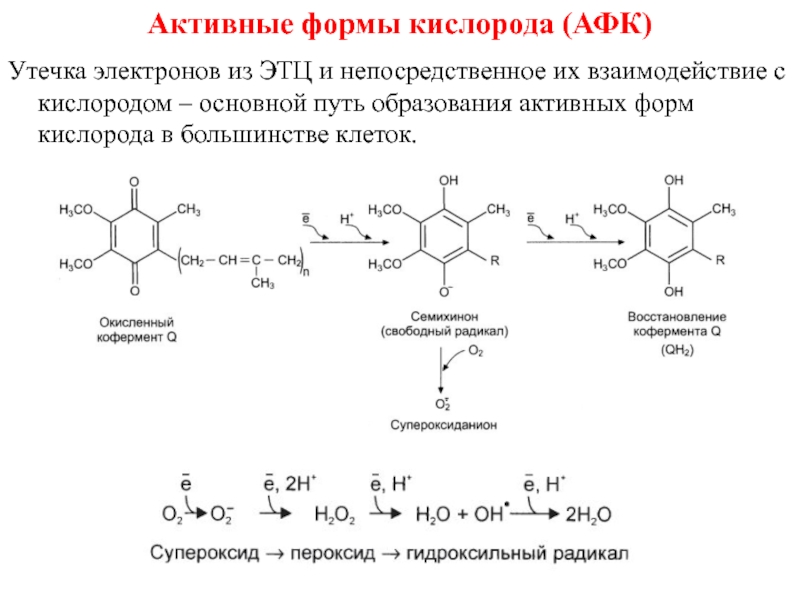
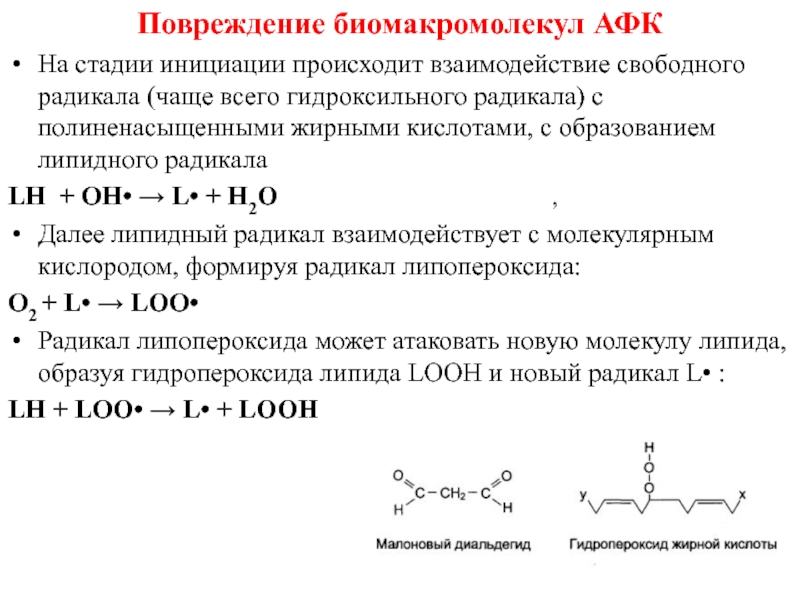
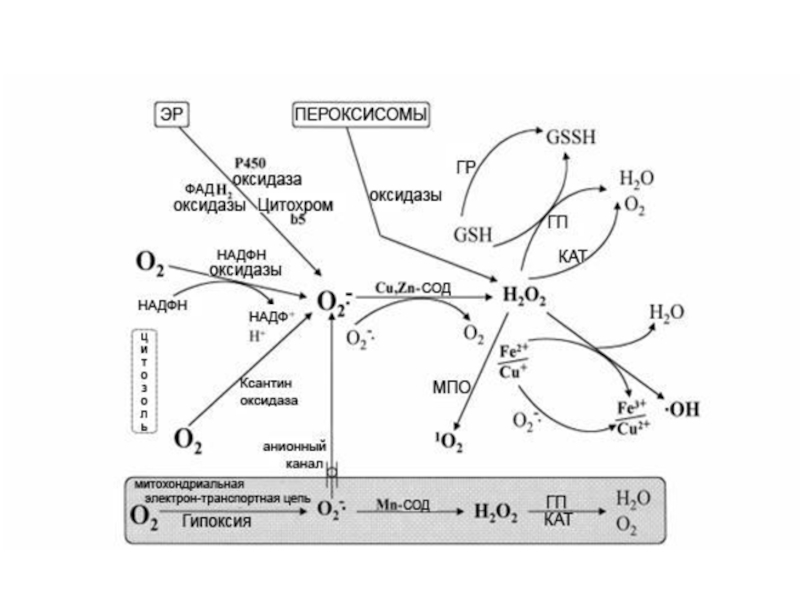
2. Свободное окисление, НЕ сопряженное с фосфорилированием АДФ