Слайд 1ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
Федеральное государственное образовательное учреждение высшего и профессионального
образования
Сибирский федеральный университет
БИОХИМИЯ
ЧАСТЬ 2. ДИНАМИЧЕСКАЯ БИОХИМИЯ
факультет физической культуры и
спорта
направление - физическая культура
2
ДИНАМИЧЕСКАЯ БИОХИМИЯ
2
Слайд 2Содержание:
ЧАСТЬ 2. ДИНАМИЧЕСКАЯ БИОХИМИЯ
Переваривание углеводов в пищеварительном тракте. Гликолиз.
Окислительное декарбоксилирование пирувата
Аэробный метаболизм углеводов
Липидный обмен
Белковый
обмен
Интеграция клеточного обмена
3
ДИНАМИЧЕСКАЯ БИОХИМИЯ
3
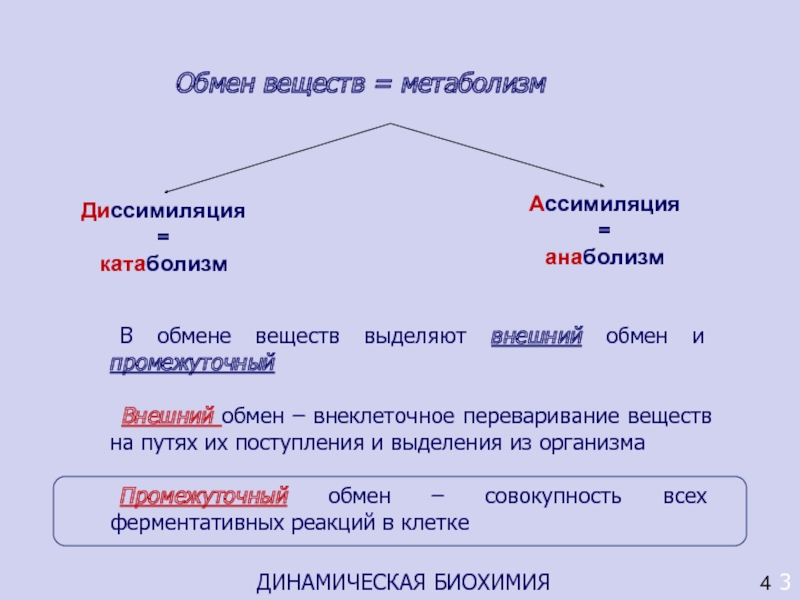
Слайд 3Обмен веществ = метаболизм
3
ДИНАМИЧЕСКАЯ БИОХИМИЯ
4
Диссимиляция
=
катаболизм
Ассимиляция
=
анаболизм
В обмене веществ выделяют внешний
обмен и промежуточный
Внешний обмен – внеклеточное переваривание
веществ на путях их поступления и выделения из организма
Промежуточный обмен – совокупность всех ферментативных реакций в клетке
Слайд 4Обмен энергии
3
4
Освобождение энергии идёт при распаде веществ;
Потребность в энергии
зависит от пола, возраста, профессии и др., например при физ
нагрузке потребность составляет 3400-4000 ккал, а при умеренной нагрузке 2400-2700ккал;
Вся энергия растительной и животной пищи – энергия солнца;
Растения накапливают энергию в процессе фотосинтеза;
Основным носителем энергии является электрон. Энергия выделяется при возбуждении и переходе электрона с одного электронного уровня на другой;
Слайд 53
4
крупные пищевые молекулы расщепляются в ЖКТ на составляющие их строительные
блоки (аминокислоты, моносахариды, жирные кислоты и др.)
продукты, образовавшиеся на
1 стадии, превращаются в клетках в более простые молекулы, число которых невелико - ацетил-КоА и др.
ацетил-КоА – главный промежуточный продукт распада
эти продукты (ацетил-КоА и др.) поступают в цикл Кребса и окисляются до СО2 и воды
Этапы освобождения энергии:
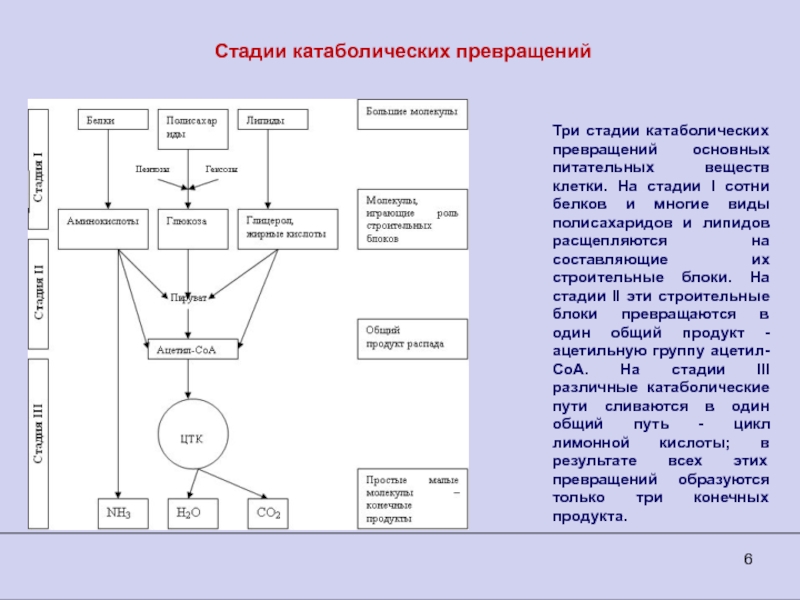
Слайд 6Стадии катаболических превращений
Три стадии катаболических превращений основных питательных веществ клетки.
На стадии I сотни белков и многие виды полисахаридов и
липидов расщепляются на составляющие их строительные блоки. На cтадии II эти строительные блоки превращаются в один общий продукт - ацетильную группу ацетил-СоА. На стадии III различные катаболические пути сливаются в один общий путь - цикл лимонной кислоты; в результате всех этих превращений образуются только три конечных продукта.
Слайд 7Цикл Кребса
=
Цикл трикарбоновых кислот
=
Цикл лимонной кислоты
3
4
Ацетил-СоА
Слайд 83
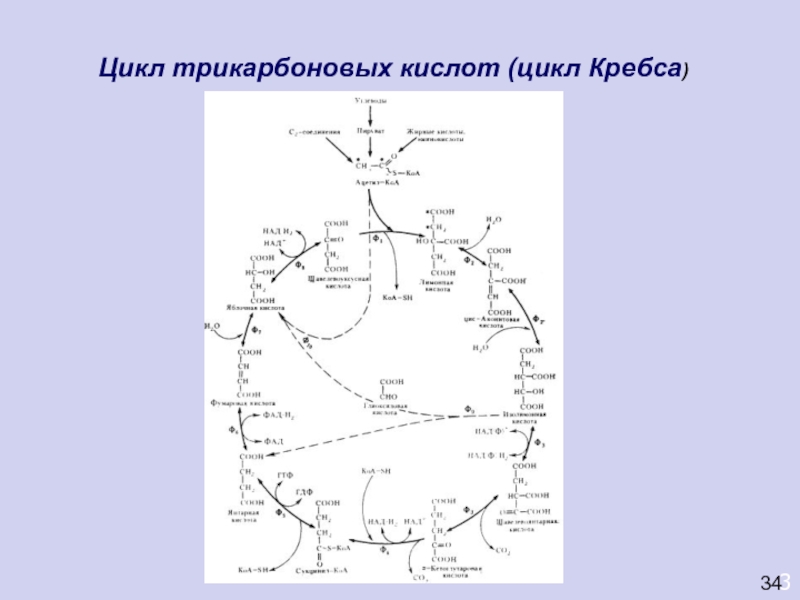
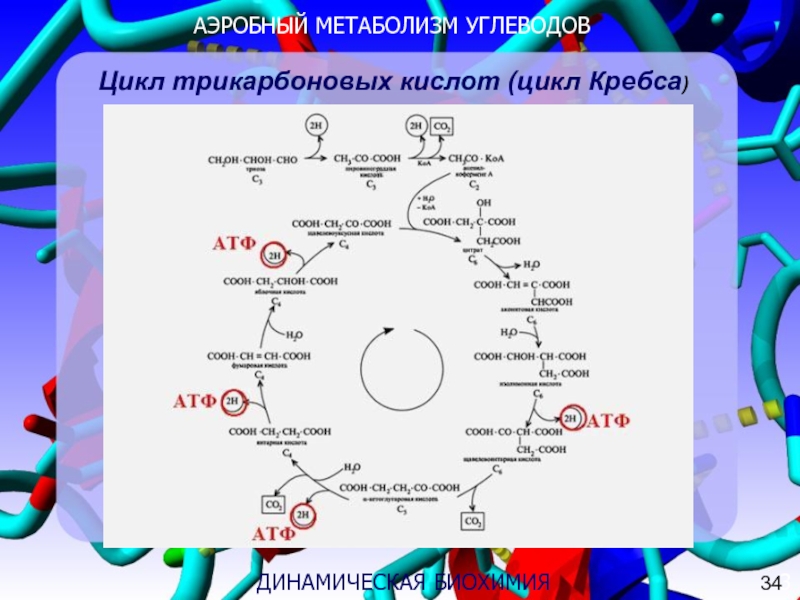
Цикл трикарбоновых кислот (цикл Кребса)
34
Слайд 9АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ
3
ДИНАМИЧЕСКАЯ БИОХИМИЯ
Цикл трикарбоновых кислот (цикл Кребса)
34
Слайд 10
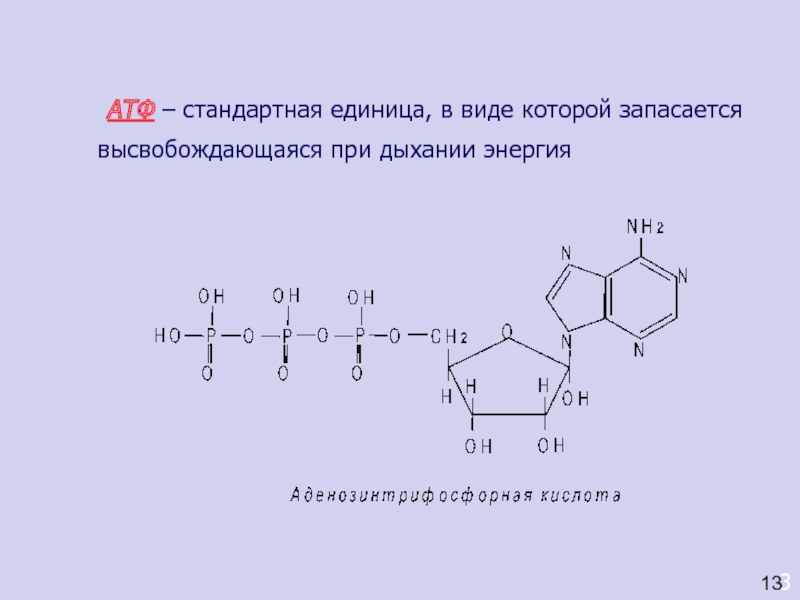
АТФ – стандартная единица, в виде которой запасается высвобождающаяся при
дыхании энергия
3
13
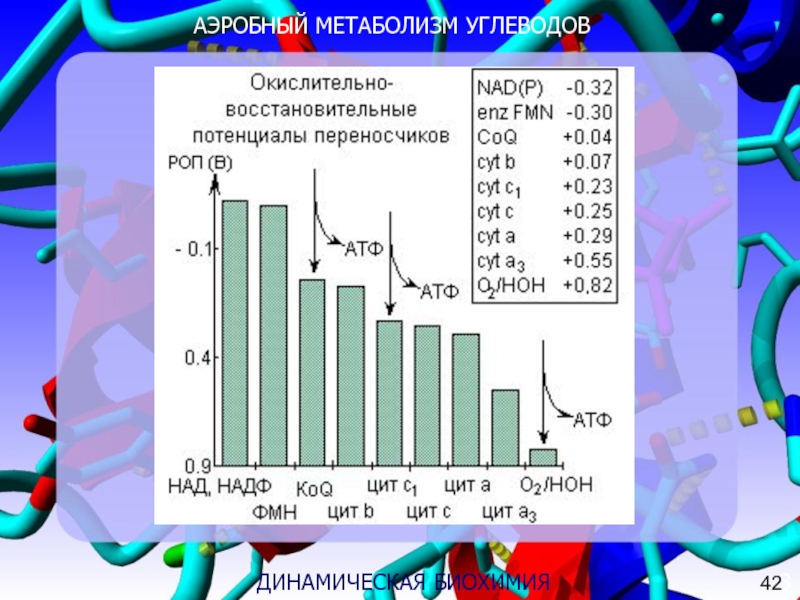
Слайд 11АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ
3
35
Тканевое дыхание = биологическое окисление
Распад органических соединений
в живых тканях, сопровождающийся потреблением молекулярного кислорода и приводящий к
выделению углекислого газа и воды и образованию биологических видов энергии, называется тканевым дыханием. Тканевое дыхание представляют как конечный этап пути превращений моносахаров (в основном глюкозы) до конечных продуктов, а также промежуточные продукты распада липидов (жирные кислоты), белков (аминокислоты) и нуклеиновых оснований. Итоговая реакция тканевого дыхания будет выглядеть следующим образом:
С6Н12О6 + 6O2 = 6СO2+ 6Н2O + 2780 кДж/моль.
Впервые сущность дыхания объяснил А.-Л. Лавуазье (1743-1794), обративший внимание на сходство между горением органических веществ вне организма и дыханием животных. Постепенно становились ясными принципиальные различия между этими двумя процессами: в организме окисление протекает при относительно низкой температуре в присутствии воды, и его скорость регулируется обменом веществ. В настоящее время биологическое окисление определяется как совокупность реакций окисления субстратов в живых клетках, основная функция которых - энергетическое обеспечение метаболизма.
Потребление кислорода тканями зависит от интенсивности реакций тканевого дыхания. Наибольшей скоростью тканевого дыхания характеризуются почки, мозг, печень, наименьшей – кожа, мышечная ткань (в покое).

Слайд 12АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ
3
ДИНАМИЧЕСКАЯ БИОХИМИЯ
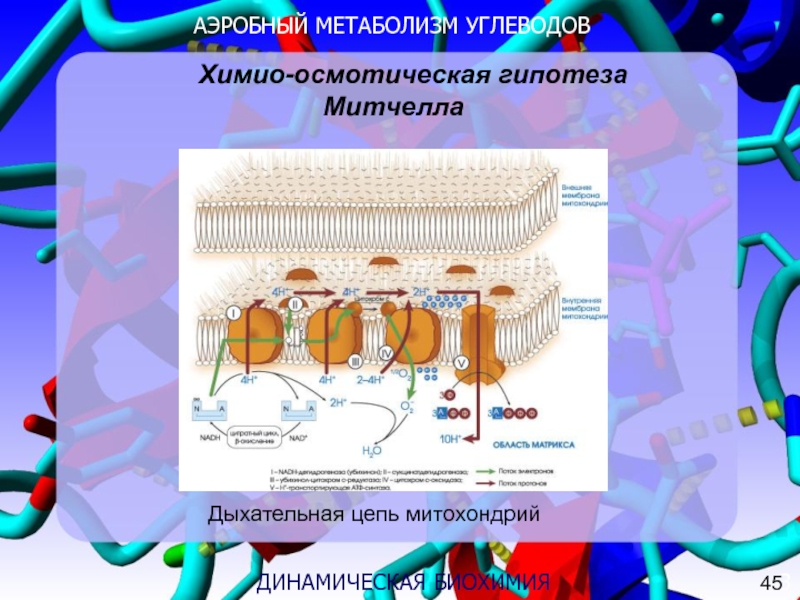
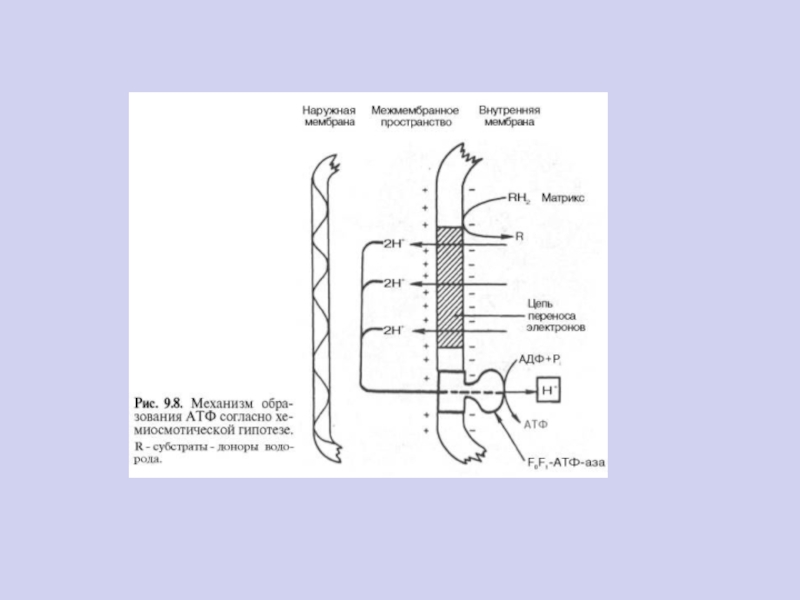
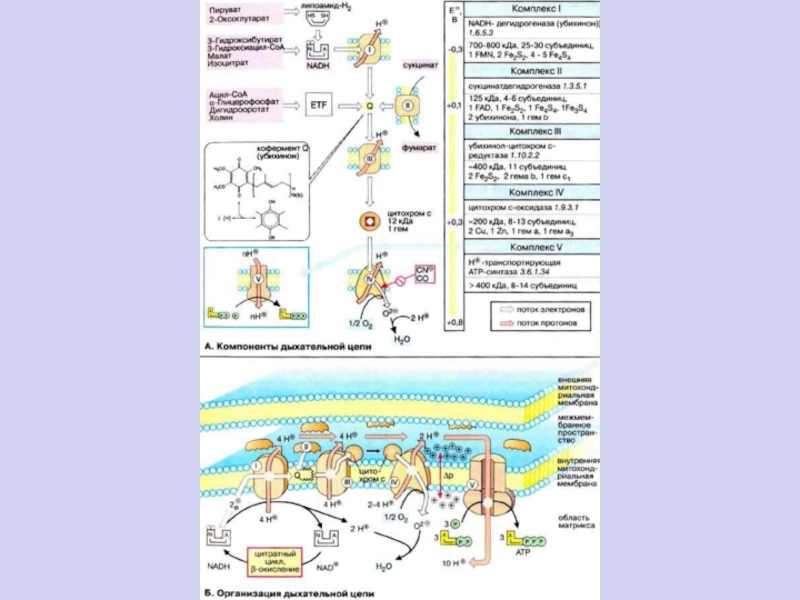
Химио-осмотическая гипотеза Митчелла
Дыхательная цепь митохондрий
45
Слайд 13АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ
3
35
Слайд 15АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ
3
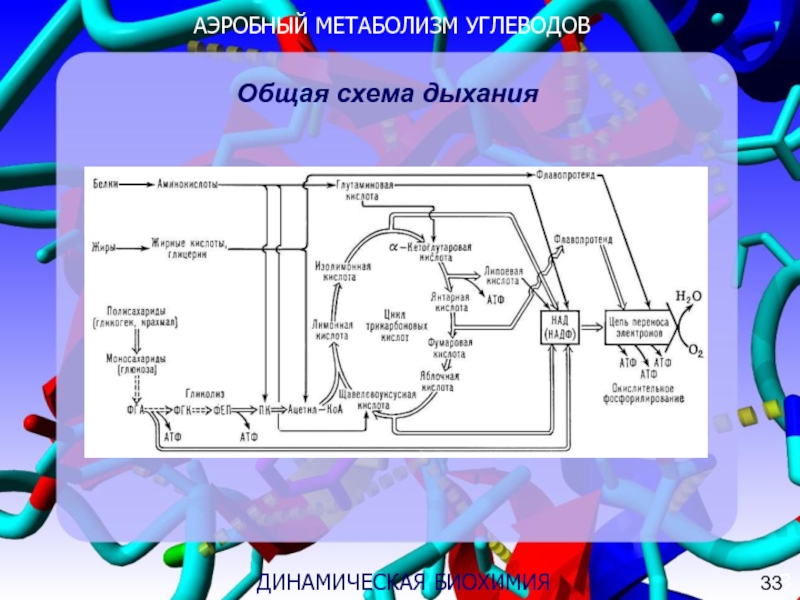
ДИНАМИЧЕСКАЯ БИОХИМИЯ
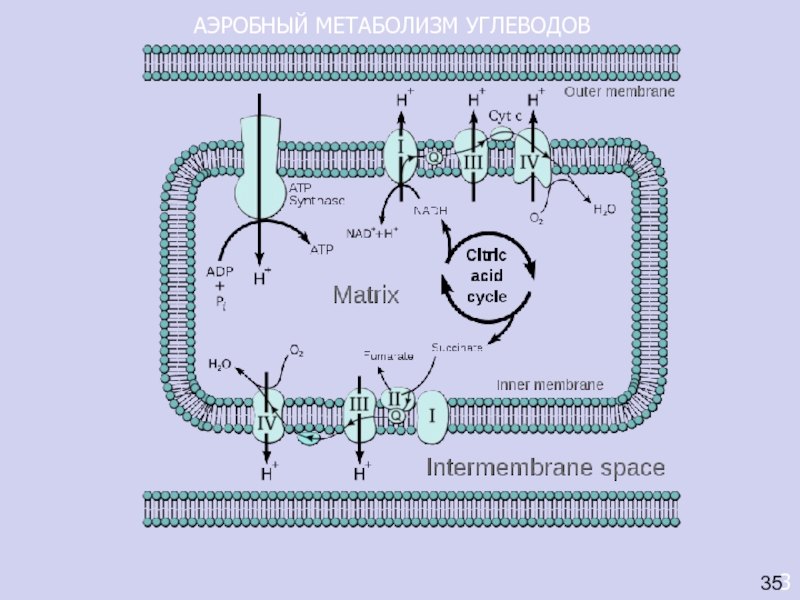
Общая схема дыхания
33
Слайд 16АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ
3
35
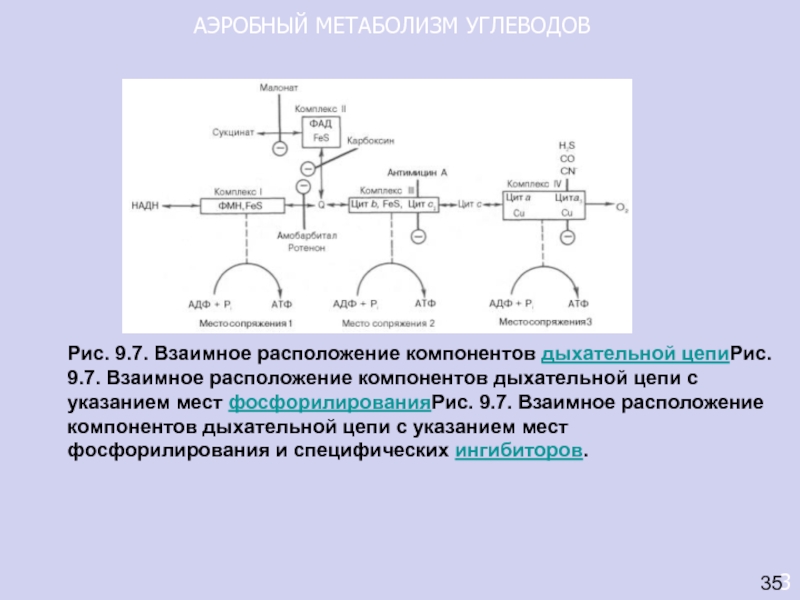
Рис. 9.7. Взаимное расположение компонентов дыхательной цепиРис. 9.7.
Взаимное расположение компонентов дыхательной цепи с указанием мест фосфорилированияРис. 9.7.
Взаимное расположение компонентов дыхательной цепи с указанием мест фосфорилирования и специфических ингибиторов.
Слайд 19АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ
3
35
Слайд 20АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ
3
ДИНАМИЧЕСКАЯ БИОХИМИЯ
РИСУНОК
42
Слайд 21АЭРОБНЫЙ МЕТАБОЛИЗМ УГЛЕВОДОВ
3
ДИНАМИЧЕСКАЯ БИОХИМИЯ
Суммарное уравнение процесса фосфорилирования
в дыхательной цепи:
НАДН +
2Н+ + 3 АДФ + Фн + 1/2 О2 →
НАД+ + 4 Н2О + 3 АТФ
Экзергонический компонент:
НАДН + 2Н+ + 1/2 О2 → НАД+ + Н2О ΔG′ = – 52,7 ккал
Эндергонический компонент:
3 АДФ + 3 Фн → 3 АТФ +3 Н2О ΔG′ = + 21,9 ккал
43
Слайд 223
35
Регуляция обмена веществ и энергии:
На уровне всего организма
На уровне клетки
Молекулярный
уровень
Общий контроль осуществляется ЦНС
Слайд 23
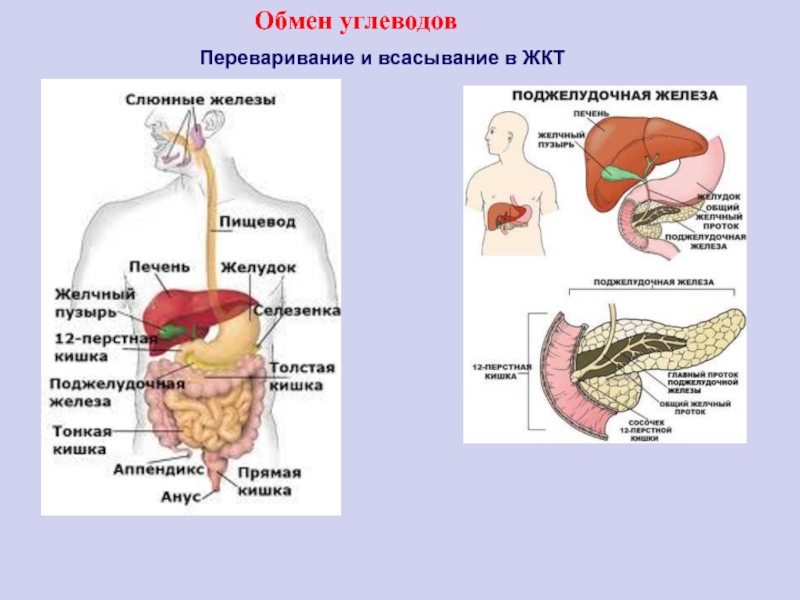
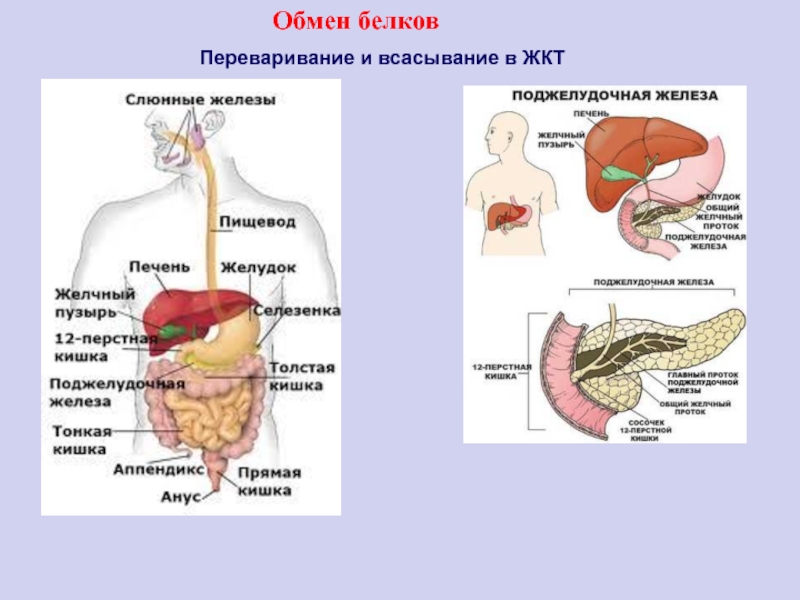
Переваривание и всасывание в ЖКТ
Обмен углеводов
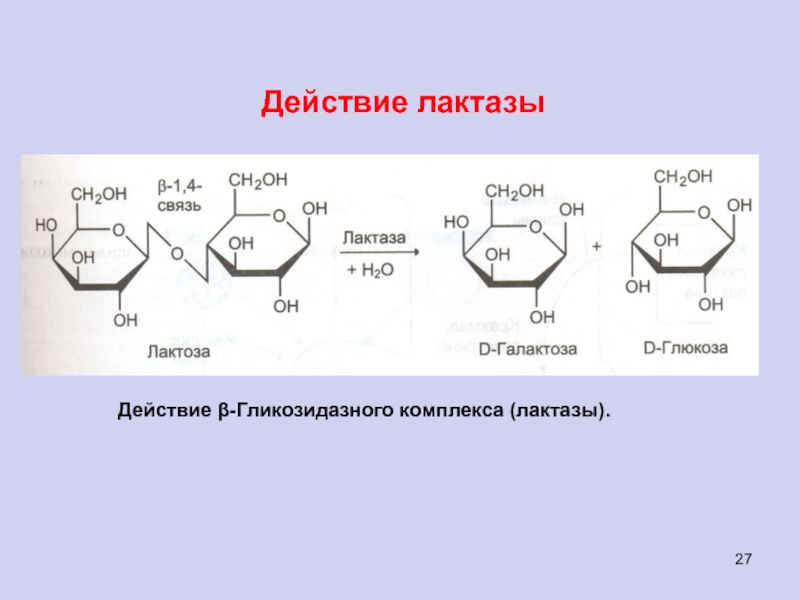
Слайд 27Действие лактазы
Действие β-Гликозидазного комплекса (лактазы).
Слайд 293
35
Роль печени в обмене углеводов
Синтез гликогена;
Гликогенолиз – распад гликогена;
Глюконеогенез –
синтез углеводов из неуглеводистых продуктов;
Взаимопревращение гексоз – образование глюкозы из
фруктозы и галактозы;
Гликолиз – окисление глюкозы с выделением энергии;
Пентозофосфатный цикл окисления углеводов или прямой путь
Из печени глюкоза с током крови разносится к клеткам других органов и тканей
Слайд 30Обмен веществ = метаболизм
3
ДИНАМИЧЕСКАЯ БИОХИМИЯ
4
Диссимиляция
=
катаболизм
Ассимиляция
=
анаболизм
В обмене веществ выделяют внешний
обмен и промежуточный
Внешний обмен – внеклеточное переваривание
веществ на путях их поступления и выделения из организма
Промежуточный обмен – совокупность всех ферментативных реакций в клетке
Слайд 313
35
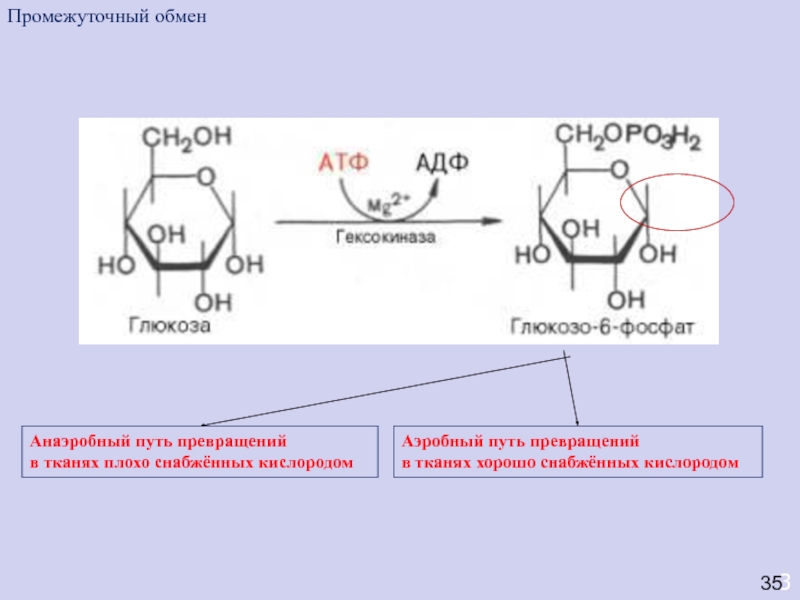
Анаэробный путь превращений
в тканях плохо снабжённых кислородом
Промежуточный обмен
Аэробный путь превращений
в
тканях хорошо снабжённых кислородом
Слайд 32
Гликолиз – центральный путь катаболизма глюкозы в животных, растительных клетках
и микроорганизмах. Это наиболее древний путь, в результате которого глюкоза
подвергается анаэробному расщеплению с образованием молочной кислоты. В процессе гликолиза образуется также АТФ.
Гликолиз может протекать в клетке в аэробных и анаэробных условиях.
3
Гликолиз
12
Анаэробный и аэробный пути распада углеводов
Слайд 333
Суммарное уравнение гликолиза
(в анаэробных условиях)
С6Н12О6 + 2 Фн +
2 АДФ → 2 СН3СНОНСООН + 2 АТФ + 2
Н2О
Глюкоза Молочная кислота
Суммарный выход энергии
Глюкоза → 2 Лактат ΔG1` = – 47,0 ккал
2Фн + 2 АДФ → 2 АТФ + 2 Н2О G2` = +2∙7,30 = +14,6 ккал
Суммарная реакция:
Глюкоза + 2 Фн + 2 АДФ → 2 Лактат + 2 АТФ + 2 Н2О
ΔGs` = ΔG1` + ΔG2` = – 47,0 + 14,6 = – 32,4 ккал
16
Анаэробный путь распада углеводов
Слайд 343
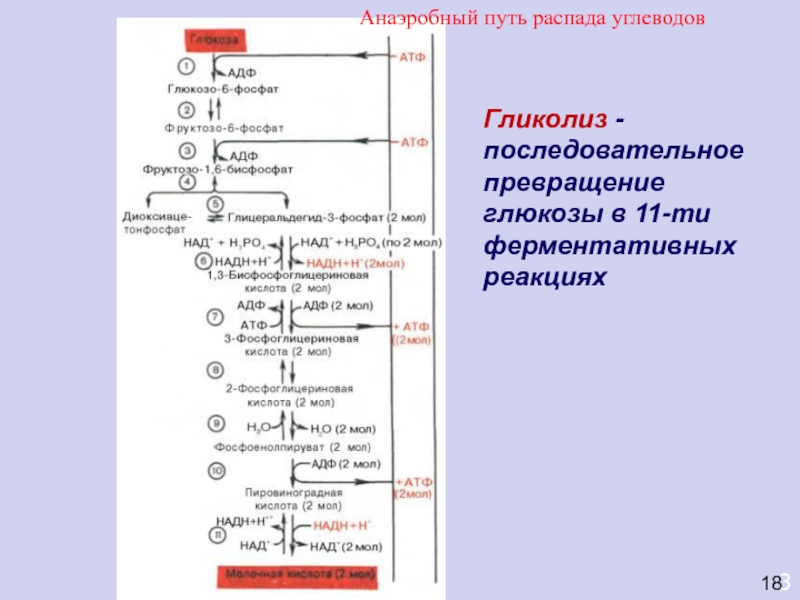
Гликолиз -
последовательное превращение глюкозы в 11-ти ферментативных реакциях
18
Анаэробный путь
распада углеводов
Слайд 353
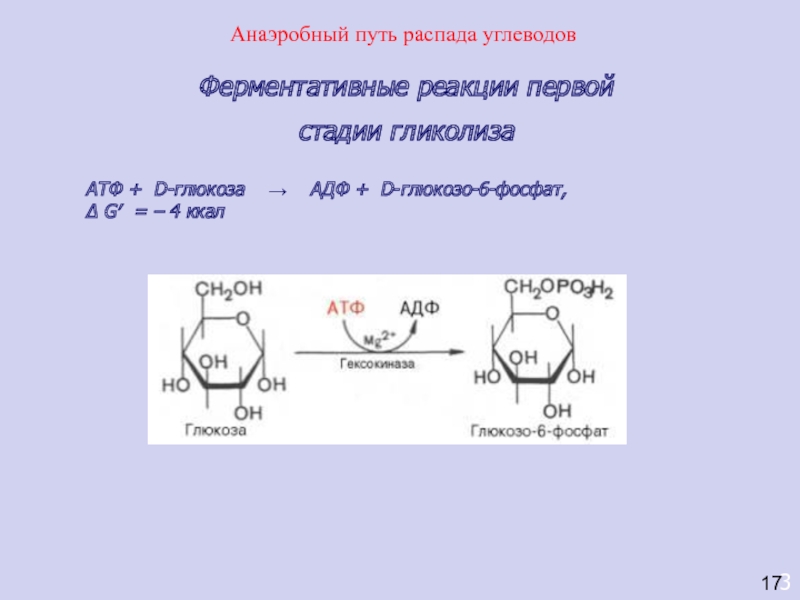
Ферментативные реакции первой
стадии гликолиза
AТФ + D-глюкоза → АДФ
+ D-глюкозо-6-фосфат,
Δ G′ = – 4 ккал
17
Анаэробный путь распада
углеводов
Слайд 363
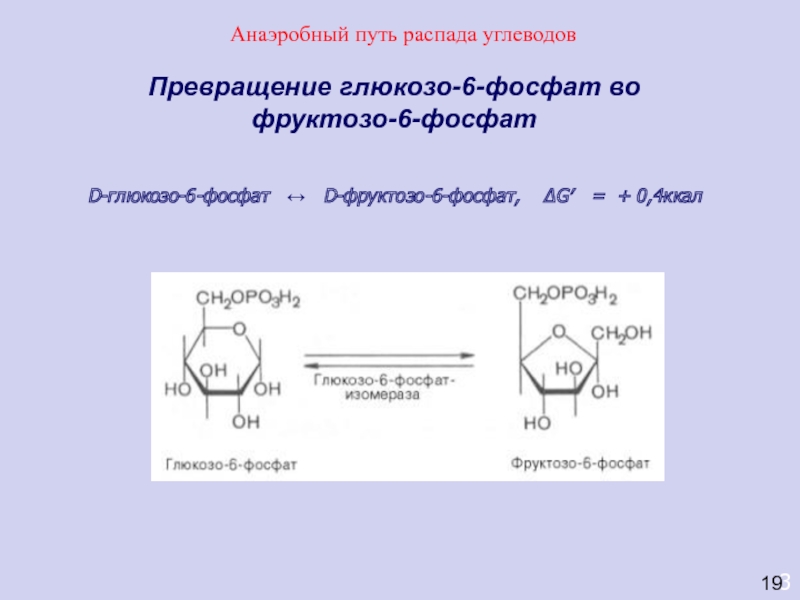
Превращение глюкозо-6-фосфат во фруктозо-6-фосфат
D-глюкозо-6-фосфат ↔ D-фруктозо-6-фосфат, ΔG′
= + 0,4ккал
19
Анаэробный путь распада углеводов
Слайд 373
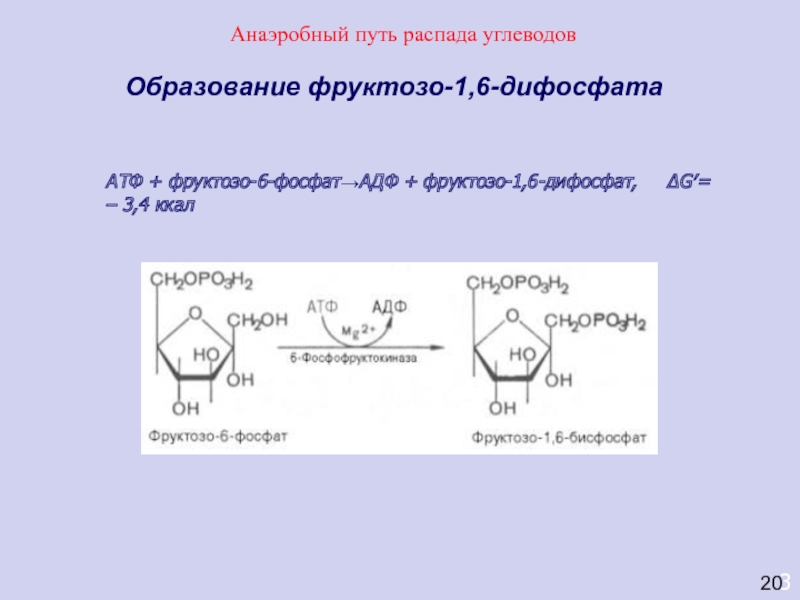
Образование фруктозо-1,6-дифосфата
АТФ + фруктозо-6-фосфат→АДФ + фруктозо-1,6-дифосфат, ΔG′= –
3,4 ккал
20
Анаэробный путь распада углеводов
Слайд 383
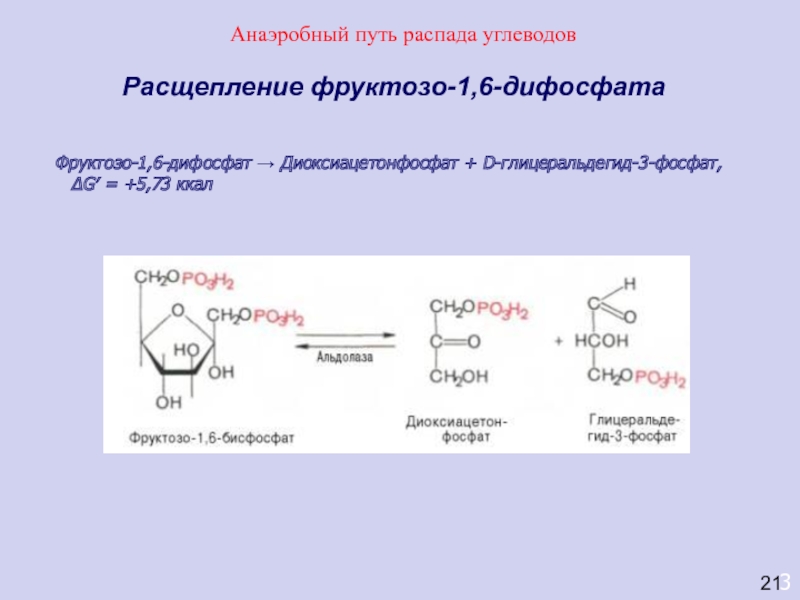
Расщепление фруктозо-1,6-дифосфата
Фруктозо-1,6-дифосфат → Диоксиацетонфосфат + D-глицеральдегид-3-фосфат,
ΔG′ =
+5,73 ккал
21
Анаэробный путь распада углеводов
Слайд 393
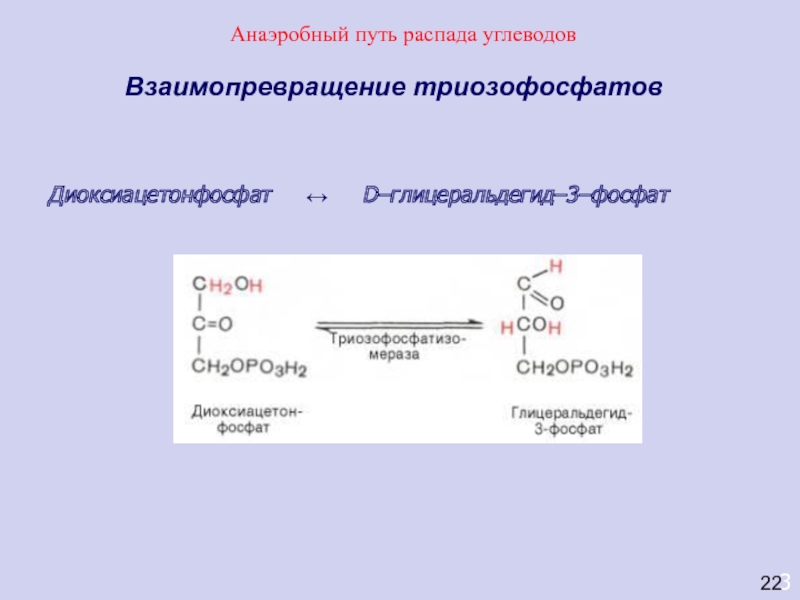
Взаимопревращение триозофосфатов
Диоксиацетонфосфат ↔ D–глицеральдегид–3–фосфат
22
Анаэробный путь распада
углеводов
Слайд 403
Окисление глицеральдегид-3-фосфата до 1,3-дифосфоглицерата
Глицеральдегид-3-фосфат+ НАД++ Фн →1,3-дифосфоглицерат + НАД*Н +
Н+
ΔG′ = +1,5 ккал
23
Анаэробный путь распада углеводов
Слайд 413
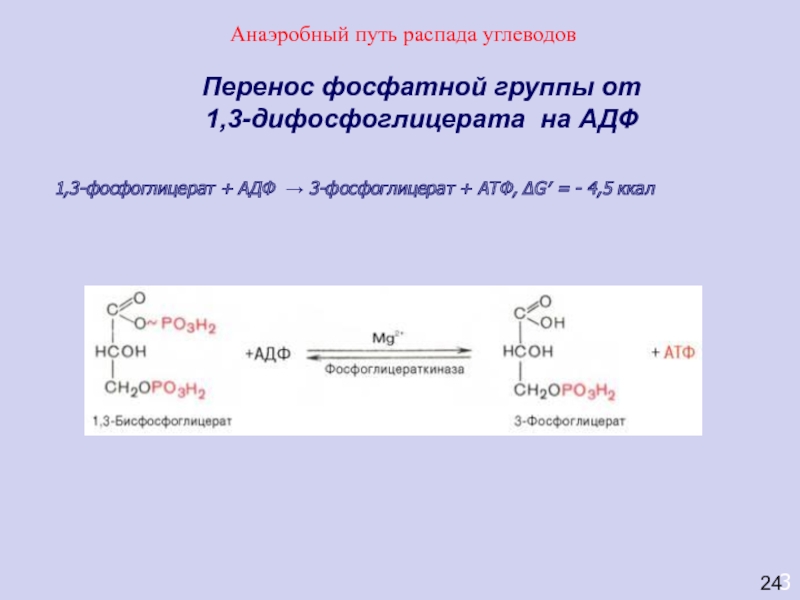
Перенос фосфатной группы от 1,3-дифосфоглицерата на АДФ
1,3-фосфоглицерат + АДФ →
3-фосфоглицерат + АТФ, ΔG′ = - 4,5 ккал
24
Анаэробный путь распада
углеводов
Слайд 423
Превращение 3-фосфоглицерата в 2-фосфоглицерат
3–фосфоглицерат ↔
2–фосфоглицерат
25
Анаэробный путь распада углеводов
Слайд 433
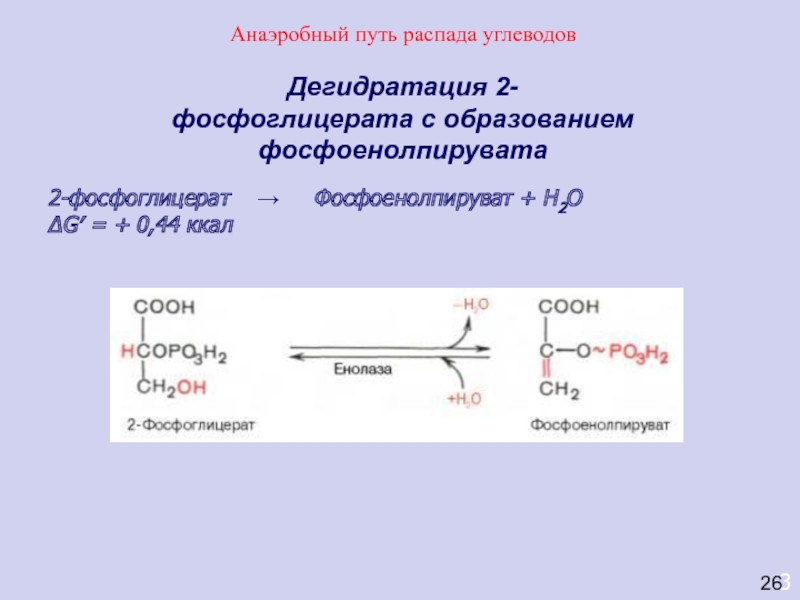
Дегидратация 2-фосфоглицерата с образованием фосфоенолпирувата
2-фосфоглицерат → Фосфоенолпируват
+ Н2О
ΔG′ = + 0,44 ккал
26
Анаэробный путь распада углеводов
Слайд 443
Перенос фосфатной группы от фосфоенолпирувата на АДФ
Фосфоенолпируват + АДФ →
Пируват + АТФ,
ΔG′ = - 7,5 ккал
27
Анаэробный путь
распада углеводов
Слайд 453
Восстановление пирувата до лактата
Пируват + НАД*Н + Н ↔
Лактат + НАД+,
ΔG′ = - 6,0 ккал
28
Анаэробный
путь распада углеводов
Слайд 463
Полный баланс гликолиза
Глюкоза + 2 АТФ + 2 НАД+ +
2 Фн + 4 АДФ + 2 НАДН +2Н+
2 Лактат+2
АДФ+2 НАДH + 2H+ + 2 НАД + + 4 АТФ + 2 Н2О
Вычеркнув одни и те же члены получим:
Глюкоза + 2 Фн + 2 АДФ → 2 Лактат + 2 АТФ + 2 Н2О
29
Анаэробный путь распада углеводов
Слайд 47Аэробный путь распада углеводов
Аэробный путь распада углеводов – основной путь
образования энергии в клетке
Аэробный путь распада углеводов
Дихотомический
(непрямой)
Апотомический
(прямой):
пентозофосфатный путь окисления углеводов
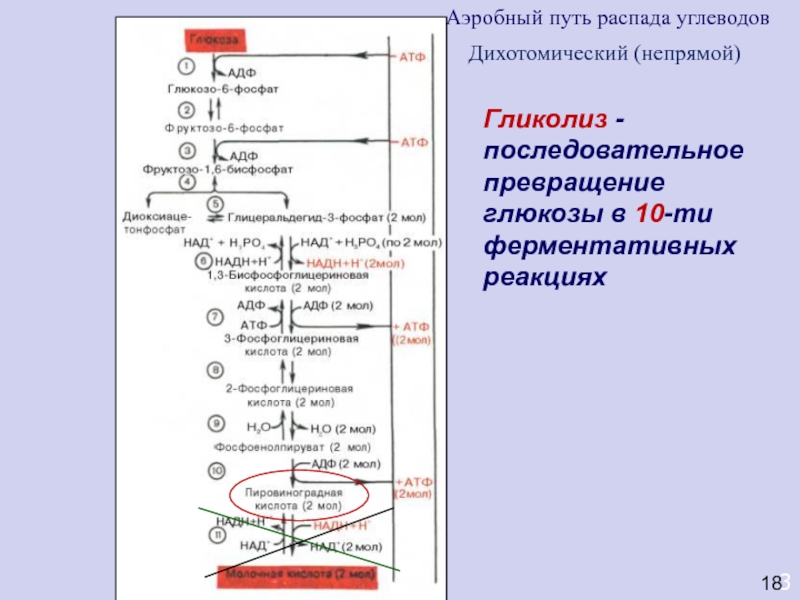
Слайд 483
Гликолиз -
последовательное превращение глюкозы в 10-ти ферментативных реакциях
18
Аэробный путь
распада углеводов
Дихотомический (непрямой)
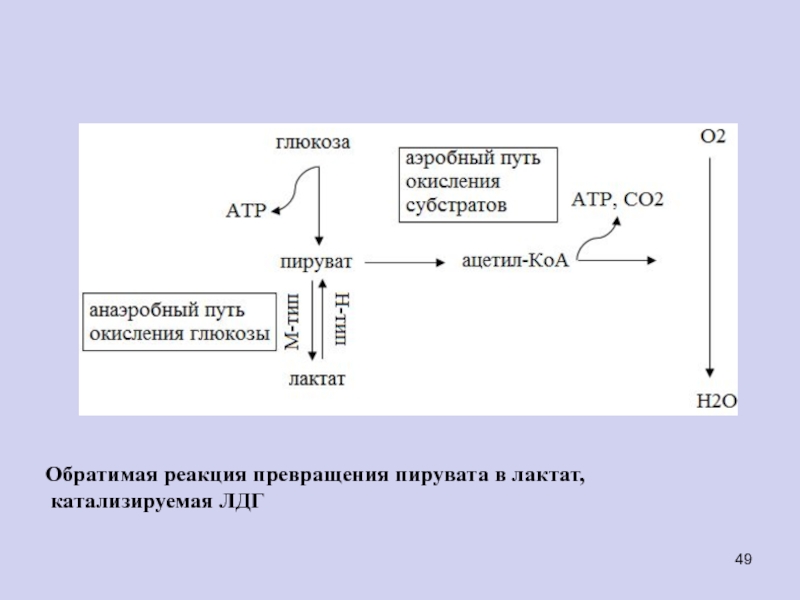
Слайд 49
Обратимая реакция превращения пирувата в лактат,
катализируемая ЛДГ
Слайд 50
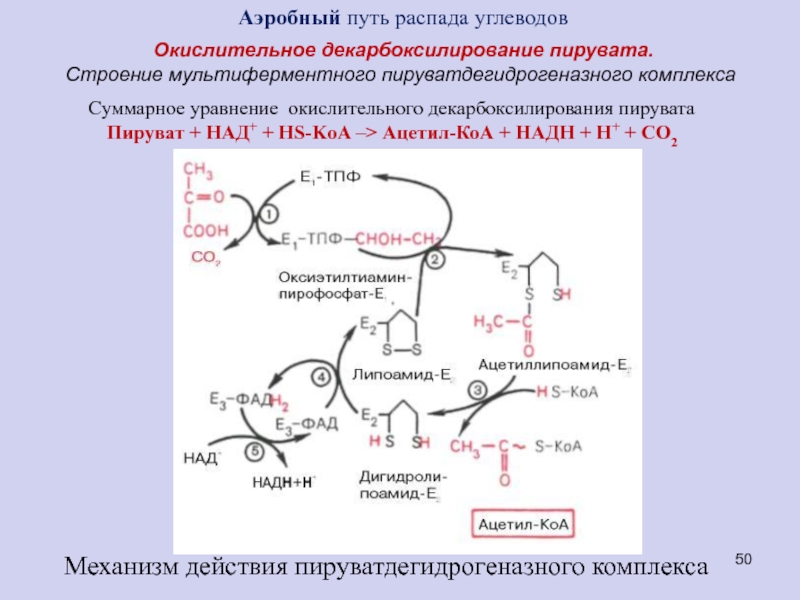
Окислительное декарбоксилирование пирувата.
Строение мультиферментного пируватдегидрогеназного комплекса
Механизм действия пируватдегидрогеназного
комплекса
Суммарное уравнение окислительного декарбоксилирования пирувата
Пируват + НАД+ + HS-KoA –>
Ацетил-КоА + НАДН + Н+ + СO2
Аэробный путь распада углеводов
Слайд 51Аэробный путь распада углеводов
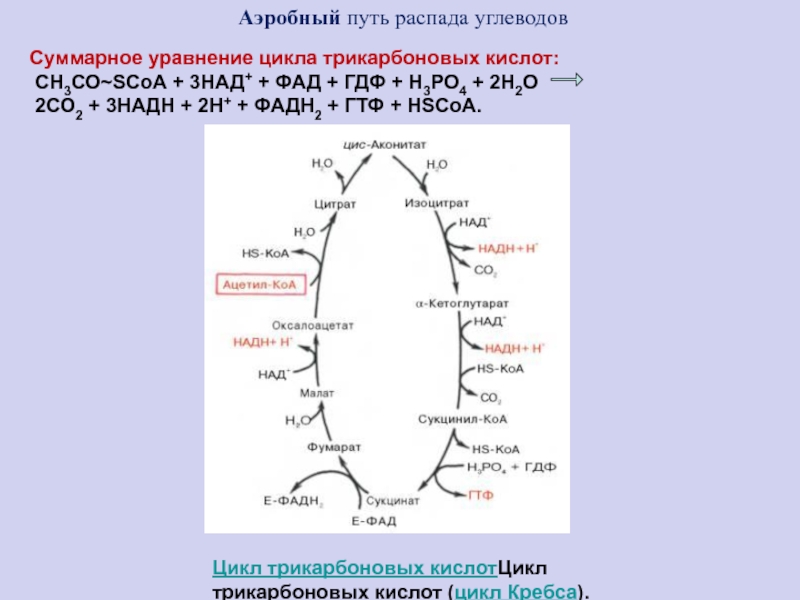
Цикл трикарбоновых кислотЦикл трикарбоновых кислот (цикл Кребса).
Суммарное
уравнение цикла трикарбоновых кислот:
СН3СО~SСоА + 3НАД+ + ФАД + ГДФ
+ Н3РО4 + 2Н2О
2СО2 + 3НАДН + 2Н+ + ФАДН2 + ГТФ + НSСоА.
Слайд 52
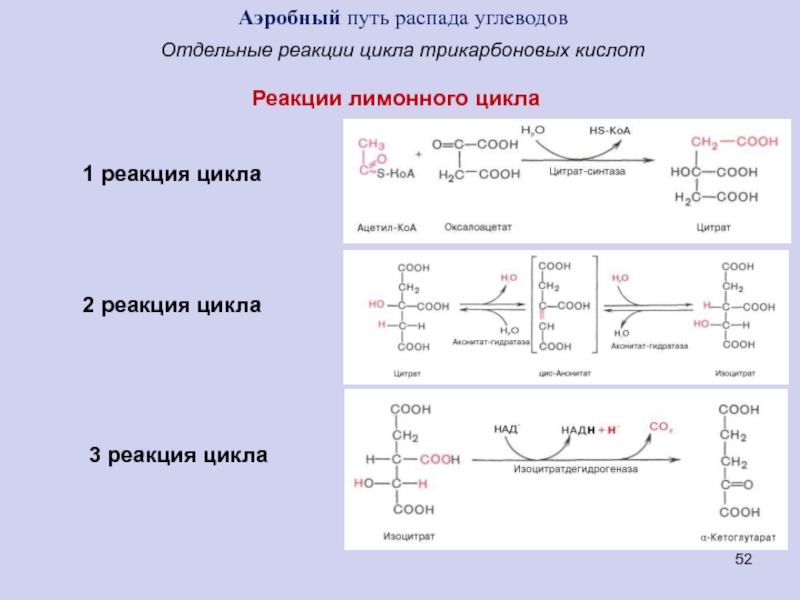
Отдельные реакции цикла трикарбоновых кислот
Реакции лимонного цикла
1 реакция цикла
2
реакция цикла
3 реакция цикла
Аэробный путь распада углеводов
Слайд 53
Отдельные реакции цикла трикарбоновых кислот
Реакции лимонного цикла
4 реакция цикла
5
реакция цикла
6 реакция цикла
Аэробный путь распада углеводов
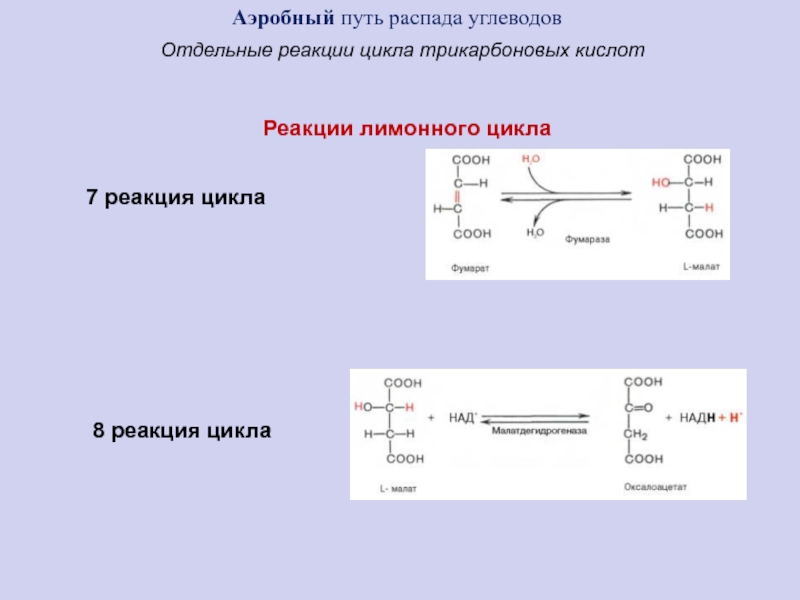
Слайд 547 реакция цикла
8 реакция цикла
Аэробный путь распада углеводов
Отдельные реакции
цикла трикарбоновых кислот
Реакции лимонного цикла
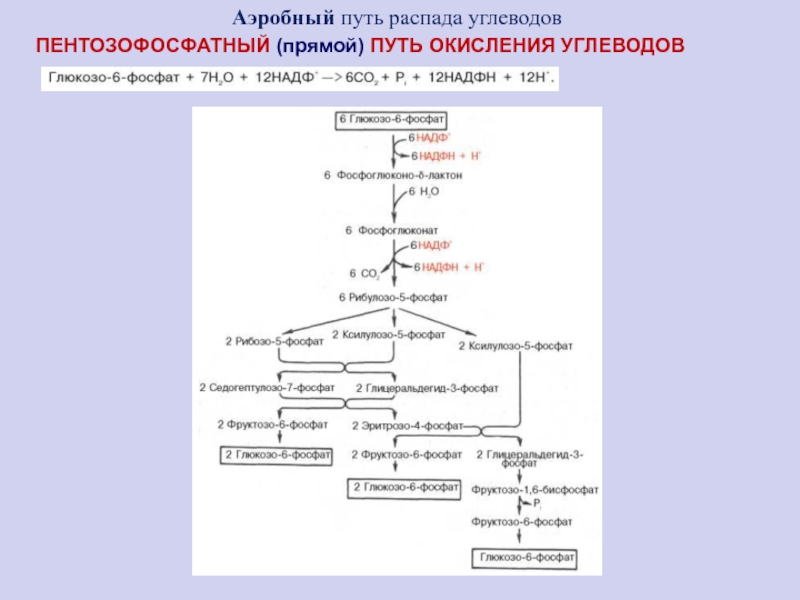
Слайд 55ПЕНТОЗОФОСФАТНЫЙ (прямой) ПУТЬ ОКИСЛЕНИЯ УГЛЕВОДОВ
Аэробный путь распада углеводов
Слайд 563
35
Регуляция обмена углеводов:
В норме глюкоза в крови – 3,3 –
5,5 ммоль\литр
Нервный механизм
Гормональный уровень
Органный уровень
Общий контроль осуществляется ЦНС
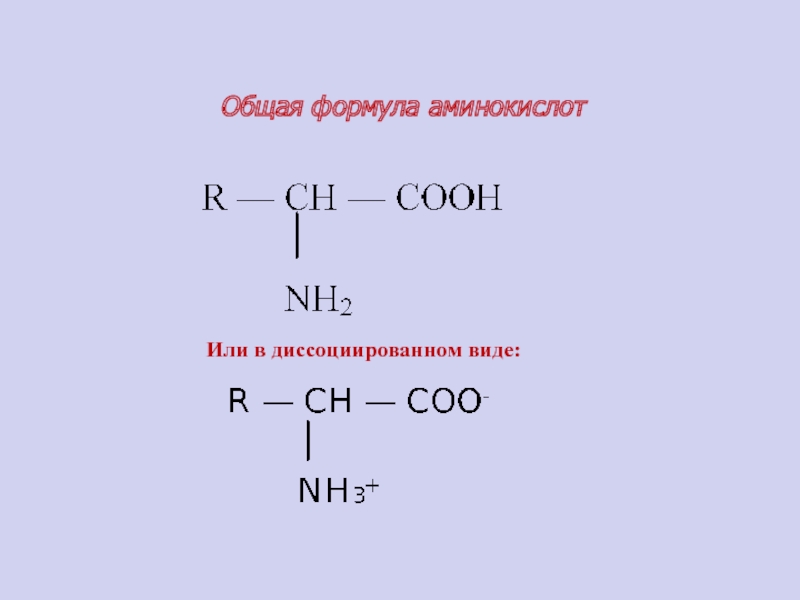
Слайд 59Общая формула аминокислот
Или в диссоциированном виде:
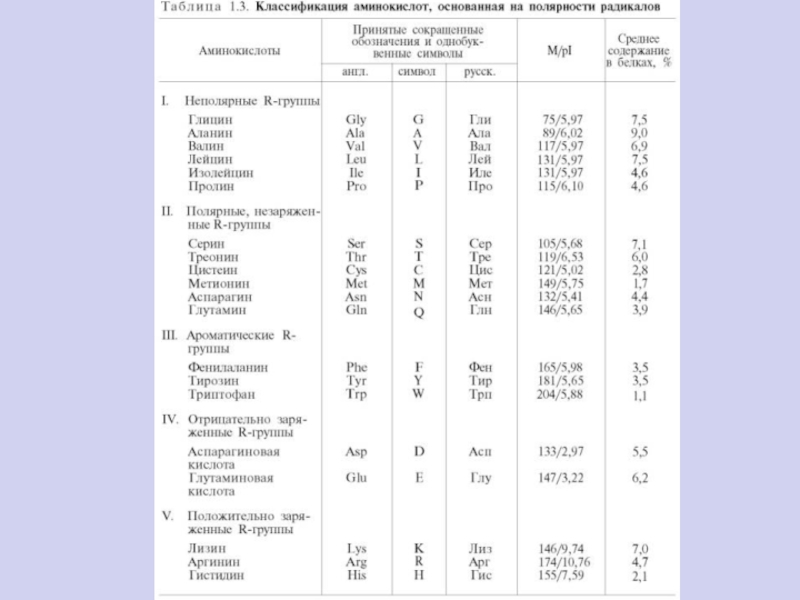
Слайд 60Незаменимыми для взрослого здорового человека являются 8 аминокислот: валин, изолейцин, лейцин, лизин, метионин, треони́н, триптофан и фенилалани́н;
Для детей
незаменимыми также являются аргинин и гистидин.
Слайд 61
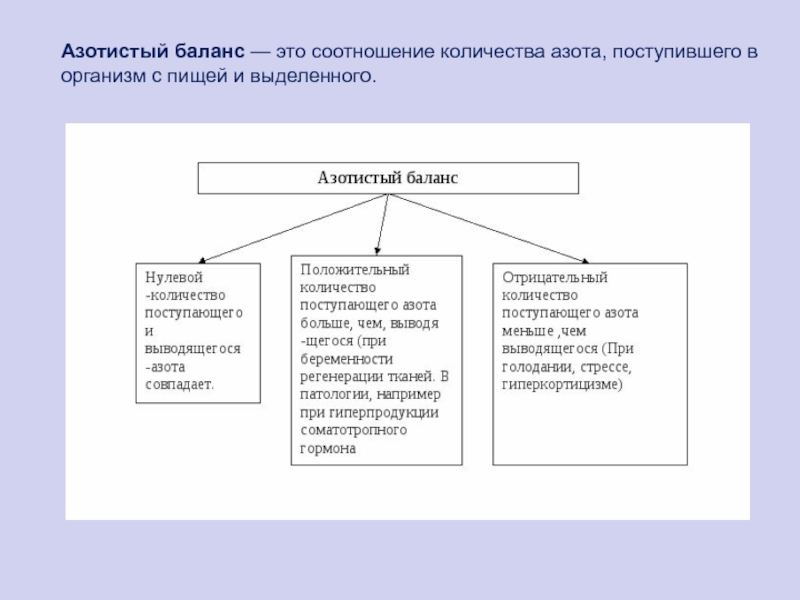
Азотистый баланс — это соотношение количества азота, поступившего в организм с
пищей и выделенного.
Слайд 62
Переваривание и всасывание в ЖКТ
Обмен белков
Слайд 63Промежуточный обмен аминокислот
=
Пути превращения аминокислот в клетках
Единые пути превращения
Дезаминирование
Переаминирование
декарбоксилирование
2.
Индивидуальные пути превращения
Слайд 64Доказано существование 4 типов дезаминирования аминокислот (отщепление аминогруппы). Выделены соответствующие
ферментные системы, катализирующие эти реакции, и идентифицированы продукты реакции. Во
всех случаях NH2-группа аминокислоты освобождается в виде аммиака.
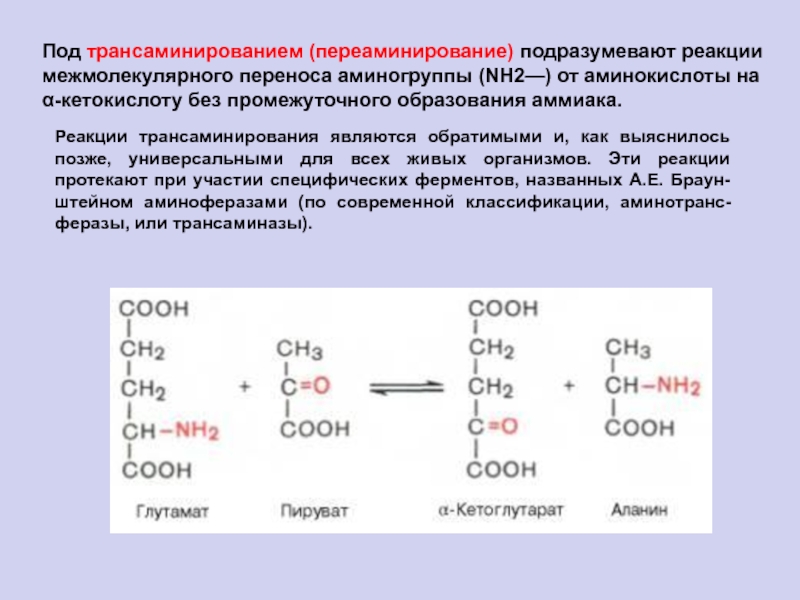
Слайд 65Под трансаминированием (переаминирование) подразумевают реакции межмолекулярного переноса аминогруппы (NH2—) от
аминокислоты на α-кетокислоту без промежуточного образования аммиака.
Реакции трансаминирования являются
обратимыми и, как выяснилось позже, универсальными для всех живых организмов. Эти реакции протекают при участии специфических ферментов, названных А.Е. Браун-штейном аминоферазами (по современной классификации, аминотранс-феразы, или трансаминазы).
Слайд 66Процесс отщепления карбоксильной группы аминокислот в виде СО2 получил название
декарбоксилирования. Несмотря на ограниченный круг аминокислот и их производных, подвергающихся
декарбоксилированию в животных тканях, образующиеся продукты реакции – биогенные амины – оказывают сильное фармакологическое действие на множество физиологических функций человека и животных. В животных тканях установлено декарбоксилирование следующих аминокислот и их производных: тирозина, триптофана, 5-окситриптофана, валина, серина, гистидина, глу-таминовой и γ-оксиглутаминовой кислот, 3,4-диоксифенилаланина, цис-теина, аргинина, орнитина, S-аденозилметионина и α-аминомалоновой кислоты. Помимо этого, у микроорганизмов и растений открыто де-карбоксилирование ряда других аминокислот.
В живых организмах открыты 4 типа декарбоксилирования аминокислот:
1. α-Декарбоксилирование, характерное для тканей животных, при котором от аминокислот отщепляется карбоксильная группа, стоящая по соседству с α-углеродным атомом. Продуктами реакции являются СО2 и биогенные амины:
Слайд 67Конечные продукты распада аминокислот:
Углекислый газ (СО2)
Вода (Н2О)
Аммиак
(NH3)
Аммиак – конечный продукт превращений аминокислот в клетках, образуется при
реакциях дезаминирования.
– источник азота в организме;
– высокотоксическое вещество;
– ингибирует многие ферменты, особенно чувствительна к NH3 ЦНС;
Слайд 68Пути обезвреживания аммиака:
1. Аммиак в клетках связывается с глюкуроновой или
аспарагиновой кислотами с образованием безвредных амидов в виде глютамина и
аспарагина;
2. Образование аммонийных солей, которые выводятся через почки с мочой;
3. Основной путь обезвреживания аммиака – синтез мочевины, которая выводится через почки.
Слайд 69Небелковые азотистые компоненты крови:
Мочевина;
Аминокислоты;
Креатин
Креатинин
Мочевая кислота
Полипептиды, нуклеотиды, билирубин,глутатион и др.
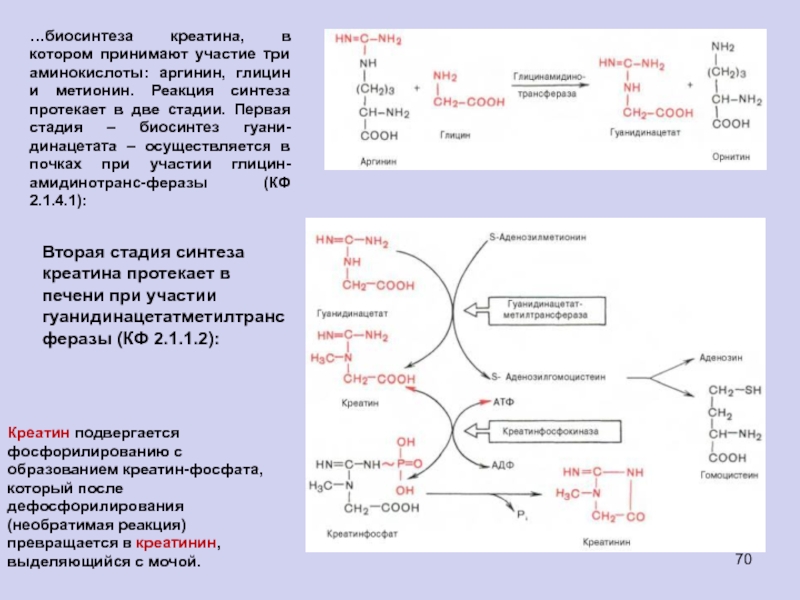
Слайд 70…биосинтеза креатина, в котором принимают участие три аминокислоты: аргинин, глицин
и метионин. Реакция синтеза протекает в две стадии. Первая стадия
– биосинтез гуани-динацетата – осуществляется в почках при участии глицин-амидинотранс-феразы (КФ 2.1.4.1):
Вторая стадия синтеза креатина протекает в печени при участии гуанидинацетатметилтрансферазы (КФ 2.1.1.2):
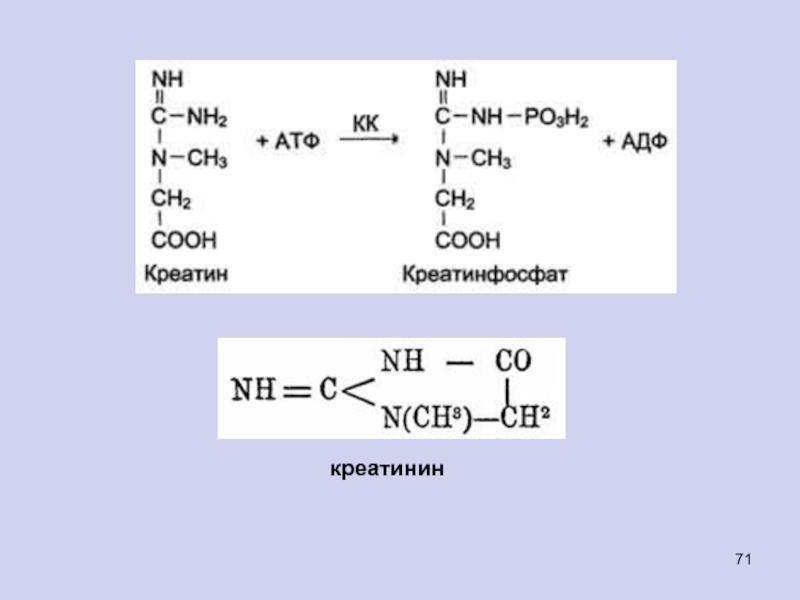
Креатин подвергается фосфорилированию с образованием креатин-фосфата, который после дефосфорилирования (необратимая реакция) превращается в креатинин, выделяющийся с мочой.
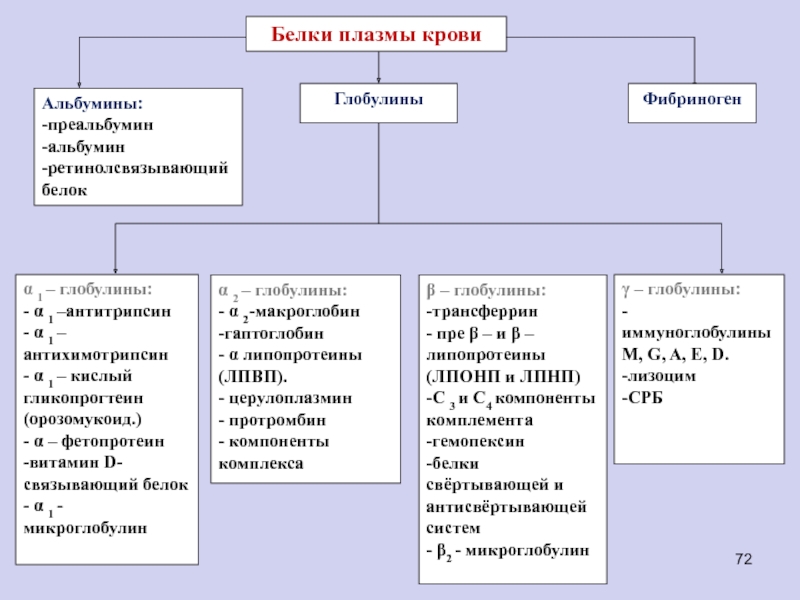
Слайд 73Белки и другие заряженные макромолекулы можно разделять методами электрофореза. Среди
различных электрофоретических методов наиболее простым является электрофорез на носителе, особенно
на ацетилцеллюлозной пленке. При этом сывороточные белки, которые из-за наличия избыточного отрицательного заряда движутся к аноду, разделяются на пять вышеупомянутых фракций. После разделения белки можно окрашивать с помощью красителей и денситометрически оценивать количества белков в полученных окрашенных полосах.
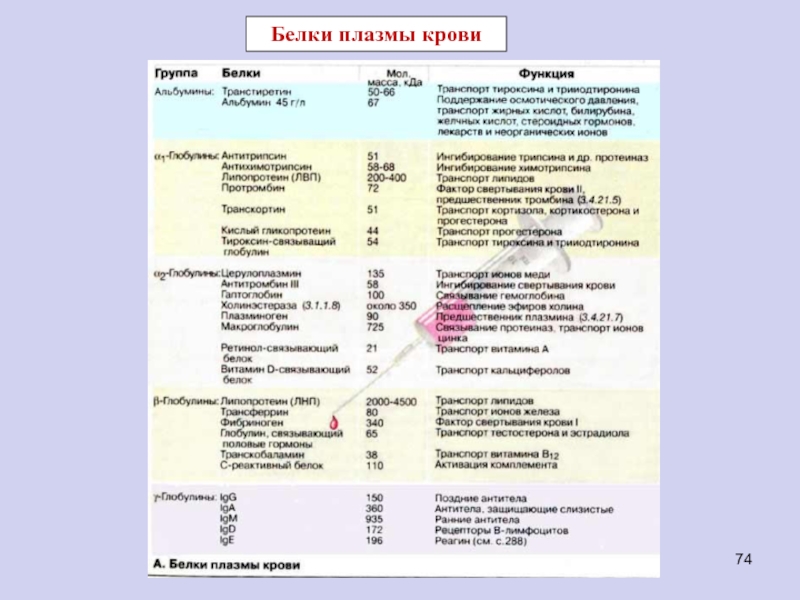
Слайд 75Белки плазмы крови выполняют следующие функции:
1. поддерживают онкотическое давление и
тем самым постоянный объём крови, т.е. связывают воду, задерживают её
и не позволяют выходить из кровяного русла;
2. определяют вязкость крови;
3. входят в состав белковой буферной системы, тем самым участвуя в регуляции рН крови;
4. связывают и транспортируют гормоны, липиды, витамины, лекарственные вещества, ионы (Ca2+, Fe2+, Cu2+) и др.
5. служат резервом заменимых и незаменимых аминокислот;
Белки плазмы крови
Слайд 76Нормальное содержание общего белка крови 65-85г/л.
Нормопротеинемия – нормальное содержание белка;
Гипопротеинемия
– пониженное содержание белка;
Гиперпротеинемия – повышенное содержание белка;
Изменение концентрации общего
белка
Относительное:
1.Относительная гипопротеинемия;
2. Относительная гиперпротеинемия;
Абсолютное:
1. Абсолютная гипопротеинемия;
2. Абсолютная гиперпротеинемия;
Белки плазмы крови
Слайд 77Диспротеинемия – нарушение соотношения белковых фракций.
Парапротеинемия – состояние, характеризующиеся
появлением в сыворотке крови белков, неопределяющихся в норме.
Белки плазмы крови
Слайд 78 Нуклеиновые кислоты играют основную роль в хранении и передаче
генетической информации
Дезоксирибонуклеиновые кислоты - обеспечивают хранение генетической информации
Рибонуклеиновые кислоты –
принимают участие в реализации генетической информации
(различные виды РНК)
ДНК у прокариот (одна молекула - хромосома) формирует нуклеоид – компактная структура
ДНК эукариот (много молекул) неравномерно распределена по хромосомам в комплексе с белками
Вирусы в качестве генетического материала могут содержать ДНК или РНК (одно и двух-цепочечную)
Обмен сложных белков - нуклеопротеинов
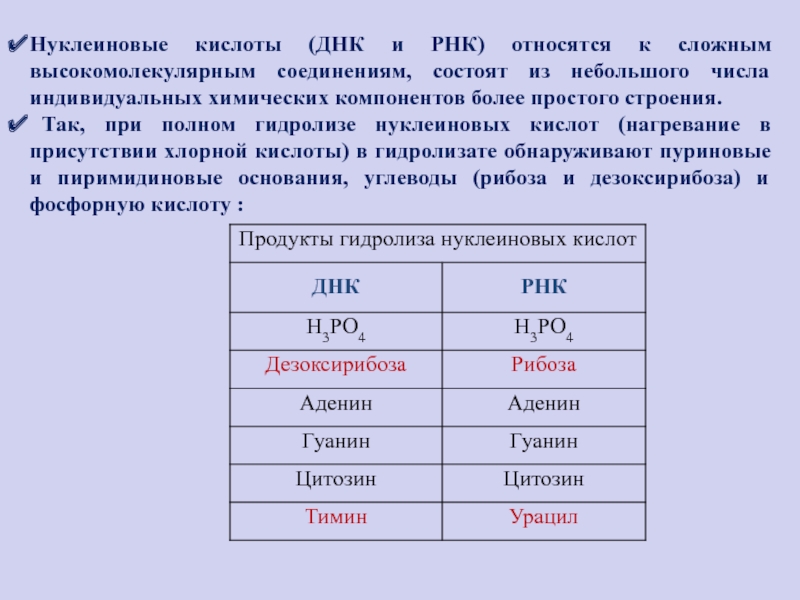
Слайд 79Нуклеиновые кислоты (ДНК и РНК) относятся к сложным высокомолекулярным соединениям,
состоят из небольшого числа индивидуальных химических компонентов более простого строения.
Так, при полном гидролизе нуклеиновых кислот (нагревание в присутствии хлорной кислоты) в гидролизате обнаруживают пуриновые и пиримидиновые основания, углеводы (рибоза и дезоксирибоза) и фосфорную кислоту :
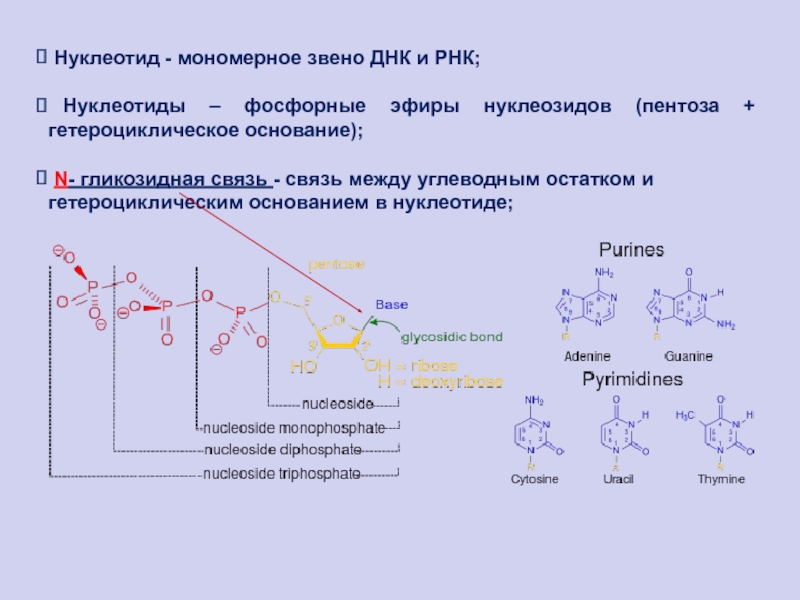
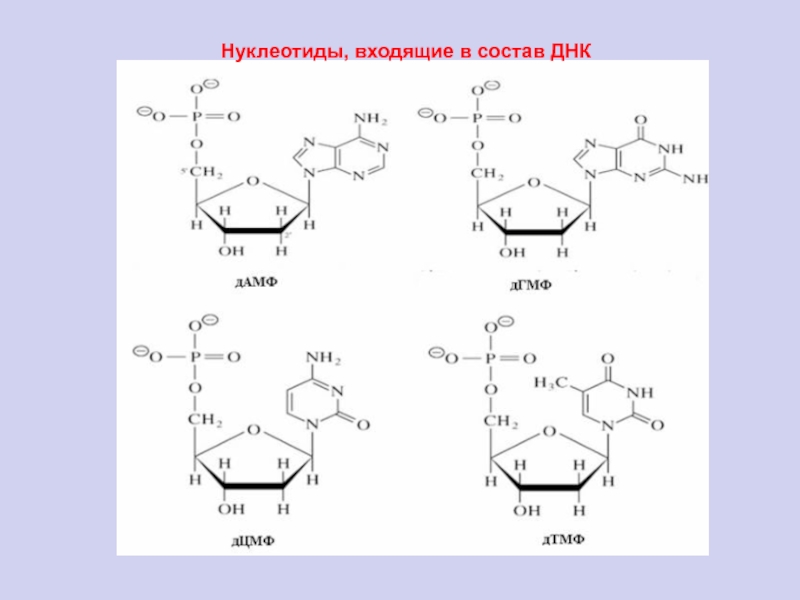
Слайд 80 Нуклеотид - мономерное звено ДНК и РНК;
Нуклеотиды –
фосфорные эфиры нуклеозидов (пентоза + гетероциклическое основание);
N- гликозидная связь
- связь между углеводным остатком и гетероциклическим основанием в нуклеотиде;
Слайд 81Нуклеотиды, входящие в состав ДНК
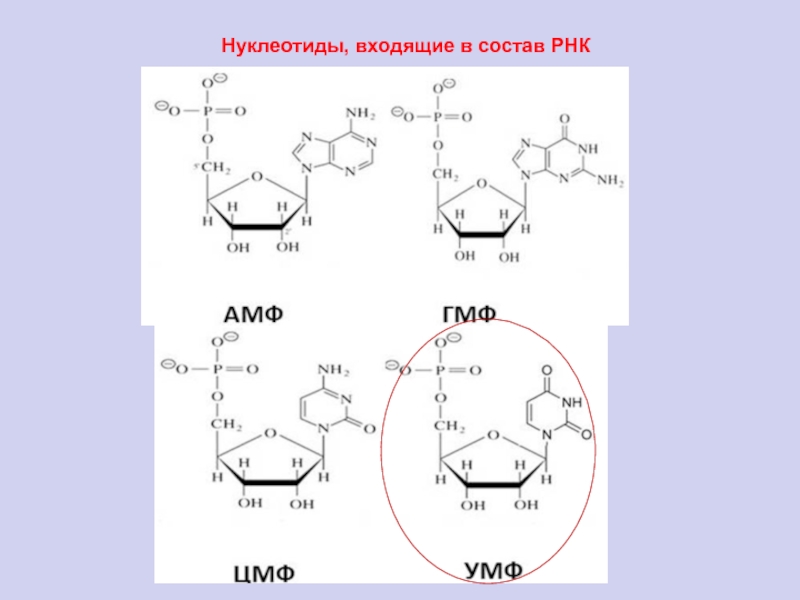
Слайд 82Нуклеотиды, входящие в состав РНК
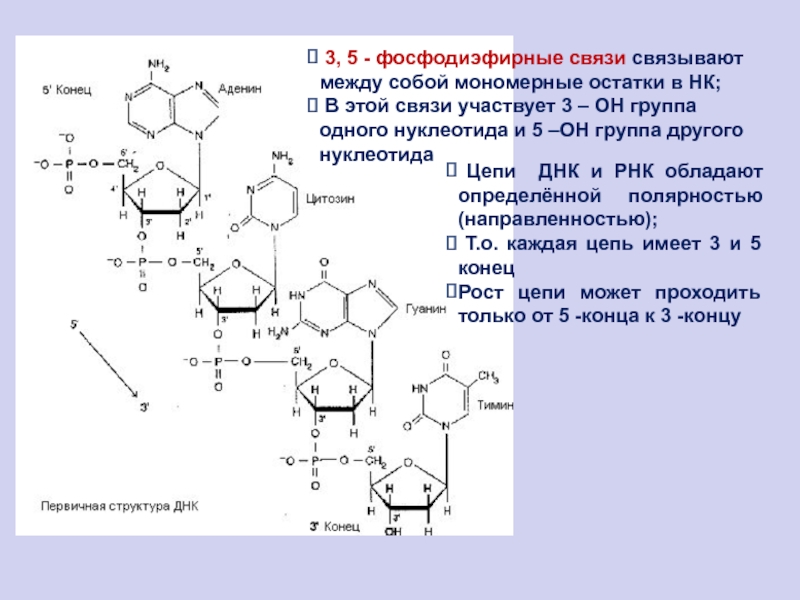
Слайд 83 3, 5 - фосфодиэфирные связи связывают между собой мономерные
остатки в НК;
В этой связи участвует 3 – ОН
группа одного нуклеотида и 5 –ОН группа другого нуклеотида
Цепи ДНК и РНК обладают определённой полярностью (направленностью);
Т.о. каждая цепь имеет 3 и 5 конец
Рост цепи может проходить только от 5 -конца к 3 -концу
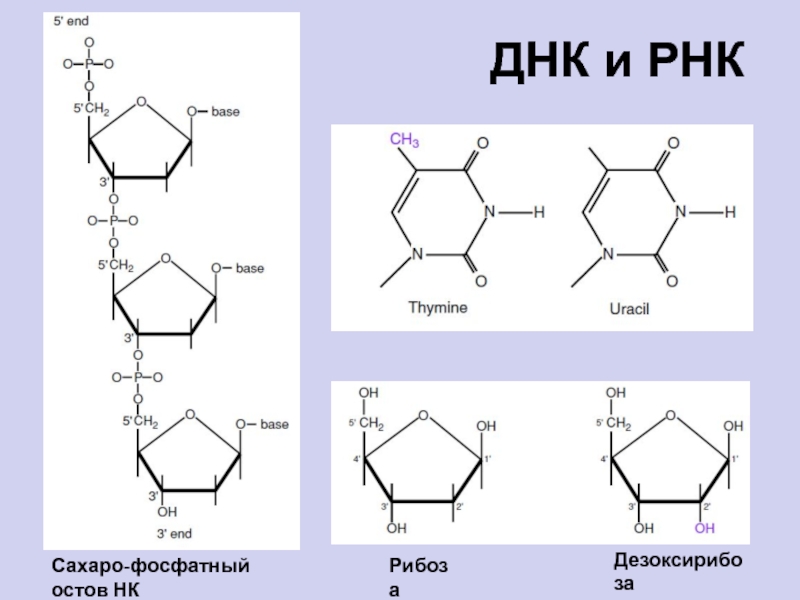
Слайд 84ДНК и РНК
Рибоза
Дезоксирибоза
Сахаро-фосфатный остов НК
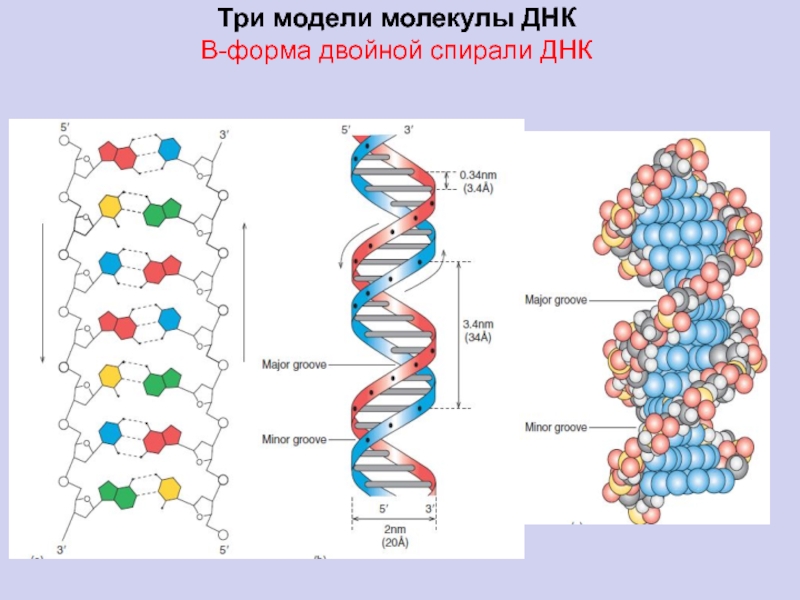
Слайд 85Три модели молекулы ДНК
В-форма двойной спирали ДНК
Слайд 86
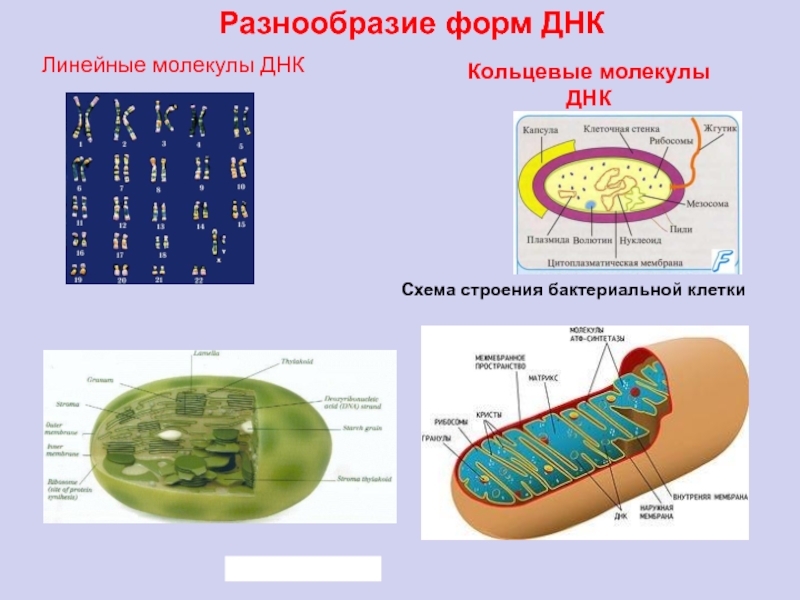
Линейные молекулы ДНК
Схема строения бактериальной клетки
Кольцевые молекулы ДНК
Разнообразие форм ДНК
Слайд 87Структура и функции РНК
Содержание РНК в любых клетках в
5 – 10 раз превышает содержание ДНК.
Основная роль РНК:
-
трансляция генетической информации с образованием белков;
осуществление некоторых специализированных эндонуклеазных функций, возможно регулирующих различные этапы экспрессии генов.
Геномы некоторых вирусов (ретровирусов и множества вирусов животных, растений и насекомых) представлены одно- и двуцепочечной молекулой РНК.
Слайд 88
--- гетерогенная ядерная РНК (гяРНК);
--- малые ядерные РНК (мяРНК =
snRNA), участвующие в процессинге предшественников мРНК эукариот;
--- рибосомные РНК (р-РНК);
---
транспортные РНК (т-РНК);
--- РНК, входящие в состав ферментов (теломерная РНК);
--- малые цитоплазматические РНК (мц-РНК);
--- микро-РНК (или природные антисмысловые РНК);
---ми-РНК (малые интерферирующие РНК);
Виды РНК
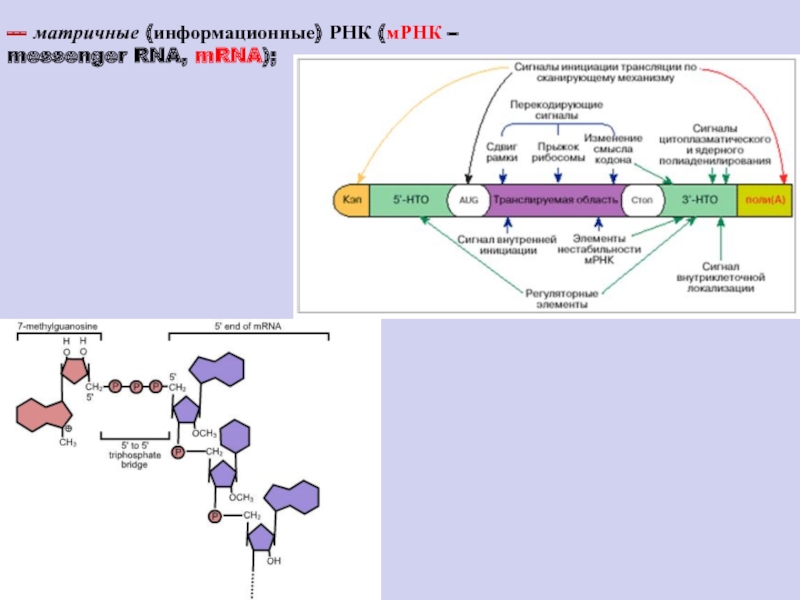
На первом этапе экспрессии генов происходит переписывание генетической информации, заключенной в генах, на матричные (информационные) РНК (мРНК – messenger RNA, mRNA), которые являются местом промежуточного хранения этой информации при ее реализации.
В некоторых случаях уже сами РНК являются конечным результатом экспрессии генов, и после ряда ферментативных модификаций они непосредственно используются в клеточных процессах:
Слайд 89Распределение РНК в клетке:
80 – 85 % массы клеточных РНК
составляют три (прокариоты) или четыре (эукариоты) вида рРНК;
около 10 %
- тРНК;
5% клеточной РНК – несколько тысяч различных матричных РНК;
менее 2% от общего количества РНК – малые ядерные и цитоплазматические РНК, число видов которых пока неизвестно.
Слайд 90--- матричные (информационные) РНК (мРНК – messenger RNA, mRNA);
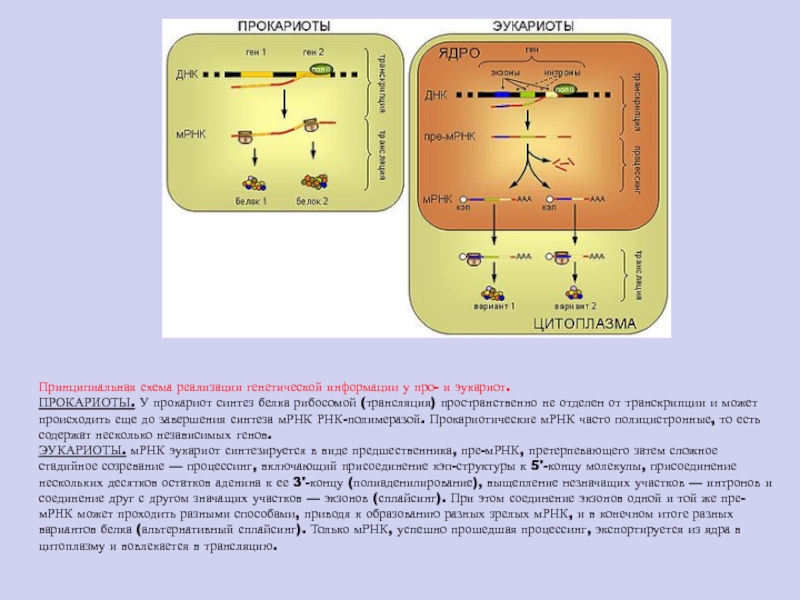
Слайд 91Принципиальная схема реализации генетической информации у про- и эукариот.
ПРОКАРИОТЫ. У
прокариот синтез белка рибосомой (трансляция) пространственно не отделен от транскрипции
и может происходить еще до завершения синтеза мРНК РНК-полимеразой. Прокариотические мРНК часто полицистронные, то есть содержат несколько независимых генов.
ЭУКАРИОТЫ. мРНК эукариот синтезируется в виде предшественника, пре-мРНК, претерпевающего затем сложное стадийное созревание — процессинг, включающий присоединение кэп-структуры к 5'-концу молекулы, присоединение нескольких десятков остатков аденина к ее 3'-концу (полиаденилирование), выщепление незначащих участков — интронов и соединение друг с другом значащих участков — экзонов (сплайсинг). При этом соединение экзонов одной и той же пре-мРНК может проходить разными способами, приводя к образованию разных зрелых мРНК, и в конечном итоге разных вариантов белка (альтернативный сплайсинг). Только мРНК, успешно прошедшая процессинг, экспортируется из ядра в цитоплазму и вовлекается в трансляцию.
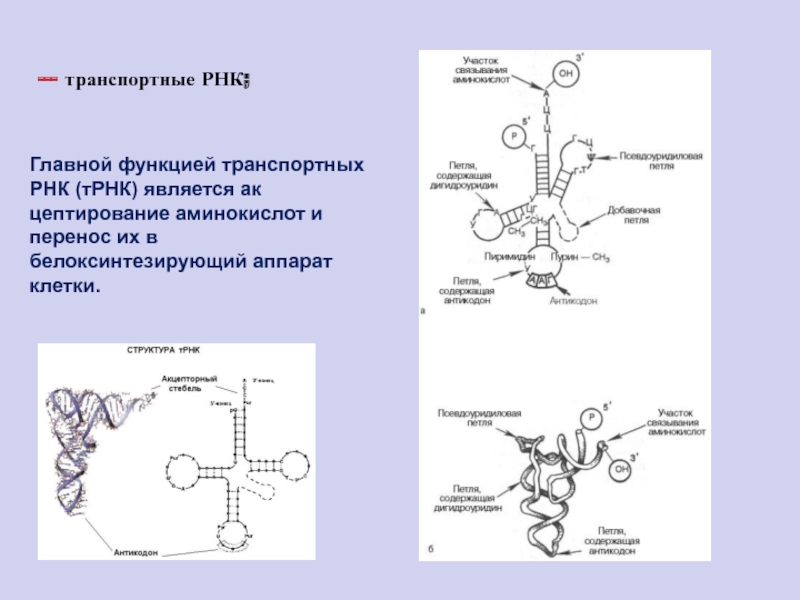
Слайд 92--- транспортные РНК;
Главной функцией транспортных РНК (тРНК) является акцептирование аминокислот
и перенос их в белоксинтезирующий аппарат клетки.
Слайд 93р-РНК
Атомарная структура бактериальной рибосомы. Молекулы рибосомных РНК окрашены в оранжевый
цвет, белки малой субчастицы — в голубой, белки большой субчастицы
— в зелёный. Молекула антибиотика (красная) химически взаимодействует с малой субчастицей. Изучение таких сложных структур помогает разрабатывать новые эффективные антибиотики.
--- рибосомные РНК;
Высокомолекулярные рибосомные РНК (рРНК) являются структурной основой для формирования рибонуклепротеиново тяжа который, складываясь в пространстве, дает начало 30-40 S и 50-60 S-субчастицам рибосомы;
рРНК взаимодействуют с м-РНК и аминоацил-тРНК в процессе трансляции.
Низкомолекулярная 5SpPHK в комплексе с рибосомными белками формирует комплекс, который называют третьей субчастицей рибосомы, где 5SpPHK выступает в роли посредника между пептидилтрансферазным центром и EF-G-связывающими доменами
Слайд 96
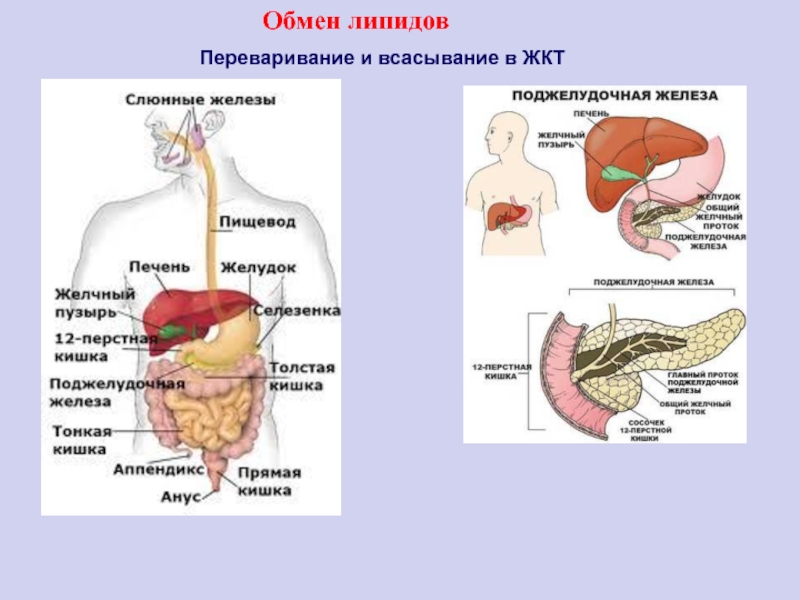
Переваривание и всасывание в ЖКТ
Обмен липидов
Слайд 97http://upload.wikimedia.org/wikipedia/commons/0/0f/Peristalsis.gif
Периста́льтика (др.-греч. περισταλτικός — обхватывающий и сжимающий) — волнообразное сокращение
стенок полых трубчатых органов (пищевода, желудка, кишечника, мочеточников и др.),
способствующее продвижению их содержимого к выходным отверстиям.
Слайд 98В живых организмах происходит ферментативный гидролиз жиров. В кишечнике под
влиянием фермента липазы жиры пищи гидрализуются на глицерин и органические
кислоты, которые всасываются стенками кишечника, и в организме синтезируются новые жиры, свойственные данному организму. Они по лимфатической системе поступают в кровь, а затем в жировую ткань. Отсюда жиры поступают в другие органы и ткани организма, где в процессе обмена веществ в клетках опять гидролиэуются и затем постепенно окисляются до оксида углерода и воды с выделеиием энергии, необходимой для жизнедеятельности.
Омыляемые липиды
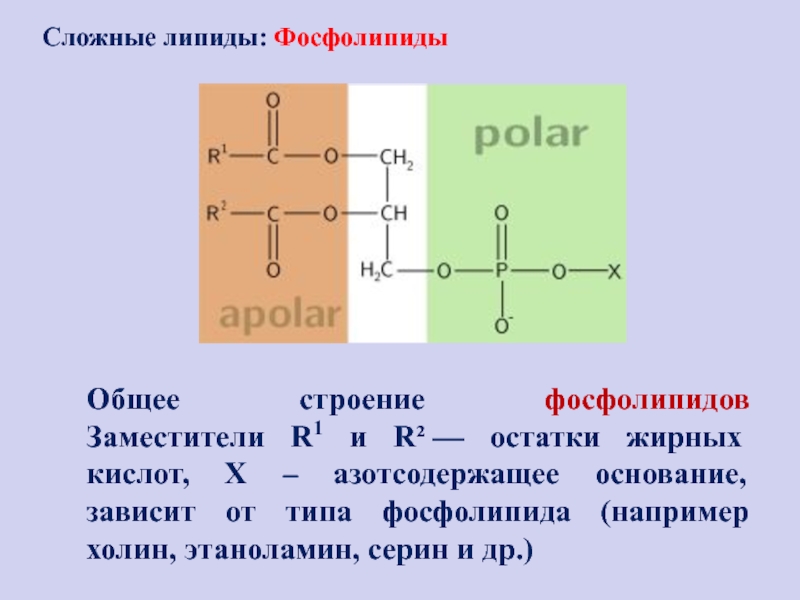
Слайд 99Общее строение фосфолипидов
Заместители R1 и R² — остатки жирных кислот, X
– азотсодержащее основание, зависит от типа фосфолипида (например холин, этаноламин,
серин и др.)
Сложные липиды: Фосфолипиды
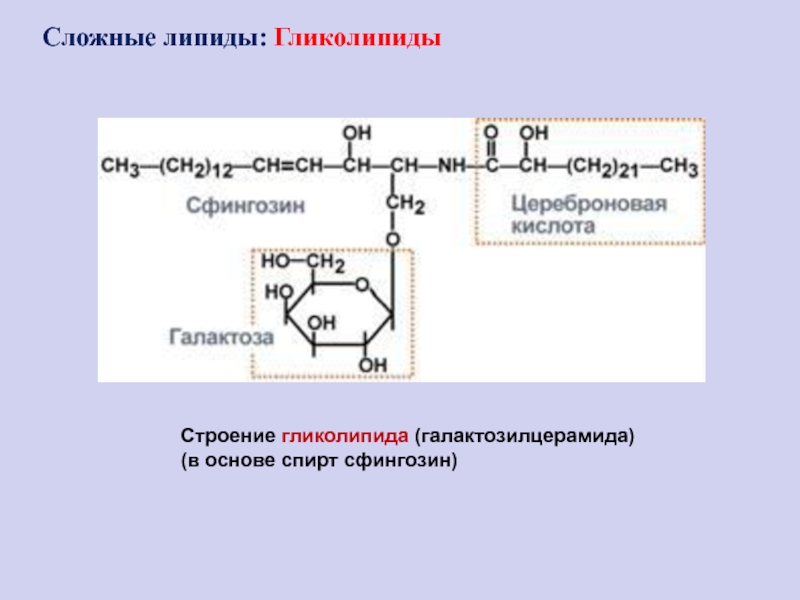
Слайд 100Строение гликолипида (галактозилцерамида)
(в основе спирт сфингозин)
Сложные липиды: Гликолипиды
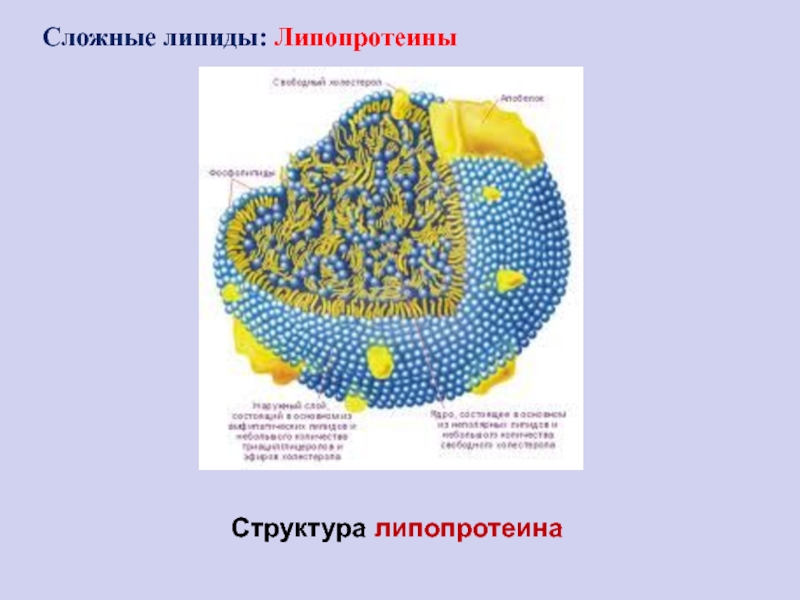
Слайд 101Структура липопротеина
Сложные липиды: Липопротеины
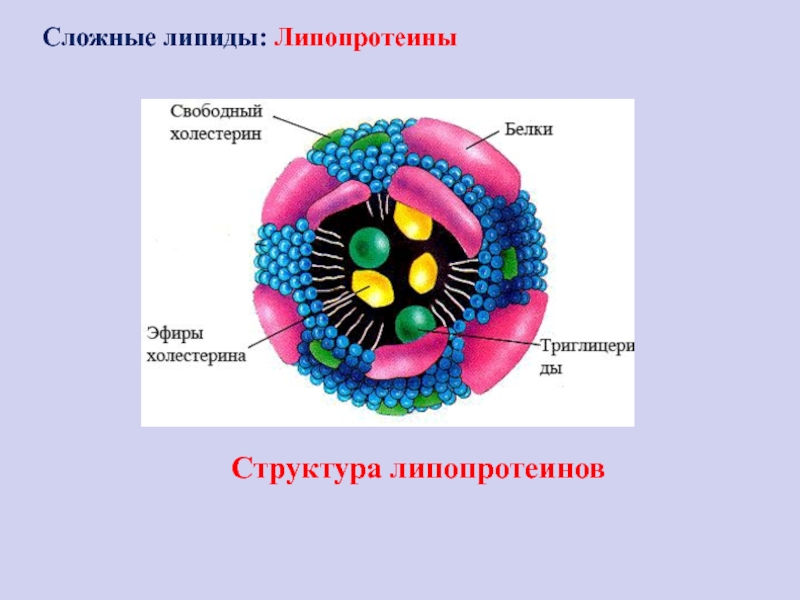
Слайд 102Структура липопротеинов
Сложные липиды: Липопротеины
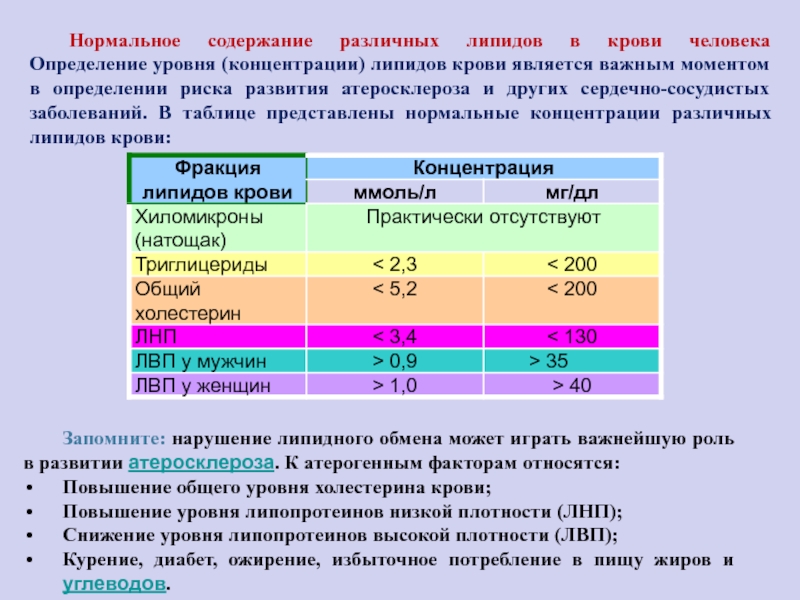
Слайд 103Нормальное содержание различных липидов в крови человека
Определение уровня (концентрации) липидов
крови является важным моментом в определении риска развития атеросклероза и
других сердечно-сосудистых заболеваний. В таблице представлены нормальные концентрации различных липидов крови:
Запомните: нарушение липидного обмена может играть важнейшую роль в развитии атеросклероза. К атерогенным факторам относятся:
Повышение общего уровня холестерина крови;
Повышение уровня липопротеинов низкой плотности (ЛНП);
Снижение уровня липопротеинов высокой плотности (ЛВП);
Курение, диабет, ожирение, избыточное потребление в пищу жиров и углеводов.
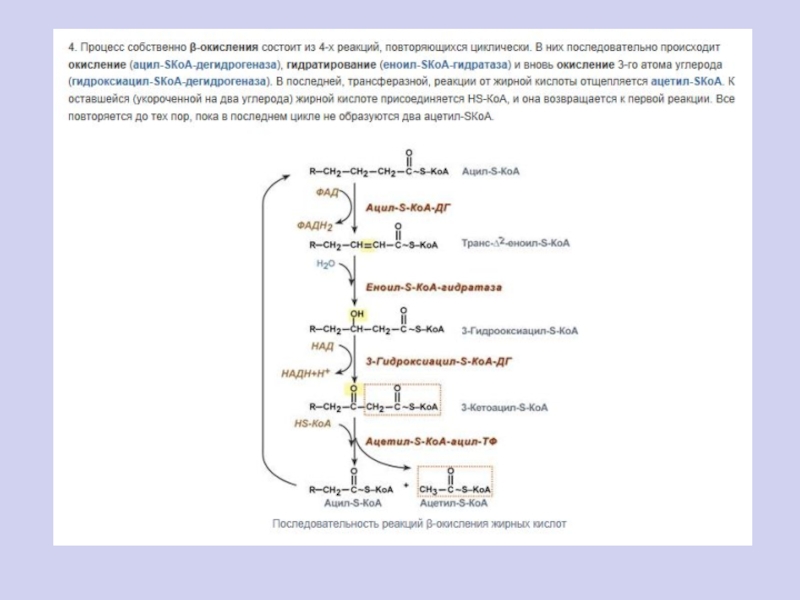
Слайд 105Активация жирных кислот.
Свободная жирная кислота независимо от длины углеводородной
цепи является метаболически инертной и не может подвергаться никаким биохимическим
превращениям, в том числе окислению, пока не будет активирована. Активация жирной кислоты протекает на наружной поверхности мембраны митохондрий при участии АТФ, коэнзима A (HS-KoA) и ионов Mg2+. Реакция катализируется ферментом ацил-КоА-синтетазой:
В результате реакции образуется ацил-КоА, являющийся активной формой жирной кислоты.