Слайд 1ДЫХАНИЕ РАСТЕНИЙ
«...Дыхание служит стимулом главнейших жизненных отправлений растений ... подобно
животным, они поглощают при переработке органических соединений в органические образования
кислород, выделяют углекислоту и освобождают тепловую энергию...»
А. С. Фаминцын
«И дышит сад легко, глубоко,
всей грудью яблонь, груш и слив»
Вс. Рождественский
Слайд 2План лекции
Энергетический цикл жизни. История развития учения о дыхании.
Дыхание и
его значение в жизни растений.
АТФ: структура и функции.
Строение и физиологические
особенности митохондрий.
Величины, определяющие дыхание: интенсивность дыхания, дыхательный коэффициент.
Влияние внешних условий и внутренних факторов на дыхание.
Схема дыхания по В.И.Палладину
Особенности химизма и энергетики дыхания в сравнении с горением.
Ферменты дыхания. Пути дыхательного обмена растений.
Гликолитический (дихотомический) путь дыхательного обмена.
Генетическая связь дыхания и брожения.
Пентозофосфатный (апотомический) путь дыхательного обмена.
Глиоксилатный цикл.
Альтернативный путь дыхания
Слайд 3С6Н12О6 + 6О2 → 6СО2 + 6Н2О + 2824 кДж
1.
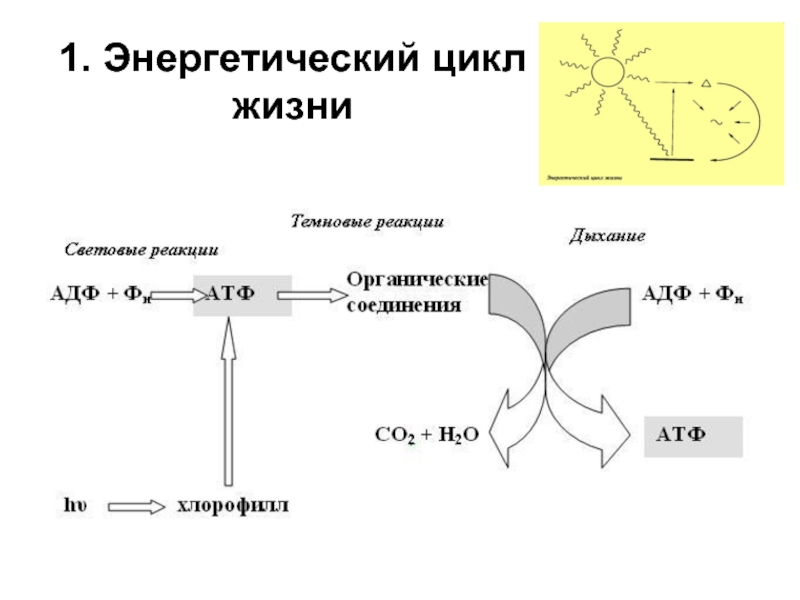
Энергетический цикл жизни
Слайд 4История развития учения о дыхании
Дыхание было обнаружено более 200 лет
назад (1771 -1779 гг.) вместе с фотосинтезом как процесс «порчения
воздуха»
Пристли Джозеф
(1733-1804)
Шееле Карл Вильгельм
(1742 –1786)
Слайд 5Лавуазье изображен во время проведения эксперимента по определению состава воды
путем поджигания смеси водорода и кислорода электрической искрой (гравюра XIX
в.).
Антуан Лавуазье (1743-1794)
А.Л. Лавуазье (1780) считал, что растения поглощают кислород для сжигания пищи. При дыхании, как и при горении поглощается кислород и образуется СО2, причем в обоих случаях выделяется теплота. Дыхание - это медленно текущее горение питательных веществ в живом организме.
УСТАНОВКА А.ЛАВУАЗЬЕ
для определения состава воздуха.
Слайд 6Показал (1778-80 гг.), что растения исправляют воздух на свету и
только зелеными частями, а незеленые части на свету и в
темноте, зеленые в темноте – портят.
Основатель учения (1797-1804 гг.). Ввел термин, уравнение, установил соотношение СО2/О2, которое как правило равно 1. Этот газообмен и есть дыхание. При этом образуется вода.
Николя-Теодор де Соссюр
(1767-1845)
Ян Ингенхауз
(1727-1806)
«Когда солнце, поднявшееся над горизонтом, разбудит своими лучами заснувшие за ночь растения, оно сделает их способными исполнять свою целительную функцию – исправлять воздух для животных; во мраке ночи эта деятельность совсем прекращается; днем же совершается с тем большим оживлением, чем светлее день и чем выгоднее расположено растение в отношении солнечных лучей. Затененные высокими зданиями или другими растениями, они не исправляют воздух, а, наоборот, выделяют вредный для дыхания животных воздух. К концу дня выработка очищенного воздуха ослабевает и при заходе солнца совершенно прекращается»
Слайд 7Ф.Ю. Мейен (Германия) в 1838 г. утверждал, что растению не
свойственно дыхание, как у животных.
Л.Гарро (Франция) – в 1850-1851 гг.установил,
что дыхание и фотосинтез – разные процессы.
Ж.Б. Буссенго в 1848 г.предложил уравнение дыхания.
Жан Батист Буссенго
(1802–1887)
Слайд 8Отто Варбург
НОБЕЛЕВСКАЯ ПРЕМИЯ 1933 г. за результаты
исследований связи
кислорода и рака
Альберт Сент-Дьёрдьи
американский биохимик, НОБЕЛЕВСКАЯ ПРЕМИЯ 1937 г.
по физиологии и медицине за работы по биологическому окислению.
Ханс Адольф Кребс (1900-1981)
английский биохимик, НОБЕЛЕВСКАЯ ПРЕМИЯ 1953 г. (совместно с Ф. Липманом) по физиологии и медицине за открытие цикла трикарбоновых кислот.
Слайд 9Вклад русских ученых
Палладин Владимир Иванович
(1859-1922)
Автор ферментативной теории дыхания растений
Бах
Алексей Николаевич
(1857-1946)
Автор перекисной теории медленного окисления
Бородин Иван Парфеньевич
(1847-1930)
В
1876 году защитил диссертацию «Физиологические исследования над дыханием листовых побегов» и получил степень магистра ботаники
Костычев Сергей Павлович (1877-1931)
экспериментально обосновал теорию о генетической связи дыхания и брожения
Слайд 102. Дыхание и его значение в жизни растений
Дыхание –
это процесс распада сложных органических соединений до СО2 и воды
при участии кислорода воздуха, сопровождаемый выделением энергии.
С6Н12О6+6О2→6СО2 + 6Н2О + 2824 кДж
Слайд 11Значение дыхания
Энергетическое. Энергия, выделяющаяся при дыхании, используется эндорганические процессы:
-
синтезы,
- поступление и транспорт веществ,
- рост
- поддержание структур
-
терморегуляция.
Дыхание → протонный потенциал → АТФ
2. Конструкционное
3. Образование воды
Ж. Б. Ламарк (1744 — 1829)
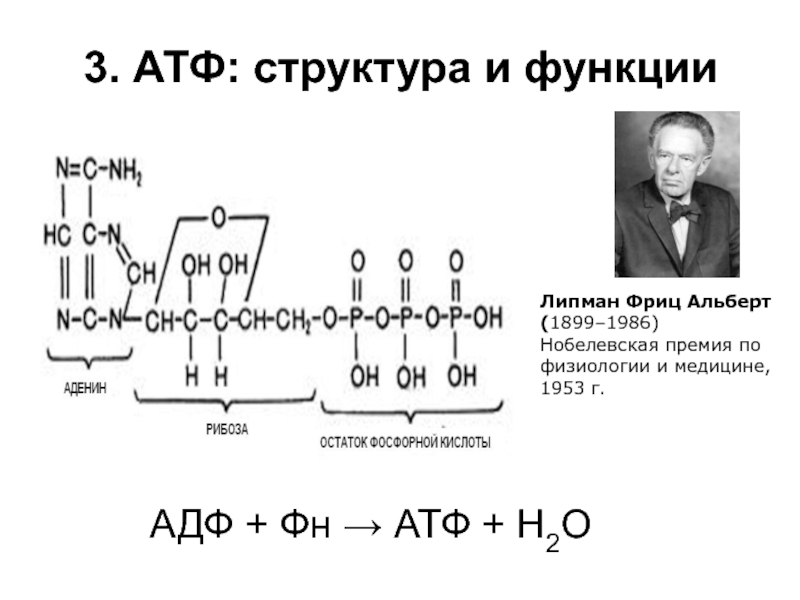
Слайд 123. АТФ: структура и функции
АДФ + Фн → АТФ +
Н2О
Липман Фриц Альберт
(1899–1986)
Нобелевская премия по
физиологии и медицине,
1953
г.
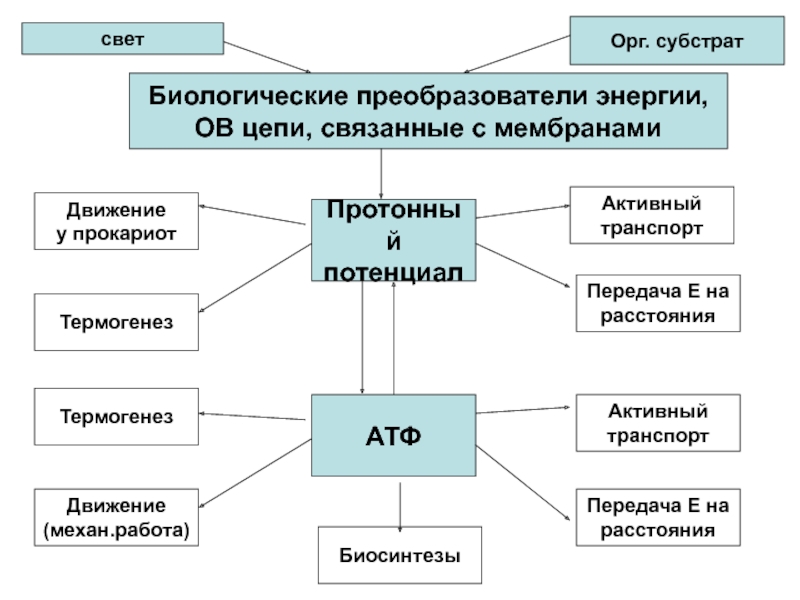
Слайд 14Протонный
потенциал
АТФ
Биологические преобразователи энергии,
ОВ цепи, связанные с мембранами
свет
Орг. субстрат
Термогенез
Движение
у прокариот
Термогенез
Движение
(механ.работа)
Активный
транспорт
Активный
транспорт
Передача Е на
расстояния
Передача Е на
расстояния
Биосинтезы
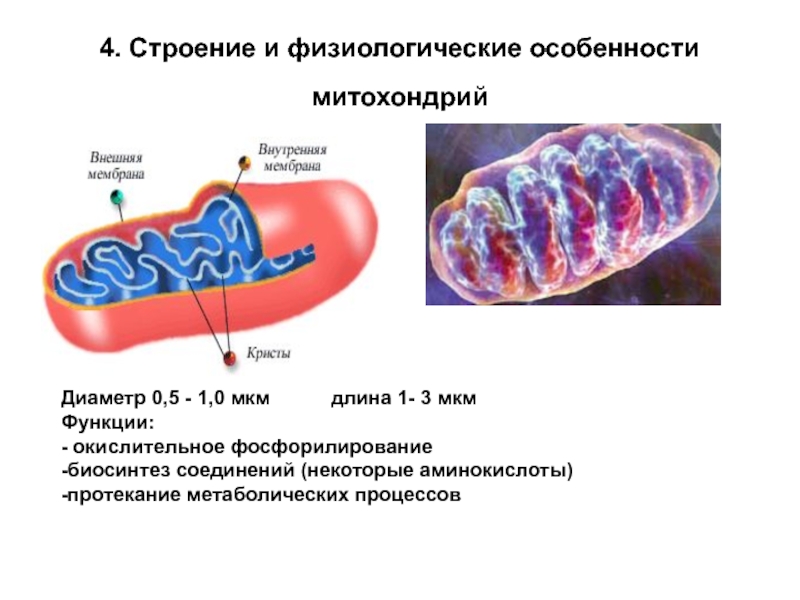
Слайд 154. Строение и физиологические особенности митохондрий
Диаметр 0,5 - 1,0
мкм длина 1- 3 мкм
Функции:
-
окислительное фосфорилирование
-биосинтез соединений (некоторые аминокислоты)
-протекание метаболических процессов
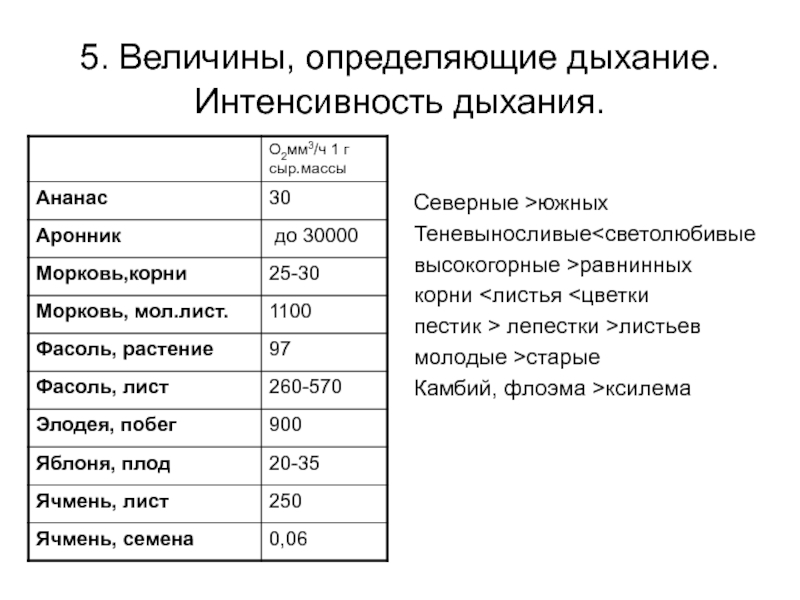
Слайд 175. Величины, определяющие дыхание. Интенсивность дыхания.
Северные >южных
Теневыносливыеравнинных
корни
> лепестки >листьев
молодые >старые
Камбий, флоэма >ксилема
Слайд 18Дыхательный коэффициент
ДК = VСО2 / VО2
Органические вещества, разрушающиеся при
дыхании – субстрат
С6Н12О6 +6 О2 → 6 СО2 + 6
Н2О 6СО2 / 6 О2 =1
2 С2Н2О4 + О2 → 4 СО2 + 2 Н2О 4 О2 / 1 О2 = 4
С18Н36О2 + 26 О2 →18 СО2 + 18 Н2О 8СО2/26О2= 0,7
Факторы влияющие на ДК:
1. Качество дыхательного материала (степень его окисленности)
2. Концентрация кислорода
3. Расположение ткани
4. Повреждение мембран
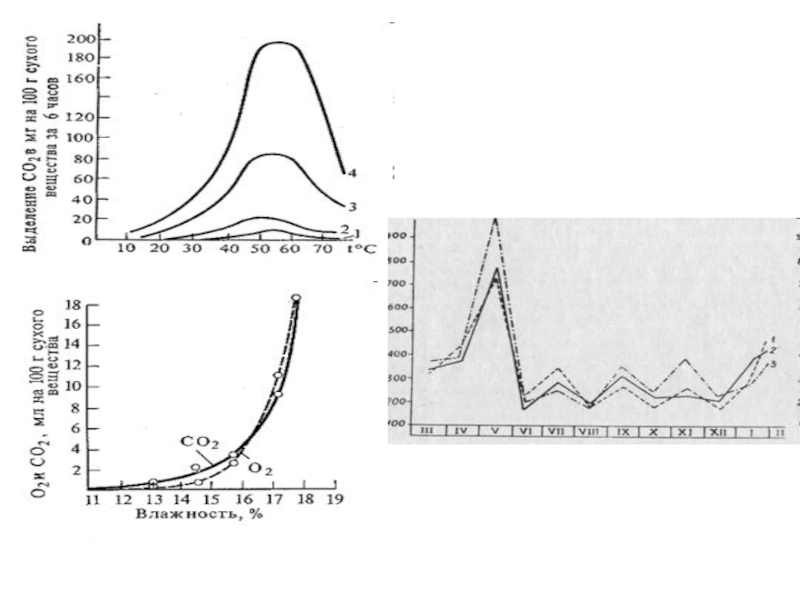
Слайд 196. Влияние внешних и внутренних факторов на интенсивность дыхания
Внешние
условия
С6Н12О6+6О2→6СО2 + 6Н2О + 2824 кДж
1. Температура
2. Содержание
кислорода
3. Содержание углекислого газа
4. Вода
5. Свет
6. Питательные соли
7. Поранение
Внутренние факторы
Экологическая группа
2. Возраст
3. Фаза роста
Слайд 217. Схема дыхания по В.И.Палладину
1 ст. - анаэробный
С6Н12О6 + 6Н2О
+ 12R→ 6СО2+12RН2
2 ст. - аэробный
12RН2 + 6О2 → 12R
+ 12Н2О
С6Н12О6 + 6О2 → 6СО2 + 6Н2О
R – дыхательный пигмент (окраш.)
RН2 – дыхательный хромоген (бесцвет)
Слайд 239. Ферменты дыхания
Оксидоредуктазы, участвующие в дыхании, делятся на следующие основные
группы:
Анаэробные дегидрогеназы передают электроны промежуточным акцепторам, но не О2.
Аэробные дегидрогеназы
передают электроны различным акцепторам, в т.ч. и О2.
Оксидазы передают электроны О2.
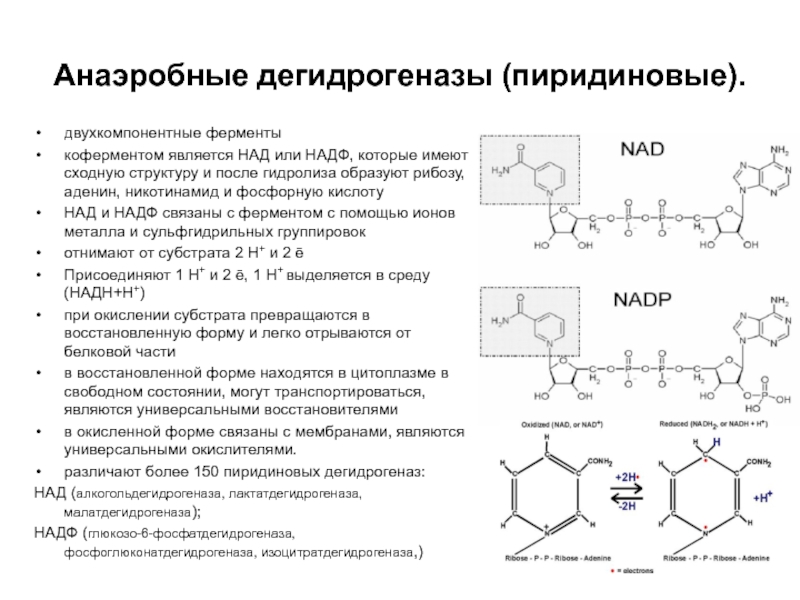
Слайд 24Анаэробные дегидрогеназы (пиридиновые).
двухкомпонентные ферменты
коферментом является НАД или НАДФ, которые
имеют сходную структуру и после гидролиза образуют рибозу, аденин, никотинамид
и фосфорную кислоту
НАД и НАДФ связаны с ферментом с помощью ионов металла и сульфгидрильных группировок
отнимают от субстрата 2 Н+ и 2 ē
Присоединяют 1 Н+ и 2 ē, 1 Н+ выделяется в среду (НАДН+Н+)
при окислении субстрата превращаются в восстановленную форму и легко отрываются от белковой части
в восстановленной форме находятся в цитоплазме в свободном состоянии, могут транспортироваться, являются универсальными восстановителями
в окисленной форме связаны с мембранами, являются универсальными окислителями.
различают более 150 пиридиновых дегидрогеназ:
НАД (алкогольдегидрогеназа, лактатдегидрогеназа, малатдегидрогеназа);
НАДФ (глюкозо-6-фосфатдегидрогеназа, фосфоглюконатдегидрогеназа, изоцитратдегидрогеназа,)
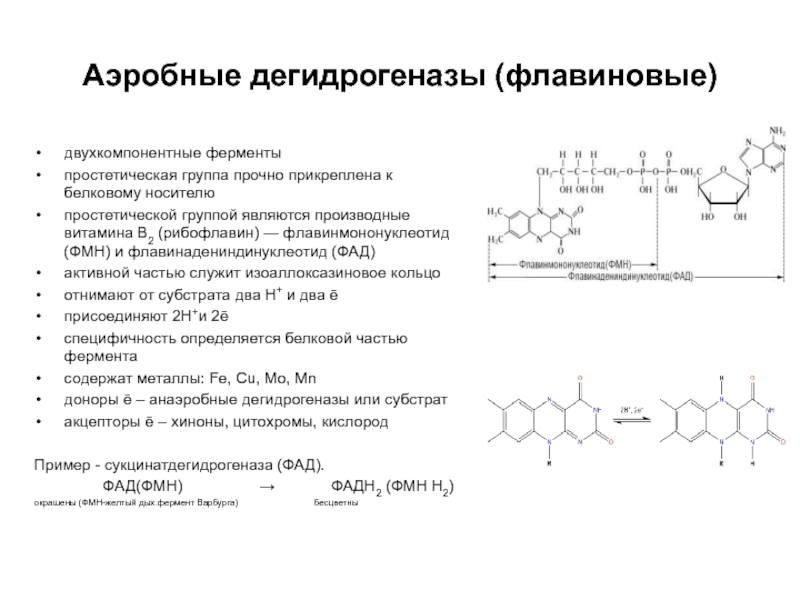
Слайд 25Аэробные дегидрогеназы (флавиновые)
двухкомпонентные ферменты
простетическая группа прочно прикреплена к белковому
носителю
простетической группой являются производные витамина В2 (рибофлавин) — флавинмононуклеотид (ФМН)
и флавинадениндинуклеотид (ФАД)
активной частью служит изоаллоксазиновое кольцо
отнимают от субстрата два Н+ и два ē
присоединяют 2Н+и 2ē
специфичность определяется белковой частью фермента
содержат металлы: Fe, Cu, Mo, Mn
доноры ē – анаэробные дегидрогеназы или субстрат
акцепторы ē – хиноны, цитохромы, кислород
Пример - сукцинатдегидрогеназа (ФАД).
ФАД(ФМН) → ФАДН2 (ФМН Н2)
окрашены (ФМН-желтый дых.фермент Варбурга) бесцветны
Слайд 26Оксидазы
аэробные дегидрогеназы, передают электроны только на кислород
при этом образуются
вода (перенос 4ē), Н2О2 -пероксид водорода (2ē) или О2-- супероксидный
анион кислорода (ē)
Примеры: цитохромоксидаза, полифенолоксидаза (вода), флавопротеиновые оксидазы (Н2О2), ксантиноксидаза (О2-)
Fe-протеиды:
геминовые: каталаза, пероксидаза, цитохромы;
негеминовые: аконитаза, ксантиноксидаза
Cu-протеиды (полифенолоксидаза и аскорбатоксидаза)
Цитохромы: известно около 20 цитохромов (а, b, с, d, отличающихся между собой природой простетической группы): Fe3+ ± ē ↔ Fe2+
цит.b→ цит.с1 → цит.с→ цит.аа3→О2
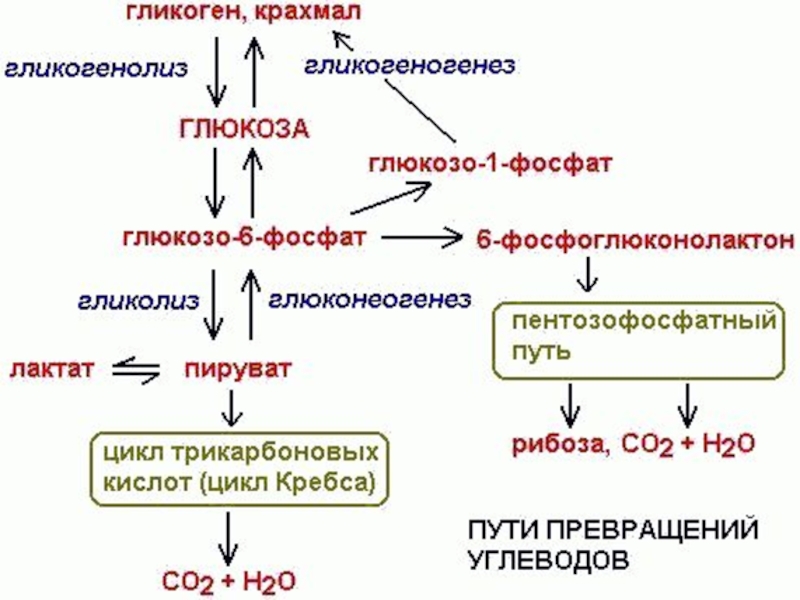
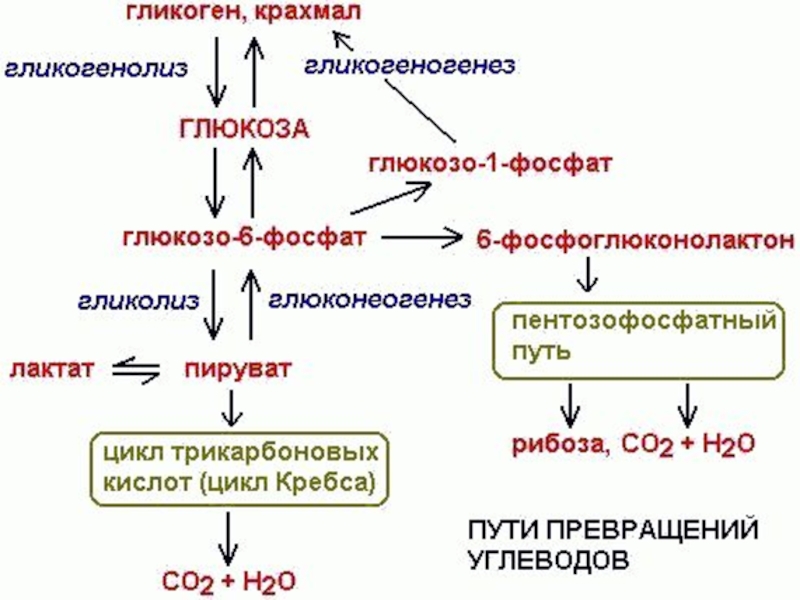
Слайд 27Пути дыхательного обмена растений
Гликолитический (дихотомический);
Пентозофосфатный (апотомический).
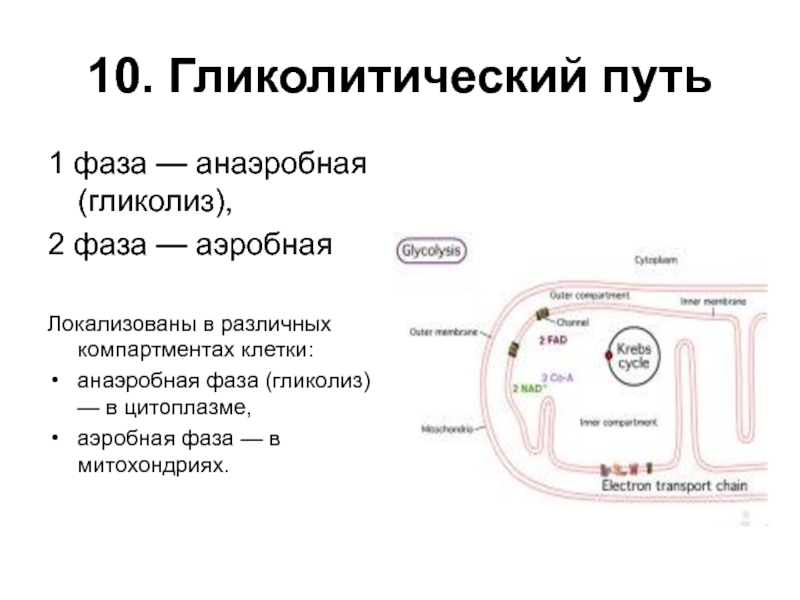
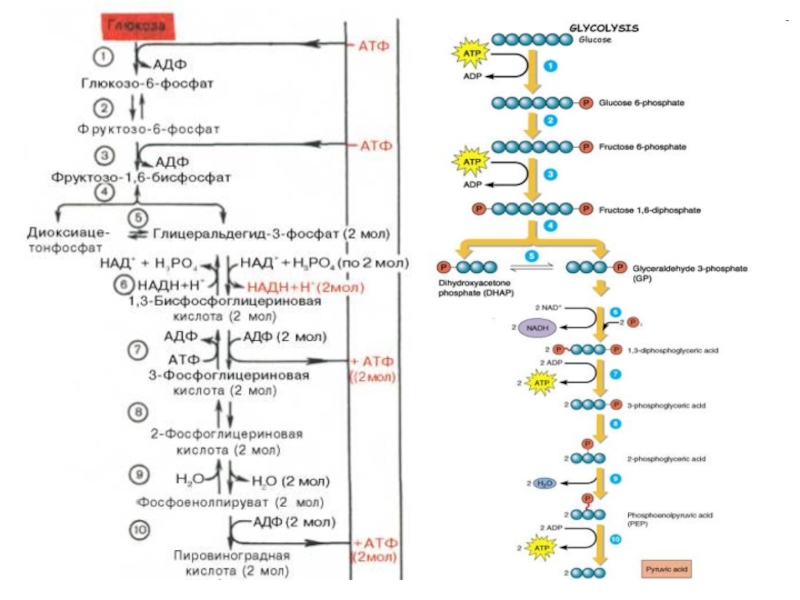
Слайд 2910. Гликолитический путь
1 фаза — анаэробная (гликолиз),
2 фаза —
аэробная
Локализованы в различных компартментах клетки:
анаэробная фаза (гликолиз) — в цитоплазме,
аэробная фаза — в митохондриях.
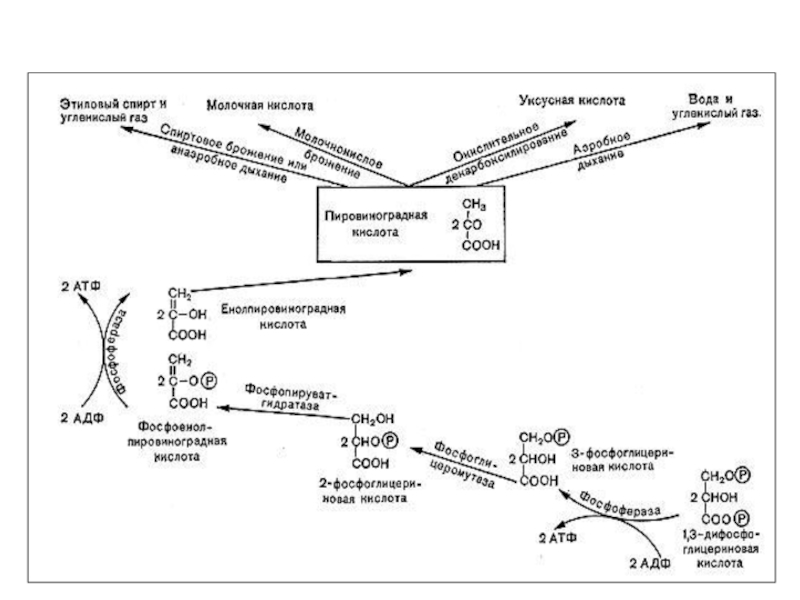
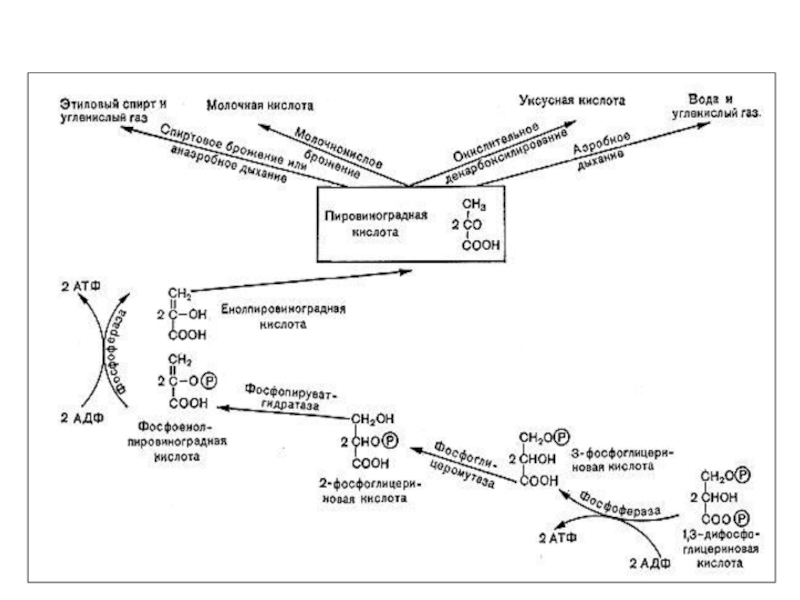
Слайд 30Гликолиз - (glycol – сахар, lysis – расщепление)
Путь Г.Эмбдена
– О.Мейергофа – Я.О.Парнаса
С.П. Костычев, Л.А.Иванов, А.Гарден
глюкоза → 2 ПВК
(аэробный)
глюкоза → 2 молочной кислоты (анаэробный)
С6Н12О6 → 2 С3Н4О2 + 2Н2O
Слайд 31Характеристика гликолиза
Универсальный, древний процесс.
Общий начальный этап дыхания и брожения.
С биологической
точки зрения процесс достаточно примитивный, менее саморегулируемый.
Все реакции гликолиза протекают
в цитозоле.
Включает 10 последовательных реакций, каждая из которых катализируется специфическим ферментом.
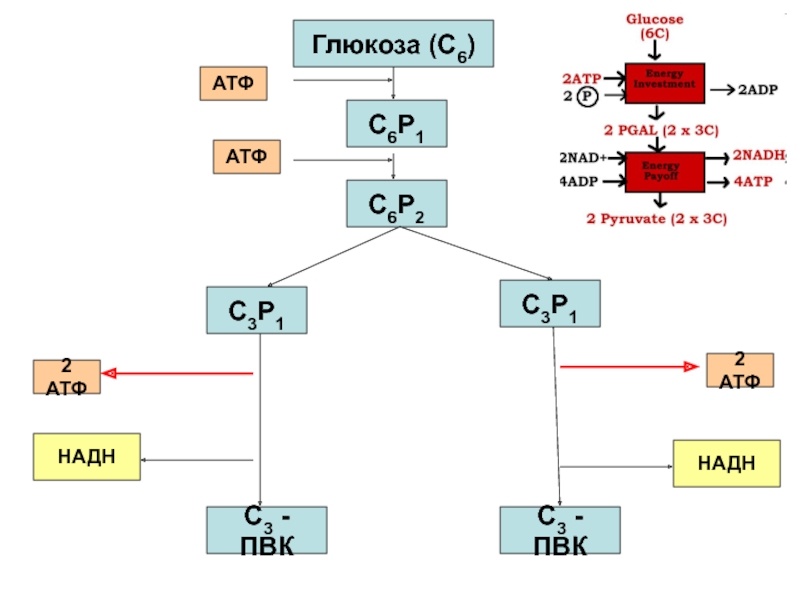
Слайд 33Глюкоза (С6)
С6Р1
С6Р2
АТФ
АТФ
С3 - ПВК
С3Р1
С3Р1
С3 - ПВК
2 АТФ
2 АТФ
НАДН
НАДН
Слайд 34Значение гликолиза
Энергетическое - образуется 2 молекулы АТФ и 2 молекулы
НАДН+Н+
Метаболическое - образование промежуточных веществ, необходимых для синтетических процессов в
клетке.
Гликолиз в хлоропластах обеспечивает синтез АТФ, метаболизацию крахмала до триоз, которые экспортируются из хлоропласта.
Первый подготовительный этап дыхания у аэробов.
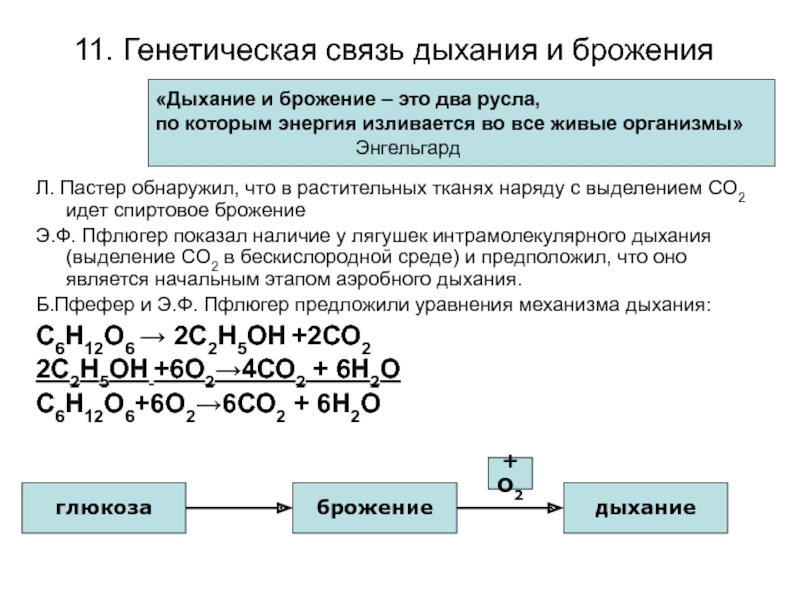
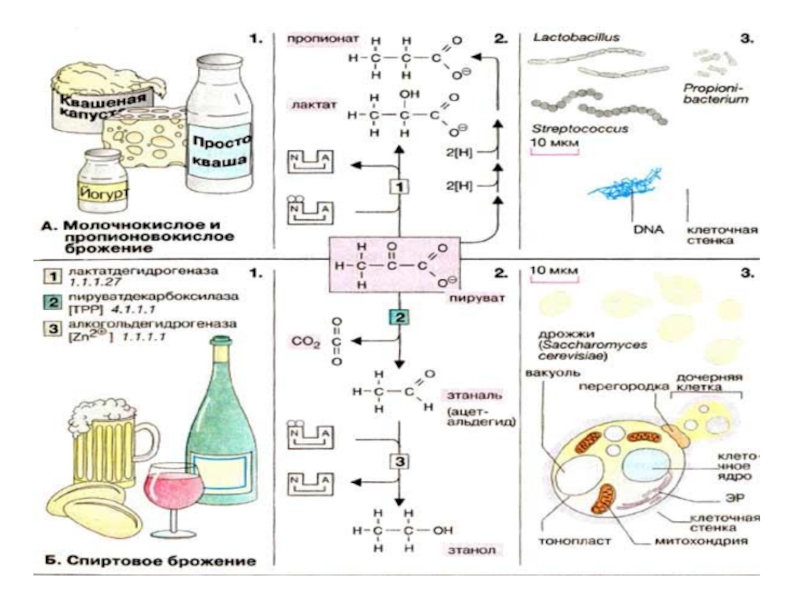
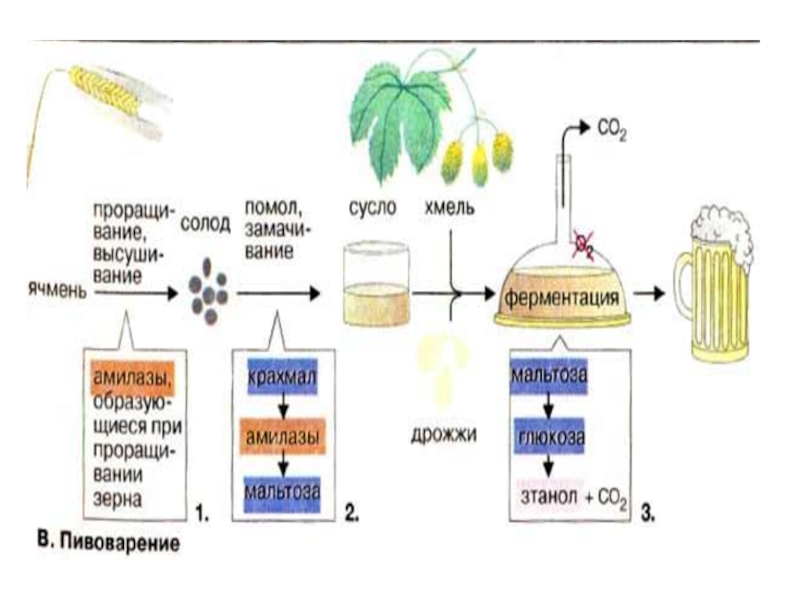
Слайд 3611. Генетическая связь дыхания и брожения
Л. Пастер обнаружил, что в
растительных тканях наряду с выделением СО2 идет спиртовое брожение
Э.Ф. Пфлюгер
показал наличие у лягушек интрамолекулярного дыхания (выделение CО2 в бескислородной среде) и предположил, что оно является начальным этапом аэробного дыхания.
Б.Пфефер и Э.Ф. Пфлюгер предложили уравнения механизма дыхания:
С6Н12О6 → 2С2Н5ОН +2СО2
2С2Н5ОН +6О2→4СО2 + 6Н2О
С6Н12О6+6О2→6СО2 + 6Н2О
«Дыхание и брожение – это два русла,
по которым энергия изливается во все живые организмы»
Энгельгард
+О2
глюкоза
дыхание
брожение
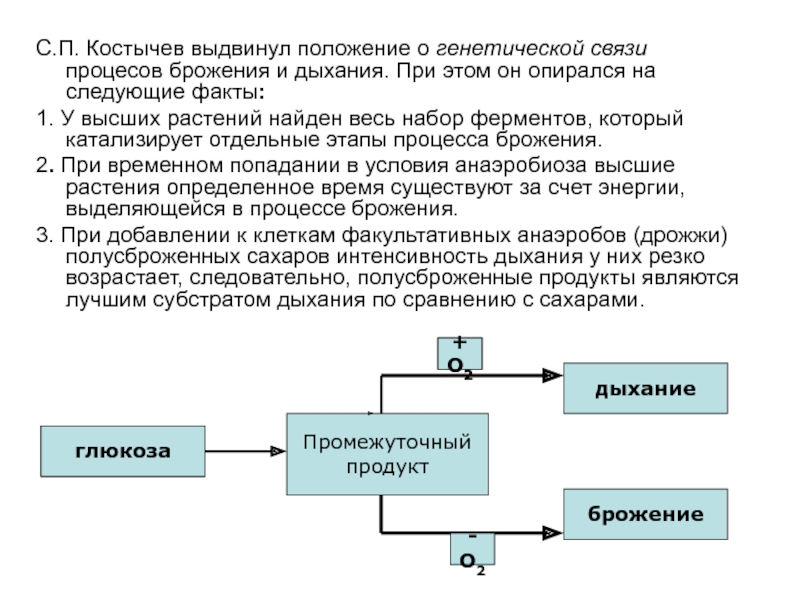
Слайд 37С.П. Костычев выдвинул положение о генетической связи процесов брожения и
дыхания. При этом он опирался на следующие факты:
1. У высших
растений найден весь набор ферментов, который катализирует отдельные этапы процесса брожения.
2. При временном попадании в условия анаэробиоза высшие растения определенное время существуют за счет энергии, выделяющейся в процессе брожения.
3. При добавлении к клеткам факультативных анаэробов (дрожжи) полусброженных сахаров интенсивность дыхания у них резко возрастает, следовательно, полусброженные продукты являются лучшим субстратом дыхания по сравнению с сахарами.
глюкоза
Промежуточный
продукт
брожение
дыхание
+О2
+О2
-О2
глюкоза
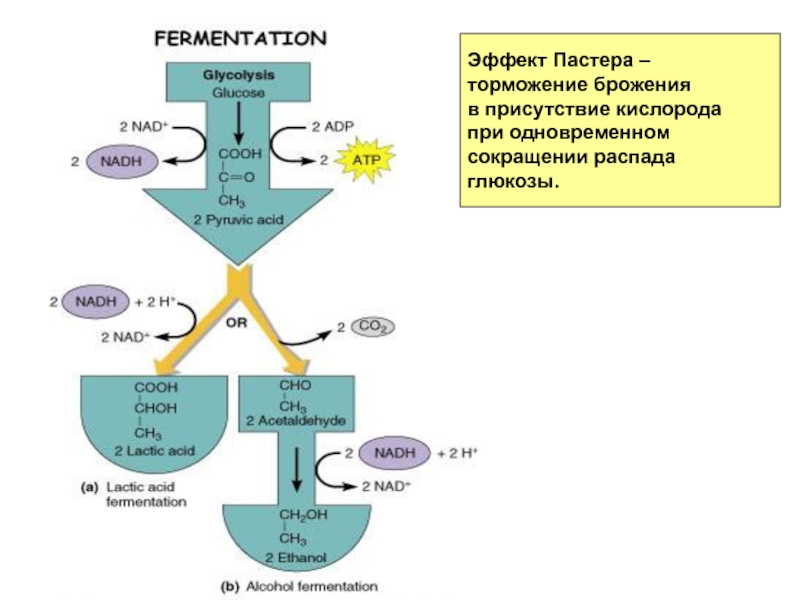
Слайд 40Эффект Пастера –
торможение брожения
в присутствие кислорода
при одновременном
сокращении распада глюкозы.
Слайд 43Аэробная фаза
2ПВК + 5О2 + 6Н2О → 6СО2 + 5Н2О
Основные
стадии:
окислительное декарбоксилирование пировиноградной кислоты;
цикл трикарбоновых кислот (цикл Кребса);
электронтранспортная цепь (ЭТЦ)
Первые две стадии происходят в матриксе митохондрий, ЭТЦ локализована на внутренней мембране митохондрий.
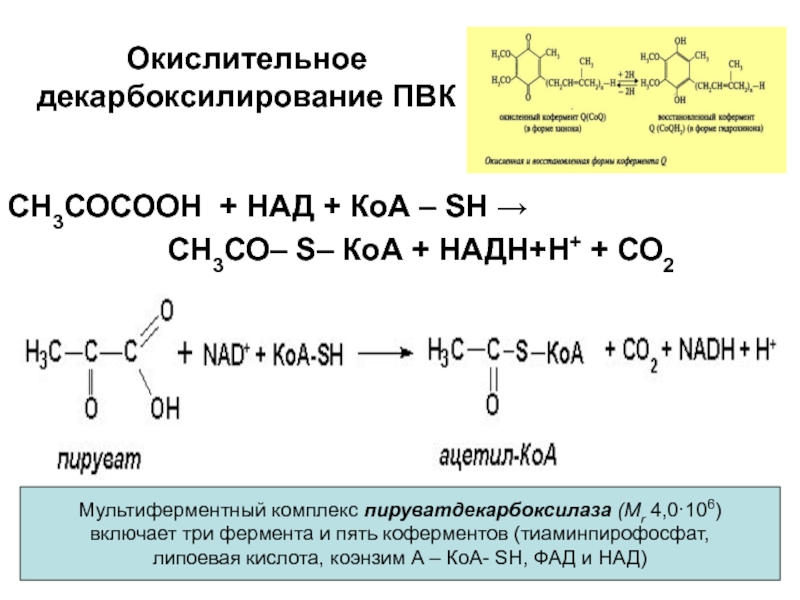
Слайд 44Окислительное декарбоксилирование ПВК
СН3СОСООН + НАД + КоА – SH
→
СН3СО– S– КоА + НАДН+H+ + СО2
Мультиферментный комплекс пируватдекарбоксилаза
(Мr 4,0·106)
включает три фермента и пять коферментов (тиаминпирофосфат,
липоевая кислота, коэнзим А – КоА- SH, ФАД и НАД)
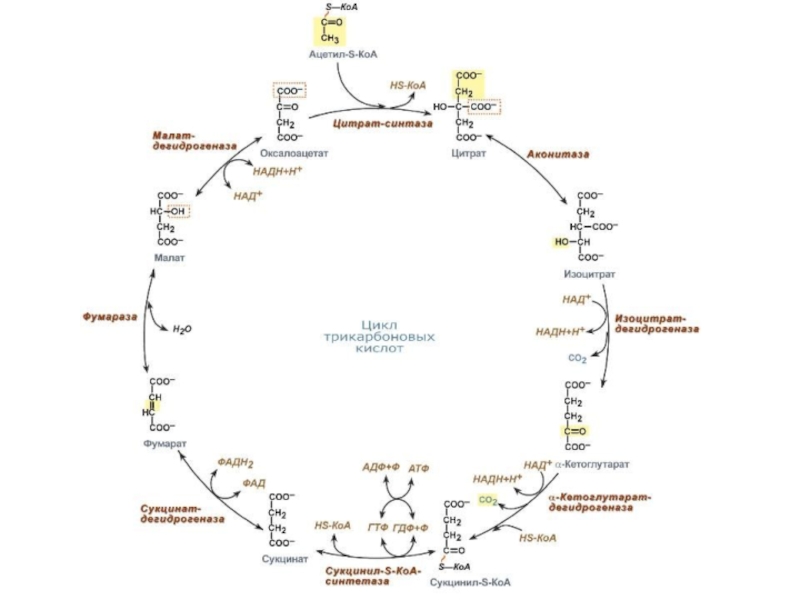
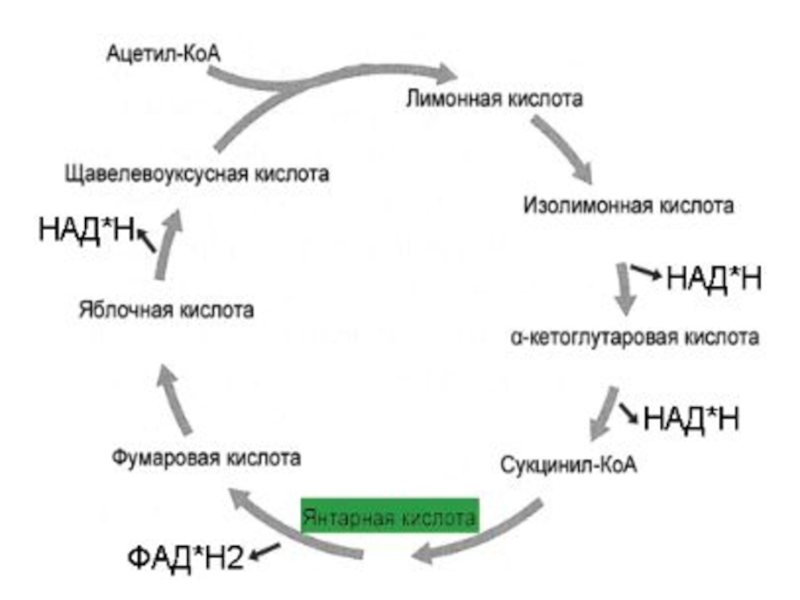
Слайд 45Цикл Кребса
Цикл трикарбоновых кислот
1910 г. швед.химик Т.Тунберг показал, что
в животных клетках содержатся ферменты, способные отнимать Н+ от некоторых
органических кислот.
1935 г. венгер. ученый А. Сент-Дьердьи установил, что добавление небольших количеств органических кислот (фумаровой, яблочной или янтарной) усиливает поглощение кислорода измельченными мышечными тканями.
1937 г. англ.биохимик Г. Кребс (университет Шеффилда, Великобритания), пришел к выводу, что главным путем окисления углеводов являются циклические реакции, в которых происходит постепенное преобразование ряда органических кислот. Эти преобразования были названы циклом трикарбоновых кислот или циклом Кребса. В 1953 году Кребс был удостоен Нобелевской премии.
1939 г. англ. Чибнелл доказал существование цикла у растений.
Слайд 46«Цикл Кребса объясняет два одновременно происходящих процесса: реакции распада, при
которых высвобождается энергия, и синтетические процессы, при которых эта энергия
расходуется»
Эрик Хаммарстен
«Наличие одного и того же механизма образования энергии у всех живых существ позволяет сделать еще два вывода.
Во-первых, этот механизм возник на очень ранних этапах эволюции, и, во-вторых, жизнь в ее настоящем виде зародилась лишь однажды».
Х.Кребс, Нобелевская лекция
Ханс Адольф Кребс
(25.08.1900– 22.11.1981)
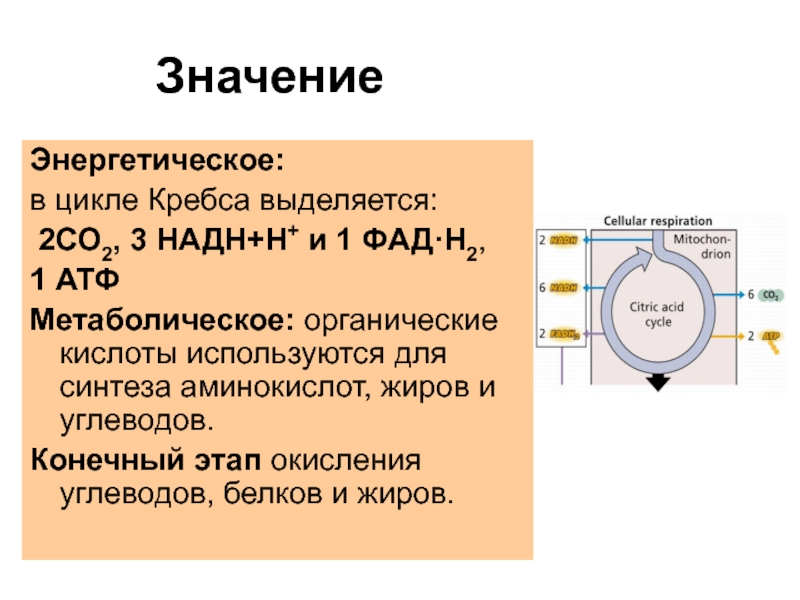
Слайд 49Значение
Энергетическое:
в цикле Кребса выделяется:
2СО2, 3 НАДН+H+ и 1
ФАД·Н2,
1 АТФ
Метаболическое: органические кислоты используются для синтеза аминокислот, жиров
и углеводов.
Конечный этап окисления углеводов, белков и жиров.
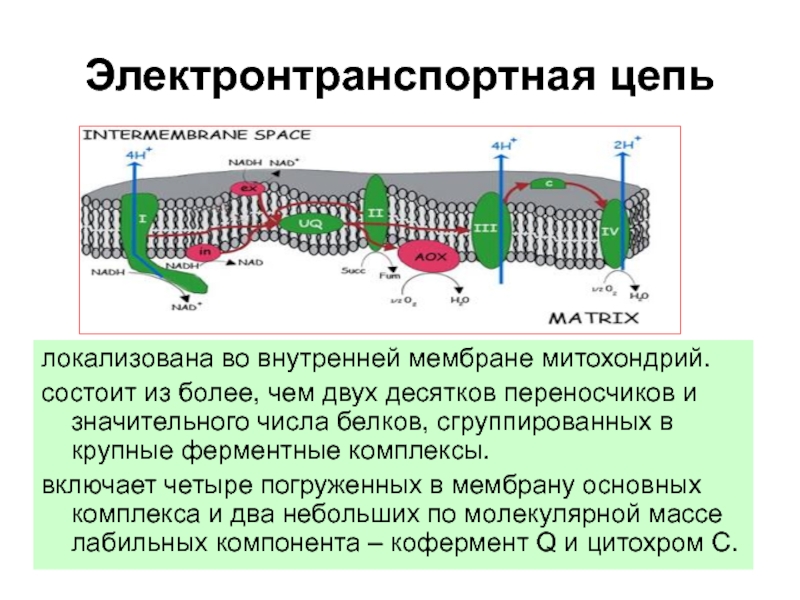
Слайд 50Электронтранспортная цепь
локализована во внутренней мембране митохондрий.
состоит из более, чем
двух десятков переносчиков и значительного числа белков, сгруппированных в крупные
ферментные комплексы.
включает четыре погруженных в мембрану основных комплекса и два небольших по молекулярной массе лабильных компонента – кофермент Q и цитохром С.
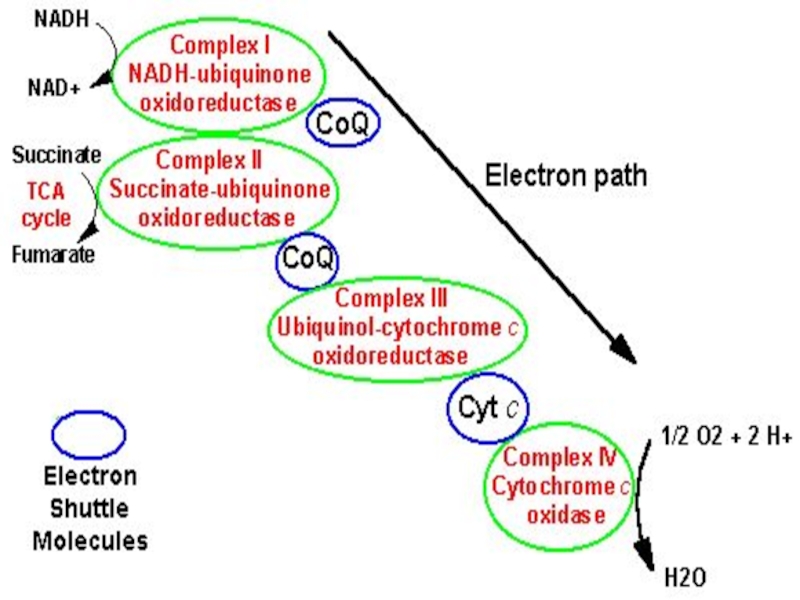
Слайд 51Электронтранспортная цепь
ЭТЦ служит для передачи электронов от восстановленных субстратов на
кислород.
С переносом электронов по ЭТЦ сопряжен синтез АТФ.
Энергия
высвобождается постепенно путем передачи протонов и электронов ряду переносчиков, связанных с белками и образующих ЭТЦ.
Расположение переносчиков в ЭТЦ определяется величиной их окислительно-восстановительного потенциала (О/В).
Движущей силой транспорта электронов в ЭТЦ является разность потенциалов.
Электроны от НАДН (-0,32 В) или ФАДН2 передаются на О2 (+0,82 В), который восстанавливается, присоединяя Н+ и образуя Н2О:
4 Н+ + 4 ē + О2 → 2 Н2О
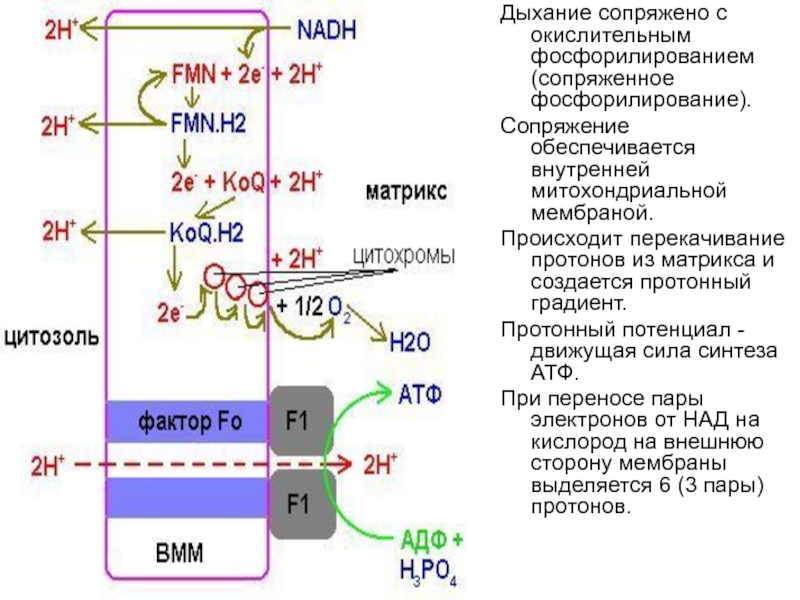
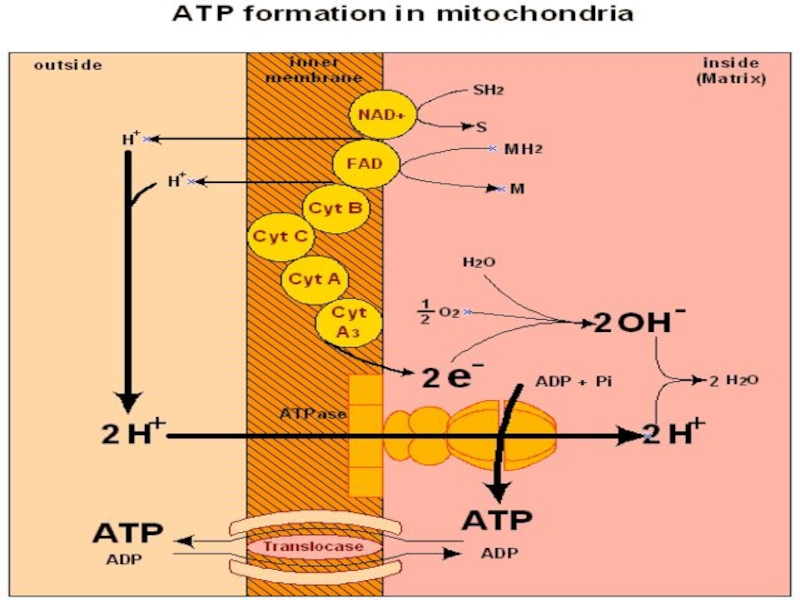
Слайд 53Дыхание сопряжено с окислительным фосфорилированием (сопряженное фосфорилирование).
Сопряжение обеспечивается внутренней митохондриальной
мембраной.
Происходит перекачивание протонов из матрикса и создается протонный градиент.
Протонный
потенциал - движущая сила синтеза АТФ.
При переносе пары электронов от НАД на кислород на внешнюю сторону мембраны выделяется 6 (3 пары) протонов.
Слайд 54Коэффициент фосфорилирования
Коэффициент фосфорилирования — отношение количества связанного неорганического фосфора (АДФ
+ Фн→АТФ) поглощенному в процессе дыхания кислороду (Р/О)
Коэффициент фосфорилирования
— показатель сопряженности окисления и фосфорилирования
Коэффициент Р/О может быть не более 3, т.к. перенос двух электронов к кислороду по дыхательной цепи сопровождается не более чем тремя фосфорилированиями.
Зависит от условий и от состояния клеток:
природы окисляемого вещества
внешних условий (температура, обезвоживание и набухание митохондрий, разобщители).
снижается при заболевании организмов.
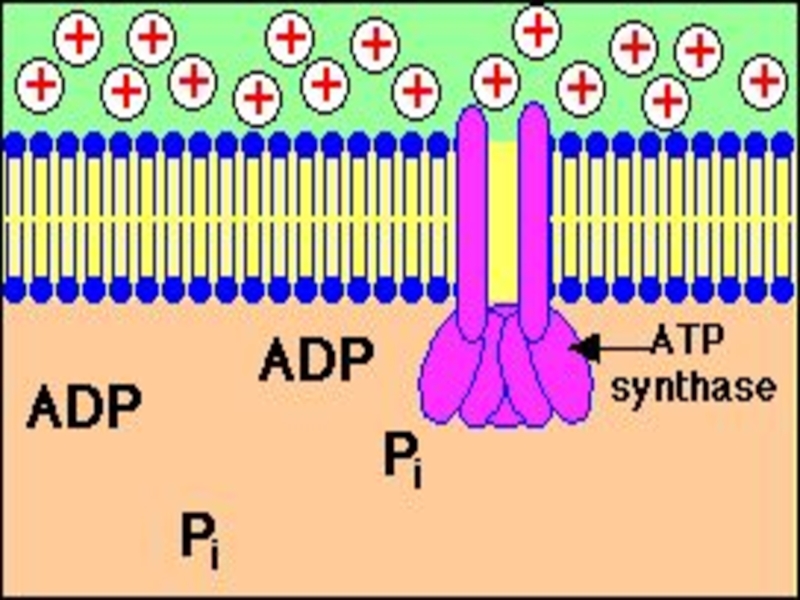
Слайд 55Окислительное фосфорилирование
это накопление энергии окисления в АТФ при продвижении
электрона по цепи переносчиков.
Хемиосмотическая теория
разработана в 1961-1966 гг.
Дыхание
→ протонный потенциал (∆μΗ+) → АТФ
Сопряжение диффузии протонов с синтезом АТФ осуществляется АТФсинтазным комплексом.
П. Митчелл, англ.биохимик, Нобелевский лауреат (1978)
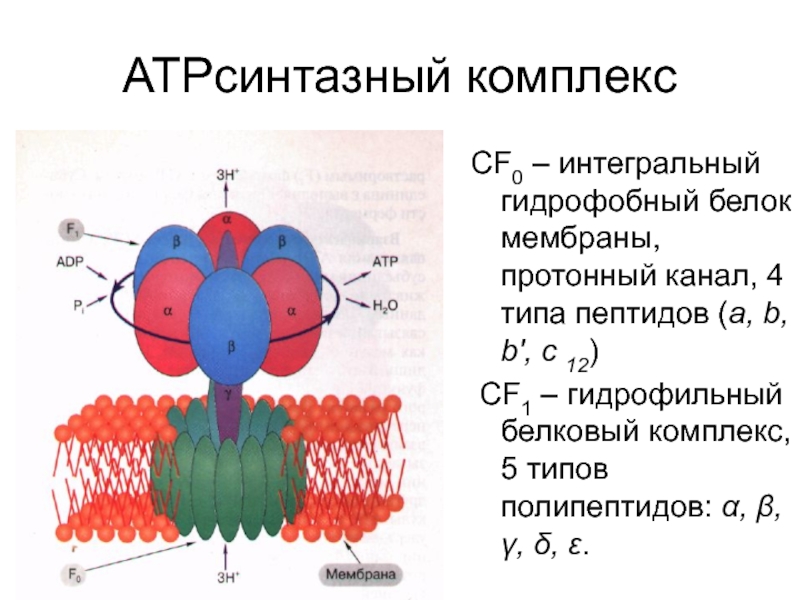
Слайд 58АТРсинтазный комплекс
СF0 – интегральный гидрофобный белок мембраны, протонный канал, 4
типа пептидов (a, b, b', c 12)
СF1 –
гидрофильный белковый комплекс, 5 типов полипептидов: α, β, γ, δ, ε.
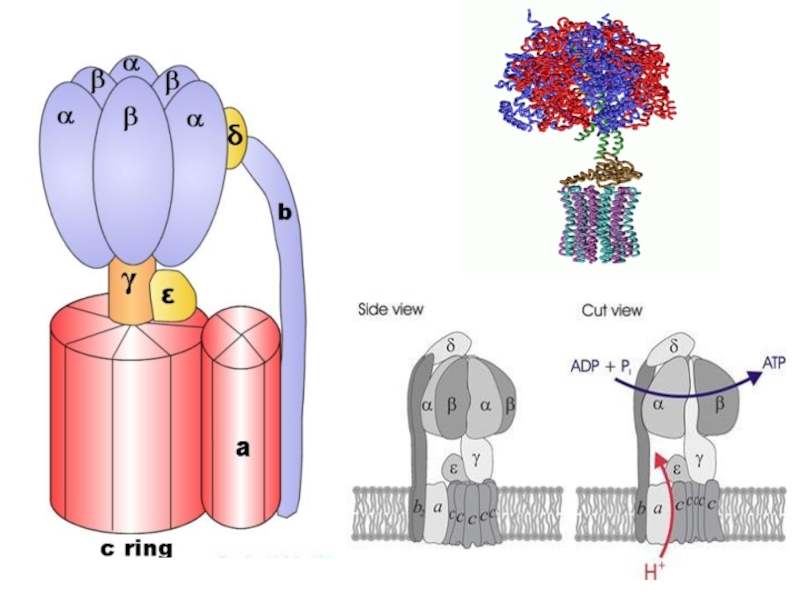
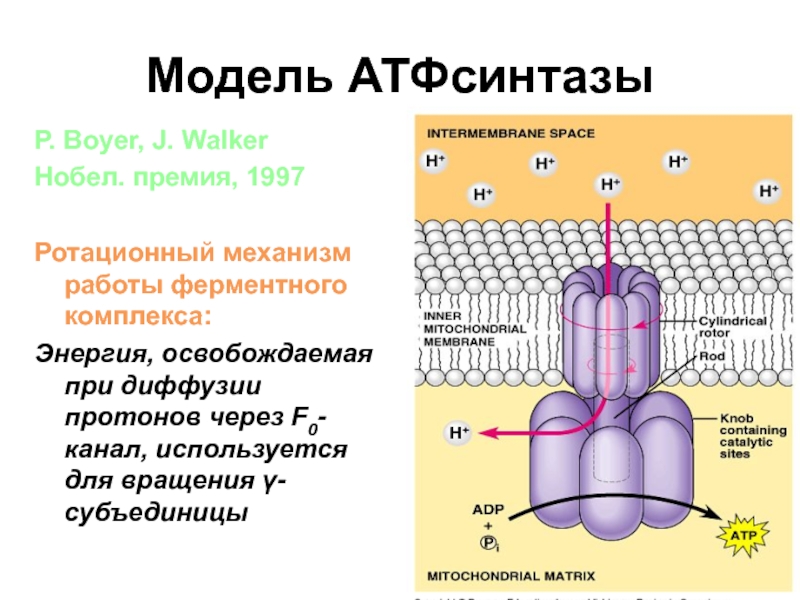
Слайд 60Модель АТФсинтазы
P. Boyer, J. Walker
Нобел. премия, 1997
Ротационный механизм работы ферментного
комплекса:
Энергия, освобождаемая при диффузии протонов через F0-канал, используется для вращения
γ-субъединицы
Слайд 61Энергозависимые изменения состояния каталитических центров
Три этапа синтеза АТФ :
Присоединение АДФ
и Фн к активному центру фермента без затраты энергии.
Конформационные
изменения фермента, синтез АТФ из АДФ и Фн.
Высвобождение АТР и возврат АТР-синтазного комплекса в исходное состояние.
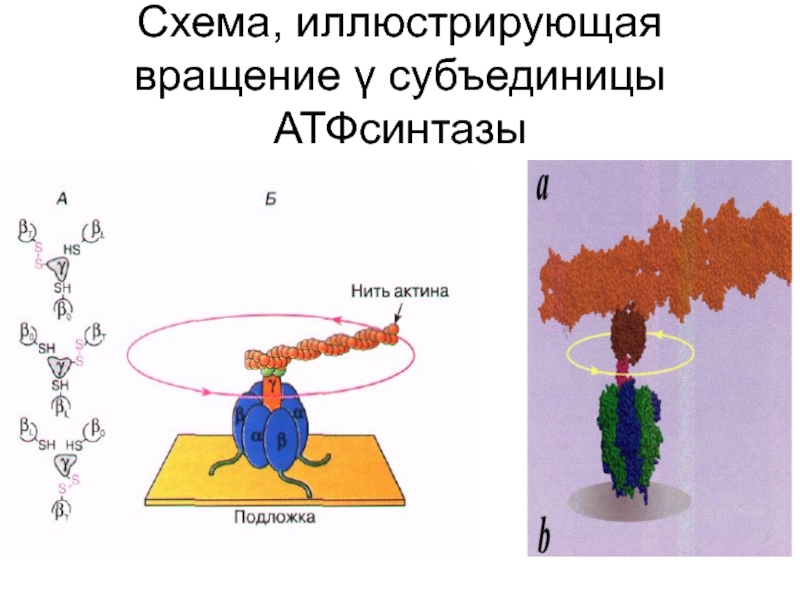
Слайд 62Схема, иллюстрирующая вращение γ субъединицы АТФсинтазы
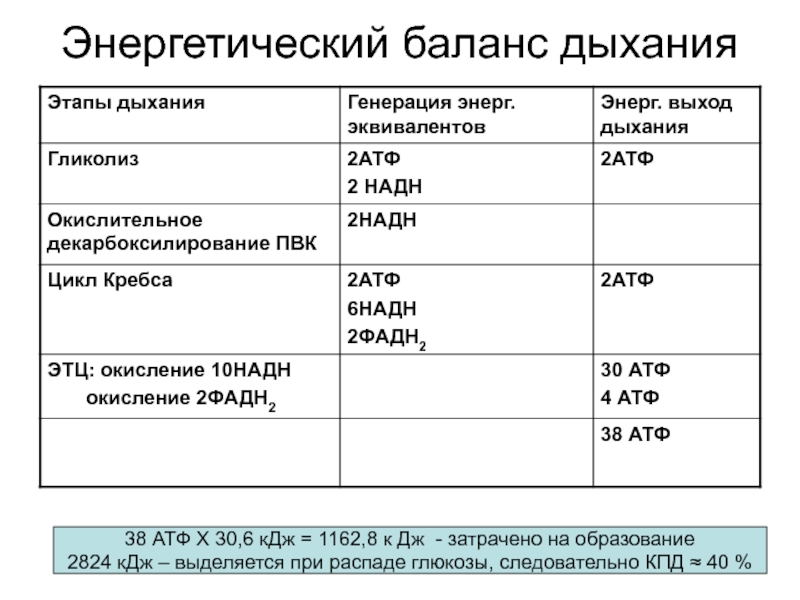
Слайд 65Энергетический баланс дыхания
38 АТФ Х 30,6 кДж = 1162,8
к Дж - затрачено на образование
2824 кДж – выделяется при распаде глюкозы, следовательно КПД ≈ 40 %
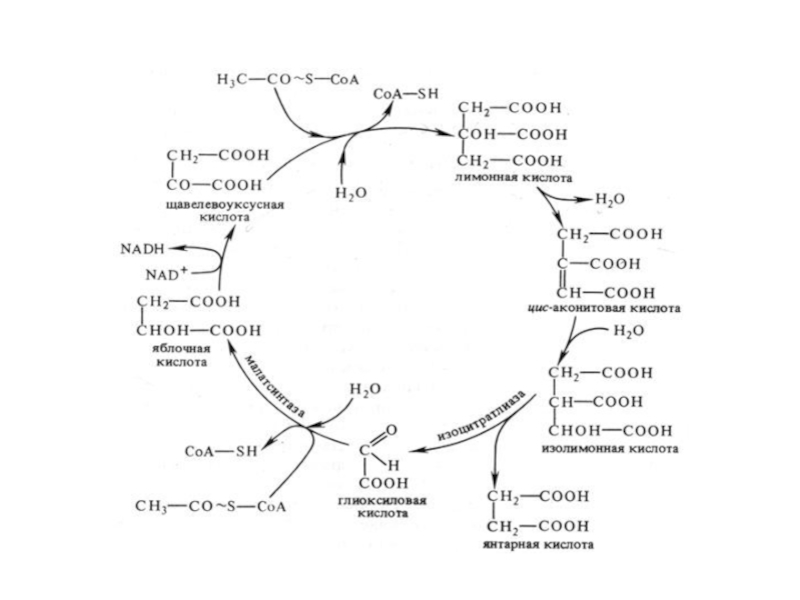
Слайд 66Глиоксилатный цикл
Впервые описан в 1957 г. у бактерий и
плесневых грибов Г.Л. Корнбергом и Г.А. Кребсом.
Характеристика:
функционирует в прорастающих
семенах масличных растений и в других объектах, где запасные жиры превращаются в сахара (стареющие листья, при созревании пыльцы)
локализован в специализированных микротельцах — глиоксисомах.
отсутствуетв клетках животных, в вегетативных тканях растений и в созревающих семенах.
Перестает функционировать после того, как израсходован весь запас жира.
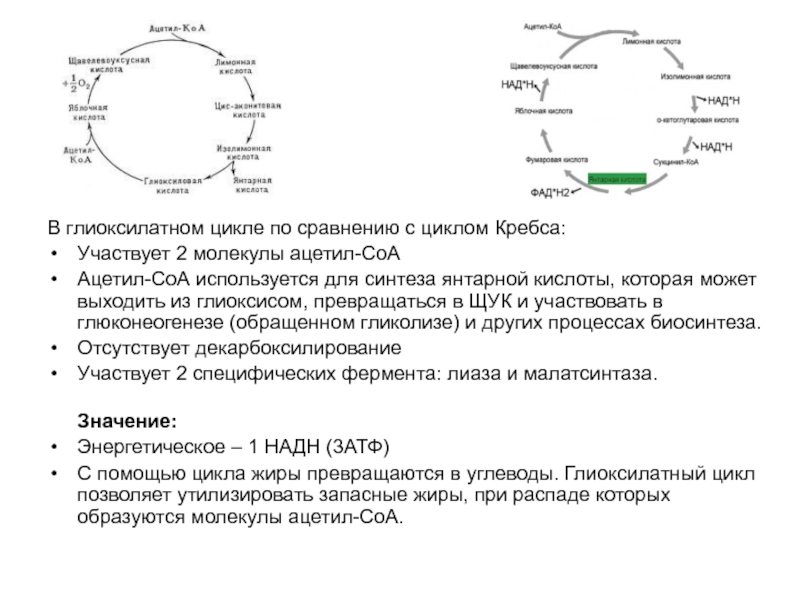
Слайд 68В глиоксилатном цикле по сравнению с циклом Кребса:
Участвует 2 молекулы
ацетил-СоА
Ацетил-СоА используется для синтеза янтарной кислоты, которая может выходить
из глиоксисом, превращаться в ЩУК и участвовать в глюконеогенезе (обращенном гликолизе) и других процессах биосинтеза.
Отсутствует декарбоксилирование
Участвует 2 специфических фермента: лиаза и малатсинтаза.
Значение:
Энергетическое – 1 НАДН (3АТФ)
С помощью цикла жиры превращаются в углеводы. Глиоксилатный цикл позволяет утилизировать запасные жиры, при распаде которых образуются молекулы ацетил-СоА.
Слайд 69Альтернативный путь дыхания
Цианидустойчивый (цианидрезистентный), не ингибируется цианидом.
Характерен для
семенных растений, грибов, водорослей.
Цианидустойчивое дыхание:
- связано с функционированием в дыхательной
цепи альтернативной оксидазы.
- энергия в основном не аккумулируется в АТФ, а рассеивается в виде тепла.
- ингибируется салициловой кислотой
- функцию альтернативной оксидазы в разных тканях выполняют 1—3 белка, которые кодируются в ядерном геноме.
- составляет 10- 25 % (до 100 %) общего поглощения кислорода.
- активируется при высоком содержании АТФ и ингибировании основной цепи транспорта электронов при дыхании.
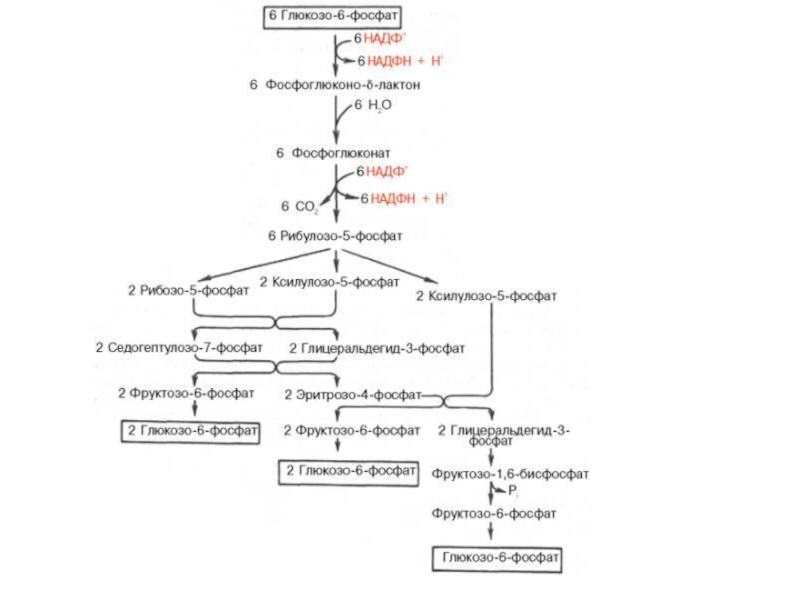
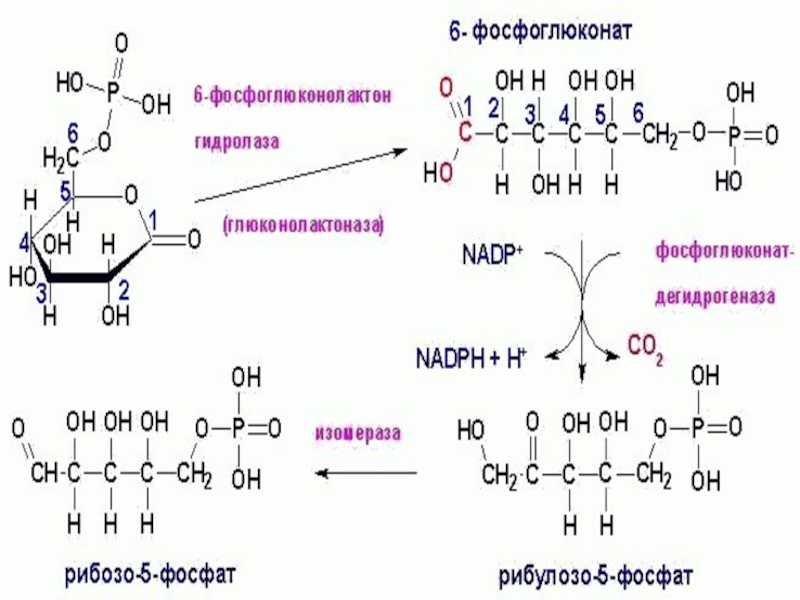
Слайд 71Пентозофосфатный путь -ПФП
апотомический, или фосфоглюконатный
Этапы:
1) Глюкозо-6-фосфат→
СО2+НАДФ+ +рибулозо-5-фосфат
2) Регенерация глюкозо-6-фосфата
Слайд 74Значение
Энергетическое.
Метаболическое, образуются:
- НАДФН, который используется на синтетические процессы
-углеводы (от С3 до С7), пентозы
-рибулозо-1,5-дифосфат и НАДФН принимают
участие в темновой фиксации СО2.
В хлоропластах функционирует в темноте, предотвращает резкое изменение концентрации НАДФН в отсутствие света.
При н.у. ПФП составляет 10-40%, зависит от типа ткани и состояния:
Преобладает в хлоропластах (ПФП > гликолиз)
Снижается в анаэробных условиях (гликолиз > ПФП), т.к. подавляется работа дегидрогеназ цикла.
При неблагоприятных условиях активность ПФП увеличивается : засуха, дефицит калия, инфекция, засоление, затенение, старение.