Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ЭЛЕКТРОПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ СТРОЕНИЕ ДВОЙНОГО ЭЛЕКТРИЧЕСКОГО СЛОЯ
Содержание
- 1. ЭЛЕКТРОПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ СТРОЕНИЕ ДВОЙНОГО ЭЛЕКТРИЧЕСКОГО СЛОЯ
- 2. Электрокинетические свойстваЭлектрокинетическими явлениями называют перемещение одной фазы
- 3. Обусловлены наличием заряда у частиц д. ф. и противоположного заряда д. с.Существует два вида:Электрокинетические явления
- 4. 1809 г. Ф.Ф. Рейсс изучал электрофорез на
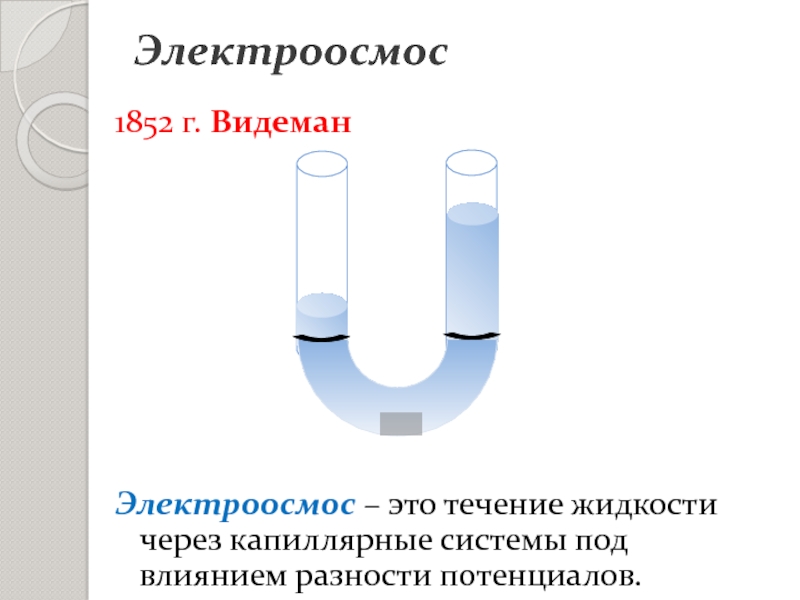
- 5. Электроосмос1852 г. ВидеманЭлектроосмос – это течение жидкости
- 6. Эффект ДорнаЭффект Дорна или потенциал седиментации (1878г.)
- 7. Эффект КвинкеЭффект Квинке или потенциал протекания (1859
- 8. ДЭСВозникает в результате двух причин:- или в
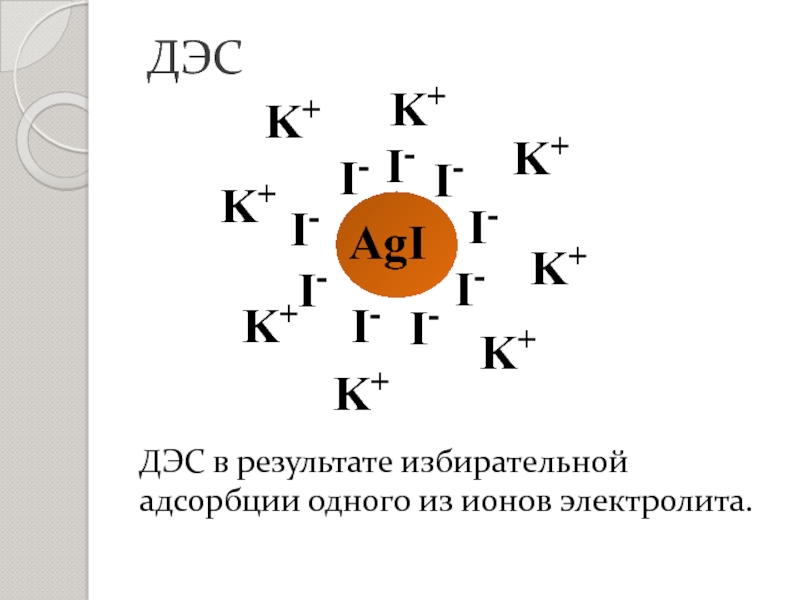
- 9. ДЭС в результате избирательной адсорбции одного из ионов электролита.ДЭС
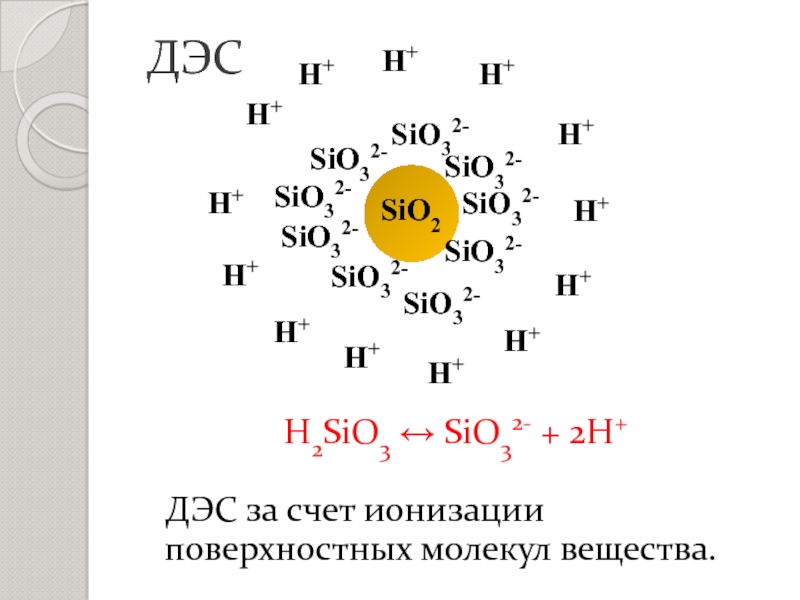
- 10. ДЭС за счет ионизации поверхностных молекул вещества.ДЭСH2SiO3 ↔ SiO32- + 2H+
- 11. Строение двойного электрического слояСуществует несколько моделей:
- 12. Модель Гельмгольца-ПерренаДЭС – это два близко расположенных
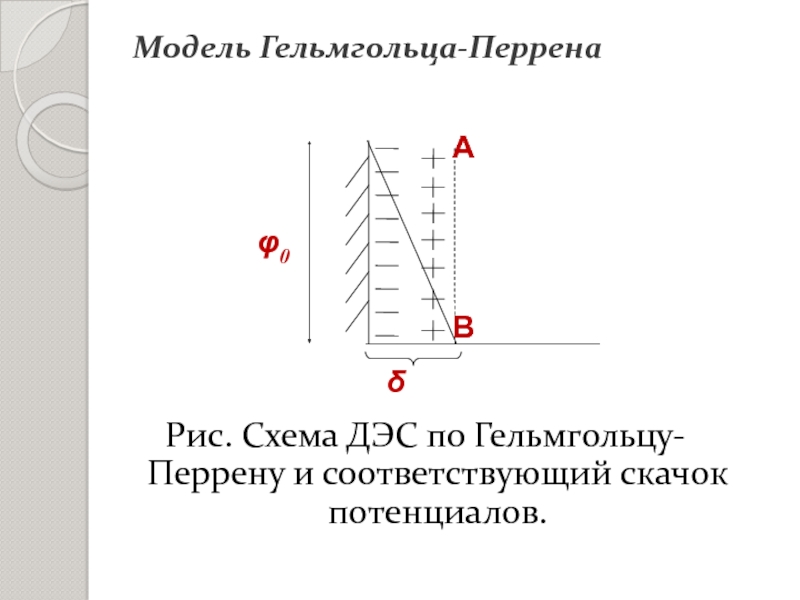
- 13. Рис. Схема ДЭС по Гельмгольцу-Перрену и соответствующий скачок потенциалов.Модель Гельмгольца-Перрена
- 14. ДЭС является как бы плоским конденсатором. где
- 15. Недостатки теории: - толщина ДЭС Гельмгольца-Перрена очень
- 16. Плоскость скольжения (АВ) – место разрыва при
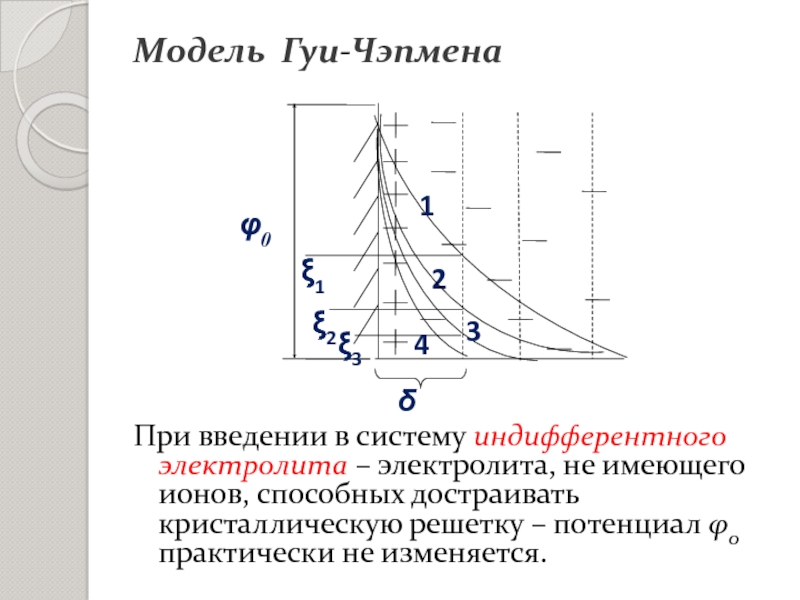
- 17. Модель Гуи-ЧэпменаТеория ДЭС с диффузным слоем противоионов
- 18. Рис. Схема ДЭС по Гуи-Чэпмену и падение в нём потенциала.Модель Гуи-Чэпмена
- 19. Величина электрокинетического потенциала зависит от:Модель Гуи-Чэпмена
- 20. При введении в систему индифферентного электролита –
- 21. С увеличением валентности противоиона резко уменьшается ξ-потенциал.Модель Гуи-Чэпмена
- 22. Недостатки теории: не принимается во внимание объем
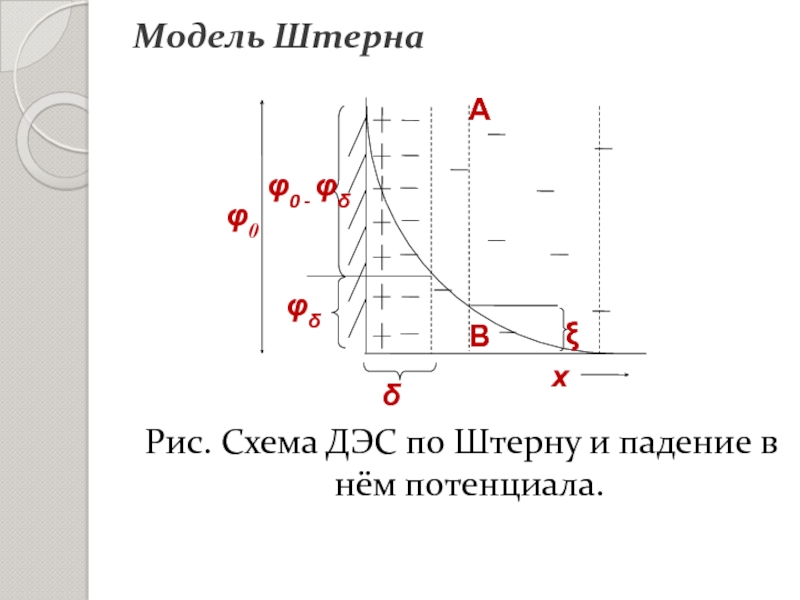
- 23. Модель Штерна1924 г. Штерн объединил схему строения ДЭС Гельмгольца-Перрена и Гуи-Чэпмена.
- 24. Рис. Схема ДЭС по Штерну и падение в нём потенциала.Модель Штерна
- 25. Падение потенциала φ0 складывается из φδ –
- 26. Зависимость электрокинетического потенциала от валентности противоиона определяется
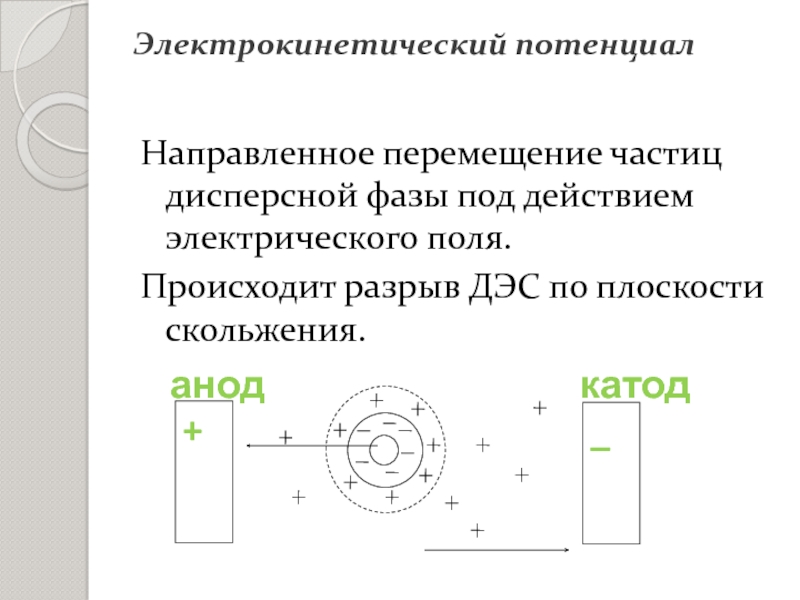
- 27. Электрокинетический потенциалНаправленное перемещение частиц дисперсной фазы под действием электрического поля.Происходит разрыв ДЭС по плоскости скольжения.
- 28. Линейная скорость (U) – движение частиц относительно
- 29. При движении частиц дисперсной фазы они вынуждены
- 30. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Электрокинетические свойства
Электрокинетическими явлениями называют перемещение одной фазы относительно другой в
Слайд 3Обусловлены наличием заряда у частиц д. ф. и противоположного заряда
д. с.
Существует два вида:
Электрокинетические явления
Слайд 41809 г. Ф.Ф. Рейсс изучал электрофорез на глине.
Д. ф. заряжена
«–»: кремнезём [mSiO2]∙nSiO- ∙ (n - x)H+]x- ∙ xH+.
Электрофорез –
перенос коллоидных частиц в электрическом поле.Электрофорез
Слайд 5Электроосмос
1852 г. Видеман
Электроосмос – это течение жидкости через капиллярные системы
под влиянием разности потенциалов.
кварц
H2O
H2O «+» заря-
женная ж-ть
Слайд 6Эффект Дорна
Эффект Дорна или потенциал седиментации (1878г.) – явление возникновения
разности потенциалов между двумя электродами при оседании дисперсной фазы.
Слайд 7Эффект Квинке
Эффект Квинке или потенциал протекания (1859 г.) –возникновение разности
потенциалов при течение воды и водных растворов через разнообразные пористые
материалы под действием перепада давлений.Слайд 8ДЭС
Возникает в результате двух причин:
- или в результате избирательной адсорбции
одного из ионов электролита;
- или за счет ионизации поверхностных молекул
вещества.Слайд 12Модель Гельмгольца-Перрена
ДЭС – это два близко расположенных слоя ионов: один
на поверхности (потенциалопределяющие ионы), другой – в растворе на расстоянии
удвоенного радиуса ионов (противоионы), в целом система электронейтральна, является как бы плоским конденсатором.Слайд 13Рис. Схема ДЭС по Гельмгольцу-Перрену и соответствующий скачок потенциалов.
Модель Гельмгольца-Перрена
Слайд 14ДЭС является как бы плоским конденсатором.
где φ0 – разность
потенциалов между дисперсной фазой и дисперсионной средой;
q – поверхностный
заряд; C – емкость конденсатора: ;
ε – диэлектрическая проницаемость дисперсионной среды;
ε0 – абсолютная диэлектрическая проницаемость:
;
δ – расстояние между пластинами. Или
Модель Гельмгольца-Перрена
Слайд 15Недостатки теории:
- толщина ДЭС Гельмгольца-Перрена очень мала и приближена
к молекулярным размерам;
– невозможно определить реальный электрокинетический потенциал.
Модель Гельмгольца-Перрена
Слайд 16Плоскость скольжения (АВ) – место разрыва при перемещении твердой и
жидкой фазы относительно друг друга.
Электрокинетический потенциал (ξ - дзета
потенциал) – это разность потенциалов между подвижной (диффузной) и неподвижной (адсорбционной) частями двойного электрического слоя.ДЭС
Слайд 17Модель Гуи-Чэпмена
Теория ДЭС с диффузным слоем противоионов предложена независимо друг
от друга Гуи (1910 г.) и Чэпменом (1913 г.).
Слайд 20При введении в систему индифферентного электролита – электролита, не имеющего
ионов, способных достраивать кристаллическую решетку – потенциал φ0 практически не
изменяется.Модель Гуи-Чэпмена
Слайд 22Недостатки теории:
не принимается во внимание объем ионов;
не объясняет явление
перезарядки - перемены знака электрокинетического потенциала при введении в систему
электролита с многовалентными ионами;не объясняет различного действия противоионов с одной и той же валентностью и разным радиусом на ДЭС.
Модель Гуи-Чэпмена
Слайд 25Падение потенциала φ0 складывается из φδ – падения потенциала в
диффузнном слое - и разности потенциалов между обкладками конденсатора φ0
- φδ .Границы скольжения не ясны, в общем случае по границе слоя Гуи.
Модель Штерна
Слайд 26Зависимость электрокинетического потенциала от валентности противоиона определяется адсорбционной способностью, обусловленной
их поляризуемостью и гидратацией.
Перезарядка ДЭС: многовалентные электроны могут втягиваться в
слой Гельмгольца из-за сильных электрических взаимодействий. Потенциал φ0 не изменяетсяМодель Штерна
Слайд 27Электрокинетический потенциал
Направленное перемещение частиц дисперсной фазы под действием электрического поля.
Происходит
разрыв ДЭС по плоскости скольжения.
Слайд 28Линейная скорость (U) – движение частиц относительно мембраны при электроосмосе
и движение частиц при электрофорезе:
- уравнение Гельмгольца-Смолуховского
где η -
вязкость. u = [м/с].


![ЭЛЕКТРОПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ СТРОЕНИЕ ДВОЙНОГО ЭЛЕКТРИЧЕСКОГО СЛОЯ 1809 г. Ф.Ф. Рейсс изучал электрофорез на глине.Д. ф. заряжена «–»: 1809 г. Ф.Ф. Рейсс изучал электрофорез на глине.Д. ф. заряжена «–»: кремнезём [mSiO2]∙nSiO- ∙ (n - x)H+]x-](/img/thumbs/c91c14fce1bf6b96559f64c7fd229ee6-800x.jpg)