Слайд 2Лекция 14. ЭЛЕМЕНТЫ ФИЗИЧЕСКОЙ КИНЕТИКИ
1. Явление переноса в газах.
2. Число
столкновений и длина свободного пробега молекул в газах.
3. Диффузия газов.
4.
Внутреннее трение. Вязкость газов.
5. Теплопроводность газов.
6. Коэффициенты переноса и их зависимость от давления.
7. Понятие о вакууме.
Слайд 31. Явления переноса в газах
Мы знаем, что молекулы в газе
движутся со скоростью пули, звука. Однако, находясь в противо-положном конце
комнаты, запах разлитой пахучей жидкости мы почувствуем через сравнительно боль-шой промежуток времени. Это происходит потому, что молекулы движутся хаотически, то есть они сталки-ваются и траектория у них ломаная.
Рассмотрим следующие явления:
1) Распространение молекул примеси в газе от источника называется диффузией.
Слайд 4 Вы встретитесь с понятием диффузия (например – теплопроводность от радиатора
транзистора и тому подобные). Основные причины и закономерности диффузии, теплопроводимости
легче понять рассматривая явления переноса в газах.
(14.1)
2) Если какое либо тело движется в газе, то оно сталкивается с молекулами газа и сообщает им импульс. С другой стороны тело тоже будет испы-тывать соударения со стороны молекул газа, и полу-чать собственный импульс, но направленный в проти-воположную сторону. Газ ускоряется, тело тормо-зиться, то есть на тело действуют силы трения.
Слайд 5 Такая же сила трения будет действовать и между двумя соседними
слоями газа, движущимися с разными скоростями. Это явление носит название
- внутреннее трение или вязкость газа, причём
(14.2)
3) Если в соседних слоях газа создана и поддерживается разность температур, то между ними будет происходить обмен тепла. Благодаря хаотическому движению, молекулы в соседних слоях будут перемешиваться, и их средние энергии будут выравниваться.
Слайд 6 Происходит перенос энергии от более нагретых к более холодным. Этот
процесс называется теплопроводностью.
– поток тепла. (14.3)
В процессе диффузии
происходит перенос вещества, при внутреннем трении – перенос импульса, при теплопроводности – перенос энергии (тепла). А в основе лежит один и тот же механизм – хаотическое движение молекул. Общность механизма, обуславливающего все эти явления переноса приводит к тому, что их закономерности должны быть похожи друг на друга.
Содержание
Слайд 72. Число столкновений и длина свободного пробега молекул в газах
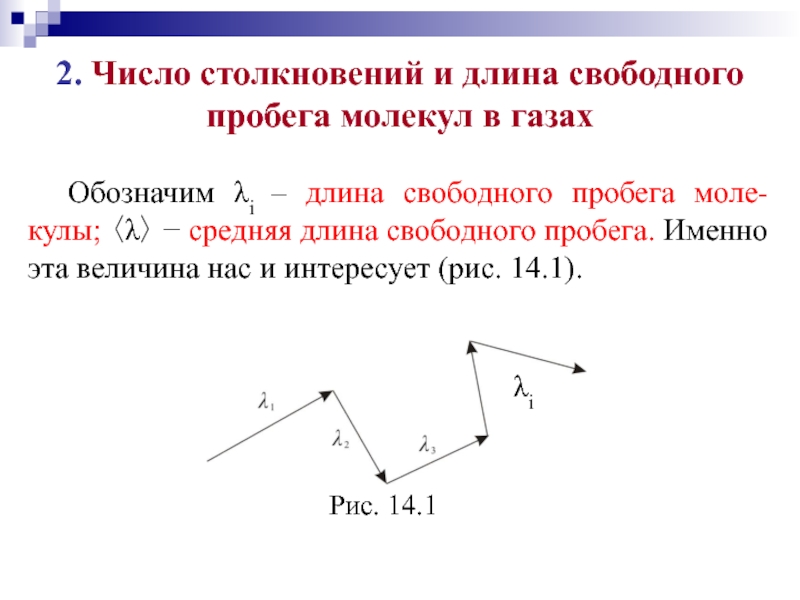
Обозначим
λi – длина свободного пробега моле-кулы; 〈λ〉 − средняя длина
свободного пробега. Именно эта величина нас и интересует (рис. 14.1).
Слайд 8Модель газа – твёрдые шарики одного диаметра взаимодействующие только при
столкновении.
Обозначим Sэфф. – эффективное сечение молекулы (рис. 14.2).
Слайд 9Sэфф=πD2/4 – площадь, в которую не может проникнуть центр любой
другой молекулы. За одну секунду молекула проходит путь, равный средней
арифметической скорости 〈υ〉. За одну секунду молекула претерпевает ν столкновений. Следовательно
(14.4)
Слайд 10 Подсчитаем число столкновений.
Предположим, что все молекулы застыли, кроме одной. Её
траектория будет представлять собой ломанную линию. Столкновения будут только с
теми молекулами, центры которых лежат внутри цилиндра радиусом d (рис. 14.3).
Длина цилиндра за одну секунду равна 〈υ'〉; умножив объём 〈υ'〉S на число молекул в единице объёма n, получим среднее число столкновений в одну секунду:
ν = πd2 〈υ'〉n (14.5)
Слайд 11 На самом деле все молекулы движутся (и в сторону и
на встречу друг другу), поэтому число соударений определяется средней скоростью
движения молекул относительно друг друга.
По закону сложения случайных величин
(14.6)
А так как то получим (14.7)
Слайд 12 Так как p = nkT, то есть
то
(14.8) то есть
Здесь можно заметить, что с учётом введения нами эффективного сечения молекулы Sэфф= πd2.,
(14.9)
Пример: при d = 3Å = 3⋅10−10 м, р = 1 атм, Т = 300 К, 〈λ〉 = 10−7 м. Т.к. 〈λ〉 = 10−7 м, то число столкновений
Содержание
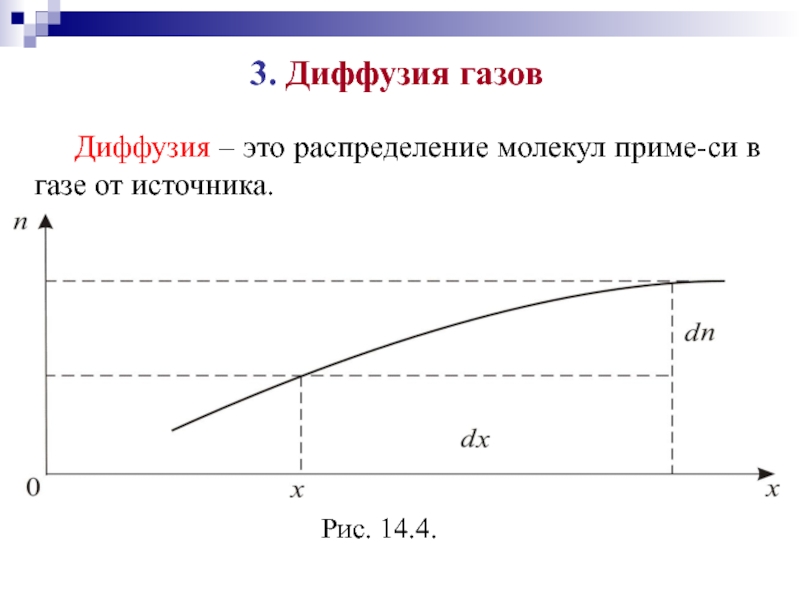
Слайд 133. Диффузия газов
Диффузия – это распределение молекул приме-си в газе
от источника.
Слайд 14 Решаем одномерную задачу. Пусть в газе присутствует примесь с концентрацией
n в точке с координатой х. Концентрация примеси зависит от
координаты х (рис. 14.4).
(14.10)
– в общем случае. Так как у нас одномерная задача, то
При наличии gradn, хаотическое движение будет более направленным – стремиться выровняться по концентрации и возникнет поток молекул примеси, направленных от мест с большей концентрацией к местам с меньшей концентрацией. Найдём этот поток.
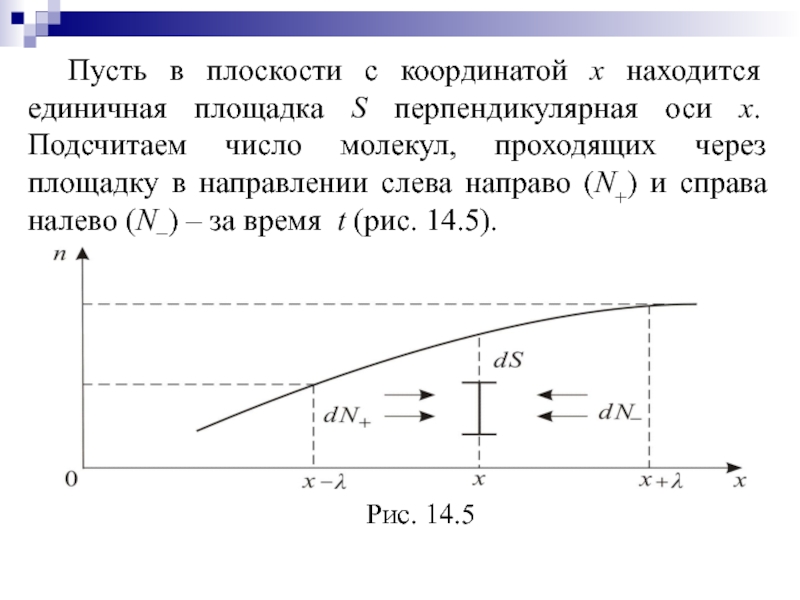
Слайд 15 Пусть в плоскости с координатой х находится единичная площадка S
перпендикулярная оси х. Подсчитаем число молекул, проходящих через площадку в
направлении слева направо (N+) и справа налево (N−) – за время t (рис. 14.5).
(14.11)
(14.12)
где n1' −
концентрация молекул слева от площади, а n2'' − концентрация молекул справа от площади.
Через поверхность S, будут пролетать молекулы, претерпевшие последнее соударение на различных расстояниях от S. Однако в среднем последнее соударение происходит на расстоянии от S, равном средней длине свободного пробега 〈λ〉 . Поэтому в качестве n1' разумно взять значение n1(x-λ), а в качестве n2'' – значение n1(x+λ). Тогда с учетом (14.11)
(14.13)
Слайд 17 Поскольку λ очень мала, то из математического анализа известно, что
и тогда
разность значений функций n(x), стоящую в квадратных скобках, можно представить в виде
Подставив это в выражение (14.13), получим, что
(14.14)
Сравнение выражения (14.14) с формулой (14.1) показывает, что исходя из молекулярно-кинетических представлений, удается не только прийти к правильной зависимости Ni от dni/dx, но и получить выражение для
Слайд 18
коэффициента диффузии D:
(14.15)
Более строгий расчет приводит к такой же формуле,
но с несколько отличным числовым коэффициентом.
(14.16)
или в общем случае
(в трёхмерной системе)
N = - D grad n (14.17)
Уравнение Фика. Поток, направленный в сторону уменьшения концентрации, численно равен потоку через единицу площади в единицу времени при grad n = 1.
Содержание
Слайд 194. Внутреннее трение. Вязкость газов
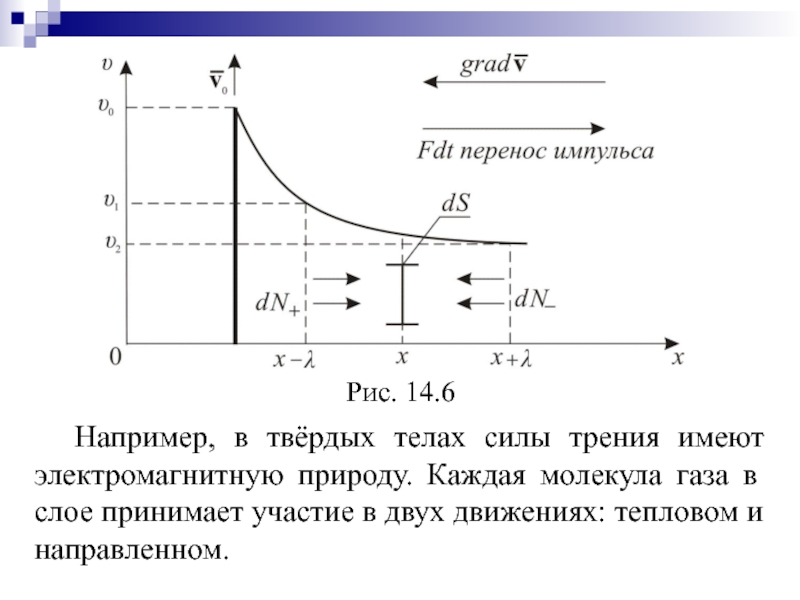
Рассмотрим ещё одну систему координат (рис.
14.6) υ от х. Пусть в покоящемся газе вверх, перпендикулярно
оси х, движется пластинка со скоростью υ0, причём υ0 << υT (υT – скорость теплового движения молекул). Пластинка увлекает за собой прилегающий слой газа, тот слой – соседний и так далее. Весь газ делится как бы на тончайшие слои, скользящие вверх тем медленнее, чем дальше они от пластинки. Раз слои газа движутся с разными скоростями, возникает трение. Какова же здесь природа трения? Ведь силы притяжения в газе малы!
Слайд 20 Например, в твёрдых телах силы трения имеют электромагнитную природу. Каждая
молекула газа в слое принимает участие в двух движениях: тепловом
и направленном.
Слайд 21 Но так как направление теплового движения хаотически меняется, то
в среднем вектор тепловой скорости равен нулю. При направленном движении
вся совокупность молекул будет дрейфовать с постоянной скоростью υ. Таким образом средний импульс отдельной молекулы в слое определяется только дрейфовой скоростью υ: p0 = m0υ. Но так как молекулы участвуют в тепловом движении, они будут переходить из слоя в слой. При этом они будут переносить с собой добавочный импульс, который будет определяться молекулами того слоя, куда перешла молекула. Перемешивание молекул разных слоёв приводит к выравниванию дрейфовых скоростей разных слоёв, что и проявляется макроскопически как действие сил трения между слоями.
Слайд 22 Вернёмся к рис. 14.6 и рассмотрим элементарную площадку dS перпендикулярно
оси х. Через эту площадку за время dt влево и
вправо переходят потоки молекул. Как мы уже говорили
(14.18)
Через площадку S в единицу времени переносится импульс K=N(mu1-mu2) (m – масса молекулы). Подстановка выражения (14.18) для N дает
(14.19)
Слайд 23 Подстановка этих значений в (14.19) дает для потока импульса в
направлении оси z выражение
(14.20)
Приняв во внимание, что произведение nm
равно плотности газа ρ, можно записать
(14.21)
Сравнение с формулой (14.2) дает выражение для коэффициента вязкости
(14.22)
Слайд 24 Уравнение (14.22) называют уравнением Ньютона, где D – коэффициент диффузии;
ρ – плотность. Физический смысл η в том, что он
численно равен импульсу, переносимому в единицу времени через единицу площади при градиенте скорости равном единице (grad⊥ S).
Содержание
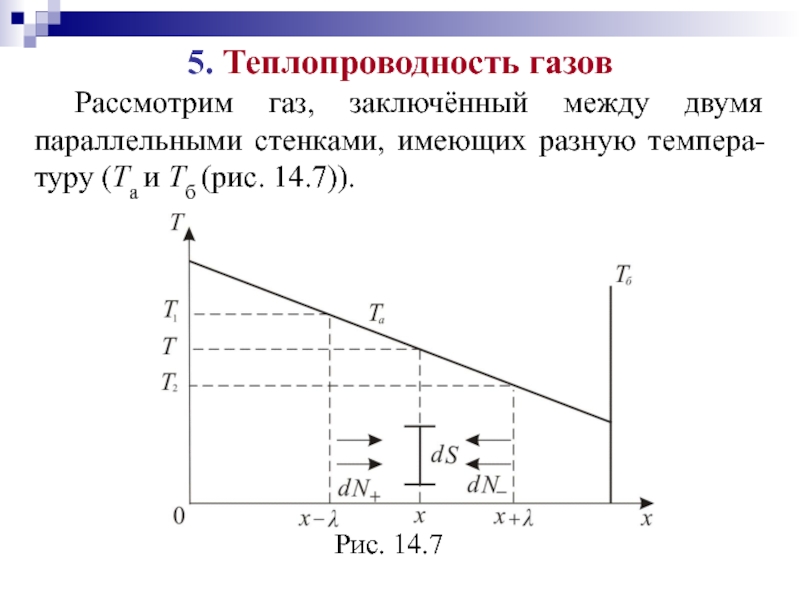
Слайд 255. Теплопроводность газов
Рассмотрим газ, заключённый между двумя параллельными стенками,
имеющих разную темпера-туру (Та и Тб (рис. 14.7)).
Слайд 26 Итак, у нас имеется градиент температуры
тогда через газ в
направлении оси х будет идти поток тепла. Хаотично двигаясь, молекулы
будут переходить из одного слоя газа в другой, перенося с собой энергию. Это движение молекул приводит к перемешиванию молекул, имеющих различную кинетическую энергию
При подсчёте потока тепла введём следующие упрощения:
1) 〈υ〉 = const (средне арифметическая скорость).
2) Примем, что концентрация молекул в соседних слоях тоже одинакова, (хотя на самом деле она различается. Это упрощение даёт ошибку ≈ 10 %).
Слайд 27 Снова вернёмся к рисунку: через площадку S за единицу времени
проходит молекул:
(14.23)
Средняя энергия этих молекул Wк – соответствует значению энергии
в том месте, где они испытывают последнее результирующее столкновение. Для одной молекулы газа:
(14.24)
соответствующую температуре в том месте, где произошло ее последнее соударение с другой молекулой.
Слайд 28 В соответствии со сказанным для потока тепла через площадку S
в положительном направлении оси x получается выражение
где N – определяется
формулой (14.23). Подстановка значений N, Wk1, Wk2 дает
(14.25)
Разность T1–T2 равна
(14.26)
Здесь - производная от Т по оси х в том месте, где расположена плоскость S. Тогда
(14.27)
Слайд 29 Сопоставление этой формулы с формулой (14.3) дает для коэффициента теплопроводности
следующее выражение
(14.28)
Вспомним, что выражение
определяет теплоемкость при постоянном объеме Сv моля газа, т.е. количество газа, содержащего NA молекул.
Слайд 30 Аналогично выражение ink/2 представляет собой теплоемкость количества газа, содержащего n
молекул, т.е. теплоемкость единицы объема газа. Эту теплоемкость можно получить,
умножив удельную теплоемкость cv (теплоемкость ед. массы) на массу ед. объема, т.е. на плотность газа ρ. Таким образом,
(14.29)
Тогда коэффициент теплопроводности
(14.30)
- уравнение Фурье (14.31)
Содержание
Слайд 316. Коэффициенты переноса и их зависимость от давления
Сопоставим
N = −D
gradU или Уравнение Фика для диффузии;
K = −η gradu или Уравнение Ньютона для трения;
Q = −χ gradT или - Уравнение Фурье для теплопроводности.
Все эти законы были установлены опытно, задолго до обоснования молекулярно – кинетической теорией.
Слайд 32 Эта теория позволила установить, что внешнее сходство уравнений обусловлено общностью
лежащих в их основе молекулярного механизма перемешивания молекул в процессе
их теплового хаотического движения. Однако к концу XIX века, несмотря на блестящие успехи молекулярно – кинетической теории ей не доставало твёрдой опоры – прямых экспериментов, доказывающих существование атомов и молекул. Это дало возможность некоторым учёным, философам (Максвелл, Освальд) – наверное вы изучали это течение – субъективный идеализм, заявлять, что схожесть формул – это произвол учёных – упрощённое математическое описание явления.
Слайд 33 Но это конечно не так. Все выше указанные коэффициенты связаны
между собой и все выводы молекулярно – кинетической теории подтверждены
опытно.
Коэффициент диффузии
Коэффициент вязкости
Коэффициент теплопроводности
(здесь m – масса одной молекулы, а nm = ρ − плотность).
Из анализа этих формул вытекает целый ряд важных выводов.
Слайд 34 Рассмотрим зависимость коэффициента переноса от давления p.
Так как скорость теплового
движения молекул
и не зависит от давления p, а коэффициент диффузии
D ~ λ, а λ зависит от давления λ(p).
При обычных давлениях в разряженных газах, в высоком вакууме D = const.
Нужно сказать, что вакуум – понятие относи-тельное. Для газа – нормальное давление 1 атм, а ~10−5 – вакуумное. С ростом давления уменьшается λ и затрудняется диффузия (D → 0).
При T = const ρ ~ p отсюда, при обычных давле-ниях: , ρ ~ p, η = const; в вакууме D = const, ρ ~ p, η ~ ρ.
Слайд 35С увеличением p и ρ, повы-шается число молекул пе-реносящих импульс
из слоя в слой, но даёт уменьшенное расстояние свободного пробега
λ. Поэтому вязкость η не зависит от давления p – это подтверждено эксперимен-тально.
На (рис. 14.8) показаны зависимости коэффициентов переноса и λ от p. То есть здесь изображено всё, о чём мы говорили выше. Эти зависимости широко используют в технике (например при измерении вакуума).
Слайд 36Молекулярное течение. Эффузия газов
Молекулярное течение – течение газов в условиях
вакуума. То есть, когда молекулы не сталкиваются друг с другом.
В вакууме происходит передача импульса непосредственно стенкам сосуда, то есть происходит трение газа о стенки сосуда. Трение перестаёт быть внутренним и понятие вязкости теряет свой прежний смысл (как трение одного слоя газа о другой). Течение газа в условиях вакуума через отверстие (под действием разности давлений) называется эффузией газа.
Слайд 37 Как при молекулярном течении, так и при эффузии количество протекающего
в единицу времени газа обратно пропорционально корню квадратному из молярной
массы:
(14.32)
Эту зависимость тоже широко используют в технике (например – при разделении изотопов газа U235 отделяют от U238, используя газ UF6).
Содержание
Слайд 387. Понятие о вакууме
Газ называется разреженным (разреженный газ), если его
плотность столь мала, что средняя длина свободного пробега молекул 〈λ〉
может быть сравнима с линейными размерами l сосуда, в котором находится газ. Такое состояние газа также называется вакуумом.
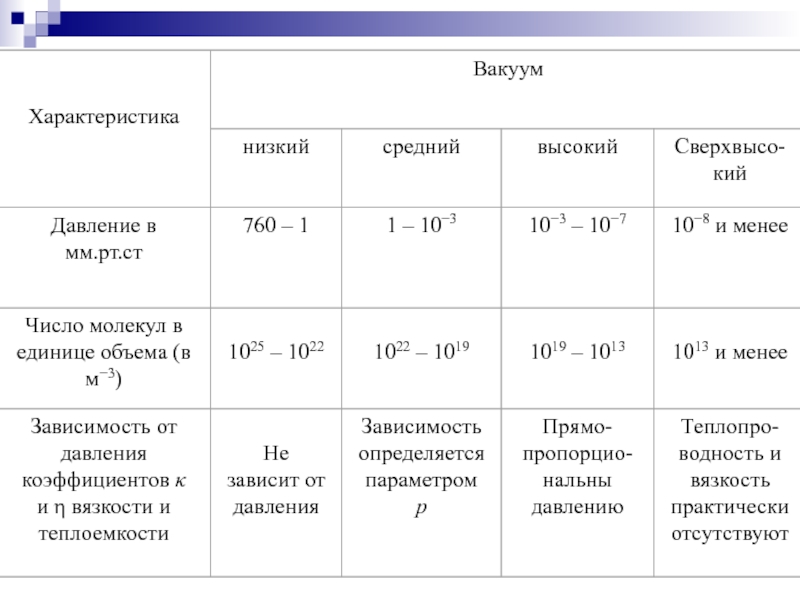
Различают следующие степени вакуума: сверхвысокий (〈λ〉>>l), высокий (〈λ〉>l), средний (〈λ〉≈l) и низкий вакуум. В трех первых степенях вакуума свойства разряженных газов отличаются от свойств неразряженных газов. Это видно из таблицы, где приведены некоторые характеристики различных степеней вакуума.
Слайд 40 В состоянии высокого вакуума уменьшение плотности разряженного газа приводит к
соответствующей убыли частиц без изменения 〈λ〉. Следовательно, уменьшается число носителей
импульса или внутренней энергии в явлениях вязкости и теплопроводности. Коэффициент переноса в этих явлениях прямо пропорциональны плотности газа. В сильно разряженных газах внутреннее трение по существу отсутствует. Вместо него возникает внешнее трение движущегося газа о стенки сосуда, связанное с тем, что молекулы изменяют свои импульсы только при взаимодействии со стенками сосуда. В этих условиях коэффициент трения в первом приближении пропорционален плотности газа и скорости его движения.
Слайд 41 Удельный тепловой поток в сильно разряженных газах пропорционален разности температур
и плотности газа.
Стационарное состояние разряженного газа, находящегося в двух сосудах,
соединенных узкой трубкой, возможно при условии равенства встречных потоков частиц, перемещающихся из одного сосуда в другой: n1〈υ1〉 = n2〈υ2〉, где n1 и n2 – число молекул в 1 см3 в обеих сосудах; 〈υ1〉 и 〈υ2〉 – их средние арифметические скорости.
Слайд 42 Если Т1 и Т2 – температуры газа в сосудах, то
предыдущее условие стационарности можно переписать в виде уравнения, выражающего эффект
Кнудсена:
где р1 и р2 – давления разряженного газа в обоих сосудах.