Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коррозия металлов
Содержание
- 1. Коррозия металлов
- 2. Основные антикоррозионные мероприятияРациональное конструированиеВыбор устойчивых к коррозии конструкционных материаловХимическая обработка средыПрименение защитных покрытийЭлектрохимическая защита
- 3. Слайд 3
- 4. 3. Химическая обработка среды3.1. Удаление деполяризаторов (кислород, ионы
- 5. 3.1. Удаление деполяризатора а) кислород (нейтральная или
- 6. 3.1. Удаление деполяризатора б) ионы водорода (кислая
- 7. 3.2. Удаление солейИспользуемые методы: дистилляция ионный обмен обратный осмос
- 8. 3.3. Удаление кислых газов Нейтрализация щелочными реагентами:H2S
- 9. 3.4. Применение ингибиторов коррозииИнгибиторы-вещества, тормозящие скорость коррозионного процесса
- 10. Классификация ингибиторов коррозии по механизму действияАнодные ингибиторы
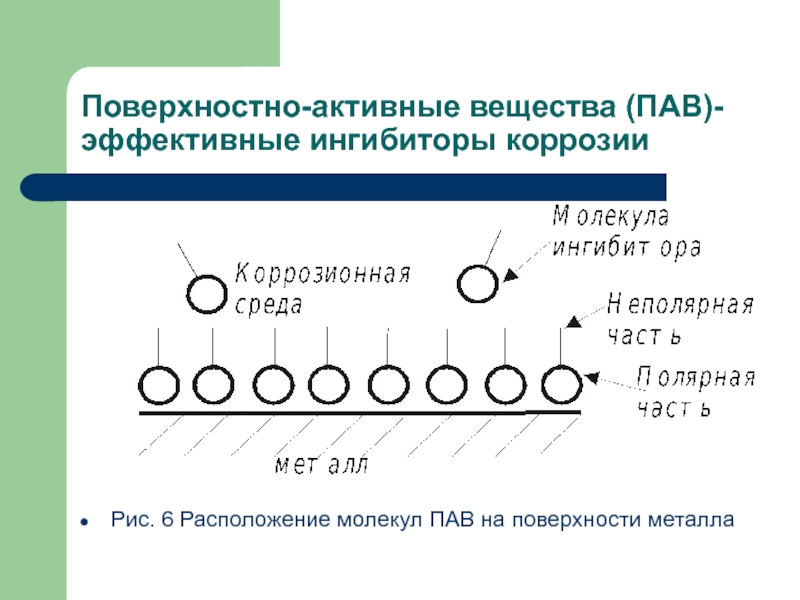
- 11. Поверхностно-активные вещества (ПАВ)- эффективные ингибиторы коррозииРис. 6 Расположение молекул ПАВ на поверхности металла
- 12. Слайд 12
- 13. 4. Применение защитных покрытийКлассификация защитных покрытий.Все защитные
- 14. 4.1. Неметаллические защитные покрытияКраскиЛакиЭмалиПолимерные материалы (каучуки, резина, эпоксидные смолы)БитумыЦементы
- 15. Слайд 15
- 16. Слайд 16
- 17. Слайд 17
- 18. Слайд 18
- 19. Слайд 19
- 20. 4.2. Металлические защитные покрытияХромирование CrНикелирование
- 21. 4.3. Металлические защитные покрытияСпособы нанесения металлических защитных и декоративных покрытий:металлизацияплакированиеэлектролиз
- 22. Классификация металлических покрытий по механизму защитного действияКатодные покрытия-покрытие менее активным металламиАнодные покрытия-покрытия более активными металлами
- 23. Механизм действия катодного металлического покрытия
- 24. Механизм действия анодного металлического покрытияКоррозия оцинкованного железа φ(Fe)= - 0,44 B, φ(zn)= -0,76 BFe-катод, Zn- анод
- 25. 4.3. Химические защитные покрытияОксидированиеРецептура состава для «воронения» стали:Фосфатирование
- 26. Слайд 26
- 27. Электрохимическая защита металлов от коррозии
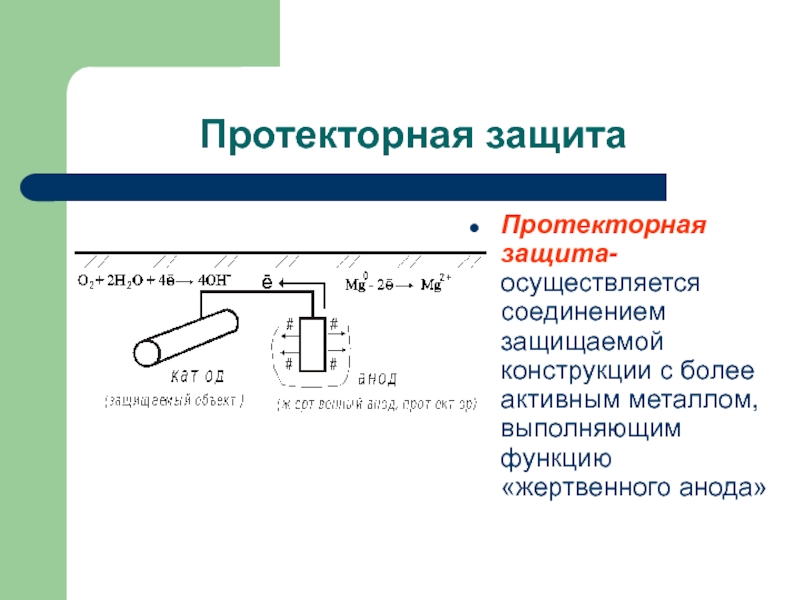
- 28. Протекторная защита Протекторная защита-осуществляется соединением защищаемой конструкции с более активным металлом, выполняющим функцию «жертвенного анода»
- 29. Слайд 29
- 30. Слайд 30
- 31. Слайд 31
- 32. Слайд 32
- 33. Катодная защитаКатодная защита обеспечивается поляризацией защищаемого объекта от внешнего источника тока (станции катодной защиты)-+
- 34. Слайд 34
- 35. Слайд 35
- 36. Скачать презентанцию
Основные антикоррозионные мероприятияРациональное конструированиеВыбор устойчивых к коррозии конструкционных материаловХимическая обработка средыПрименение защитных покрытийЭлектрохимическая защита
Слайды и текст этой презентации
Слайд 2Основные антикоррозионные мероприятия
Рациональное конструирование
Выбор устойчивых к коррозии конструкционных материалов
Химическая обработка
среды
Слайд 43. Химическая обработка среды
3.1. Удаление деполяризаторов
(кислород, ионы водорода)
3.2. Удаление солей
3.3.
Удаление кислых газов
3.4. Применение ингибиторов коррозии
Слайд 53.1. Удаление деполяризатора
а) кислород (нейтральная или щелочная среда)
Кипячение
Пропускание через поглощающие
кислород фильтры
Содержащая кислород → Фильтр с железной → Среда
с меньшимжидкая среда стружкой содержанием
Обработка сульфитами
Обработка гидразином
Слайд 63.1. Удаление деполяризатора
б) ионы водорода (кислая среда)
Нейтрализация растворами щелочей
(
гидроксид натрия, гидроксид кальция)
Обработка растворами гидролизующихся по аниону солей
( карбонат натрия, фосфат натрия)Слайд 83.3. Удаление кислых газов
Нейтрализация щелочными реагентами:
H2S + 2NaOH →
Na2S + 2H2O
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Осаждение в
виде малорастворимых соединений (сульфидов, карбонатов)H2S + CuSO4 → CuS↓ + 2H2SO4
Окисление сероводорода сильными окислителями (KMnO4, K2Cr2O7) S-2 -2e → So
Слайд 93.4. Применение ингибиторов коррозии
Ингибиторы-вещества, тормозящие скорость коррозионного процесса
Слайд 10Классификация ингибиторов коррозии по механизму действия
Анодные ингибиторы тормозят скорость процесса
перехода ионов металла в раствор.
Катодные ингибиторы тормозят скорость процесса деполяризации
Ингибиторы
экранирующего действия осуществляют смешанный контрольСлайд 11Поверхностно-активные вещества (ПАВ)- эффективные ингибиторы коррозии
Рис. 6 Расположение молекул ПАВ
на поверхности металла
Слайд 134. Применение защитных покрытий
Классификация защитных покрытий.
Все защитные покрытия подразделяются на:
неметаллические
металлические
химические
Слайд 144.1. Неметаллические защитные покрытия
Краски
Лаки
Эмали
Полимерные материалы
(каучуки, резина, эпоксидные смолы)
Битумы
Цементы
Слайд 204.2. Металлические защитные покрытия
Хромирование Cr
Никелирование Ni
Алитирование
Al
Меднение
CuСеребрение Ag
Золочение Au
Кадмирование Cd
Цинкование Zn
Лужение Sn
На защиту металлов от коррозии расходуется от мирового производства:
Ni - 15%,
Sn - 25%,
Cd - 50%