Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Механизмы сульфирования
Содержание
- 1. Механизмы сульфирования
- 2. СульфированиеArH + H2SO4
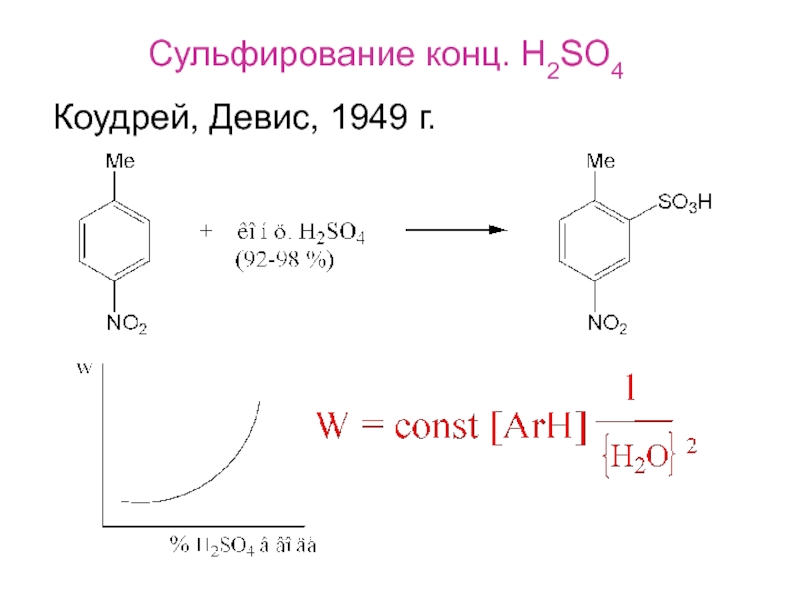
- 3. Сульфирование конц. H2SO4Коудрей, Девис, 1949 г.
- 4. 2H2SO4 H3SO4+
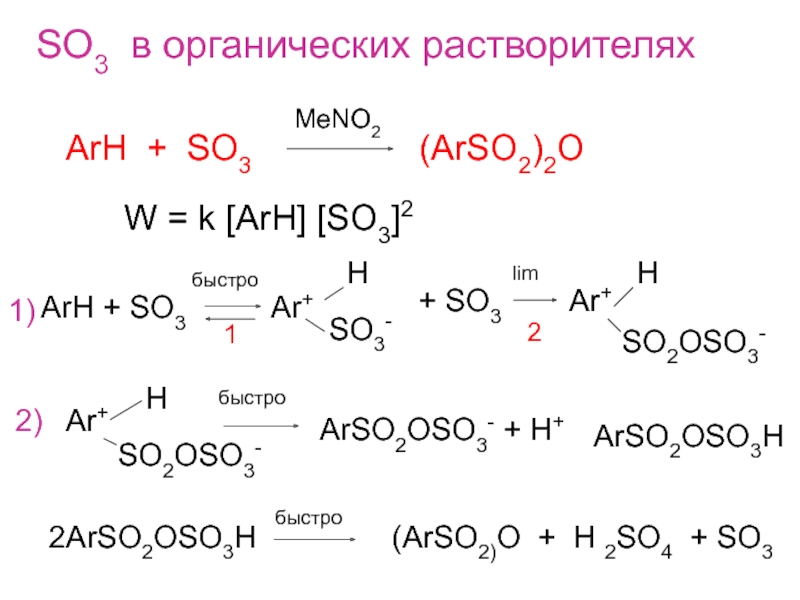
- 5. SO3 в органических растворителяхArH + SO3
- 6. Кинетические изотопные эффектып-СlC6H4D
- 7. Реакция фриделя-Крафтса(алкилирование, ацилирование)AlkHal + MHalnAlkOH + H+R-CH=CH2
- 8. Природа MX4 + С*H3CD2F BF3CD2C*H3+ С*H3CH2F -
- 9. RX + MXn
- 10. АцилированиеArH + RCOHal
- 11. ABB1) Обычно: W = k[ArH]
- 12. ГалоидированиеТенденция к гетеролизу у галогенов мала:
- 13. J.K. Kochi et al., New J. Chem.2002,
- 14. Электрофильное фторированиеArH
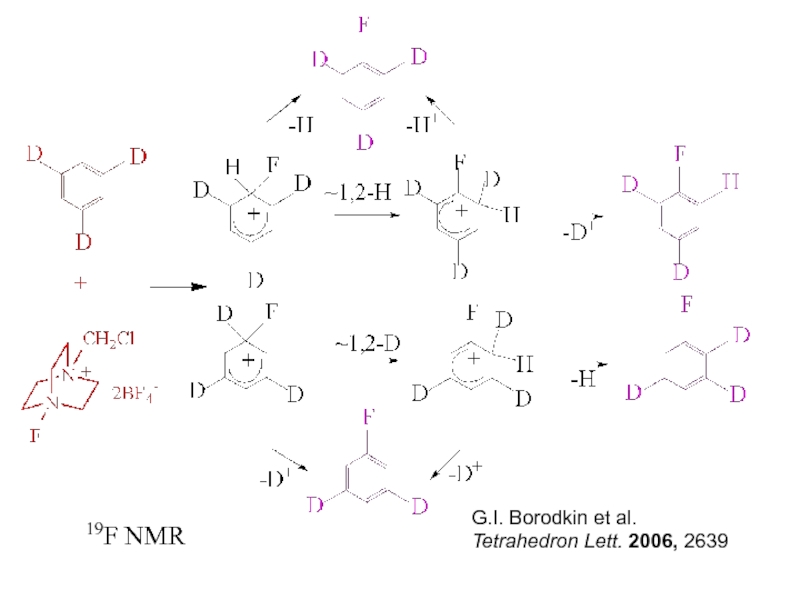
- 15. G.I. Borodkin et al.Tetrahedron Lett. 2006, 2639 19F NMR
- 16. Влияние природы заместителейPhH + X+
- 17. Фактор парциальной скорости замещения (fi) - отношение
- 18. 56% 3%
- 19. Соотношение селективностей Брауна-Стокаlgfp = AxFslgfm = BxFsFs = lg(fp/fm)субстратнаяселективностьпозиционнаяселективность
- 20. Соотношение селективностей Брауна-Стокаи уравнение Гамметаfp = kp-X/kHfm
- 21. OlahSchofieldдифф. пределNO2+ssssssPhMessssNO2+ PhMessssssssбарьер
- 22. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Теоретические основы органической
химии
Механизмы сульфирования,
галоидирования аренов.
Реакция Фриделя-Крафтса.
Лекция 29
(электронно-лекционный курс)
Проф.
Бородкин Г.И.
Слайд 2Сульфирование
ArH + H2SO4
ArSO3H + H2O
SO3 + H2SO4 (сложная система, пиросерная кислота +
др.)SO3 (MeNO2, PhNO2 и др.)
ClSO2OH, ClSO2NMe2/In(OTf)3 (Frost, C.G.et al. Synlett 2002,
1928)
Слайд 42H2SO4 H3SO4+ + HSO4-
[H3SO4+] =
2H2SO4
SO3 + H2O + HSO4- [SO3] = 3H2SO4 HSO3+ + H3O+ + 2HSO4-
[HSO3+] =
4) 3H2SO4 H2S2O7+ + HSO4-
[H2S2O7] =
[HSO4-]
c1
c2
[H3O+] [HSO4-]
c3
[H3O+] [HSO4-]2
c4
[H3O+] [HSO4-]
H2O + H2SO4 H3O+ + HSO4-
Слайд 5SO3 в органических растворителях
ArH + SO3
(ArSO2)2O
MeNO2
W = k [ArH] [SO3]2
ArH +
SO3 Ar+ H
SO3-
быстро
+ SO3 Ar+
H
SO2OSO3-
lim
1
2
1)
SO2OSO3-
H
2)
Ar+
ArSO2OSO3- + H+
ArSO2OSO3H
2ArSO2OSO3H
быстро
(ArSO2)O + H 2SO4 + SO3
быстро
Слайд 6Кинетические изотопные эффекты
п-СlC6H4D
п-ClC6H4SO3H
97% H2SO4
kH / kD = 3.2
Реакция сульфирования обратима
!Механизм сульфирования сложен и зависит от
среды. В водной Н2SO4 (80 – 85%) – активная
частица - H3SO4+
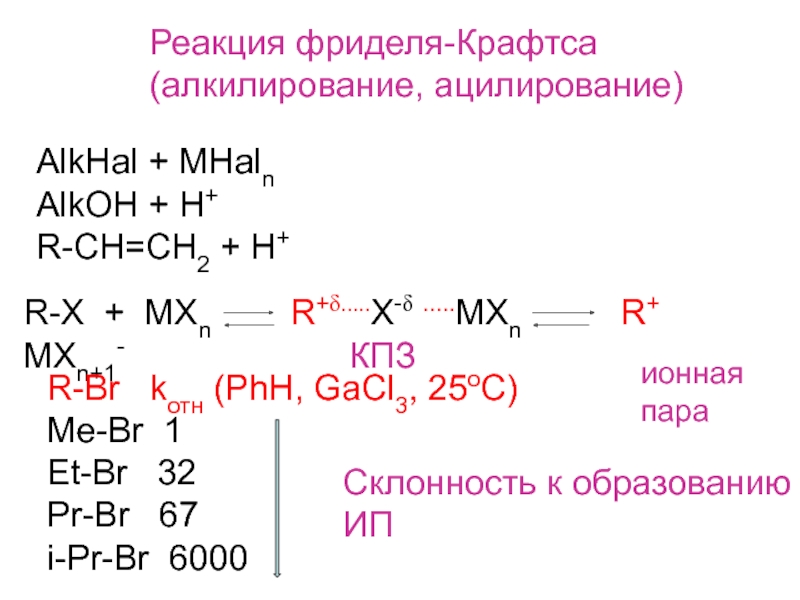
Слайд 7Реакция фриделя-Крафтса
(алкилирование, ацилирование)
AlkHal + MHaln
AlkOH + H+
R-CH=CH2 + H+
R-X +
MXn R+δ.....X-δ .....MXn
R+ MXn+1-КПЗ
ионная
пара
R-Br kотн (PhH, GaCl3, 25oC)
Me-Br 1
Et-Br 32
Pr-Br 67
i-Pr-Br 6000
Склонность к образованию
ИП
Слайд 8Природа MX4
+ С*H3CD2F BF3
CD2C*H3
+ С*H3CH2F - [HOBF3-]
C*H2C*H3
50% ПГ !
Нет
ПГ
(EtF + BF3/H2O)
Природа X в AlkX
F > Cl > Br
> I концепцияПирсона
Nokane et al. Bull. Chem. Soc. Jap.
1978, 1441
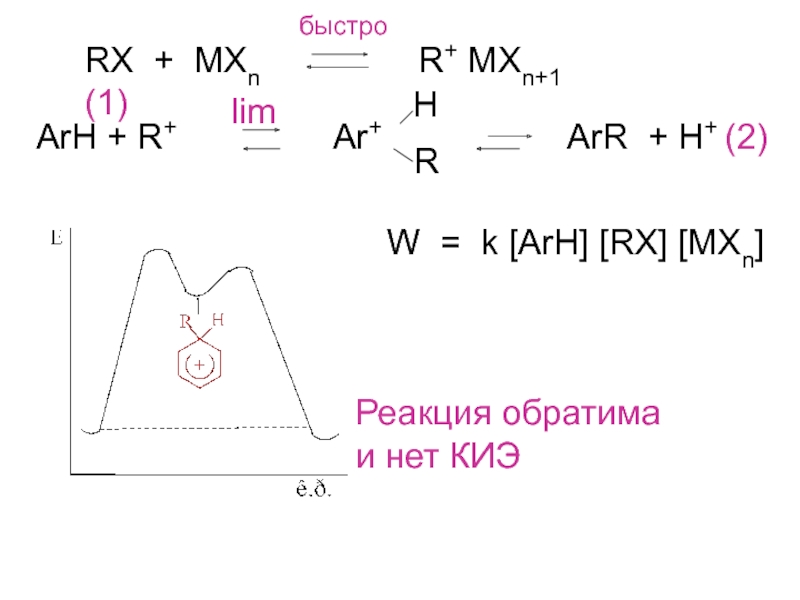
Слайд 9RX + MXn
R+ MXn+1 (1)
быстро
ArH + R+
Ar+ ArR + H+ (2)H
R
W = k [ArH] [RX] [MXn]
Реакция обратима
и нет КИЭ
lim
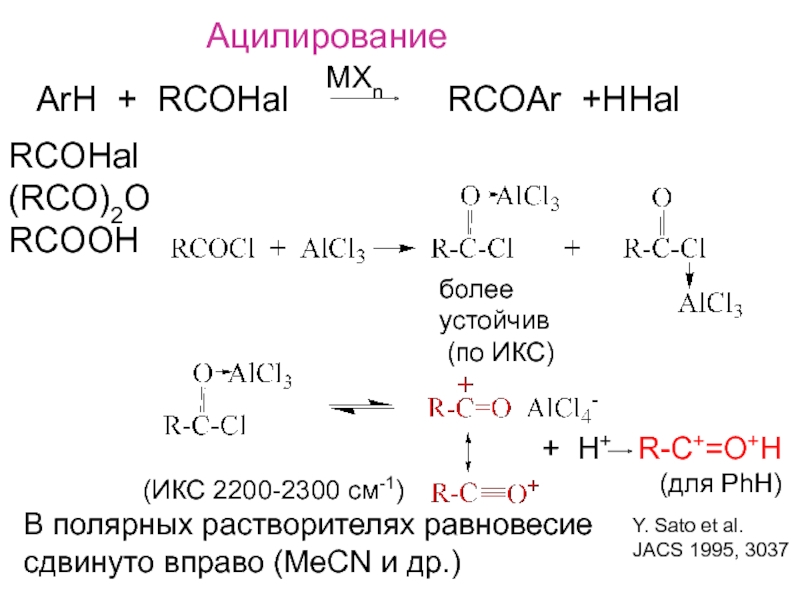
Слайд 10Ацилирование
ArH + RCOHal
RCOAr +HHal
MXn
RCOHal
(RCO)2O
RCOOH
более
устойчив
(по ИКС)
В полярных растворителях
равновесиесдвинуто вправо (MeCN и др.)
(ИКС 2200-2300 см-1)
+ H+ R-C+=O+H
(для PhH)
Y. Sato et al.
JACS 1995, 3037
Слайд 11A
B
B
1) Обычно: W = k[ArH] [RCOX] [MXn]
2) MeCOF,
MeCOCl, MeCOBr реагируют с PhMe
c одинаковой скоростью
3) RCO+ стабилизирован мезомерией
имолореакционноспособен
ρ+ велико по абс. величине ( ~ -10 !)
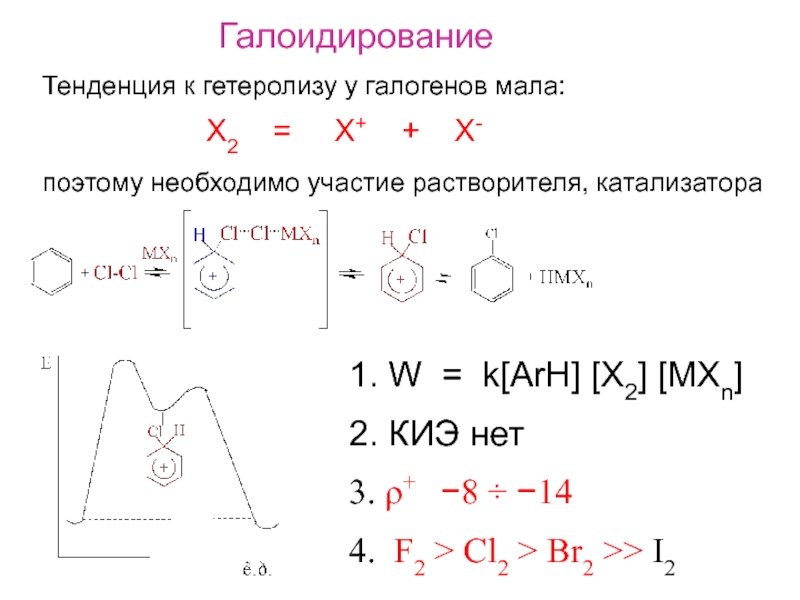
Слайд 12Галоидирование
Тенденция к гетеролизу у галогенов мала:
X2 =
X+ + X-поэтому необходимо участие растворителя, катализатора
1. W = k[ArH] [X2] [MXn]
2. КИЭ нет
3. ρ+ −8 ÷ −14
4. F2 > Cl2 > Br2 >> I2
Слайд 13J.K. Kochi et al., New J. Chem.2002, 582
Å
X-ray, -40
-70oC
Kp = 1.0 M-1
Облучение на СТ-полосе π-комплекса
Слайд 14
Электрофильное фторирование
ArH
kH/kD
C6D6
0.92Мезтитилен-d3 0.89
Нафталин-d8 0.86
в MeCN
ArH +
ArF + H+
КИЭ против SET
Слайд 16Влияние природы заместителей
PhH + X+
PhX + H+
PhY + X+
YC6H4X + H+kPhH
kPhY
Относительная скорость замещения
ОСЗ = kPhY / kPhH
Нитрование HNO3 / AcOH, 45 oC ОСЗ
X = H 1
X = Me 24.5
X = COOET 0.0037
X = Cl 0.033
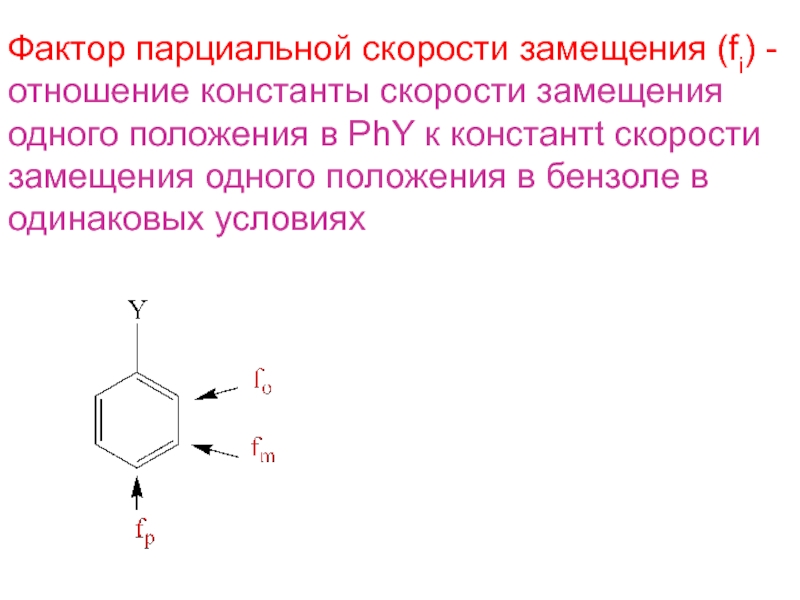
Слайд 17Фактор парциальной скорости замещения (fi) -
отношение константы скорости замещения
одного
положения в PhY к константt скорости
замещения одного положения в бензоле
водинаковых условиях
Слайд 1856% 3%
41%
ОСЗ = kPhMe/kPhH
= 24.5
fo = ОСЗ
0.56 . 6
2
= 41
fм
= ОСЗ0.03 . 6
2
= 2.3
fp = ОСЗ
0.41 . 6
1
= 59
f = fofp = 41.59 = 2419
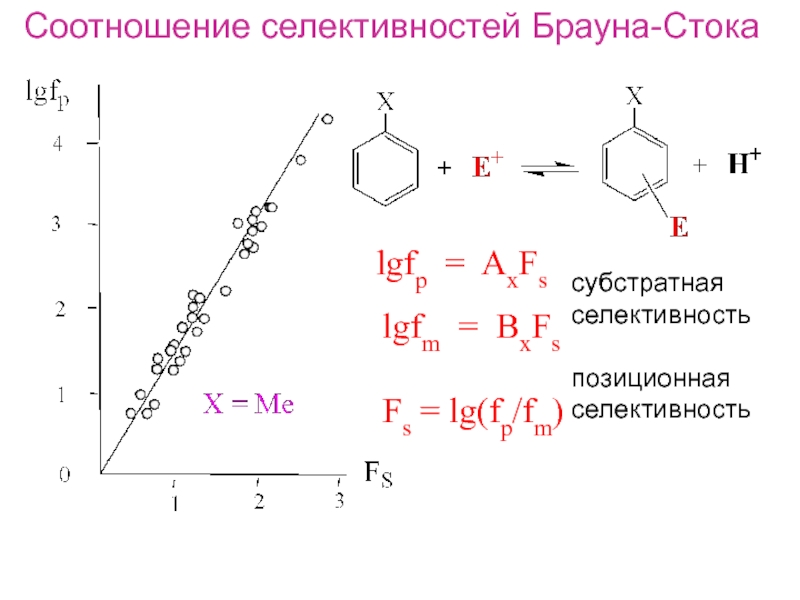
Слайд 19Соотношение селективностей Брауна-Стока
lgfp = AxFs
lgfm = BxFs
Fs = lg(fp/fm)
субстратная
селективность
позиционная
селективность
Слайд 20Соотношение селективностей Брауна-Стока
и уравнение Гаммета
fp = kp-X/kH
fm = km-X/kH
lgfp =
σp+ρ
lgfm = σm+ρ
Fs = lg (fp/fm) = lgfp – lgfm
= (σp+ - σm+) ρlgfp = AXFs AX = (lgfp)/Fs =
σp+ρ
(σp+ -
σm+)ρ
σp+
σp+ -
σm+
tg α =


![Механизмы сульфирования 2H2SO4 H3SO4+ + HSO4- [H3SO4+] = 2H2SO4 2H2SO4 H3SO4+ + HSO4- [H3SO4+] = 2H2SO4](/img/thumbs/2c57d36fd54b53de4ef74fd548cf4a3c-800x.jpg)

![Механизмы сульфирования Природа MX4 + С*H3CD2F BF3CD2C*H3+ С*H3CH2F - [HOBF3-]C*H2C*H350% ПГ !Нет ПГ(EtF Природа MX4 + С*H3CD2F BF3CD2C*H3+ С*H3CH2F - [HOBF3-]C*H2C*H350% ПГ !Нет ПГ(EtF + BF3/H2O)Природа X в AlkXF >](/img/thumbs/6adbd9d09d08678ebe4c1d19cbf707cc-800x.jpg)
![Механизмы сульфирования ABB1) Обычно: W = k[ArH] [RCOX] [MXn]2) MeCOF, MeCOCl, MeCOBr ABB1) Обычно: W = k[ArH] [RCOX] [MXn]2) MeCOF, MeCOCl, MeCOBr реагируют с PhMec одинаковой скоростью3)](/img/thumbs/fefdeee3fd74faabeea626b8d269e721-800x.jpg)