Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Непредельные углеводороды содержат одну или несколько углеродных
Содержание
- 1. Непредельные углеводороды содержат одну или несколько углеродных
- 2. Физические свойства алкеновЭтилен — бесцветный газ, почти без запаха, немного легче воздуха, плохо растворим в воде.Этилен
- 3. SbroolsПропиленФизические свойства алкеновБутенПропилен и бутилен — также
- 4. Алкены плохо растворимы в воде, но хорошо
- 5. Химические свойства алкеновДвойная связь в алкенах состоит
- 6. Кратная связь представляет собой область повышенной электронной
- 7. Реакции присоединенияРеакция гидрирования (гидрогенизация) — это реакция взаимодействия
- 8. Реакции присоединенияАлкены вступают в реакцию галогенирования — это реакция взаимодействия с галогенами. CnH2n + Г2 → CnH2nГ2
- 9. Периодическая система химических элементов Дмитрия Ивановича Менделеева
- 10. Качественной реакцией для алкенов является обесцвечивание бромной
- 11. Реакции присоединенияРеакция гидрогалогенирование —это реакция взаимодействия с
- 12. Гидратация — реакция присоединения молекул воды так
- 13. Марковников Владимир Васильевич1803–1873 гг. Присоединение галогенводородов и
- 14. Ещё одной характерной реакцией для алкенов и для всех органических соединений является реакция окисления.
- 15. Реакция горения — разновидность быстропротекающей реакции окисления.CnH2n
- 16. Окисление перманганатом калия в нейтральной среде —
- 17. Реакции полимеризацииnCH2 = CH2 → (—CH2—CH2—)nt, p
- 18. Реакция полимеризации — процесс последовательного соединения одинаковых молекул в большие по размерам молекулы.
- 19. Этиленовые углеводороды с воздухом образуют небезопасные взрывные
- 20. Для этиленовых углеводородов характерны реакции:– присоединения;– окисления;– полимеризации.
- 21. Скачать презентанцию
Физические свойства алкеновЭтилен — бесцветный газ, почти без запаха, немного легче воздуха, плохо растворим в воде.Этилен
Слайды и текст этой презентации
Слайд 1Непредельные углеводороды содержат одну или несколько углеродных связей.
Простейший представитель
— этилен или этен.
Слайд 2Физические свойства алкенов
Этилен — бесцветный газ, почти без запаха, немного
легче воздуха, плохо растворим в воде.
Этилен
Слайд 3Sbrools
Пропилен
Физические свойства алкенов
Бутен
Пропилен и бутилен — также газообразны.
От пентена до
октадецена включительно углеводороды находятся в жидком состоянии, а начиная
с
нонадецена — в твёрдом.
Слайд 4Алкены плохо растворимы в воде, но хорошо —
в органических
растворителях. Этилен и пропилен горят коптящим пламенем.
Физические свойства алкенов
Слайд 5Химические свойства алкенов
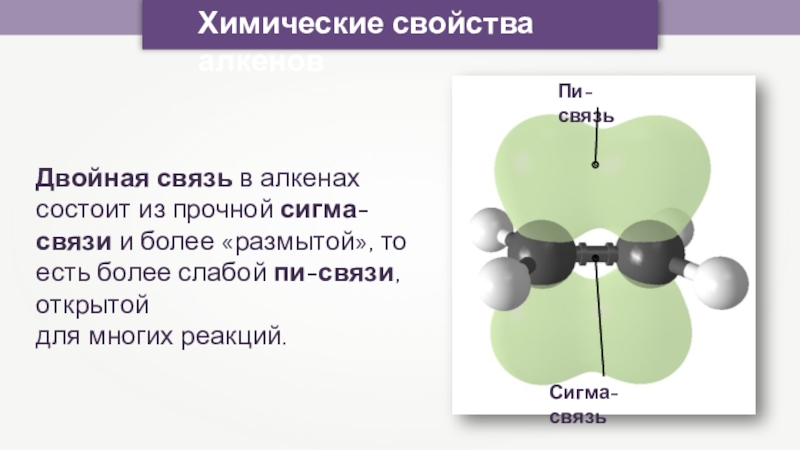
Двойная связь в алкенах состоит из прочной сигма-связи
и более «размытой», то есть более слабой пи-связи, открытой
для
многих реакций. Сигма-связь
Пи-связь
Слайд 6Кратная связь представляет собой область повышенной электронной плотности, которая доступна
для частиц с полным или частичным положительным зарядом — электрофилов.
Слайд 7Реакции присоединения
Реакция гидрирования (гидрогенизация) — это реакция взаимодействия с водородом, которая
происходит в присутствии катализатора никеля и при повышенной температуре.
CnH2n + H2
→ CnH2n+2t, Ni
Слайд 8Реакции присоединения
Алкены вступают в реакцию галогенирования — это реакция взаимодействия с
галогенами.
CnH2n + Г2 → CnH2nГ2
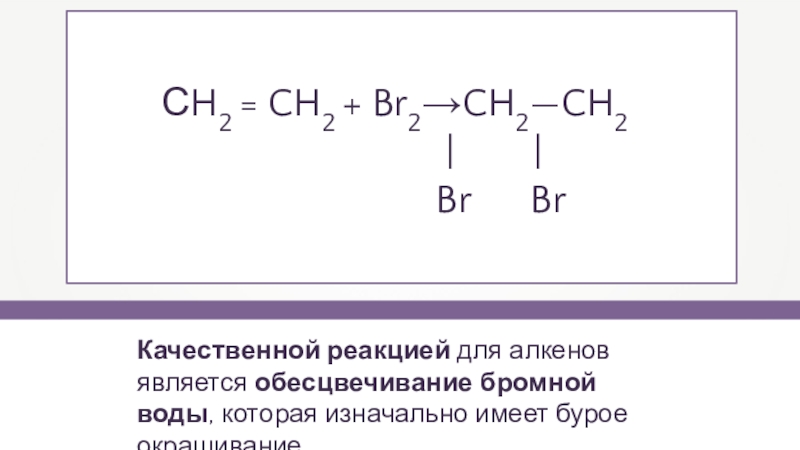
Слайд 10Качественной реакцией для алкенов является обесцвечивание бромной воды, которая изначально
имеет бурое окрашивание.
СH2 = CH2 + Br2→CH2—CH2
| | Br Br
Слайд 11Реакции присоединения
Реакция гидрогалогенирование —
это реакция взаимодействия
с галогенводородами.
R—CH = CH2
+ НГ → R—CH—CH3
|Г
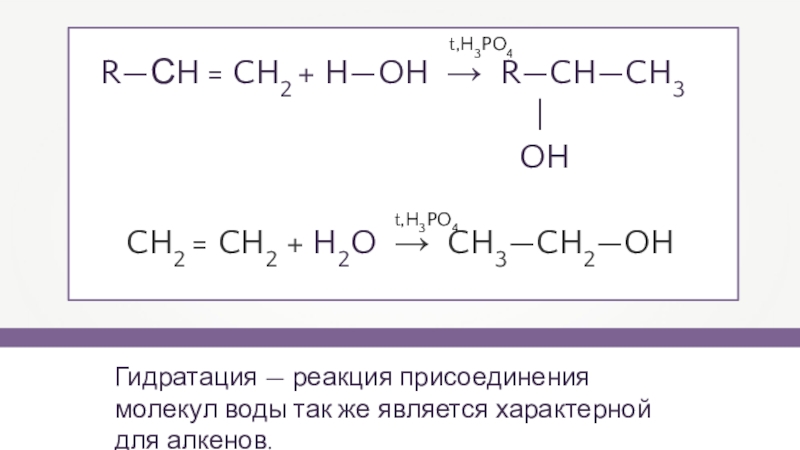
Слайд 12Гидратация — реакция присоединения молекул воды так же является характерной
для алкенов.
R—СH = CH2 + H—OH → R—CH—CH3
| OH
t,H3PO4
CH2 = CH2 + H2O → CH3—CH2—OH
t,H3PO4
Слайд 13Марковников Владимир Васильевич
1803–1873 гг.
Присоединение галогенводородов и воды
к несимметричным
алкенам происходит по правилу Марковникова Владимира Васильевича.
Слайд 14Ещё одной характерной реакцией для алкенов и для всех органических
соединений является реакция окисления.
Слайд 15Реакция горения — разновидность быстропротекающей реакции окисления.
CnH2n +3n : 2O2
→ nCO2 + nH2O + Q
t, p, kat
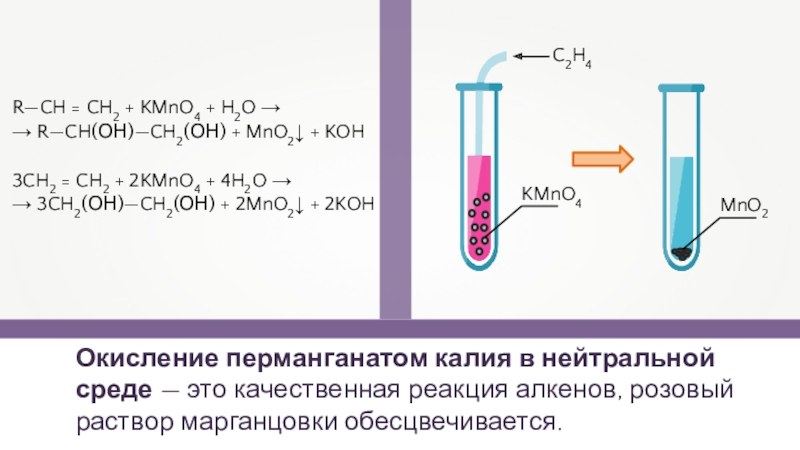
Слайд 16Окисление перманганатом калия в нейтральной среде — это качественная реакция
алкенов, розовый раствор марганцовки обесцвечивается.
R—CH = CH2 + KMnO4 +
H2O →→ R—CH(ОН)—CH2(ОН) + MnO2↓ + KOH
3CH2 = CH2 + 2KMnO4 + 4H2O →
→ 3CH2(ОН)—CH2(ОН) + 2MnO2↓ + 2KOH
KMnO4
C2H4
MnO2
Слайд 17Реакции полимеризации
nCH2 = CH2 → (—CH2—CH2—)n
t, p
nCH2 = CH—CH3
→ (—CH2—CH—)n
|CH3
t, p, kat
Мономер
Мономер
Полимер
Полимер
Этилен
Полиэтилен
Полипропилен
Этилен