Слайд 1Патофизиология почек
Лекция для студентов 3-го курса
Специальность «педиатрия»
Кафедра патофизиологии КрасГМА
Слайд 2Цель: Сформировать у студентов современные представления об этиопатогенезе нарушений функции
почек.
Содержание лекции:
1. основное назначение почек.
2. процесс фильтрации.
3.
Процесс реабсорбции.
4. Процесс секреции.
5. Роль почек в поддержании КОС.
6. Мочевой синдром.
7. Нефротический синдром.
8. Острая почечная недостаточность.
9. Хроническая почечная недостаточность.
10. Уремия.
11. Гломерулонефрит.
12. Пиелонефрит.
Слайд 3Механизмы типовых нарушений экскреторной функции почек
Нарушение мочеобразования является следствием расстройств процессов клубочковой фильтрации, канальцевой реабсорбции
(транспорта ионов, воды, глюкозы, аминокислот и других веществ из канальцевой жидкости в кровь), экскреции (транспорта ионов, жидкости и ряда веществ из крови в канальцевую мочу) и секреции (транспорта ионов и веществ из клеток эпителия канальцев в мочу).
Слайд 4Процессы фильтрации в почках
Образование мочи происходит путем фильтрации крови через
клубочки нефронов.
Не проходят крупнодисперсные белки, форменные элементы крови.
Образование фильтрата осуществляется
через структуры гломерулярного фильтра (базальная мембрана, эндотелий сосуда, подоциты). Препятствует фильтрации электрический заряд, который покрывает фильтр и создается за счет полианиона – сиалогликопротеина.
Фильтрация зависит от:
Состояния гломерулярного фильтра;
Площади фильтрующей поверхности;
От эффективного фильтрационного давления (ЭФД).
ЭФД разница между гидростатическим давлением и суммой онкотического и внутрикапсулярного давления. ЭФД=КД- (ОД+ГД); КД-капиллярное давление, ОД- онкотическое давление крови, ГД – гидродинамическое давление мочи.
Слайд 5Нарушения клубочковой фильтрации
Снижение клубочковой фильтрации (< 70 мл в
мин) может происходить в результате воздействия внепочечных факторов снижения ОЦК:
сердечной недостаточности, гипотензивных состояний, шока, коллапса (клубочковая фильтрация прекращается при снижении уровня почечного кровотока < 50 мл/мин); воздействия патогенных факторов на сами почки: артериосклероз почек, некроз, хронический гломерулонефрит, сахарный диабет, амилоидоз и другие болезни, при которых уменьшается площадь клубочкового фильтра.
Увеличение объема клубочковой фильтрации результат возрастания эффективного фильтрационного давления при повышении тонуса выносящих артериол клубочков под влиянием катехоламинов, простагландинов, ангиотензина, вазопрессина.
К усилению клубочковой фильтрации приводит и ⇓ тонуса приносящих артериол клубочков (воздействие кининов, простагландинов), гипоонкия крови и увеличение проницаемости мембран клубочков под влиянием гистамина.
Слайд 6Снижение канальцевой реабсорбции
Причинами подавления активных механизмов реабсорбции часто являются генетические
энзимопатии, приводящие к цистин-, аминоацид-, или фосфатуриям, бикарбонатурии, почечному ацидозу.
Активные и пассивные механизмы реабсорбции могут нарушаться вследствие поражения эпителия канальцев при воспалении, аллергических реакциях, дистрофических процессах, интоксикациях. Это сопровождается нарушением реабсорбции Na+, К+, Са2+, Mg2+, глюкозы, лактата, аминокислот, хлоридов и др.
Слайд 7Изменения показателей диуреза
В норме суточный
диурез около 1,5 литра.
Полиурия при выделении за
сутки > 2–2,5 литров мочи. Анурия полное прекращение выделения мочи.
Для того чтобы определить, за счет какой из парциальных функций почек (фильтрации, реабсорбции, секреции, экскреции) произошло нарушение диуреза, используют методы, в основе которых лежит определение клиренса или коэффициента очищения плазмы крови от различных веществ (инулин выводится только путем фильтрации).
Слайд 8Изменения способности почек к разведению и концентрации мочи
Анализ по
Зимницкому: 8 порций мочи, взятой в течение суток через каждые
3 часа.
В норме колебания объема в каждой порции — от 50 до 200–300 мл, относительной плотности — не < 12–16 единиц между максимальным и минимальным показателем.
Низкие показатели относительной плотности (<1010) гипостенурия, а мало меняющаяся в течение суток относительная плотность изостенуриюя, что свидетельствует о нарушении концентрационной способности почек.
Низкая относительная плотность при резком ⇓ амплитуды ее колебаний в разных порциях мочи (1004–1008; 1006–1010) гипоизостенурия (свойственна поздней стадии ХПН и свидетельствует о тяжелых нарушениях концентрационной способности почек). Увеличение относительной плотности мочи > 1029 — гиперстенурия, встречается реже (следствие ↑ реабсорбции воды в канальцах).
Слайд 9Изменение ритма мочеиспускания
Частое мочеиспускание поллакиурия — сопровождает полиурию
или встречается при раздражении мочевыводящих путей (воспаление, конкременты), заболеваниях предстательной
железы.
При олигурии (↓ суточного количества мочи) редкое мочеиспускание (оллакиурия).
При преобладании ночного диуреза над дневным никтурия (энурез — ночное недержание мочи, чаще у детей). У взрослых никтурия → результат нарушения кровоснабжения почек, аденомы простаты, амилоидоза почек, цистита, уретрита сердечной недостаточности.
Слайд 10Изменения состава мочи
Практически при всех заболеваниях
почек и мочевыводящих путей в моче появляются отсутствующие в норме
компоненты: белок, эритроциты, лейкоциты, цилиндры.
Протеинурия в сочетании с гематурией, лейкоцитурией и цилиндрурией объединяются в понятие «мочевой синдром».
Слайд 11Протеинурия
Патологическая протеинурия — один из наиболее важных признаков
заболевания почек.
Главные факторы генеза ⇑ проницаемости клубочкового фильтра
(базальной мембраны) для белков плазмы и ⇓ канальцевой реабсорбции профильтровавшегося в первичную мочу белка.
Секреция белка клетками патологически измененного эпителия канальцев и выделение белка вследствие тубулорексиса (распада клеток канальцевого эпителия) играют второстепенную роль.
Слайд 12Внепочечная протеинурия
Преренальная протеинурия (переполнения) обусловлена действием на организм патогенных факторов
(охлаждение, длительная инсоляция), а также патологией (синдром размозжения, гемолиз, анафилаксия),
которая приводит к изменению концентрации белка в плазме, качества и количества белковых фракций, появлению патологических белков (Бенс–Джонса).
Постренальная протеинурия обусловлена выделением с мочой слизи и белкового экссудата при воспалении мочевыводящих путей.
Пре- и постренальная протеинурия встречаются относительно редко и бывают незначительными (до 1 г белка в сутки).
Слайд 13Гематурия
Это выделение с мочой эритроцитов.
Когда количество эритроцитов, выделяемых с мочой, в течение суток превышает
2х106.
В зависимости от интенсивности экскреции эритроцитов различают микрогематурию ( до 13 эритроцитов в поле зрения) и макрогематурию (моча цвета «мясных помоев», количество клеток в моче подсчету не поддается).
Для дифференцирования причины гематурии применяют «трехстаканную пробу». При одном мочеиспускании последовательно мочатся в три сосуда. Если кровь в первой порции источник скорее всего в мочеиспускательном канале, если в первой и второй в мочевом пузыре, а если во всех трех → либо поражены лоханки, либо сами почки.
Слайд 14Лейкоцитурия
Это экскреция с мочой лейкоцитов, количество которых превышает норму: при
микроскопии > 5-6 в поле зрения, при исследовании суточной мочи
— более 4 х 106 в сутки.
Лейкоцитурия может указывать на повреждение и почек и мочевыводящих путей. Если выявляется более 11–12 клеток в поле зрения пиурия.
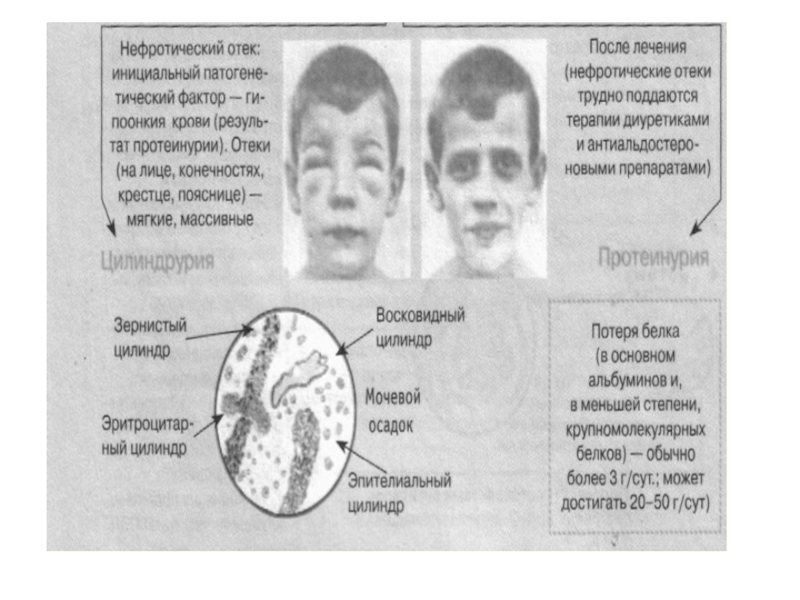
Слайд 15Цилиндрурия
Это экскреция с мочой цилиндров, которые представляют собой образующийся в
просвете канальцев слепок из белка и (или) клеток. В зависимости
от того, какие частицы и в каком количестве покрывают белковый слепок, различают гиалиновые (не адсорбировавшийся и свернувшийся белок), зернистые (измененные и некротизированные клетки эпителия проксимальных отделов канальцев), восковидные (погибшие клетки эпителия дистальных отделов канальцев), эритроцитарные, лейкоцитарные и жировые цилиндры.
Все цилиндры имеют исключительно почечный генез, так как они образуются только в почечных канальцах.
Слайд 16Экстраренальные признаки заболеваний почек
Относят так называемые общие нефрогенные синдромы:
отечный и тромбо-геморрагический, артериальную гипертензию, анемию, изменение показателей объема и
состава крови.
К последним двум принадлежат: гиперволемия, гиповолемия, азотемия (↑ концентрации небелкового или остаточного азота), гипопротеинемия, диспротеинемия, негазовый почечный ацидоз (из-за ограничения выведения кислых метаболитов, ↓ в почках интенсивности ацидогенеза, аммониогенеза).
Слайд 17Этиология и патогенез основных заболеваний почек
Все основные заболевания почек
объединяют в понятие нефропатии.
В зависимости от того, какой критерий
положен в основу дифференцировки разных видов патологии почек (морфологический, этиологический, патогенетический и др.), выделяют: нефропатии с преимущественным поражением тех или иных структур (гломерулопатии, тубулопатии), инфекционные (нефриты, пиелонефриты), паразитарные, иммуноаллергические, радиационные, лекарственные нефропатии; «сопутствующие» нефропатии, обусловленные коллагенозами, сахарным диабетом, амилоидозом, атеросклерозом, беременностью и др.
Слайд 19 Нефротический синдром – неспецифический клинико-лабораторный симптомокомплекс,
включающий массивную протеинурию, нарушения белкового, липидного и водно-солевого обменов, а
также – отеки разной локализации и выраженности, вплоть до анасарки (генерализованного отека подкожной клетчатки).
Слайд 20Нефротический синдром
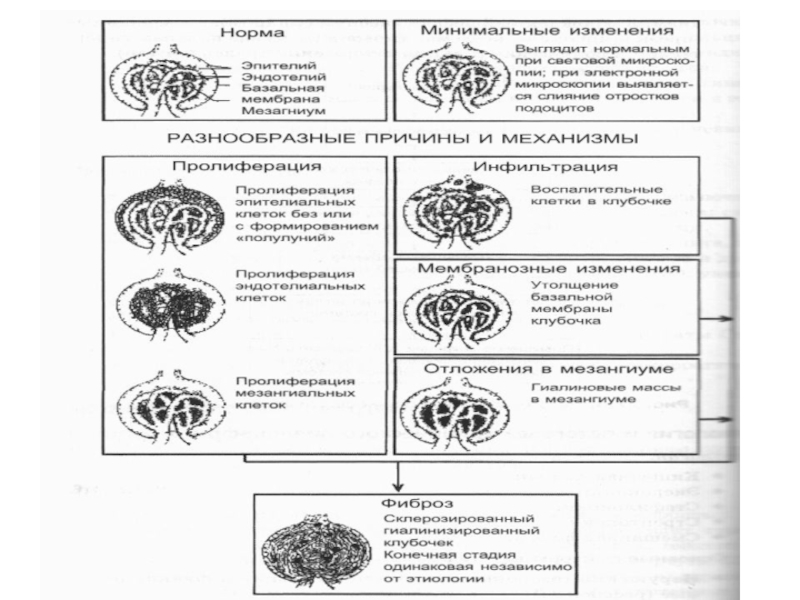
Ведущими морфологическими изменениями при нефротическом синдроме являются воспалительные изменения
в почечных клубочках (гломерулонефрит). Поражение канальцев развивается позже.
Нефротический синдром
проявляется массивной протеинурией (на 80–90 % за счет альбуминов), гипо- и диспротеинемией (коэф. альбумины/глобулины ⇓), гиперлипидемией и отеками.
Является единой «маской» многих, очень не схожих между собой, принципиально различающихся заболеваний: поражения клубочков (гломерулонефриты), метаболические расстройства (сахарный диабет, амилоидоз), серповидно-клеточная анемия, лекарственные поражения и др.
Различают первичный (результат первичного поражения почек, в 80% случаев — гломерулонефрит) и вторичный (сопровождает многие заболевания) нефротический синдром.
Слайд 21Патогенез нефротического синдрома
Одним из начальных звеньев патогенеза синдрома является образование
в крови иммунных комплексов (ИК) в результате взаимодействия антител с
антигенами как экзогенного (бактериальные, вирусные, пищевые и др.), так и эндогенного происхождения с участием комплемента сыворотки. В других ситуациях ИК образуются вследствие реакции, в которую вступают поврежденные компоненты базальных мембран клубочковых капилляров и вырабатывающиеся к ним АТ. Осаждаясь на базальной мембране клубочков, либо образуясь непосредственно на них, ИК повреждают базальные мембраны.
Аутоаллергические механизмы активируют гуморальные и клеточные звенья воспалительной реакции с освобождением медиаторов и модуляторов воспаления, что приводит к ⇑ проницаемости базальных мембран, нарушению микроциркуляции в клубочковых капиллярах.
Слайд 23Нефриты
К нефритам относится группа нефропатий, характеризующаяся двусторонним диффузным
поражением почечной ткани воспалительного или иммуно-воспалительного генеза с вовлечением в
патологический процесс всех отделов нефрона, интерстициальной ткани, почечных сосудов.
Слайд 24Острый диффузный гломерулонефрит (ОДГ)
Причиной ОДГ является
чаще всего β-гемолитический стрептококк (12-го типа группы А). Для него
характерна высокая способность к поражению базальной мембраны клубочков.
Гломерулонефрит своеобразная мембранная патология. Антитела, образующиеся против стрептококка, взаимодействуют не только с ним, но и с белками базальных мембран клубочков, имеющих сходные со стрептококком антигены ►► повреждение белков и других компонентов мембран, которые после подобных изменений становятся аутоантигенами.
Другие механизмы, приводящие к образованию почечных аутоантигенов: 1) прямое воздействие токсинов стрептококка на базальные мембраны; 2) воздействие на почки ИК, образующихся в крови вследствие связывания антител с внепочечными и внеклубочковыми антигенами (при участии комплемента С3). ИК фиксируются на базальных мембранах клубочковых капилляров либо в мезангии нарушение микроциркуляции с развитием микротромбозов и микронекрозов в структурах клубочка.
существенную роль в патогенезе играет нарушение почечной гемодинамики, микроциркуляции и реологических свойств крови

Слайд 25Хронический диффузный гломерулонефрит (ХДГ)
Это тоже воспалительное заболевание почек иммунопатологического генеза
с преимущественным поражением почечных клубочков. У 10–20 % пациентов ХДГ является
исходом острого гломерулонефрита, а у 80–90 % — самостоятельным заболеванием с вялым, клинически слабо выраженным, «скрытым» течением.
Когда ХДГ следствие острого гломерулонефрита, причины развития патологии те же, что при ОДГ. При возникновении первично хронического ДГ очень важны обострения очаговой стрептококковой и иной инфекции, повторные охлаждения, неблагоприятные условия труда и быта, злоупотребление алкоголем, травмы.
Слайд 26Пиелонефриты
Острый или хронический пиелонефриты неспецифическое инфекционное воспаление слизистой лоханок,
чашечек и паренхимы почек.
Возбудителями чаще являются бактерии, главным образом
кишечная палочка, реже — энтерококки, стрептококки, протей. Не исключается возможность участия вирусной инфекции. Источниками инфекции могут быть: кариес зубов, фурункулез, тонзиллит, холецистит, мастит, остеомиелит, уретрит и др.
Проникновение инфекции в почки возможно нисходящим (гематогенным и лимфогенным) либо восходящим (урогенным) путем.
В механизме проникновении инфекции из лоханок в почечную ткань важным предрасполагающим фактором являются нарушения уродинамики и уростаз, которые возникают при атонии или стриктуре мочеточников, конкрементах в мочевых путях, аденоме простаты.
Слайд 27Почечно- каменная болезнь
Образованию конкрементов способствуют:
1) ↓концентрации в моче, во-первых, солюбилизаторов (веществ, поддерживающих соли
мочи в растворенном состоянии — мочевина, креатинин, цитраты), во-вторых, ингибиторов кристаллизации солей (неорганический пирофосфат) и, в-третьих, комплексообразователей (ионов Mg, цитратов);
2) ↑ содержания в моче так называемых «нуклеаторов», веществ, инициирующих кристаллизацию солей в моче (коллаген, эластин, мукопротеины, сульфаниламиды);
3) сдвиги рН мочи (при рН около 5 образуются в основном ураты; при рН >7 — фосфаты кальция и т.п.);
4) ↑ в моче содержания камнеобразующих солей (кальциевых);
5) затруднение оттока мочи.
Слайд 28Механизм образования камней
Механизм образования камней объясняется двумя теориями: кристаллизационной (а)
и коллоидной (б).
А образование камней начинается с процесса кристаллизации
солей, в ходе которой в состав камня включаются и органические компоненты (фибрин, коллаген, клеточный детрит).
Б вначале образуется органическая матрица, на которой уже впоследствии кристаллизуются соли.
Слайд 29Острая почечная недостаточность
ОПН — это синдром, развивающийся в
результате быстрого снижения или прекращения функции почек, в первую очередь
экскреторной.
В зависимости от того, какой фактор вызвал ОПН, последнюю подразделяют на преренальную, ренальную и постренальную.
В процессе развития эти формы трансформируются в ренальную форму ОПН.
Слайд 30Патогенез ОПН
Главными причинами преренальной ОПН являются шок и коллапс различной
этиологии, массивная кровопотеря, сердечная недостаточность, тромбоз почечной артерии, нарушения водно-электролитного
баланса (неукротимая рвота, длительная диарея, декомпенсированный стеноз привратника и др.).
Эти состояния обусловливают развитие выраженной ишемии почек, и, несмотря на то, что функции самих почек на начальных этапах ОПН остаются сохраненными, они не могут реализоваться из-за значительного ↓величины почечного кровотока.
Слайд 31Патогенез ОПН
Наиболее частая причина возникновения ренальных форм ОПН —
прямое повреждающее действие на почки нефротоксических веществ (CCL4, тяжелые металлы,
антибиотики, сульфаниламиды, органические растворители). Возможно как непосредственное их токсическое действие на эпителий канальцев (концентрация веществ в моче больше, чем в крови), так и влияние с помощью других механизмов (обструкция почечных канальцев уратами или участие аллергических компонентов).
К этой форме ОПН относят и случаи ее возникновения на фоне собственно почечной патологии (гломерулонефрит, пиелонефрит, волчаночный нефрит и др.).
Слайд 32Постренальная почечная недостаточность развивается вследствие нарушения оттока мочи различного генеза
(камни, опухоли, сгустки крови, воспалительный отек, сдавление маткой при беременности…)
Слайд 33Патогенез ОПН
Главное звено патогенеза ОПН нарушение почечного кровотока, сопровождающееся
значительным снижением объема клубочковой фильтрации.
Важны: критическое ↓ системного АД
(до 40–60 мм рт. ст.) и шунтирование почечного кровотока, вазоконстрикция почечных артериол как реакция на артериальную гипотонию, микротромбозы и агрегация клеток крови в микрососудах почек (особенно при сепсисе, травматическом и геморрагическом шоке). В происхождении артериальной констрикции существенная роль принадлежит серотонину, гистамину, простагландинам и катехоламинам.
Дополнительные факторы патогенеза сужение просвета канальцев в результате накопления в поврежденных клетках ионов кальция, отека и набухания эпителия, закрытие канальцев клеточным детритом или цилиндрами.
Слайд 34Дифдиагностика форм ОПН
Для преренальной характерны: гипонатрийурия, ⇓мочевины и креатинина мочи.
Для ренальной ОПН: гипернатрийурия, рост мочевины, креатинина и осмолярности мочи:
С
целью дифдиагностики производят также расчет индекса экскретируемой фракции натрия.
Na+мочи: Na+крови
Naэкс = ----------------------------
Cr мочи: Cr крови
где Cr — креатинин.
Для преренальной ОПН индекс экскретируемой фракции натрия < 1, при остром канальцевом некрозе — > 1.
Слайд 35Хроническая почечная недостаточность
ХПН — это неизбежный исход многих неизлеченных хронических
заболеваний почек, представляющий собой синдром, развивающийся как результат прогрессирующей гибели
и уменьшения количества функционирующих нефронов. !!Клинические проявления начинаются при снижении числа функционирующих нефронов до 30 %.
Причины ХПН преренальные (хронические АГ, медленно прогрессирующий стеноз почечных артерий), ренальные (неизлеченные гломерулонефриты, пиелонефриты, тубулопатии и др.) и постренальные (длительная обструкция мочевыводящих путей).
При ХПН происходит постепенное ↓ количества действующих нефронов► постепенно прогрессирует фибропластический процесс, атрофия канальцев и практически полное отсутствие регенерации. Как следствие → нарушение всех механизмов мочеобразования.
Слайд 36 Обычно медленно прогрессирующее течение ХПН. Обостряют развитие
интеркуррентные инфекции (грипп, отит, пневмония и др.) и обострение основного
процесса в почках.
Характерный признак обострения ХПН !! быстрое развитие уремической интоксикации (нарастание азотемии, снижение диуреза, нарушения КОС и др.).
Особенность ХПН вплоть до развития уремии у больных сохраняется достаточный диурез или даже полиурия (остающийся интактный нефрон компенсаторно выводит большее, чем в норме, количество осмотически активных веществ). Вместе с этими веществами в первичной моче ↑ содержание воды, что в совокупности с атрофическими изменениями в канальцах приводит к ↓ канальцевой реабсорбции и прогрессирующему падению концентрационной способности почек.→ Моча выделяется с монотонно низкой относительной плотностью, изотоничной плазме (около 1011) гипоизостенурия.
!! Олигурия развивается в терминальной стадии ХПН
Слайд 37 Уремия (мочекровие) - синдром аутоинтоксикации организма продуктами обмена веществ
и экзогенными соединениями, в норме выводящимися почками. Непосредственные причины развития
ОПН или ХПН.
Уремия часто приводит к почечной коме (характеризуется угнетением функции ЦНС).
Слайд 38Патогенетические механизмы интоксикации при уремии
Гиперазотемия (накопление в крови мочевины, мочевой
кислоты, креатинина! – это критерий тяжести);
Токсическое действие продуктов обмена ароматических
аминокислот: фенолов, индолов, скатолов;
Токсическое действие веществ с молекулярной массой 200–2000, которые принято называть «средними молекулами»;
Повреждение упомянутыми продуктами метаболизма мембран и ферментных систем клеток;
Нарушение кислотно-основного состояния (ацидоз);
Дисбаланс жидкости и ионов в клетках (↑в крови содержания калия и магния, ↓ кальция);
Гипергидратация и гипоксия головного мозга;
Нарушение электрофизиологических процессов в ткани мозга и сердца (лежит в основе потери сознания, расстройств ССС, дыхания и НС).