Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ph ВОДЫ
Содержание
- 1. Ph ВОДЫ
- 2. Слайд 2
- 3. Ионная формула (заряженные, электро- и хемо
- 4. Слайд 4
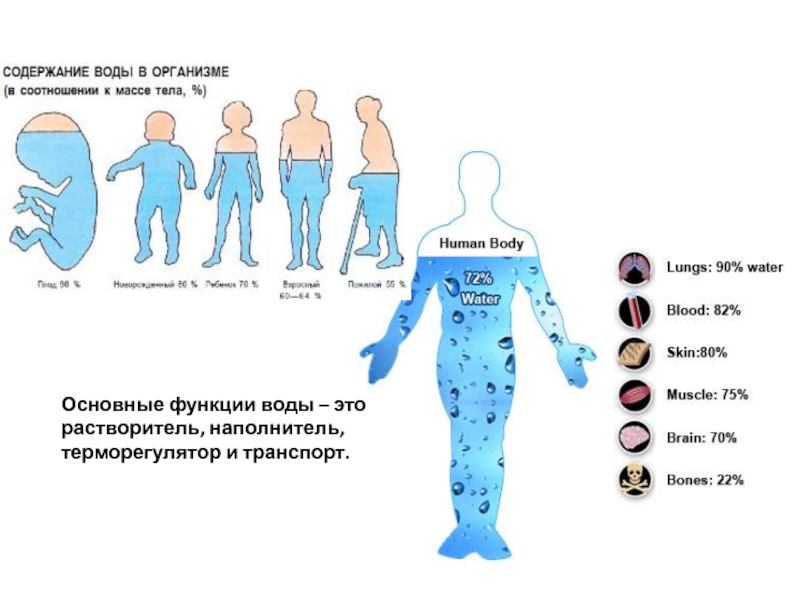
- 5. Основные функции воды – это растворитель, наполнитель, терморегулятор и транспорт.
- 6. Слайд 6
- 7. Слайд 7
- 8. Слайд 8
- 9. Слайд 9
- 10. Слайд 10
- 11. Определение PhВодоро́дный показа́тель, pH (лат. potentia hydrogeni
- 12. Уровень Ph определяет термодинамическую активность гидроксоний-ионов.В чистой
- 13. Существуют данные всемирной организации здравоохранения, определяющие показания
- 14. В современном мире существует несколько стандартов, предъявляемых
- 15. Карта воды России http://www.watermap.ru/map
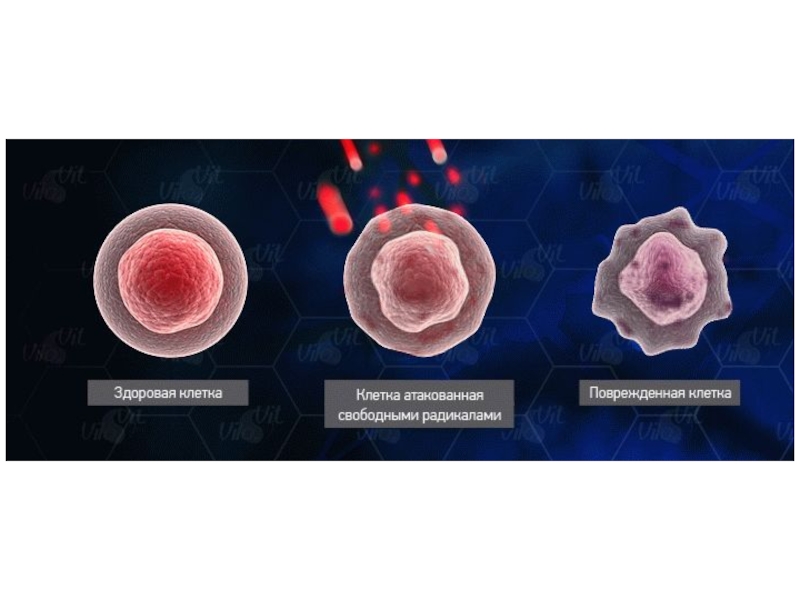
- 16. Свободные радикалы Функции контролируемых свободных радикалов:• Разрушение вирусов
- 17. Причины появления свободных радикалов: Ультрафиолетовое излучение –
- 18. Возможные последствия свободных радикалов: • Болезнь Альцгеймера;• Появления морщин
- 19. Наиболее доступные антиоксиданты:• альфа-липоевая кислота,• Витамин A, E, C
- 20. Слайд 20
- 21. Слайд 21
- 22. Слайд 22
- 23. Скачать презентанцию
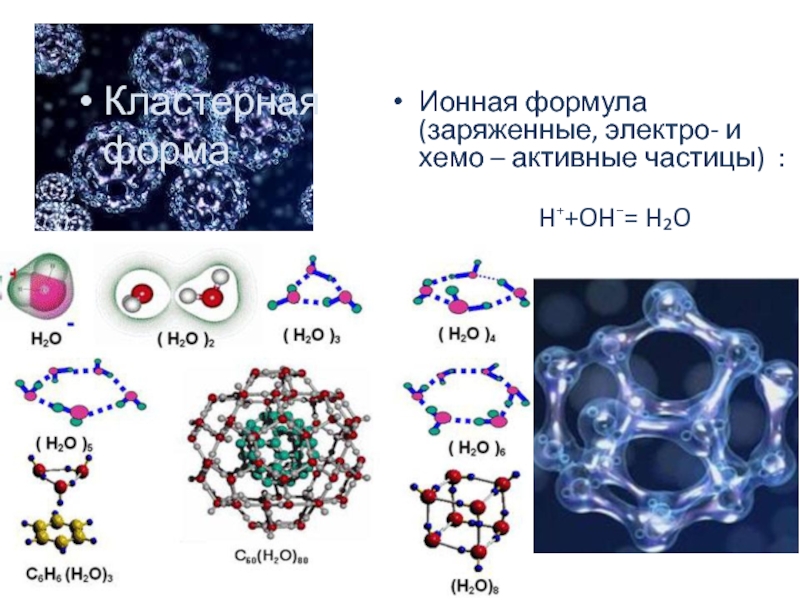
Ионная формула (заряженные, электро- и хемо – активные частицы) : H⁺+OH⁻= H₂O Кластерная форма
Слайды и текст этой презентации
Слайд 1Ph ВОДЫ
Презентацию подготовила Трофименко Елена ,
октябрь 2017
для сотрудников Crystal
Spa&Lounge
Слайд 3Ионная формула (заряженные, электро- и хемо – активные частицы) :
Кластерная форма
Слайд 11Определение Ph
Водоро́дный показа́тель, pH (лат. potentia hydrogeni — сила водорода,
или pondus hydrogeni — вес водорода, произносится «пэ-аш» в старой
традиции и «пи-эйч» в соответствии с нормами английского языка) — мера активности (в очень разбавленных растворах она эквивалентна концентрации) ионов водорода в растворе, количественно выражающая его кислотность. Равен по модулю и противоположен по знаку десятичному логарифму активности водородных ионов, выраженной в молях на один литр:pH=-lg [H+]
Это понятие было введено в 1909 году датским химиком Сёренсеном.
Слайд 12Уровень Ph определяет термодинамическую активность гидроксоний-ионов.
В чистой воде при 22
°C концентрации ионов водорода ([H+]) и гидроксид-ионов ([OH−]) одинаковы и
составляют 10−7 моль/л, это напрямую следует из определенияионного произведения воды, которое равно [H+] · [OH−] и составляет 10−14 моль²/л² (при 25 °C).Слайд 13Существуют данные всемирной организации здравоохранения, определяющие показания ph
pH
воды;
pH 3-5 - кислые воды;
pH 5-6,5 - слабокислые воды;
pH 6,5-7,5
- нейтральная вода;pH 7,5-8,5 - слабощелочная вода;
pH 8,5-9,5 - щелочная вода;
pH>9,5 - сильнощелочная вода.
Наиболее оптимальным значением уровня pH для питьевой воды является значение в диапазоне от 6 до 9
Слайд 14В современном мире существует несколько стандартов, предъявляемых к чистой питьевой
воде:
Санитарные Правила и Нормы Российской Федерации (СанПиН РФ);
Стандарт Всемирной Организации
Здравоохранения (ВОЗ);Стандарт Стран Европейского Союза.
В соответствии с указанными выше стандартами, чистой питьевой водой признается вода, с pH от 7 до 7,5 ммоль/л и жесткостью не более 7 ммоль/л, суммарное количество полезных минералов в которой не более 1 г/л, вредные химические примеси не превышают предельно допустимых концентраций, а болезнетворные бактерии и вирусы отсутствуют.
Слайд 16Свободные радикалы
Функции контролируемых свободных радикалов:
• Разрушение вирусов и бактерий;
• Активизация необходимых ферментов;
• Производство
важнейших гормонов;
• Производство энергии и нужных человеку субстанций.
Примером контролируемых свободных радикалов
является коллоидное сереброСлайд 17Причины появления свободных радикалов:
Ультрафиолетовое излучение – УФ-лучи лишают молекулы электронов,
разрушают мембраны клеток и их составляющие.
Побочные эффекты, передозировка лекарственных средств
– молекулы химических соединений препаратов вступают в реакции и ферментативные превращения, превращаются в свободные радикалы.Курение – никотин и образующиеся при этом смолы запускают реакции окисления.
Нарушенное экологическое равновесие – химически соединения из продуктов, выхлопных газов, бытовой химии попадают в организм человека и запускают реакции окисления.
Негативное действие стресса – гормоны стресса (адреналин, кортизол) нарушают дыхание и питание клетки, делая ее мишенью для свободных радикалов.
Слайд 18Возможные последствия свободных радикалов:
• Болезнь Альцгеймера;
• Появления морщин и пигментных пятен;
• Воспалительные изменения
в суставах;
• Заболевания сердца и сосудов;
• Ослабление мышц, поддерживающих скелет;
• Потеря эластичности кожи;
• Снижение
зрения и слуха;• Возрастные психические процессы;
• Рак.
Слайд 19Наиболее доступные антиоксиданты:
• альфа-липоевая кислота,
• Витамин A, E, C и бетта-каротин (любые
овощи и фрукты)
• Цистеин
• Цинк (рекордсменом по содержанию цинка являются тыквенные семечки)
• Флавоноиды
(рекордсменами по содержанию флавоноидов являются ягоды, особенно темного цвета)• Глутатион (данный антиоксидант вырабатывается самим организмом)
• Гинкго Билоба




![Ph ВОДЫ Уровень Ph определяет термодинамическую активность гидроксоний-ионов.В чистой воде при 22 °C Уровень Ph определяет термодинамическую активность гидроксоний-ионов.В чистой воде при 22 °C концентрации ионов водорода ([H+]) и гидроксид-ионов](/img/thumbs/af71e3d19b5401bdcdf7601b662a5e82-800x.jpg)