Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Понятие об иммунитете и его видах. Факторы врожденного иммунитета
Содержание
- 1. Понятие об иммунитете и его видах. Факторы врожденного иммунитета
- 2. Этапы развития иммунологии1. Период протоиммунологии (от античного
- 3. 3. Развитие иммунологии до середины XX века
- 4. Эдуард Дженнер прививка человеку коровьей оспыЛуи Пастерпринцип получения живых вакцинОсновоположники иммунологии
- 5. Илья Ильич Мечниковклеточная теория иммунитета Пауль Эрлихгипотеза об антителах
- 6. Габричевский Георгий Норбертоич описал явления хемотаксиса лейкоцитовЗдродовскийПавел Феликсовичобосновал физиологическое направление в иммунологии
- 7. Н. А. Гайский вакцины против чумы, туляремииЛев Зильбериммунология рака
- 8. Чумаков Михаил Петровичвакцина против полиомиелита, кори, гриппа, паротитаСмородинцевАнатолий Александрович
- 9. Иммунитет- это способ защиты живых многоклеточных организмов
- 10. Основные источники экзогенной агрессии (проникающие из внешней
- 11. При формировании иммунного ответа наблюдается последовательная триада
- 12. Классификация видов иммунитета по этиологической направленностипротивоопухолевыйантиинфекционныйтрансплантационныйантибактериальныйантитоксическийантивирусныйантигрибковыйантипротозойныйантигельминтный
- 13. Классификация видов иммунитета по локализацииКлассификация видов иммунитета по происхождениюместныйгенерализованныйврожденныйадаптивныйПо способу формированияПо условиям формированияактивныйпассивныйестественныйискусственный
- 14. Адаптивный иммунитетЕстественныйИскусственныйАктивный (постинфекционный, коллективный)Пассивный (передача антител через плаценту, с молоком матери)Активный (поствакцинальный)Пассивный (введение иммунных сывороток, иммуноглобулинов)
- 15. 1. PAMP -образы патогенности, или патогенассоциированныемолекулярные паттерны(Pathogen-associated molecular patterns)2. Антигены3. Стрессорные молекулы и образцы oпасности (DAMP)
- 16. PAMP -группы молекул, отсутствующие в организме
- 17. Антигены ―высокомолекулярные соединения, способные специфически стимулировать иммунокомпетентные
- 18. Рецепторы клеток организма, распознающие мишени иммунитетапаттернраспознающие рецепторымиелоидных
- 19. Классификация патогенраспознающих рецепторов по функциям1. эндоцитозные -
- 20. Врожденный иммунитет —наследственно закрепленная система защиты, объектом
- 21. Клетки врожденного иммунитета1. клетки миелоидного ряда (сегментоядерные
- 22. Нейтрофилы- созревают в костном мозге, после чего
- 23. Эозинофилыгранулярные сегментоядерные лейкоциты крови (0,5-2,0%), после циркуляции
- 24. Базофилы и тучные клетки (мастоциты)Имеют сегментированное
- 25. Дендритные клетки (ДК)Клетки, преимущественно миелоидного ряда,
- 26. Моноциты и макрофаги Моноциты – циркулирующие в
- 27. Основные функции моноцитов/макрофагов:распознавание всех видов PAMP,фаго- и
- 28. Естественные, или нормальные, киллерыбольшие гранулярные лимфоциты; отделяются
- 29. Основные типы рецепторов и других молекул, представленных
- 30. Основные эффекторные механизмы врожденного иммунитета реализуемые клетками1. фагоцитоз (внутриклеточный киллинг)2. контактный цитолиз клеток-мишеней3. внеклеточный цитолиз
- 31. ФагоцитозЭто захват и поглощение специализированными клетками организма
- 32. Стадии фагоцитозаХемотаксис,Адгезия,Активация мембраны,Погружение,Образование фагосомы,Образование фаголизосомы,Киллинг и переваривание,Выброс продуктов деградации
- 33. АдгезияОпсонизация- это «обволакивание» объекта белками-опсонинами (С3в-компонентом
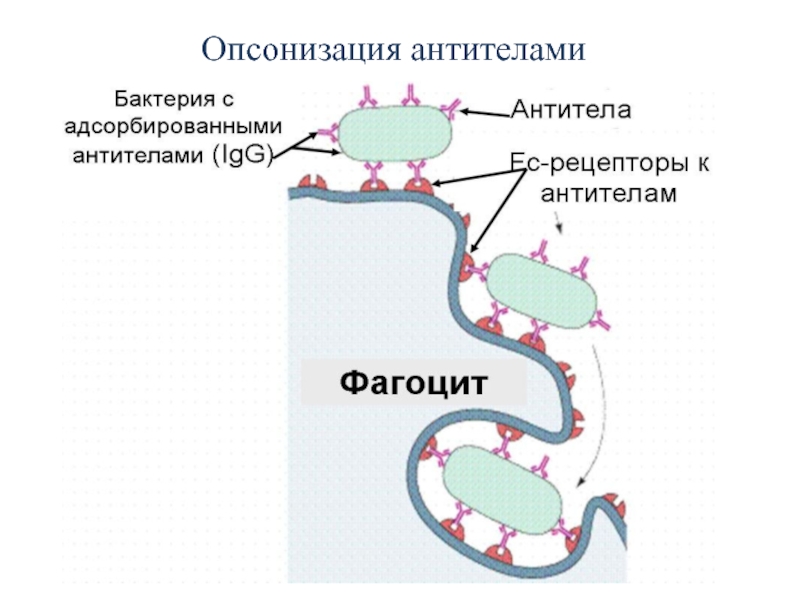
- 34. Опсонизация антителами
- 35. ФагоцитозНезавершенный при котором не происходит разрушение патогена
- 36. Гуморальные факторы врожденного иммунитетаСистема комплементаЦитокиновая сетьНормальные антителаБактерицидные
- 37. Система комплемента – это многокомпонентная самособирающаяся система
- 38. Фазы активации комплемента1. Запуск активации (участвуют факторы
- 39. Классический путь1. Активатор – иммунный комплекс Аг-Ат,
- 40. Лектиновый путь1. Распознавание углеводов на поверхности микробной
- 41. Альтернативный путь 1. Гидролиз C3 на поверхности
- 42. 3.9.14
- 43. Биологические эффекты комплемента1. Лизис клеток (все пути
- 44. ЦитокиныЭто система низкомолекулярных белков организма, синтезируемых преимущественно
- 45. Классификация цитокиновУчаствующие в развитии воспаления(провоспалительные): ИЛ-1, ФНО,
- 46. Структурно-функциональные семейства цитокинов1. интерфероны типа I —
- 47. Свойства цитокиновОтсутствие специфичности в отношении антигенов,Функционирование по
- 48. Результат активации гуморальных и клеточных факторов врожденного
- 49. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Этапы развития иммунологии
1. Период протоиммунологии (от античного периода до 80-х
годов XIX века) – связан со стихийным, эмпирическим познанием защитных
реакций организма.2. Период зарождения экспериментальной и теоретической иммунологии (с 80-х годов XIX века до второго десятилетия XX века) – выделение иммунологии в самостоятельную науку, завершение формирования классической (инфекционной) иммунологии.
Слайд 33. Развитие иммунологии до середины XX века — описание новых
иммунологических феноменов, развитие инфекционной иммунологии
4. «Новая иммунология» 50-80-х годов
XX века — отличался доминированием неинфекционного клеточного направления.5. Современный этап — характерно широкое использование молекулярно-биологических методов и технологий
Этапы развития иммунологии
Слайд 4Эдуард Дженнер
прививка человеку коровьей оспы
Луи Пастер
принцип получения живых вакцин
Основоположники иммунологии
Слайд 6Габричевский
Георгий Норбертоич
описал явления хемотаксиса лейкоцитов
Здродовский
Павел Феликсович
обосновал физиологическое
направление в иммунологии
Слайд 8Чумаков
Михаил Петрович
вакцина против полиомиелита,
кори, гриппа, паротита
Смородинцев
Анатолий
Александрович
Слайд 9Иммунитет
- это способ защиты живых
многоклеточных организмов от потенциально
опасных клеток
и молекул, необходимый для
поддержания клеточного гомеостаза.
Врожденного
иммунитета
Адаптивного
(приобретенного)
иммунитета
Обеспечивается факторами
Слайд 10Основные источники экзогенной агрессии
(проникающие из внешней среды):
1. микроорганизмы
2.
высокомолекулярные продукты биологического происхождения (яды животных, токсины бактерий)
3. аллергены
Основные источники
эндогенной агрессии (видоизмененные клетки и молекулы собственного организма):
1. опухолевые клетки
2. клетки, инфицированные внутриклеточными паразитами (вирусами, внутриклеточными бактериями)
3. некротизированные и апоптотические клетки
Слайд 11При формировании иммунного ответа наблюдается последовательная
триада реакций:
1. распознавание потенциально
опасных объектов экзогенного и эндогенного происхождения
2. их элиминация
3. запоминание информации
о контакте с ними (формирование иммунологической памяти)Слайд 12Классификация видов иммунитета по этиологической направленности
противоопухолевый
антиинфекционный
трансплантационный
антибактериальный
антитоксический
антивирусный
антигрибковый
антипротозойный
антигельминтный
Слайд 13Классификация видов иммунитета по локализации
Классификация видов иммунитета по происхождению
местный
генерализованный
врожденный
адаптивный
По способу
формирования
По условиям формирования
активный
пассивный
естественный
искусственный
Слайд 14Адаптивный иммунитет
Естественный
Искусственный
Активный (постинфекционный, коллективный)
Пассивный
(передача антител через плаценту, с молоком
матери)
Активный (поствакцинальный)
Пассивный
(введение иммунных сывороток, иммуноглобулинов)
Слайд 151. PAMP -
образы патогенности, или патогенассоциированные
молекулярные паттерны
(Pathogen-associated molecular patterns)
2. Антигены
3.
Стрессорные молекулы и образцы
oпасности (DAMP)
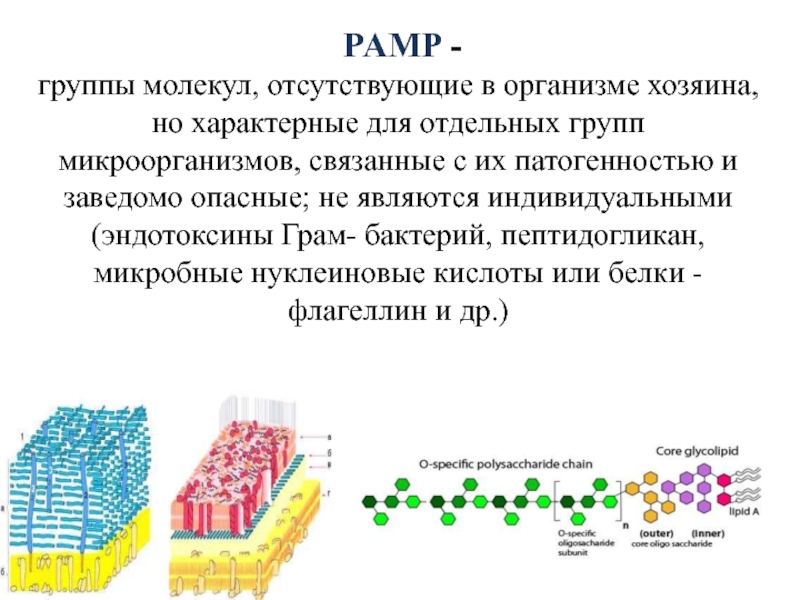
Слайд 16 PAMP -
группы молекул, отсутствующие в организме хозяина, но характерные
для отдельных групп микроорганизмов, связанные с их патогенностью и заведомо
опасные; не являются индивидуальными (эндотоксины Грам- бактерий, пептидогликан, микробные нуклеиновые кислоты или белки - флагеллин и др.)Слайд 17Антигены ―
высокомолекулярные соединения, способные специфически стимулировать иммунокомпетентные лимфоидные клетки и
обеспечивать тем самым развитие иммунного ответа
Стрессорные молекулы и образцы опасности
(DAMP) ―собственные молекулы организма на мембранах клеток, сигнализирующие преимущественно об опасности эндогенного происхождения (трансформации, повреждении, клеточном стрессе)
Слайд 18Рецепторы клеток организма, распознающие мишени иммунитета
паттернраспознающие рецепторы
миелоидных и др. клеток
врожд.иммунитета
антигенраспознающие рецепторы
(на Т- и В-лимфоцитах)
Рецепторы, распознающие стрессорные молекулы
(представлены в основном
на NK-клетках)Слайд 19Классификация патогенраспознающих рецепторов по функциям
1. эндоцитозные - опосредуют поглощение и
доставку патогена к лизосомам, где впоследствии происходит его разрушение с
образованием антигенных детерминант; запускают классический иммунный ответ:а). маннозные;
б). scavenger-рецепторы
2. сигнальные - системы «оповещения о несанкционированном прорыве» любого микроорганизма внутрь клетки или «побега» его из фаголизосомы:
а). Toll-подобные рецепторы;
б). NOD-рецепторы
Слайд 20Врожденный иммунитет —
наследственно закрепленная система защиты, объектом распознавания для которой
являются PAMP и DAMP, формирующаяся в онтогенезе постоянно, вне зависимости
от «запроса»(возникла эволюционно раньше адаптивного):
а). формируется в период внутриутробного развития организма;
б). предсуществует в организме всегда, независимо от наличия/ отсутствия биологической агрессии;
в). популяция клеток реагирует как единое целое, при этом клетки не образуют клонов;
г). обеспечивает распознавание и элиминацию объектов в первые несколько минут или часов после их обнаружения;
д). характерно вовлечение в процесс клеток других систем организма
е). не формируется иммунологической памяти
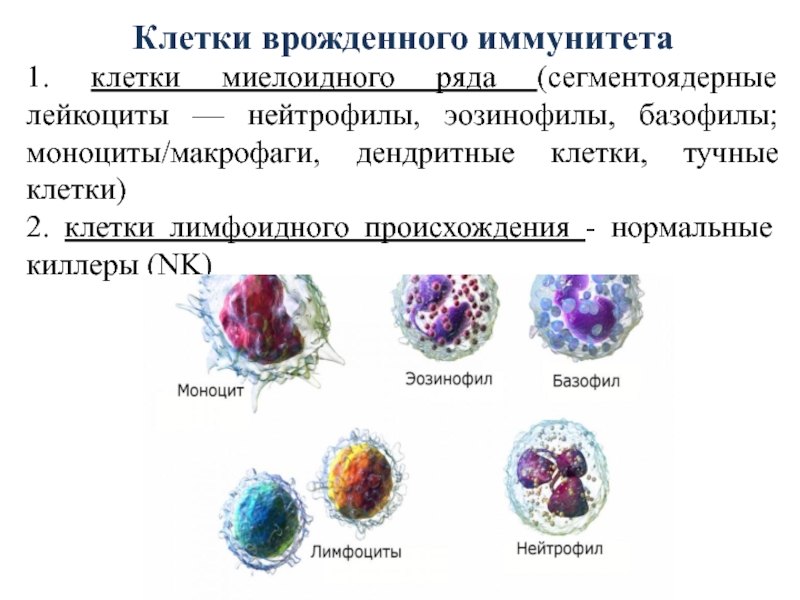
Слайд 21Клетки врожденного иммунитета
1. клетки миелоидного ряда (сегментоядерные лейкоциты — нейтрофилы,
эозинофилы, базофилы; моноциты/макрофаги, дендритные клетки, тучные клетки)
2. клетки лимфоидного происхождения
- нормальные киллеры (NK)Слайд 22Нейтрофилы
- созревают в костном мозге, после чего 70% депонируется на
его территории, остальные выходят в кровоток;
- это наиболее многочисленная (50-70%)
фракция лейкоцитов периферической крови, имеют 4 типа гранул;- очень мобильны, под действием хемокинов экстренно мигрируют из кровотока в очаг тканевого воспаления;
короткоживущие клетки, погибающие после миграции в ткань в течение 3-5 суток в результате апоптоза.
Основные функции
1. фагоцитоз с молниеносным запуском внутриклеточного переваривания и наиболее выраженной его интенсивностью
2. секреция цитокинов
3. внеклеточный киллинг клеток-мишеней при дегрануляции
Слайд 23Эозинофилы
гранулярные сегментоядерные лейкоциты крови (0,5-2,0%), после циркуляции в крови мигрирует
в ткани, преимущественно пищеварительного тракта.
Основные функции
уничтожение многоклеточных паразитов (гельминтов, мелких
эукариотов) путем внеклеточного цитолиза;2. разрушение вирусной РНК за счет фермента РНК-азы;
3. секреция цитокинов
4.обладают слабой фагоцитарной активностью
Слайд 24Базофилы и тучные
клетки (мастоциты)
Имеют сегментированное ядро, базофильные гранулы и
дополнительные этапы созревания после костного мозга в селезенке и др.
органах.Базофилы являются клетками крови, но быстро мигрируют в ткани; мастоциты — тканевые клетки.
Основные функции — участие в формировании:
1. воспаления
2. реакций аллергической гиперчувствительности
3. защиты от многоклеточных паразитов (внеклеточный цитолиз)
Слайд 25Дендритные
клетки (ДК)
Клетки, преимущественно миелоидного ряда, малая часть — лимфоидного.
Имеют
характерную отростчатую форму.
Незрелые ДК мигрируют из кровотока в барьерные
тканиСозревают при перемещении их из барьерных тканей в лимфу, далее в Т-зоны лимфоузлов.
Зрелые миелоидные ДК заселяют селезенку, брыжеечные лимфоузлы, лимфоузлы кожи; лимфоидные ДК - тимус.
Основная функция:
Распознавание PAMP и презентация
антигенов Т-лимфоцитам
Слайд 26Моноциты и макрофаги
Моноциты – циркулирующие в крови клетки, при
миграции в ткань трансформируются в макрофаги и дендритные клетки.
Разновидности макрофагов:
1.
резидентные (возникают при спонтанной миграции практически во все ткани, имеют различия в морфологии и названии в зависимости от типа ткани);2. воспалительные (формируются при экстренной миграции в очаг воспаления)
Продолжительность жизни – 40-60 суток
Слайд 27Основные функции моноцитов/макрофагов:
распознавание всех видов PAMP,
фаго- и пиноцитоз клеток-мишеней и
клеточных фрагментов с последующим
внутриклеточным киллингом,секреция широкого спектра цитокинов (семейства
ИЛ-1 и провоспалительных), гормонов,
компонентов комплемента, белков межклеточного
матрикса и др. (иммунорегуляция)
процессинг и представление антигенов Т-лимфоцитам
Слайд 28Естественные, или нормальные, киллеры
большие гранулярные лимфоциты; отделяются в костном мозге
от Т-клеточной линии; мигрируют в периферические лимфоидные органы.
не имеют
антигенраспознающих рецепторов.компоненты гранул: перфорины, гранзимы, гранулолизин
распознают эндогенные стрессорные молекулы, появляющиеся на клетках-мишенях собственного организма при их трансформации, инфицировании вирусами, при клеточном стрессе и др.
Механизм уничтожения клеток-мишеней
— контактный цитолиз.
Основные маркеры: CD56, CD16
Слайд 29Основные типы рецепторов и других молекул, представленных на клетках врожденного
иммунитета:
1. рецепторы , распознающие PAMP и DAMP
2. рецепторы к цитокинам,
факторам комплемента,Fc-фрагменту иммуноглобулинов
3. молекулы главного комплекса гистосовместимости I класса, а на антигенпредставляющих клетках - I и II классов
4. СD-антигены, набор и сочетание которых специфичен для каждой популяции и субпопуляции клеток
Слайд 30Основные эффекторные механизмы врожденного иммунитета реализуемые клетками
1. фагоцитоз (внутриклеточный киллинг)
2.
контактный цитолиз клеток-мишеней
3. внеклеточный цитолиз
Слайд 31Фагоцитоз
Это захват и поглощение специализированными клетками организма корпускулярных частиц размером
не менее 0,5 мкм.
Клетки, обладающие фагоцитарной активностью:
1. «Профессиональные» фагоциты
– Нф и Мн/Мф,2. Прочие клетки – эозинофилы, базофилы, тучные и дендритные клетки.
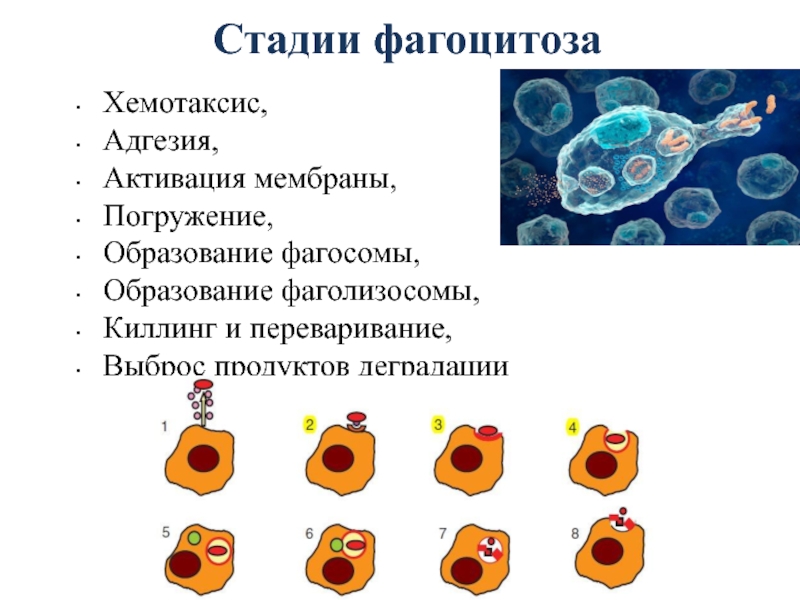
Слайд 32Стадии фагоцитоза
Хемотаксис,
Адгезия,
Активация мембраны,
Погружение,
Образование фагосомы,
Образование фаголизосомы,
Киллинг и переваривание,
Выброс продуктов деградации
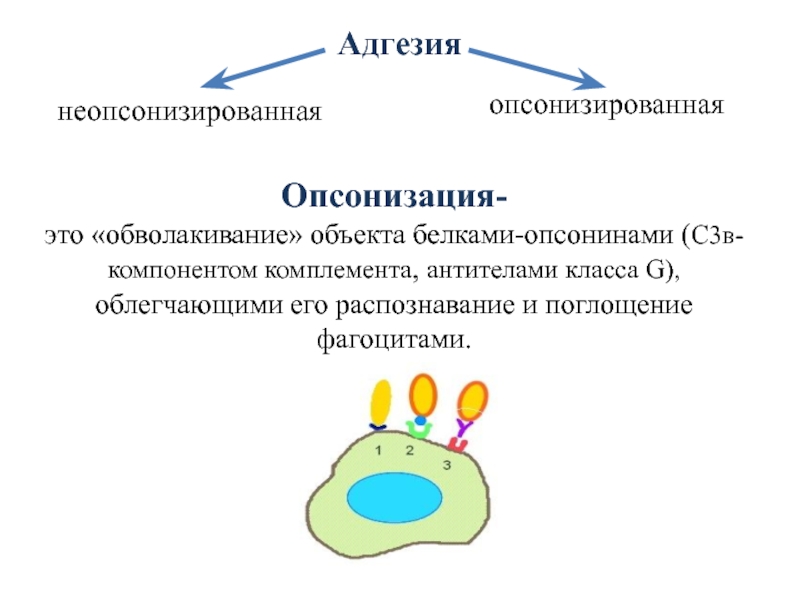
Слайд 33Адгезия
Опсонизация-
это «обволакивание» объекта белками-опсонинами (С3в-компонентом комплемента, антителами класса G),
облегчающими его распознавание и поглощение фагоцитами.
неопсонизированная
опсонизированная
Слайд 35Фагоцитоз
Незавершенный при котором не происходит разрушение патогена (при туберкулезе, гонорее,
менингококковых, стафилококковых инфекциях, бруцеллезе, чуме и др.)
Завершенный
(с лизисом мишени)
Слайд 36Гуморальные факторы врожденного иммунитета
Система комплемента
Цитокиновая сеть
Нормальные антитела
Бактерицидные пептиды: дефензины; белок,
связывающий
ЛПС, и др.
Факторы развития аллергических реакций: биогенные
амины (гистамин, серотонин), эйкозаноиды
и др.Белки воспаления (острой фазы): пентраксины,
в т.ч. С-реактивный белок
Слайд 37Система комплемента
– это многокомпонентная самособирающаяся система сывороточных белков (более
20), которые в норме находятся в неактивном состоянии.
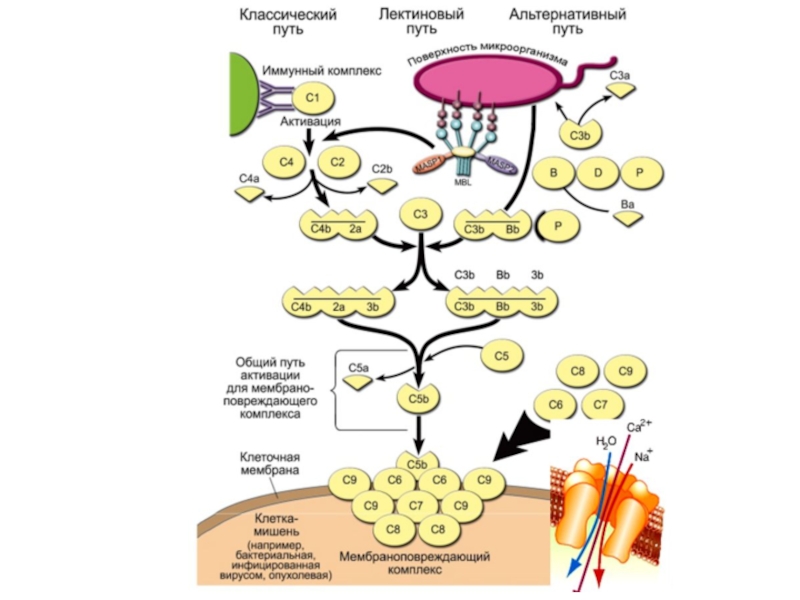
Пути активации:
1. классический
2.
альтернативный3. лектиновый
Слайд 38Фазы активации комплемента
1. Запуск активации (участвуют факторы С1-С5, конвертазы С3,
С5 и ряд других белков)
2. Формирование литического комплекса факторами С5-С9,
атака клеточной мембраны, ее перфорция и лизис клетки-мишениПути активации отличаются особенностями 1-й фазы, а фаза клеточного лизиса проходит однотипно.
Слайд 39Классический путь
1. Активатор – иммунный комплекс Аг-Ат, который узнается С1-компонентом;
2. Последующая активация С4 и С2 и
формирование фермента С3-конвертазы;3. Расщепление С3 на фрагменты С3в и С3а;
4. Формирование С5-конвертазы и расщепление С5 на фрагменты «а» и «в» .
Слайд 40Лектиновый путь
1. Распознавание углеводов на поверхности микробной клетки маннозосвязывающим лектином
сыворотки крови.
2. Активация сразу с С4 и С2-компонентов.
3. Далее идет
аналогично классическому пути.Слайд 41Альтернативный путь
1. Гидролиз C3 на поверхности микробной клетки (обычно
на ЛПС клеточной стенки Гр- бактерий)
2. Образование C3-конвертазы с
участием белков системы комплемента В, D и Р (пропердина), фиксированной на ЛПС3. Запуск дальнейшей цепочки, минуя С1, С4 и С2.
Слайд 43Биологические эффекты комплемента
1. Лизис клеток
(все пути активации завершаются образованием
мембраноатакующего комплекса);
2. «Анафилотоксическое» действие
(С3а, С4а и С5а связываются с
рецепторами базофилов, индуцируют выброс гистамина, серотонина и др. медиаторов воспаления, привлекают фагоциты в очаг);3. Опсонинизация
(С3b, С4b повышают адгезию объекта фагоцитоза на мембранах Мф, Нф, Эф и тем самым усиливают поглотительную активность фагоцитов.
Слайд 44Цитокины
Это система низкомолекулярных белков организма, синтезируемых преимущественно активированными клетками иммунной
и кроветворной систем, регулирующих межклеточные взаимодействия.
(«универсальный» язык общения всех клеток)
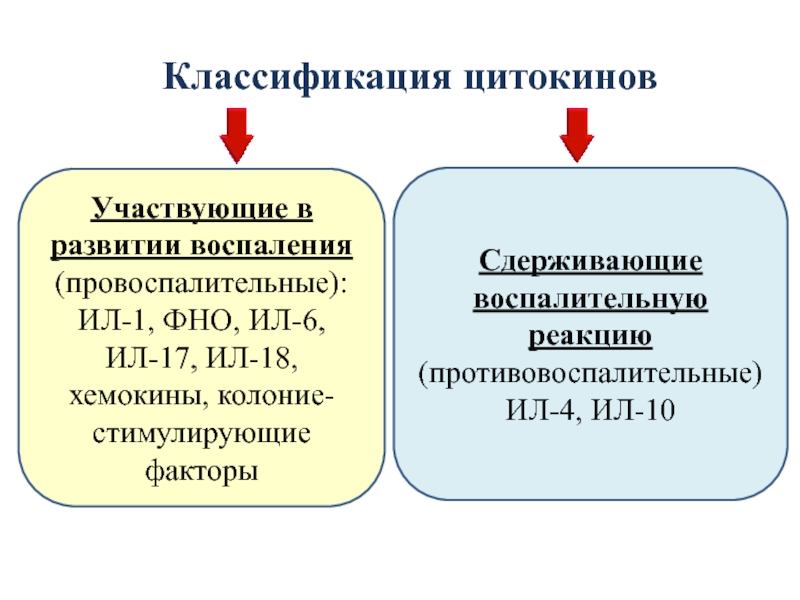
Слайд 45Классификация цитокинов
Участвующие в развитии воспаления
(провоспалительные):
ИЛ-1, ФНО, ИЛ-6,
ИЛ-17, ИЛ-18,
хемокины, колоние-стимулирующие факторы
Сдерживающие воспалительную реакцию (противовоспалительные)ИЛ-4, ИЛ-10
Слайд 46Структурно-функциональные семейства цитокинов
1. интерфероны типа I — III (ИФН-α, β,
γ и др.);
2. интерлейкины 1, 6, 10, 12, 17 (в
настоящее время насчитывается до 34 различных ИЛ);3. хемокины;
4. фактор некроза опухолей;
5. цитокины Т-хелперов (1 и 2);
6. гемопоэтические факторы и др.