Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Протолитическая теория кислот и оснований
Содержание
- 1. Протолитическая теория кислот и оснований
- 2. Лекция №1Лектор: кандидат химических наук, доцентИванова Надежда
- 3. Синквейн1я строка – существительное (дисциплина)2я строка –
- 4. Основная литератураЕршов Ю.А., Попков В.А. Общая химия.
- 5. Основная литератураПопков В.А., Пузаков С.А.Общая химияИздательство: ГЭОТАР-Медиа, 2007.- 976 с.
- 6. Основная литератураЛенский А.С.Биофизическая и бионеограническая химияИздательство: МИА, 2008. – 416 с.Издательство: ВШ, 1989. – 245 с.
- 7. Основная литератураПузаков С.А.ХимияИздательство: ГЭОТАР-Медиа, 2006.- 640 с.
- 8. Основная литератураСлесарев В.И.Химия. Основы химии живогоИздательство: Химиздат, 2009. – 784 с.
- 9. Дополнительная литератураГлинка Н.Л.Общая химияИздательство: любое
- 10. Дополнительная литератураТюрина Е.Ф., Иванова Н.С.Общая химия. Вопросы и ответыИздательство: Медицина ДВ, 2008. - 172с.
- 11. Дополнительная литератураИванова Н.С., Мусина С.А.Введение в химию биогенных элементовИздательство: Полисфера, 2005. – 89 с.
- 12. Дополнительная литератураТюрина Е.Ф.Химия. Теоретические основы. Вопросы. Тесты. Задачи с решениямиИздательство: Медицина ДВ, 2008. – 248 с.
- 13. Дополнительная литератураХарвуд Л., Мак-Кендрик Дж., Уайтхед Р.Наглядная органическая химияИздательство: «ГОЭТАР-Медиа», 2010г. – с.120.
- 14. Дополнительная литератураСонина Г.П.Практические умения по биоорганической химииИздательство: Медицина ДВ, 2005г.
- 15. ВведениеВ результате метаболизма в организме образуется большое
- 16. Теория Бренстеда Лаури (Б-Л), предложенная в
- 17. Кислоты и основания Б-ЛКислота протон-донорное вещество.Основание
- 18. Тогда протолитическое равновесие может быть выражено схемой:
- 19. СН3СООТипы кислот и оснований Б-ЛСН3СООНNH3NH4+SO42HSO4
- 20. Типы протолитических реакцийДля сопряжённой кисл.осн. пары
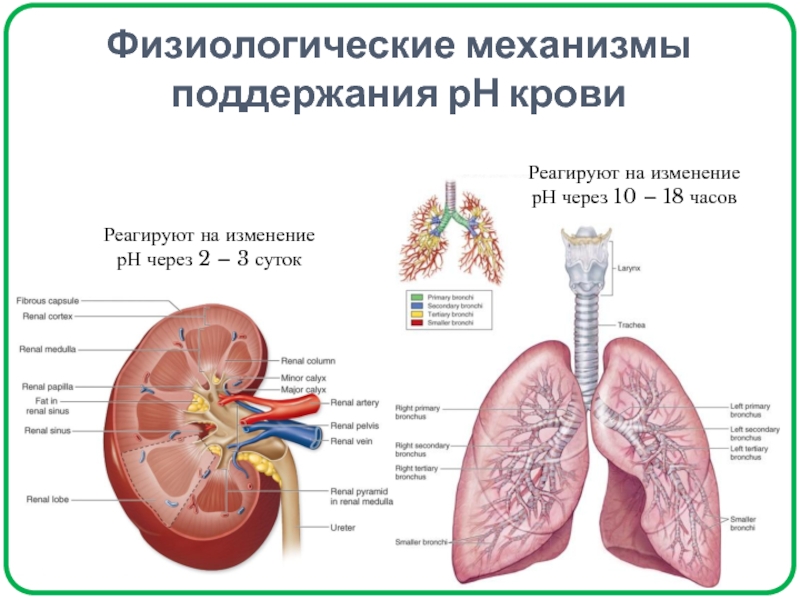
- 21. Физиологические механизмы поддержания рН кровиРеагируют на изменение
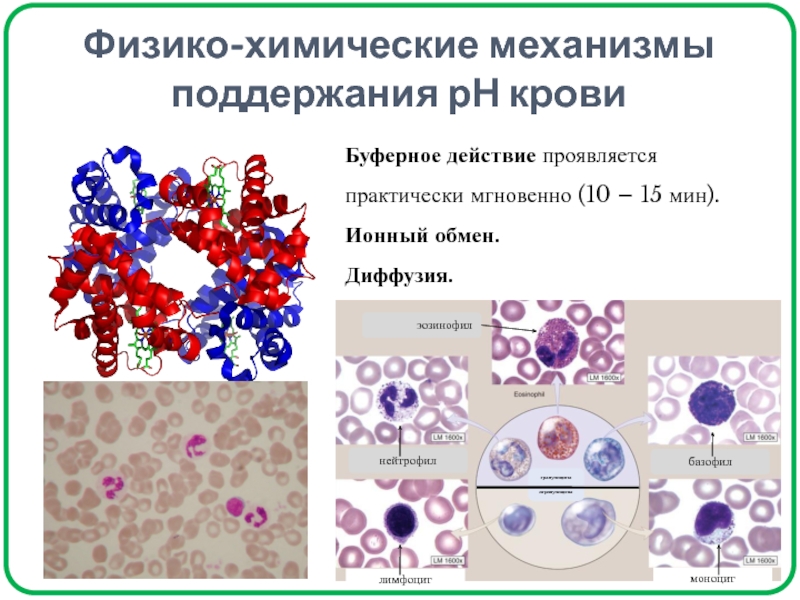
- 22. Физико-химические механизмы поддержания рН кровиБуферное действие проявляется практически мгновенно (10 – 15 мин). Ионный обмен.Диффузия.нейтрофилэозинофилбазофилмоноцитлимфоцитгранулоцитыагранулоциты
- 23. Буферные системы – …… раствор, содержащий протолитическую
- 24. Состав буферных системИз определения в состав буферной
- 25. Типы буферных системкислая буферная система: слабая кислота
- 26. Расчёт рН буферных систем. Уравнение Гендерсона – Гассельбахакислая буферная системаосновная буферная система
- 27. Из уравнения очевидно:рН буферной системы определяется Ка
- 28. … и основные свойства буфера (противостоять изменению
- 29. При добавлении HClСН3СООНСН3СОО– + Н+ ↔ СН3СООНHCl
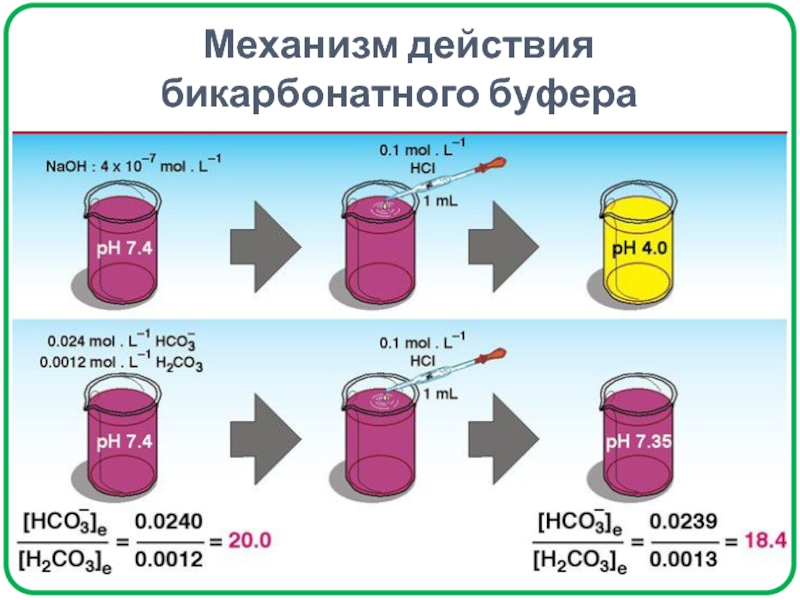
- 30. Механизм действия бикарбонатного буфера
- 31. Основные характеристики буферной системыБуферная ёмкость (В, β)
- 32. Факторы, влияющие на βКонцентрации компонентов буферной системы:
- 33. Основные характеристики буферной системыЗона буферного действия ‒
- 34. рН биожидкостей в нормеВнутриклеточный рНВнутри эритроцита рН
- 35. Совмещённые протолитические равновесия …… в буферной системе
- 36. Совмещённое протолитическое равновесиеН+В–А–Вывод: в совмещённом протолитическом равновесии
- 37. Спасибо за внимание!
- 38. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Лекция №1
Лектор:
кандидат химических наук, доцент
Иванова Надежда Семёновна
Протолитическая теория кислот
и оснований. Протолитическое равновесие.
Буферные растворы
Слайд 3Синквейн
1я строка – существительное (дисциплина)
2я строка – 2 прилагательных (признаки
и свойства существительного)
3я строка – 3 глагола, характеризующих существительное
4я строка
– фраза из 4х слов (отношение к существительному)5я строка – 1 слово (резюме).
Слайд 4Основная литература
Ершов Ю.А.,
Попков В.А.
Общая химия. Биофизическая химия. Химия
биогенных элементов
Издательство: Высшая школа, 2005. - 560 с.
Слайд 5Основная литература
Попков В.А.,
Пузаков С.А.
Общая химия
Издательство: ГЭОТАР-Медиа, 2007.- 976 с.
Слайд 6Основная литература
Ленский А.С.
Биофизическая и бионеограническая химия
Издательство: МИА, 2008. – 416
с.
Издательство: ВШ, 1989. – 245 с.
Слайд 8Основная литература
Слесарев В.И.
Химия. Основы химии живого
Издательство: Химиздат, 2009. – 784
Слайд 10Дополнительная литература
Тюрина Е.Ф.,
Иванова Н.С.
Общая химия. Вопросы и ответы
Издательство: Медицина
ДВ, 2008. - 172с.
Слайд 11Дополнительная литература
Иванова Н.С.,
Мусина С.А.
Введение в химию биогенных элементов
Издательство: Полисфера,
2005. – 89 с.
Слайд 12Дополнительная литература
Тюрина Е.Ф.
Химия. Теоретические основы. Вопросы. Тесты. Задачи с решениями
Издательство:
Медицина ДВ, 2008. – 248 с.
Слайд 13Дополнительная литература
Харвуд Л.,
Мак-Кендрик Дж., Уайтхед Р.
Наглядная органическая химия
Издательство: «ГОЭТАР-Медиа»,
2010г. – с.120.
Слайд 14Дополнительная литература
Сонина Г.П.
Практические умения по биоорганической химии
Издательство: Медицина ДВ, 2005г.
Слайд 15Введение
В результате метаболизма в организме образуется большое количество кислот, а
больше всего Н2СО3 (до 13 моль ежедневно). Выводится она, в
основном, при дыхании в виде СО2 и Н2О, но задержка её до 0,15 моль в организме ведёт к нарушению кислотно – основного состояния (КОС).Слайд 16Теория Бренстеда Лаури (Б-Л), предложенная в 1923 г., определяет
кислоты и основания по отношению к одному партнёру Н+.
Поэтому кислоты и основания называются протолитами;Йоханнес-Николаус Брёнстед
(1879-1947)
обратимые реакции, в которых осуществляется перенос протонов, протолитическими равновесиями, а теория Б-Л протолитической теорией.
Слайд 17Кислоты и основания Б-Л
Кислота протон-донорное вещество.
Основание протон-акцепторное вещество.
Из
этого можно записать соотношение:
Кислоту и основание, связанные приведённым соотношением, называют
сопряжённой кислотно-основной парой:Слайд 18Тогда протолитическое равновесие может быть выражено схемой:
Направление протолитического равновесия
устанавливается в результате конкуренции за Н+ между основаниями сопряжённых кислотно-основных
пар и всегда смещается в сторону более слабой кислоты.Кислота 1
Основание 2
Сопр. основание 1
Сопр. кислота 2
Слайд 20Типы протолитических реакций
Для сопряжённой кисл.осн. пары Ka Kb
=1014 чем сильнее кислота в паре, тем слабее
основание и наоборот.Слайд 21Физиологические механизмы поддержания рН крови
Реагируют на изменение рН через 2
– 3 суток
Реагируют на изменение рН через 10 – 18
часовСлайд 22Физико-химические механизмы поддержания рН крови
Буферное действие проявляется практически мгновенно (10
– 15 мин).
Ионный обмен.
Диффузия.
нейтрофил
эозинофил
базофил
моноцит
лимфоцит
гранулоциты
агранулоциты
Слайд 23Буферные системы – …
… раствор, содержащий протолитическую равновесную систему, способную
поддерживать практически постоянный рН при разбавлении или добавлении небольших количеств
кислоты и щёлочи.… система, состоящая из слабого протолита и избытка сопряжённого с ним основания или кислоты. рН буферных систем незначительно изменяется при добавлении сильного протолита и разбавления.
Слайд 24Состав буферных систем
Из определения в состав буферной системы входит слабый
протолит:
НА + Н2О ↔ Н3О+ + А–
Избыток сопряжённого основания
(А–) образуется за счёт соли этой кислоты с сильным основанием.МеА Ме+ + А–
кисл
с. осн
с. осн
Слайд 25Типы буферных систем
кислая буферная система: слабая кислота и её соль
с сильным основанием
СН3СООН + СН3СООNa;
основная буферная система: слабое основание
и его соль с сильной кислотой NH4OH + NH4Cl.
Слайд 26Расчёт рН буферных систем.
Уравнение Гендерсона – Гассельбаха
кислая буферная система
основная буферная
система
Слайд 27Из уравнения очевидно:
рН буферной системы определяется Ка или Кb слабого
протолита:
рКа = –lgKa
pKb = –lgKb
рН зависит от соотношения количеств компонентов
буферной системы.рН зависит от температуры, т.к. величины рКа и рКb зависят от температуры.
Выводы
Слайд 28… и основные свойства буфера (противостоять изменению рН при добавлении
сильных протолитов и разбавлению) заключаются в совмещении нескольких протолитических равновесий:
HB
+ H2O ↔ B‒ + H3O+B‒ + H2O ↔ HB + OH‒
Вывод: в протолитической буферной системе имеет место совмещённое равновесие процессов ионизации и гидролиза.
кисл.
кисл.
с.осн
с.осн
Механизм действия буферной системы …
Слайд 29При добавлении HCl
СН3СООН
СН3СОО– + Н+ ↔ СН3СООН
HCl заменяется эквивалентным количеством
СН3СООН, что приводит к незначительному уменьшению рН буфера.
При добавлении NaOH
СН3СОО–
СН3СООН
+ OН- ↔ СН3СОО– + H2ONaOH заменяется эквивалентным количеством СН3СООNa, что приводит к незначительному увеличению рН буфера.
Разбавление буферной системы до концентрации компонентов буфера ≈ 0,01 моль/дм3 практически не влияет на рН буфера.
Механизм действия буферной системы
Слайд 31Основные характеристики буферной системы
Буферная ёмкость (В, β) ‒ количество вещества
эквивалента сильного протолита Х, которое нужно добавить к 1 дм3
буферной системы, чтобы изменить её рН на единицу.Слайд 32Факторы, влияющие на β
Концентрации компонентов буферной системы: чем выше концентрации,
тем выше β.
Соотношение концентраций компонентов буферной системы: чем ближе к
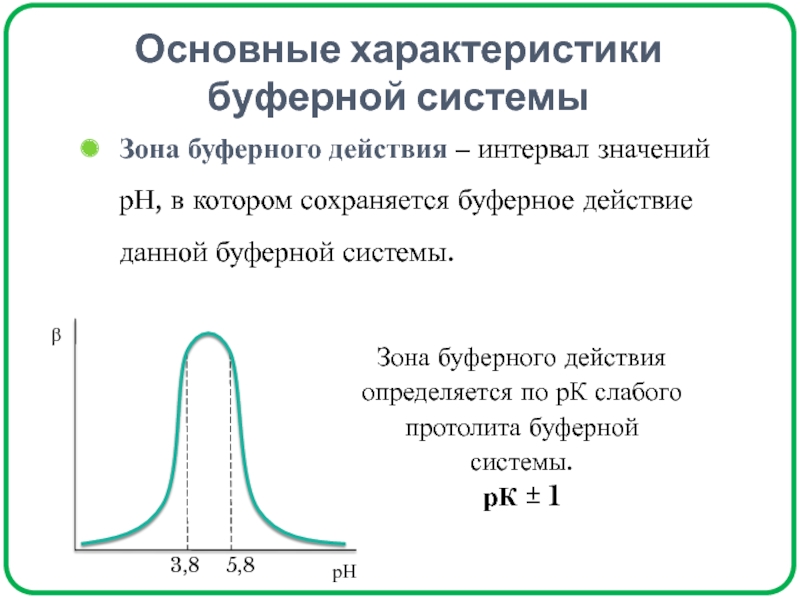
1, тем выше β.Слайд 33Основные характеристики буферной системы
Зона буферного действия ‒ интервал значений рН,
в котором сохраняется буферное действие данной буферной системы.
3,8
5,8
β
рН
Зона буферного действия
определяется по рК слабого протолита буферной системы.рК ± 1
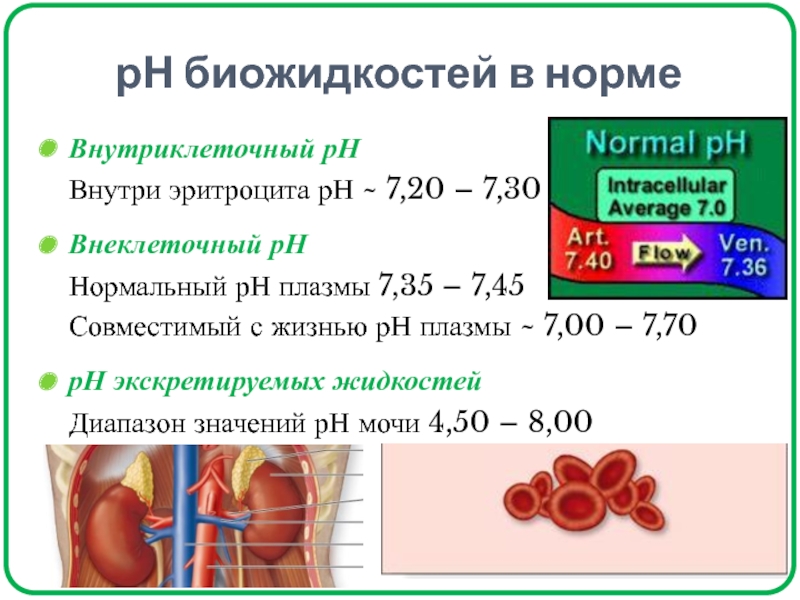
Слайд 34рН биожидкостей в норме
Внутриклеточный рН
Внутри эритроцита рН ~ 7,20 –
7,30
Внеклеточный рН
Нормальный рН плазмы 7,35 – 7,45
Совместимый с жизнью рН
плазмы ~ 7,00 – 7,70рН экскретируемых жидкостей
Диапазон значений рН мочи 4,50 – 8,00
Слайд 35Совмещённые протолитические равновесия …
… в буферной системе имеют место при
одновременном присутствии в ней нескольких буферных систем.
Условия совмещённого равновесия:
оба основания
(А–, В–) буф. системы связывают Н+ в другой компонент – кислоту;«работает» буфер, образующий более прочный протолит (более слабую кислоту);
Ка (НА) < Ка (НВ).
НА
МеА
НВ
МеВ
Слайд 36Совмещённое протолитическое равновесие
Н+
В–
А–
Вывод: в совмещённом протолитическом равновесии доминирует тот процесс,
в результате которого образуется более прочный протолит.
H2PO4–
HHbHPO42– Hb–
Ka = 6,210–8 Ка=6,3110–9