%-ной кислоты (плотность 1,5 г/мл). Вычислите массовую долю кислоты в
полученном растворе. Ответ дайте в процентах с точностью до десятых.Решение
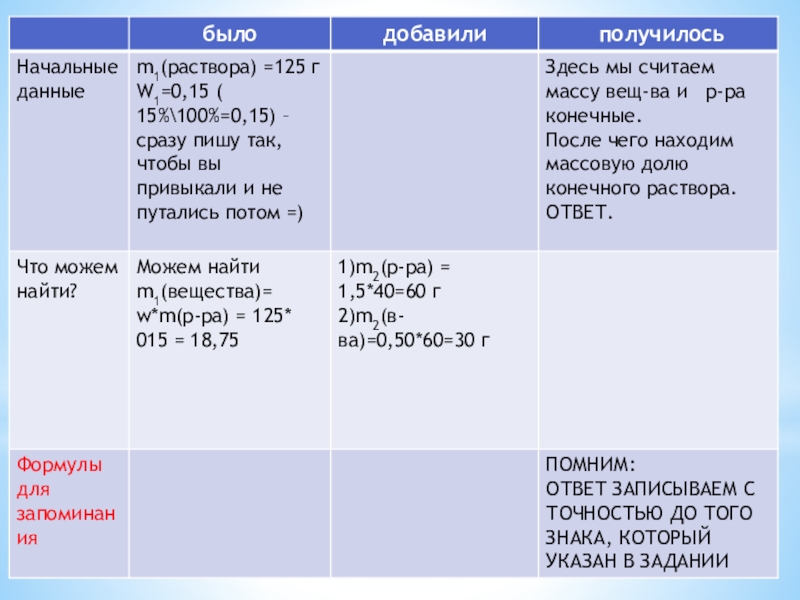
1. Смотрим на то, что у нас было в начале, что добавили и что будет в конце.
2.Составляем табличку (или рисуем стаканы, каждая колонка – это один стакан) – следующий слайд
3.ПОМНИМ: Что в этом номере не важно какие именно вещества вам даны(серная, соляная, фосфорная кислоты, любые соли, основания и т.д.). Учимся оперировать только словами РАСТВОР, ВЕЩЕСТВО(соль), массовая доля, плотность, объём, кол-во вещества.
Задание 27