Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
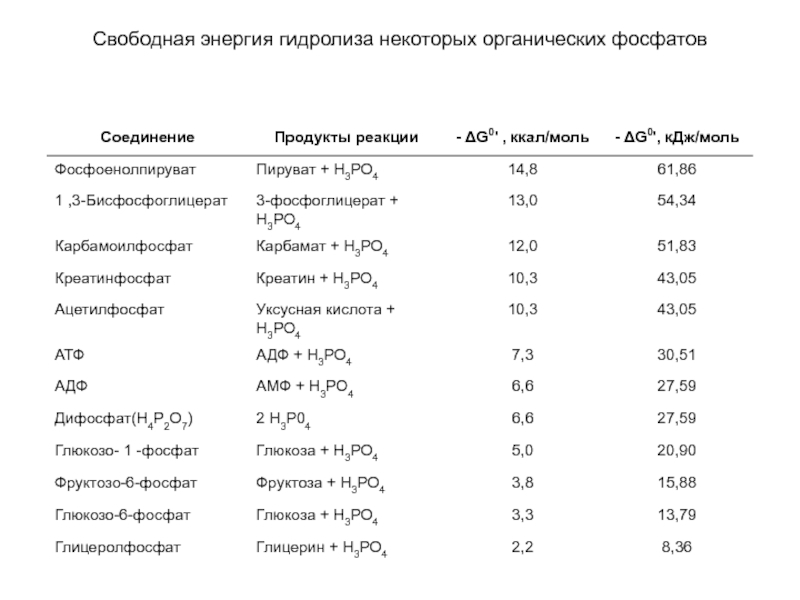
Соединение Продукты реакции - ΔG 0 ', ккал/моль - ΔG 0 ',
Содержание
- 1. Соединение Продукты реакции - ΔG 0 ', ккал/моль - ΔG 0 ',
- 2. Слайд 2
- 3. Стандартные окислительно-восстановительные потенциалы некоторых сопряжённых пар
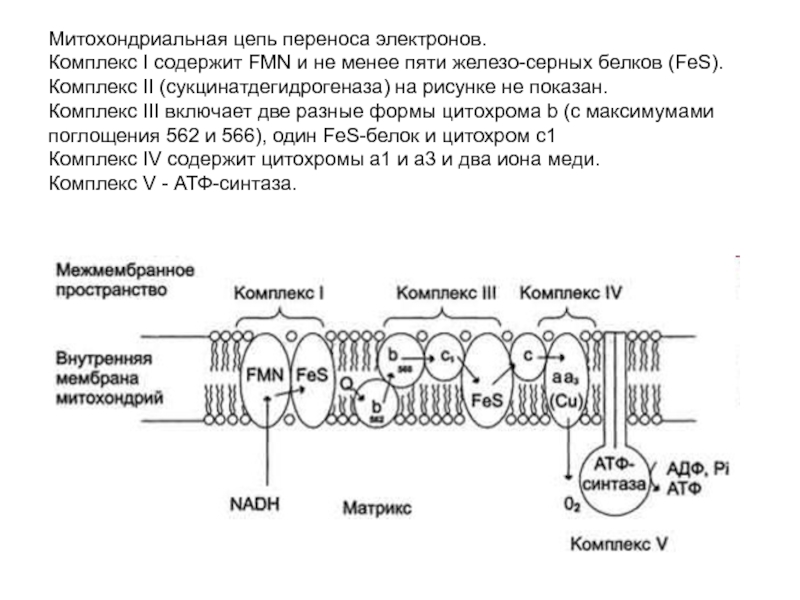
- 4. Митохондриальная цепь переноса электронов. Комплекс I
- 5. Структурные формулы рабочей части коферментов NAD+ и
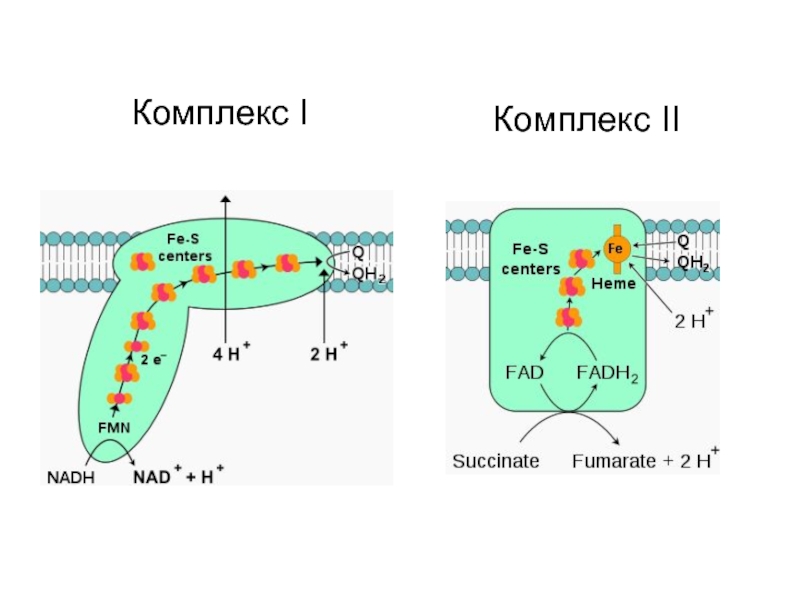
- 6. Комплекс IКомплекс II
- 7. Строение железо-серных центров. Атомы железа в FeS-центрах
- 8. Структура убихинона (кофермента Q). n - число
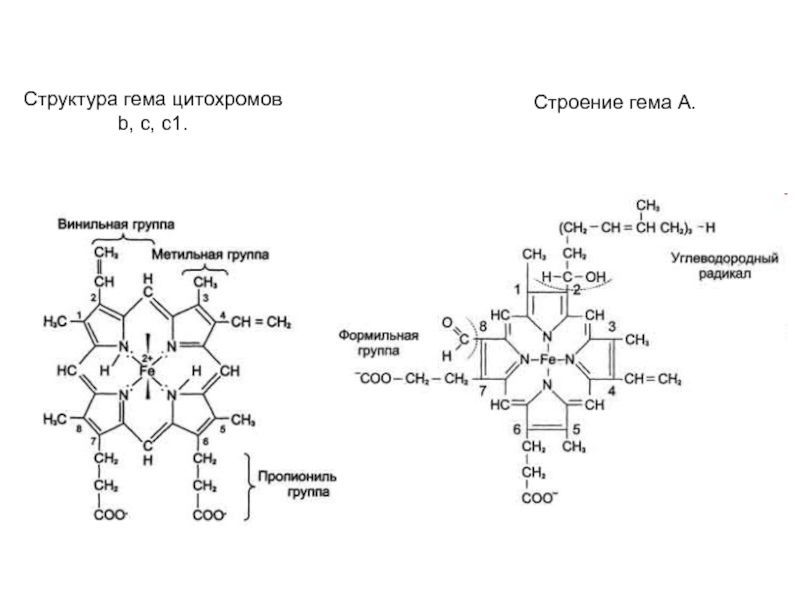
- 9. Структура гема цитохромов b, с, с1.Строение гема А.
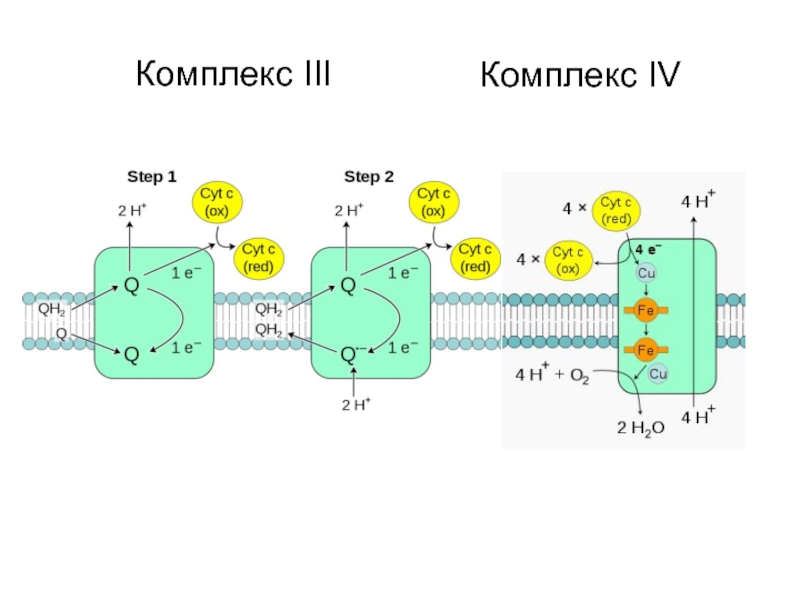
- 10. Комплекс IVКомплекс III
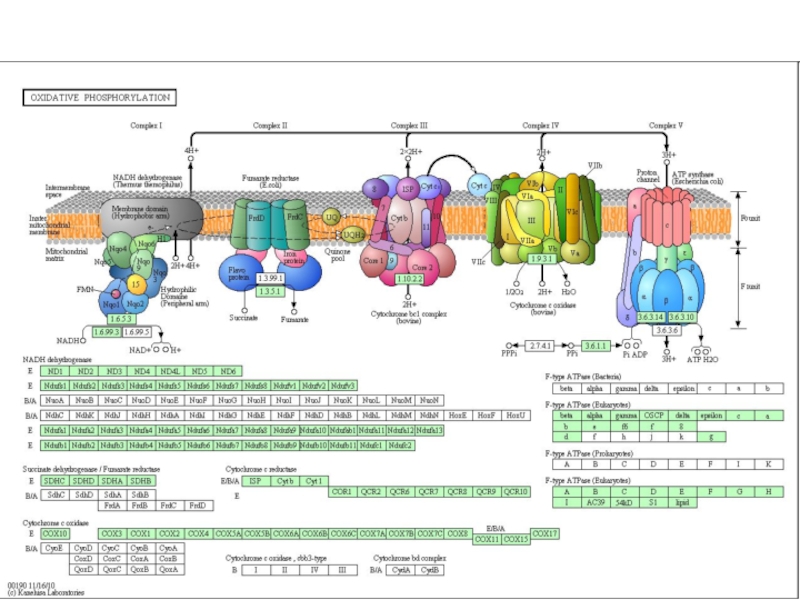
- 11. Компоненты митохондриальной цепи переноса электронов
- 12. Слайд 12
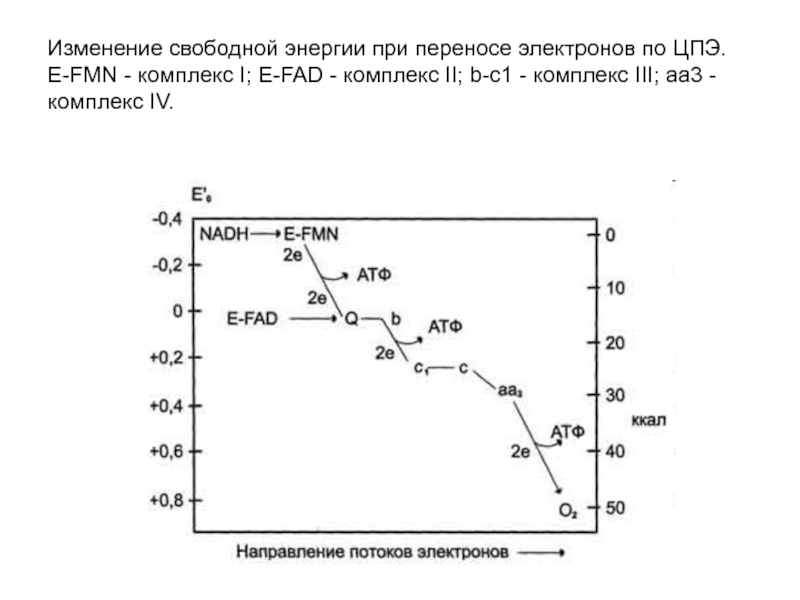
- 13. Изменение свободной энергии при переносе электронов по
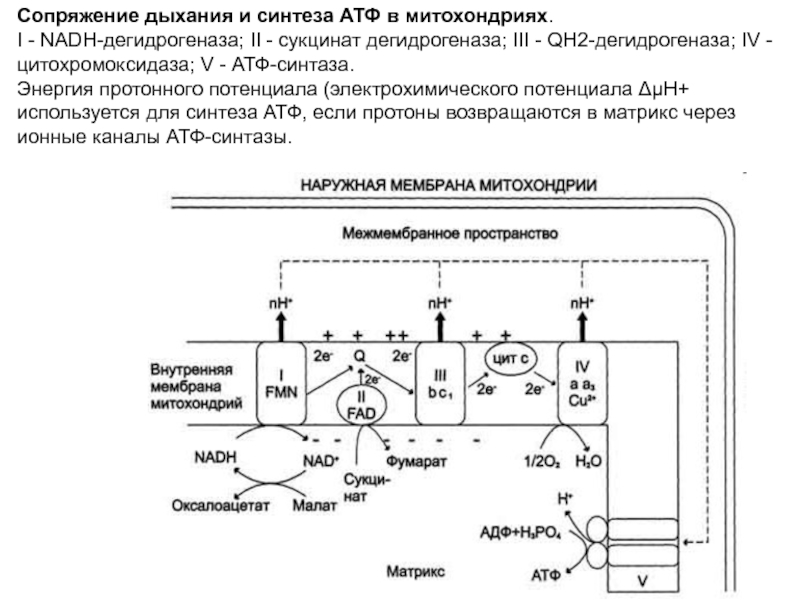
- 14. Сопряжение дыхания и синтеза АТФ в митохондриях.
- 15. Сопряжение переноса электронов через дыхательный комплекс III
- 16. Строение АТФ-синтазы.F0 и F1 - комплексы АТФ-синтазы,
- 17. Механизм действия АТФ-синтазы.Каталитический цикл синтеза АТФ включает
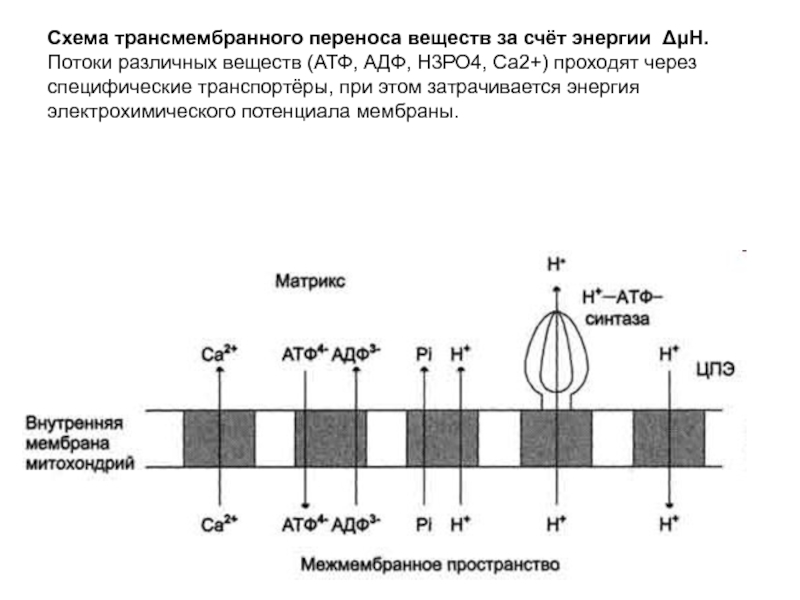
- 18. Схема трансмембранного переноса веществ за счёт энергии
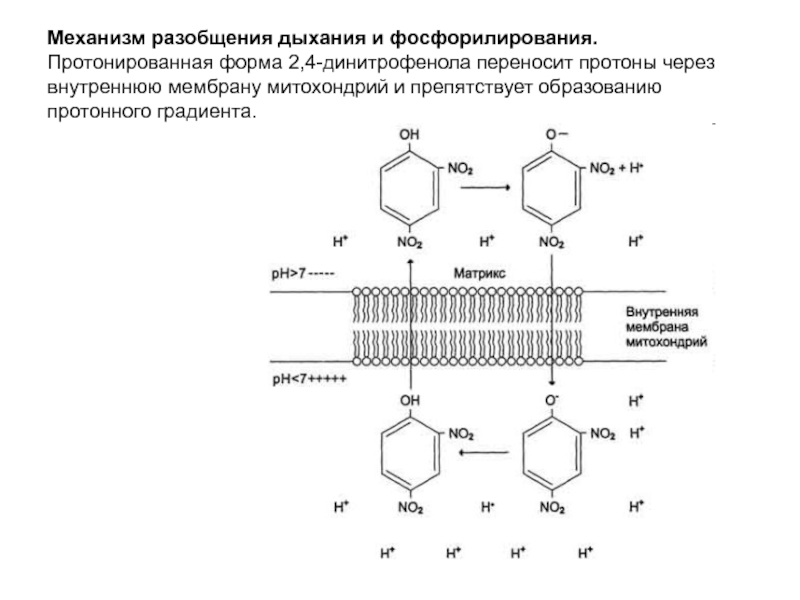
- 19. Механизм разобщения дыхания и фосфорилирования. Протонированная
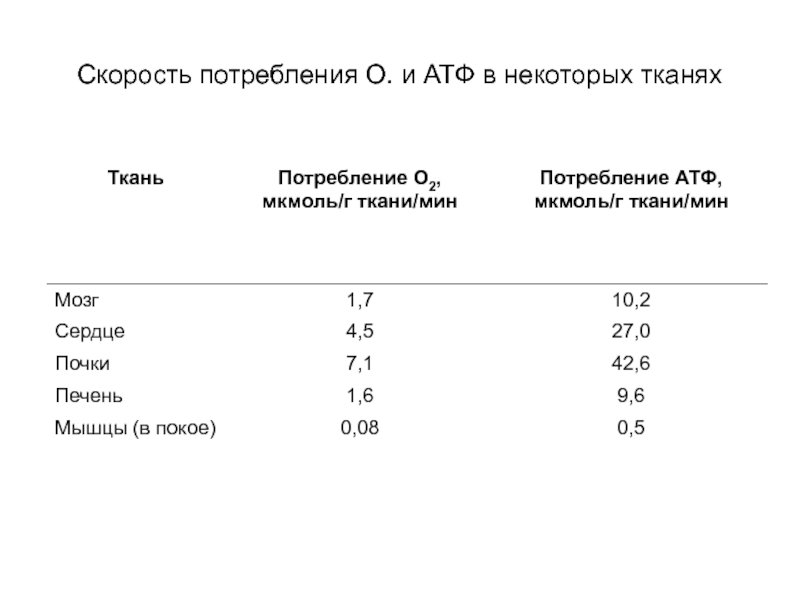
- 20. Скорость потребления О. и АТФ в некоторых тканях
- 21. Скачать презентанцию
Стандартные окислительно-восстановительные потенциалы некоторых сопряжённых пар
Слайды и текст этой презентации
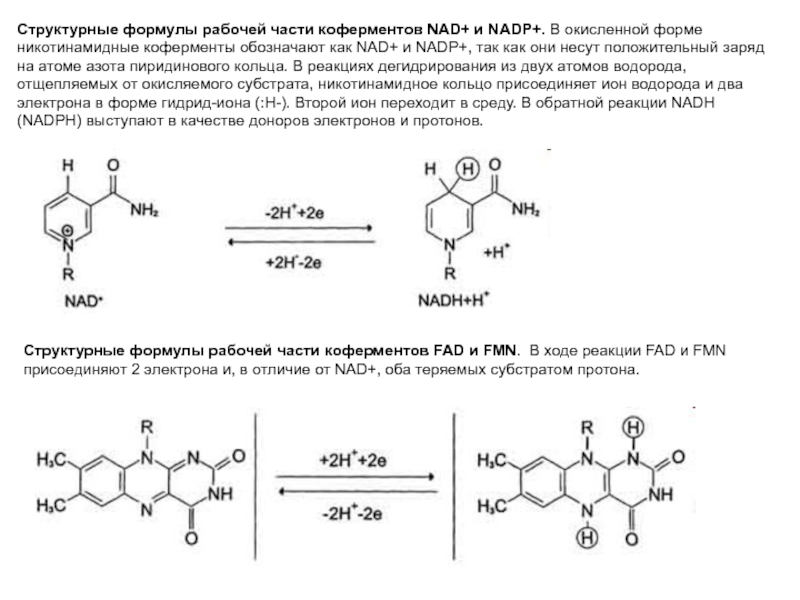
Слайд 5Структурные формулы рабочей части коферментов NAD+ и NADP+. В окисленной
форме никотинамидные коферменты обозначают как NAD+ и NADP+, так как
они несут положительный заряд на атоме азота пиридинового кольца. В реакциях дегидрирования из двух атомов водорода, отщепляемых от окисляемого субстрата, никотинамидное кольцо присоединяет ион водорода и два электрона в форме гидрид-иона (:Н-). Второй ион переходит в среду. В обратной реакции NADH (NADPH) выступают в качестве доноров электронов и протонов.Структурные формулы рабочей части коферментов FAD и FMN. В ходе реакции FAD и FMN присоединяют 2 электрона и, в отличие от NAD+, оба теряемых субстратом протона.
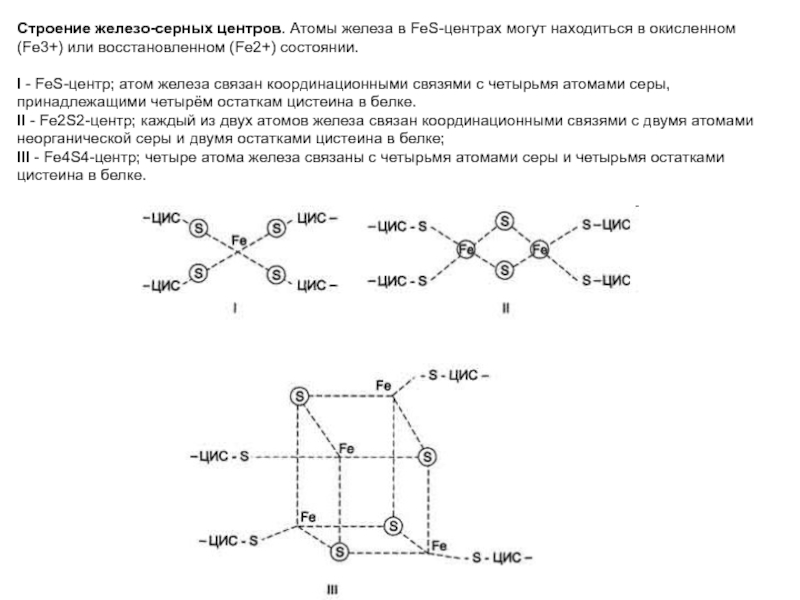
Слайд 7Строение железо-серных центров. Атомы железа в FeS-центрах могут находиться в
окисленном (Fe3+) или восстановленном (Fe2+) состоянии. I - FeS-центр; атом
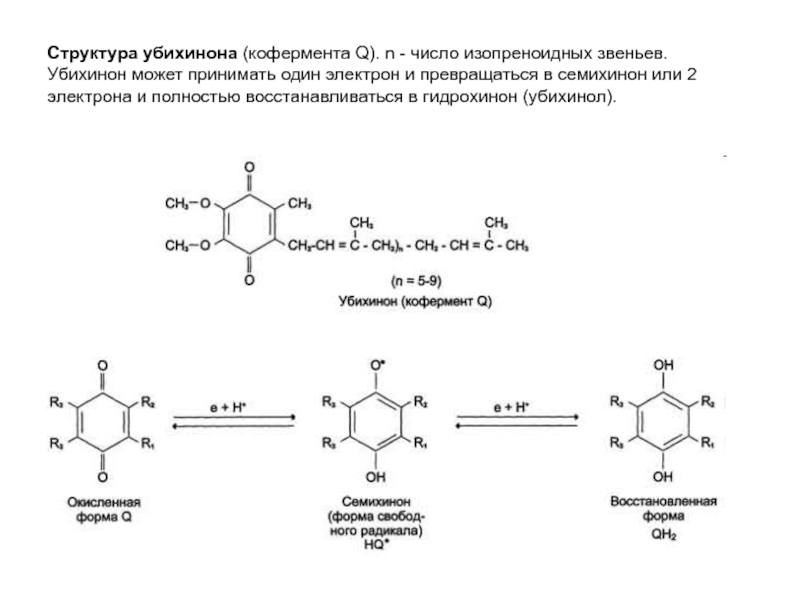
железа связан координационными связями с четырьмя атомами серы, принадлежащими четырём остаткам цистеина в белке. II - Fе2S2-центр; каждый из двух атомов железа связан координационными связями с двумя атомами неорганической серы и двумя остатками цистеина в белке; III - Fe4S4-центр; четыре атома железа связаны с четырьмя атомами серы и четырьмя остатками цистеина в белке.Слайд 8Структура убихинона (кофермента Q). n - число изопреноидных звеньев. Убихинон
может принимать один электрон и превращаться в семихинон или 2
электрона и полностью восстанавливаться в гидрохинон (убихинол).Слайд 13Изменение свободной энергии при переносе электронов по ЦПЭ. E-FMN -
комплекс I; E-FAD - комплекс II; b-с1 - комплекс III;
aa3 - комплекс IV.Слайд 14Сопряжение дыхания и синтеза АТФ в митохондриях. I - NADH-дегидрогеназа;
II - сукцинат дегидрогеназа; III - QН2-дегидрогеназа; IV - цитохромоксидаза;
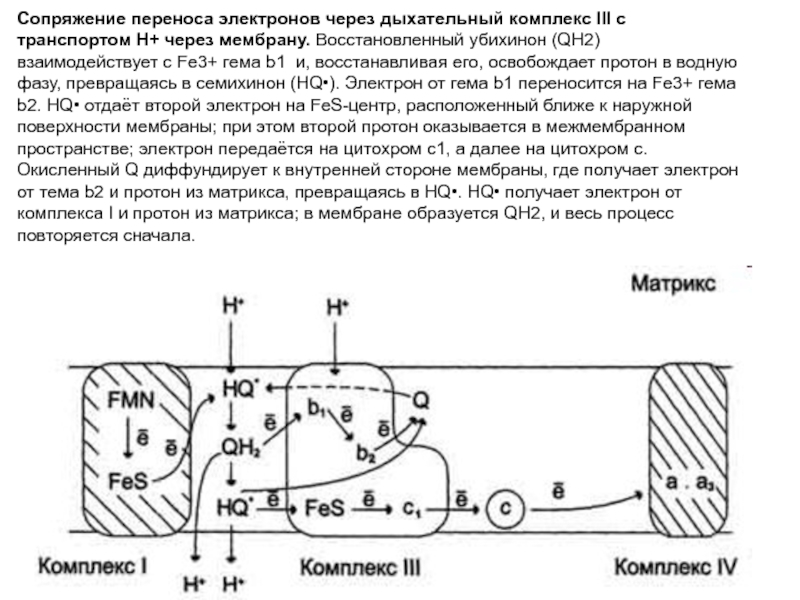
V - АТФ-синтаза. Энергия протонного потенциала (электрохимического потенциала ΔμН+ используется для синтеза АТФ, если протоны возвращаются в матрикс через ионные каналы АТФ-синтазы.Слайд 15Сопряжение переноса электронов через дыхательный комплекс III с транспортом Н+
через мембрану. Восстановленный убихинон (QH2) взаимодействует с Fе3+ гема b1
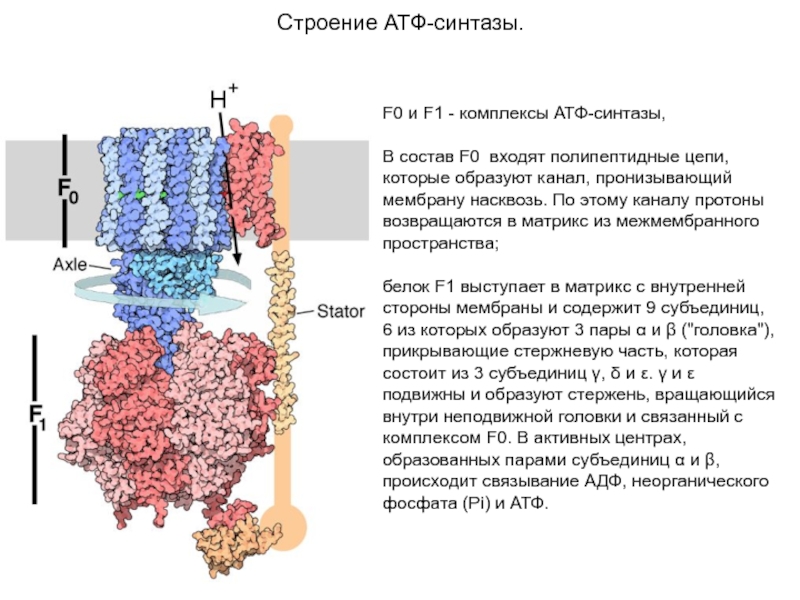
и, восстанавливая его, освобождает протон в водную фазу, превращаясь в семихинон (НQ•). Электрон от гема b1 переносится на Fe3+ гема b2. HQ• отдаёт второй электрон на FeS-центр, расположенный ближе к наружной поверхности мембраны; при этом второй протон оказывается в межмембранном пространстве; электрон передаётся на цитохром с1, а далее на цитохром с. Окисленный Q диффундирует к внутренней стороне мембраны, где получает электрон от тема b2 и протон из матрикса, превращаясь в НQ•. НQ• получает электрон от комплекса I и протон из матрикса; в мембране образуется QН2, и весь процесс повторяется сначала.Слайд 16Строение АТФ-синтазы.
F0 и F1 - комплексы АТФ-синтазы,
В состав F0
входят полипептидные цепи, которые образуют канал, пронизывающий мембрану насквозь. По
этому каналу протоны возвращаются в матрикс из межмембранного пространства;белок F1 выступает в матрикс с внутренней стороны мембраны и содержит 9 субъединиц, 6 из которых образуют 3 пары α и β ("головка"), прикрывающие стержневую часть, которая состоит из 3 субъединиц γ, δ и ε. γ и ε подвижны и образуют стержень, вращающийся внутри неподвижной головки и связанный с комплексом F0. В активных центрах, образованных парами субъединиц α и β, происходит связывание АДФ, неорганического фосфата (Рi) и АТФ.
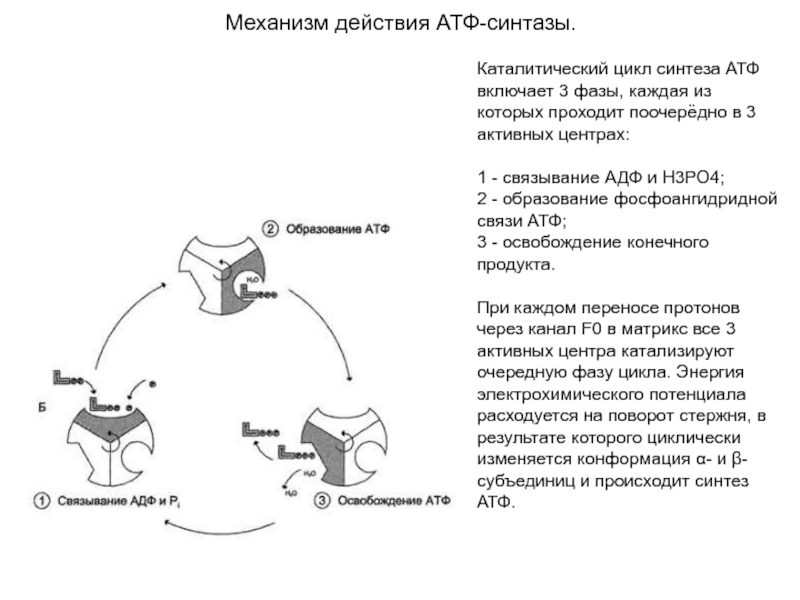
Слайд 17Механизм действия АТФ-синтазы.
Каталитический цикл синтеза АТФ включает 3 фазы, каждая
из которых проходит поочерёдно в 3 активных центрах:
1 -
связывание АДФ и Н3РО4; 2 - образование фосфоангидридной связи АТФ;
3 - освобождение конечного продукта.
При каждом переносе протонов через канал F0 в матрикс все 3 активных центра катализируют очередную фазу цикла. Энергия электрохимического потенциала расходуется на поворот стержня, в результате которого циклически изменяется конформация α- и β-субъединиц и происходит синтез АТФ.