Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение и свойства свободных радикалов
Содержание
- 1. Строение и свойства свободных радикалов
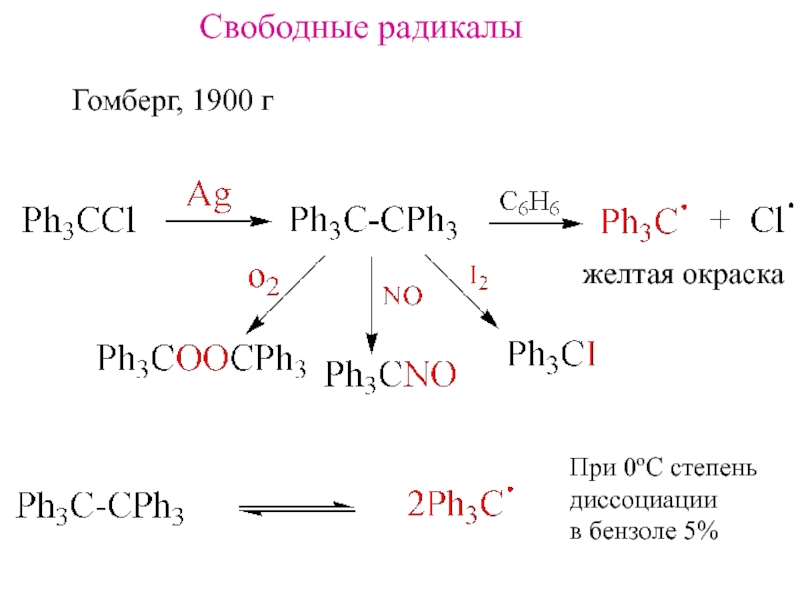
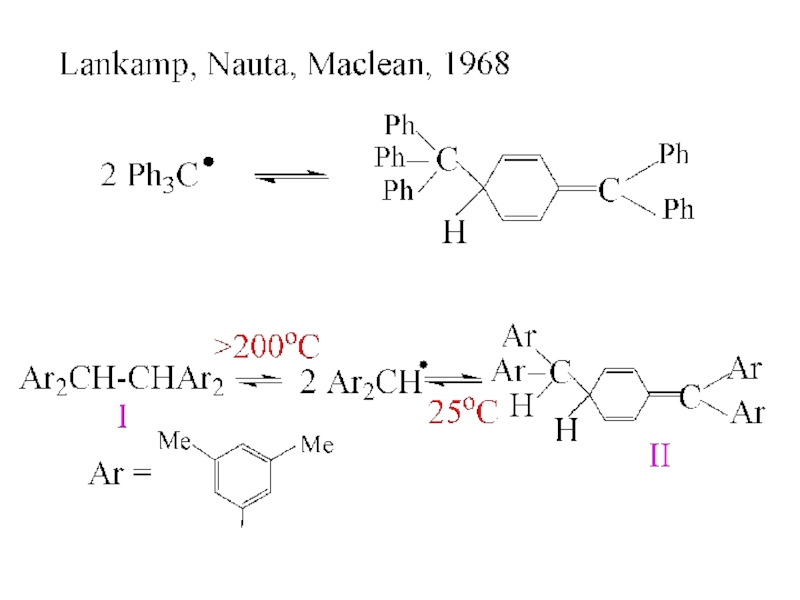
- 2. Свободные радикалыГомберг, 1900 гжелтая окраскаПри 0оС степеньдиссоциации в бензоле 5%
- 3. OH-. , RO2., OH. эндогенные повреждающие
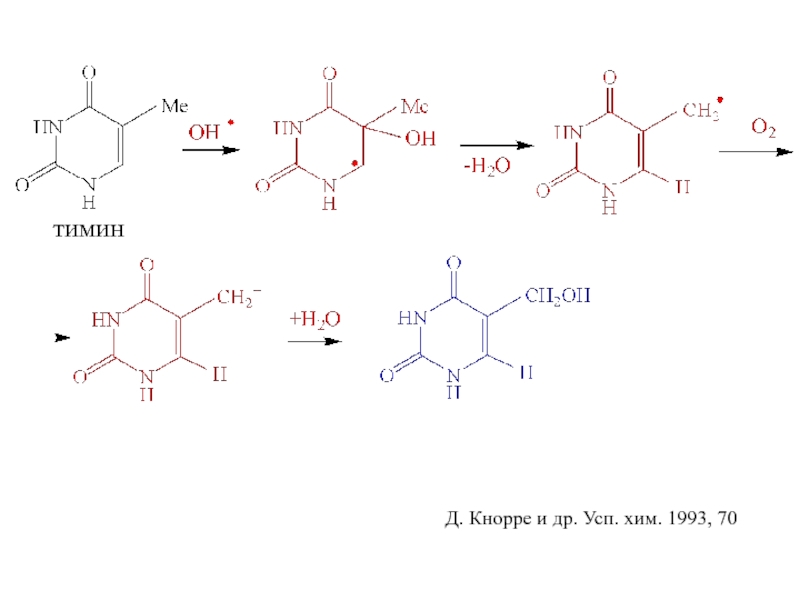
- 4. Д. Кнорре и др. Усп. хим. 1993, 70 тимин
- 5. Методы генерации1. Термическиетрет-бутилпероксидбензоилпероксидτ1/2 = 2 часа (140оС); 35 сек. (180о)τ1/2 = 0.5 часа (100оС)
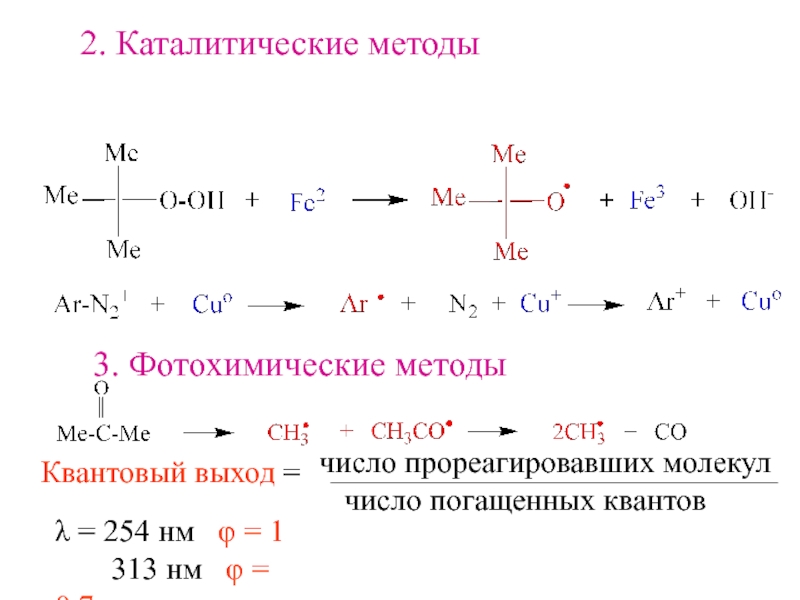
- 6. 2. Каталитические методы 3. Фотохимические методыКвантовый выход
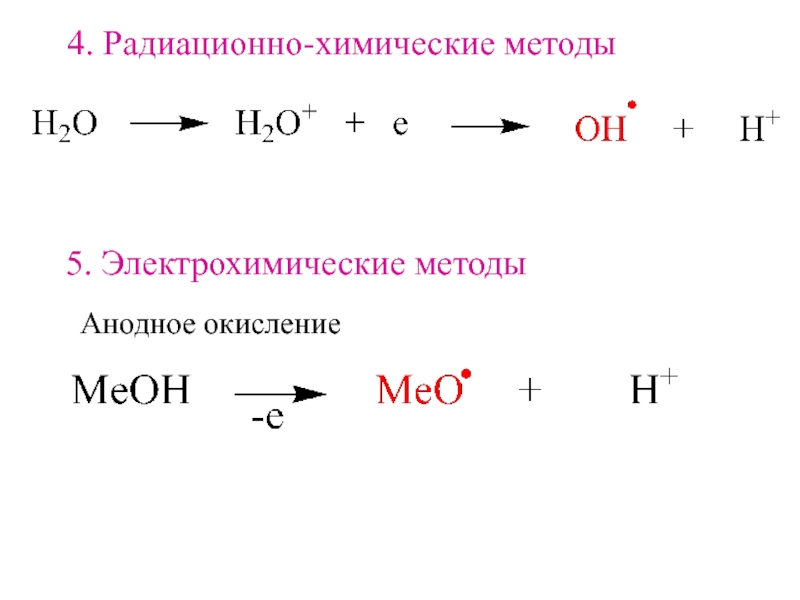
- 7. 4. Радиационно-химические методы 5. Электрохимические методыАнодное окисление
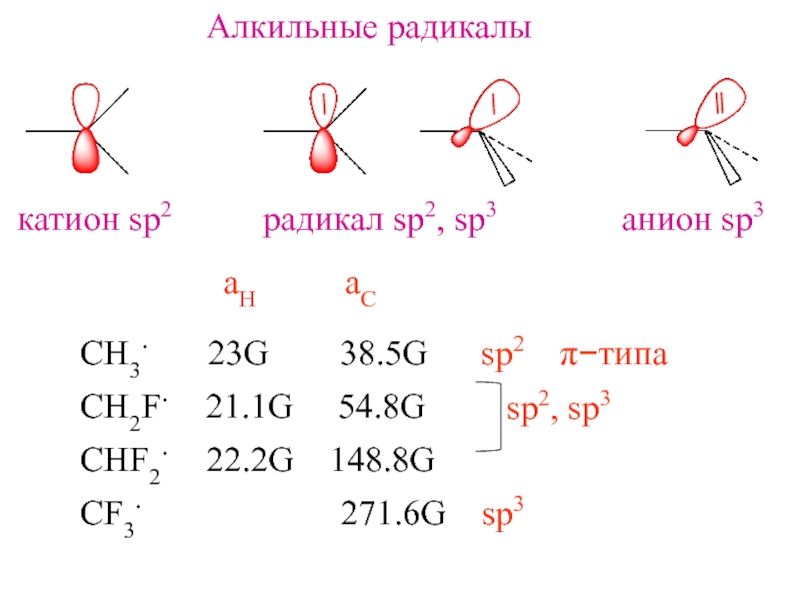
- 8. Алкильные радикалыкатион sp2радикал sp2, sp3анион sp3СH3.
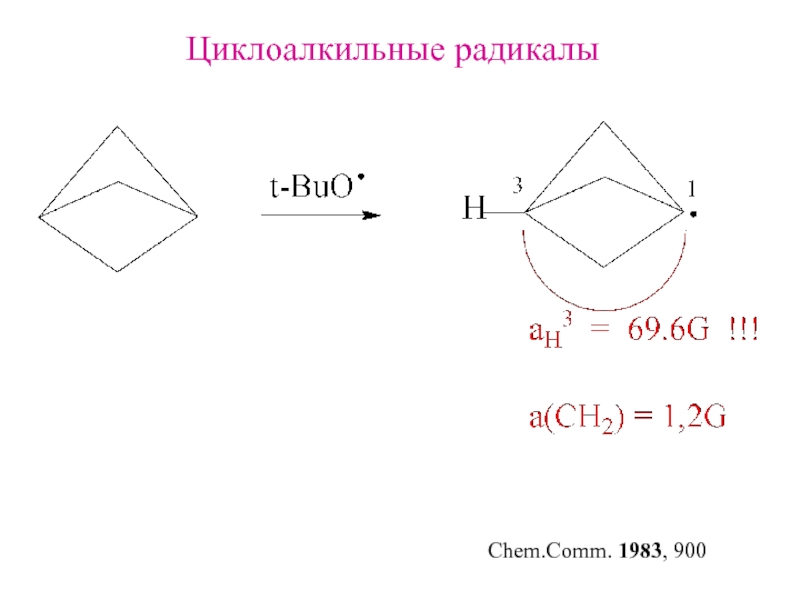
- 9. Циклоалкильные радикалыChem.Comm. 1983, 900
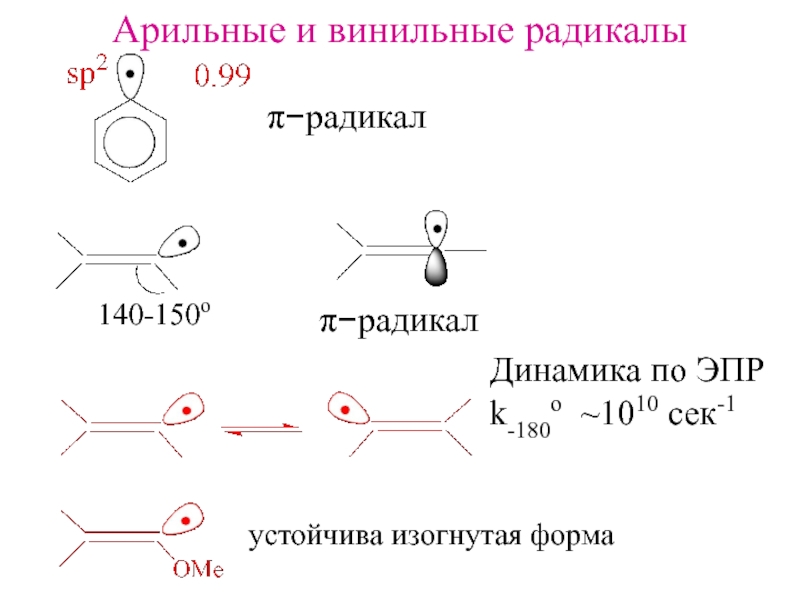
- 10. Арильные и винильные радикалыπ−радикал140-150oπ−радикалДинамика по ЭПРk-180o ~1010 сек-1устойчива изогнутая форма
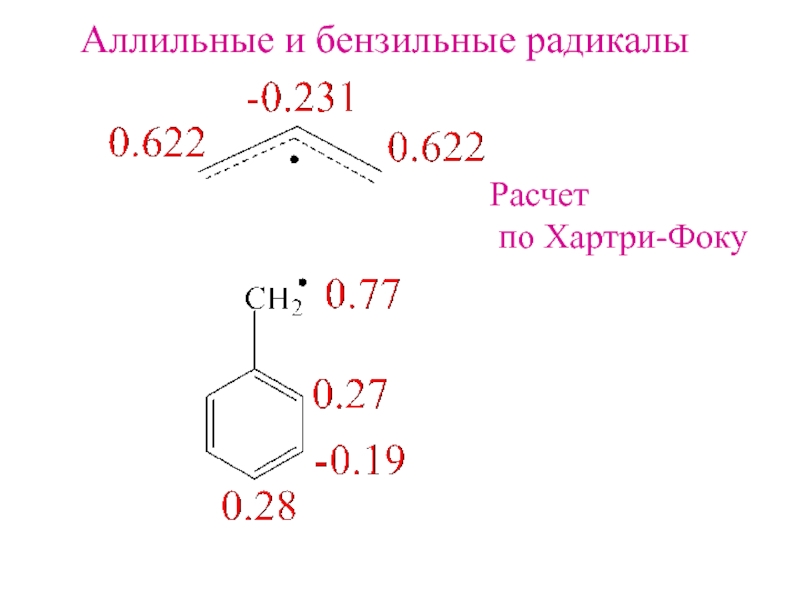
- 11. Аллильные и бензильные радикалыРасчет по Хартри-Фоку
- 12. Дифракция электронов: пропеллер, кольцаповернуты на 40-45о, р-орбитали С. и Ph некопланарныи перекрывание неполноерасчет спиновойплотностиЭПР
- 13. Слайд 13
- 14. B. Kahr, D. van Engen, K. Mislow,
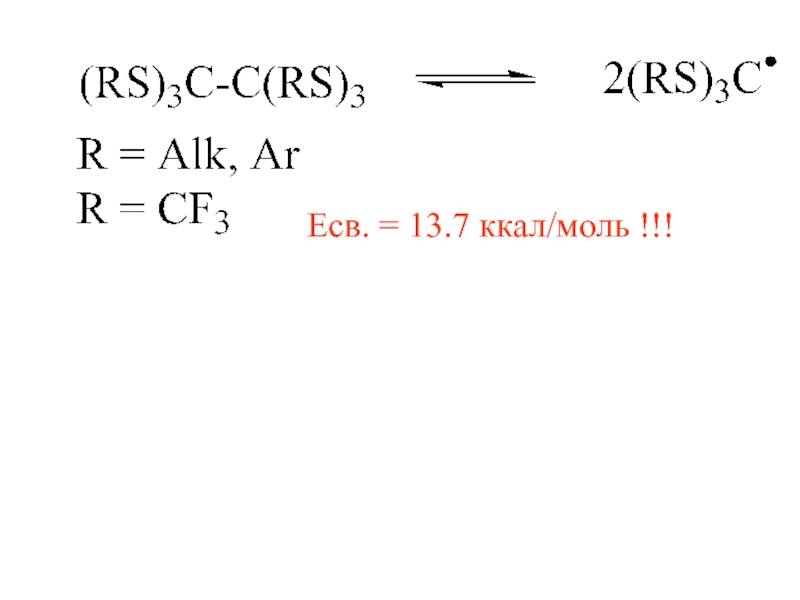
- 15. Есв. = 13.7 ккал/моль !!!
- 16. Устойчивые радикалы π−типаX-rayЭПРAng. Chem. Int 2003, 1723K. Schlosser et al. JACS 1979, 6283I
- 17. aH1 = 6.2GaH2 = 2Gg = 2.0018Из природных аппатитов при 300-450оССтабилен несколько месяцевЖСХ 2010, 788
- 18. Неклассические взаимодействия(0.72 + 3.53)/2 = 2.12IБлизок по строениюк классической структуре
- 19. Кинетическая устойчивость радикаловОпределяется энергиейВЗМО и стерическойдоступностью радикальногоцентра
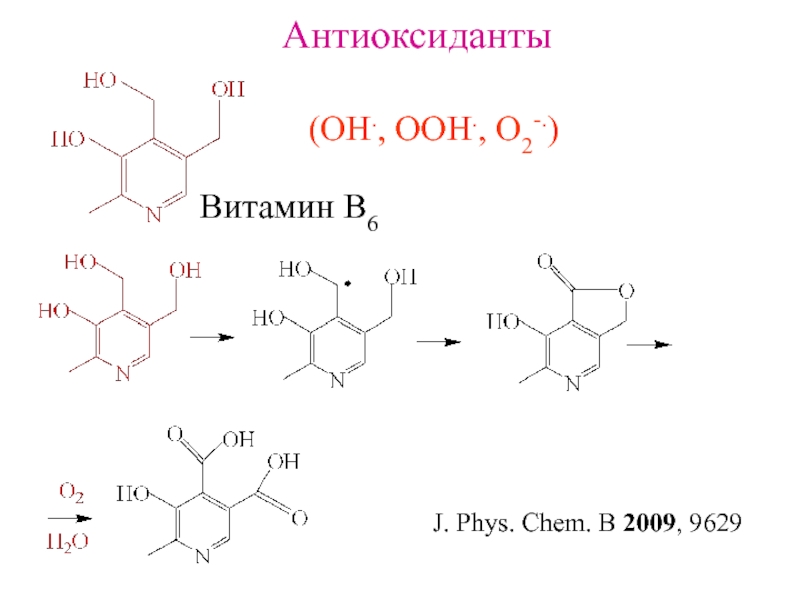
- 20. Антиоксиданты (OH., OOH., O2-.) Витамин B6J. Phys. Chem. B 2009, 9629
- 21. Термодинамическая устойчивостьR-H
- 22. Высокоспиновые системыЭПР g = 2.0023для органических магнитныхматериаловИКС
- 23. σ,σ,σ,σ−Радикалы (бенздиины)123Meyerson et al. J. Org. Chem.
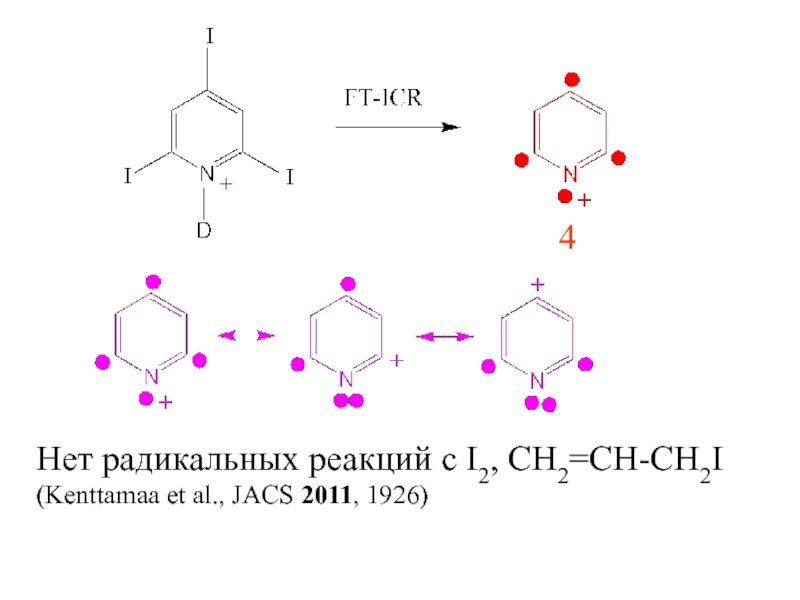
- 24. 4Нет радикальных реакций с I2, CH2=CH-CH2I(Kenttamaa et al., JACS 2011, 1926)
- 25. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Теоретические основы органической
химии
Строение и свойства свободных радикалов
Лекция 24
(электронно-лекционный курс)
Проф. Бородкин
Г.И.
Слайд 3OH-. , RO2., OH.
эндогенные повреждающие
агенты
Свободно-радикальная теория
старения
OH-.
реагирует с биомолекулами с диффузионными
скоростями
Увеличение O2 в атмосфере сокращает
жизньдрозофилы
Химические геропротекторы – вещества,
уменьшающие скорость старения живых
клеток
Слайд 5Методы генерации
1. Термические
трет-бутилпероксид
бензоилпероксид
τ1/2 = 2 часа (140оС); 35 сек. (180о)
τ1/2
= 0.5 часа (100оС)
Слайд 62. Каталитические методы
3. Фотохимические методы
Квантовый выход =
число прореагировавших
молекул
число погащенных квантов
λ = 254 нм φ = 1
313 нм φ = 0.7Слайд 8Алкильные радикалы
катион sp2
радикал sp2, sp3
анион sp3
СH3.
23G 38.5G sp2 π−типа
CH2F.
21.1G 54.8GCHF2. 22.2G 148.8G
CF3. 271.6G sp3
sp2, sp3
aH aC
Слайд 10Арильные и винильные радикалы
π−радикал
140-150o
π−радикал
Динамика по ЭПР
k-180o ~1010 сек-1
устойчива изогнутая
форма
Слайд 12Дифракция электронов: пропеллер, кольца
повернуты на 40-45о, р-орбитали С. и Ph
некопланарны
и перекрывание неполное
расчет спиновой
плотности
ЭПР
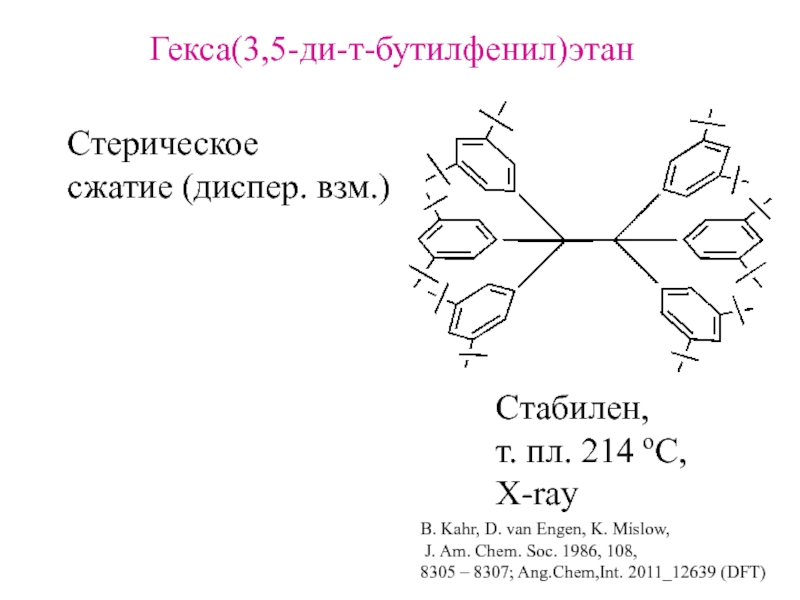
Слайд 14B. Kahr, D. van Engen, K. Mislow,
J. Am. Chem.
Soc. 1986, 108,
8305 – 8307; Ang.Chem,Int. 2011_12639 (DFT)
Cтабилен,
т. пл.
214 оС,X-ray
Стерическое
сжатие (диспер. взм.)
Гекса(3,5-ди-т-бутилфенил)этан
Слайд 16Устойчивые радикалы π−типа
X-ray
ЭПР
Ang. Chem. Int 2003, 1723
K. Schlosser et al.
JACS 1979, 6283
I
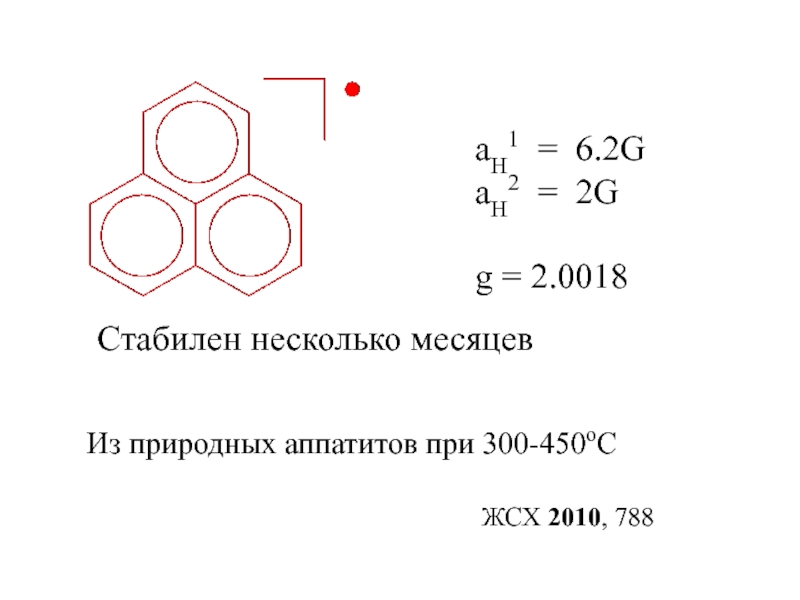
Слайд 17aH1 = 6.2G
aH2 = 2G
g = 2.0018
Из природных аппатитов при
300-450оС
Стабилен несколько месяцев
ЖСХ 2010, 788
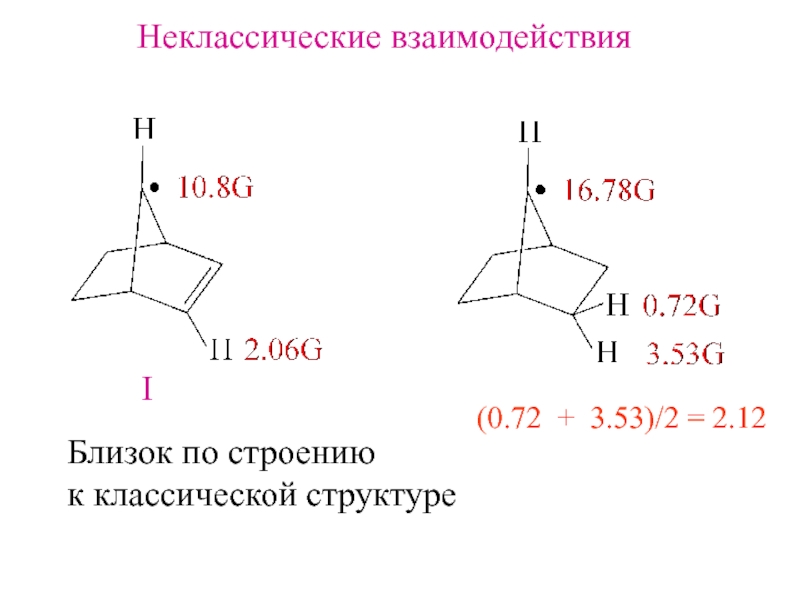
Слайд 18Неклассические взаимодействия
(0.72 + 3.53)/2 = 2.12
I
Близок по строению
к классической структуре
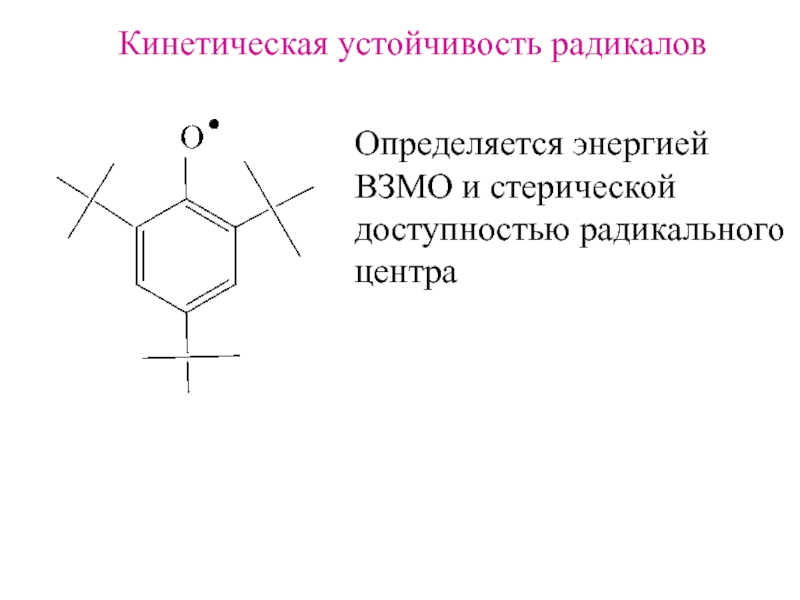
Слайд 19Кинетическая устойчивость радикалов
Определяется энергией
ВЗМО и стерической
доступностью радикального
центра
Слайд 21Термодинамическая устойчивость
R-H
R. + H.
RH
Eсв. ккал/мольPh-H 112
CH2=CH-H 104
CH3-H 104
Et-H 98
T-Bu-H 91
CH2=CH-CH2-H 88
PhCH2-H 85
Ph. >винил > Me. >
Et. > t-Bu. > бензил~
аллил
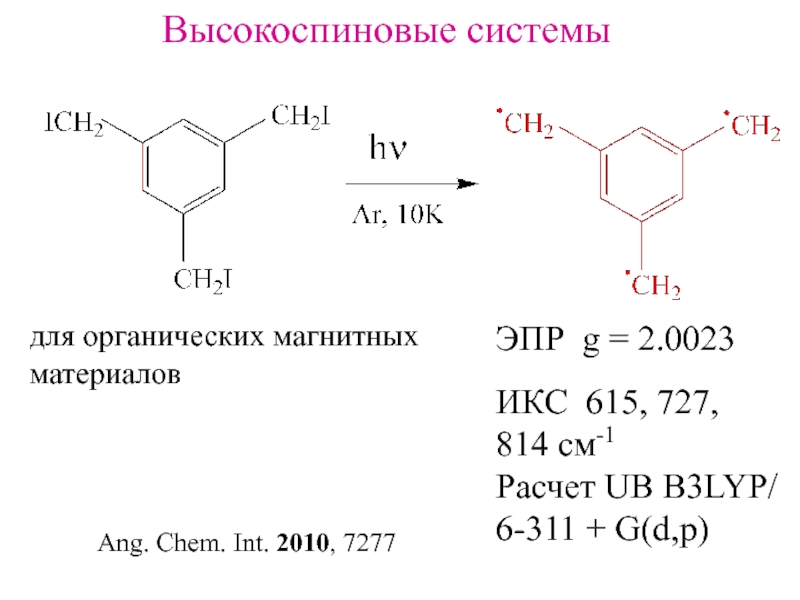
Слайд 22Высокоспиновые системы
ЭПР g = 2.0023
для органических магнитных
материалов
ИКС 615, 727,
814 см-1
Расчет
UB B3LYP/
6-311 + G(d,p)
Ang. Chem. Int. 2010, 7277
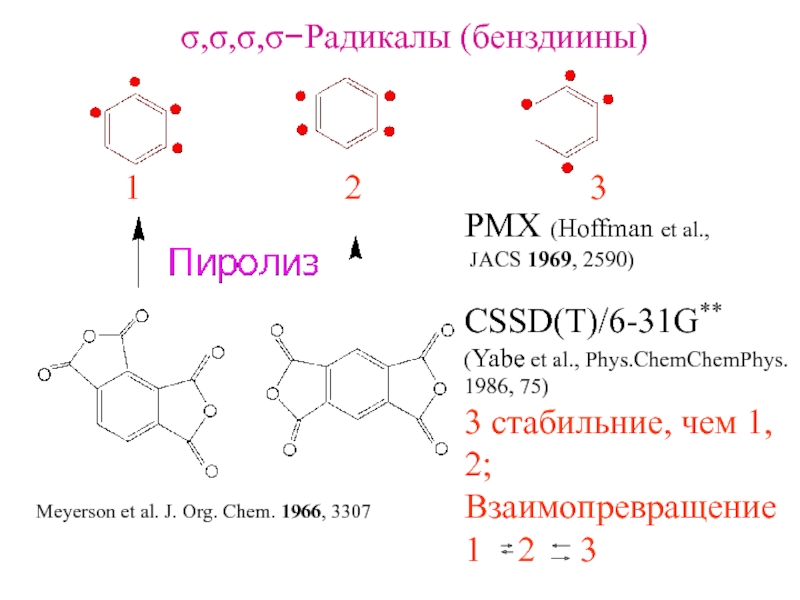
Слайд 23σ,σ,σ,σ−Радикалы (бенздиины)
1
2
3
Meyerson et al. J. Org. Chem. 1966, 3307
PMX
(Hoffman et al.,
JACS 1969, 2590)
CSSD(T)/6-31G**
(Yabe et al., Phys.ChemChemPhys.
1986, 75)
3
стабильние, чем 1, 2;Взаимопревращение
1 2 3