Слайд 1Свойства элементов III-й группы ПСЭ
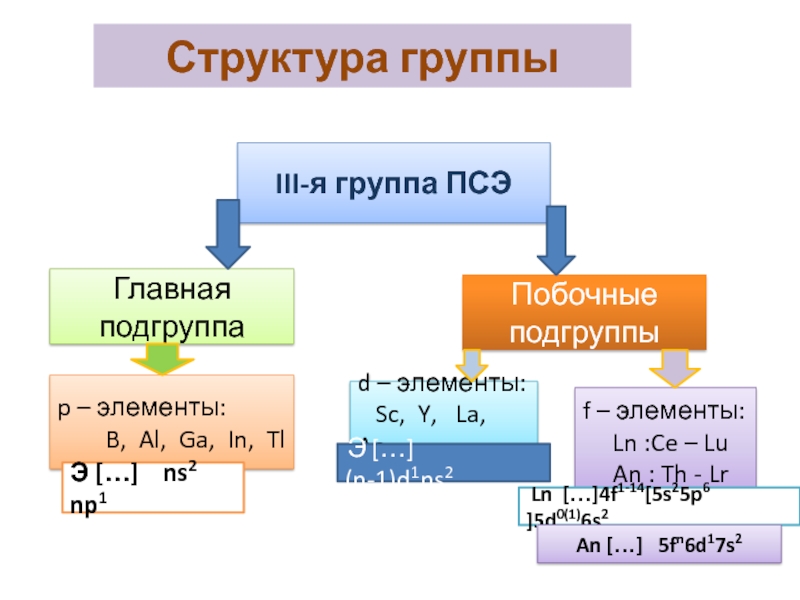
Слайд 2Структура группы
III-я группа ПСЭ
Главная подгруппа
Побочные подгруппы
p – элементы:
B, Al, Ga, In, Tl
d – элементы:
Sc, Y, La, Ac
f – элементы:
Ln :Ce – Lu
An : Th - Lr
Э […] ns2 np1
Э […] (n-1)d1ns2
Ln […]4f1-14[5s25p6 ]5d0(1)6s2
An […] 5fn6d17s2
Слайд 3
Свойства элементов III группы
Общие свойства:
Все элементы имеют общую валентность
III и общий состав химических соединений.
Элементы характеризуются металлическими свойствами ,за
исключением бора.
Для оксидов и гидроксидов характерны основные свойства ,кроме Al, Ga, Sc.
Элементы имеют подобные растворимые и нерастворимые соединения.
Слайд 4
Различные свойства
Элементы главной подгруппы имеют иное электронное строение.
Являются
p-элементами (менее активные металлы).
d- и f-
элементы имеют на внешнем уровне ns- два электрона, поэтому являются типичными металлами
Различие в свойствах элементов побочных подгрупп определяется электронным строением предшествующих электронных слоев.
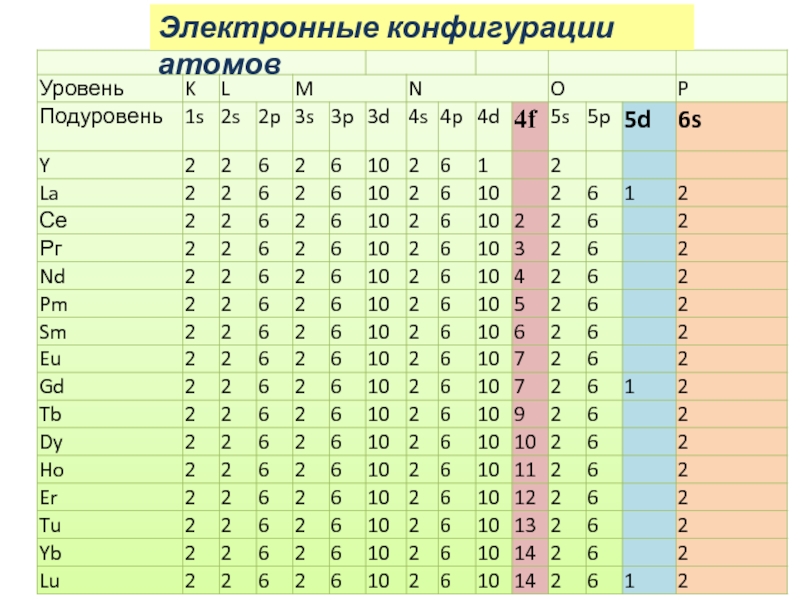
Слайд 5Электронные конфигурации атомов
Слайд 6Характеристика РЗЭ
Лантаноиды – элементы, следующие за лантаном и имеющие сходные
с ним свойства.
Лантаноиды относятся к f-элементам и имеют общее
электронное строение:
Ln […]4f1-14[5s25p6 ]5d0(1) 6s2
Лантан, гадолиний и лютеций склонны проявлять только валентность равную III
Церий, празеодим, тербий могут проявлять как валентность III, так и валентность IV
Самарий, Европий, иттербий могут проявлять валентность II
Радиусы атомов и ионов РЗЭ уменьшаются от La к Lu - эффект «лантаноидного сжатия»
Слайд 9Основные Химические свойства РЗЭ
На воздухе легкиеLnокисляются при комнатной t,остальные-при t=180-200
°С:
4Ln0+3O20 t2Ln2+3O3-2
Ln0-3еLn+3
O02+4е 2O-2
Се и богатые Се сплавы пирофорны.
Се0+О20Се+4О2-2
Се0-4еСе+4
O02+4е 2O-2
С
галогенами взаимодействуют при сравнительно невысокой температуре
2РЗЭ+3Cl2 t 2РЗЭCl3
РЗЭ0-3е РЗЭ+3
Cl02+2е 2Cl-
интенсивность взаимодействия уменьшается от фтора к йоду.
Слайд 104РЗЭ+2(OH)2+O02+2H2O4РЗЭ+3(O-2H)3
РЗЭ+2-е РЗЭ+3
O02+4е 2O-2
РЗЭ реагируют с водой (при нагревании – быстро).
2РЗЭ0+6H+2O
2РЗЭ+3(OH)3+3H02
РЗЭ0-3е РЗЭ+3
2H+ +2еH02
Замещаются металлами:
2РЗЭ+3Cl3+Ca0 t2РЗЭ0+3Ca+2Cl2
РЗЭ+3+3еРЗЭ0
Ca0-2еCa+2
Слайд 11При плавлении с серой, теллуром, селеном образуют сульфиды, теллуриды, хлориды.
2РЗЭ0+3S0+6O02
tРЗЭ+32(S-2O-24)3
С углеродом и углеродсодержащими газами образуют карбиды
РЗЭ2О3+7С t2РЗЭС2+3СО
РЗЭ2(CO3)3 t РЗЭ2O3+ 3CO2
РЗЭ2(C2O4)4 t РЗЭ2O3+ 5 CO+ 3CO2
с Н2(медленно- при комнатной температуре,
быстро–при надревании) образуют гидриды LnH3 и LnH2
2 Ln0+3H202Ln+3H3-
Ln0+H20LnH2- нестехиометрический гидрид
При нагревании до температуры красного каления реагируют с азотом, образуя нитриды LnN
2Ln0+3N20 +9О20 2Ln(NО3)3
Слайд 12РЗЭ реагируют с кислотами: соляной, серной, азотной.
2РЗЭ+3H2SO4РЗЭ2(SO4)3+3H2
РЗЭ0-3е РЗЭ+3
2H+ +2еH02
8РЗЭ0+30HN+5O33N-3H4NO3+8РЗЭ(NO3)3+9H2O
РЗЭ0-3е РЗЭ+3
N+5+8е
N-3
Реагируют с солями:
РЗЭ2(SO4)3 +3Na2CO3РЗЭ2(CO3)3 +3Na2 SO4
РЗЭ+3+3NH4FРЗЭ F3+3NH4+
Щелочи на них
не действуют даже при нагревании.
РЗЭ+NaOH tне идет
Слайд 13Редкоземельные металлы – хорошие восстановители;
2РЗЭ+3СО t 3C+РЗЭ2O3
4РЗЭ+3СО2 t 3C+2РЗЭ2O3
РЗЭ
образуют комплексные соединения:
Се(С2О4)2+2(NH4)2С2O4 (NH4)4[Се(С2О4)4](кч=8)
Слайд 15Cвойства церия
Электронная конфигурация атома церия
58Се [ ] 4f
2[5s25p6]5d06s2
Церий активный металл.
Церий взаимодействует при нагревании
с большинством неметаллов (O2, H2, N2, Cl2, C, S, P и т.д.) с образованием соответствующих бинарных соединений.
2Ce + N2 2CeN
Бурно взаимодействует с кислородом
Ce + O2 → CeO2
Слайд 16Хим. свойства церия
Реагирует с водой с выделением Н2.
В
ряду активности Церий и др. лантаноиды можно расположить между Са
и Mg.
Се +3Н2ОCe (OН)3+3H2
Карбонаты Церия горят на воздухе:
Ce+32(CO3)3 + O02 t Ce+4O2 + 6CO2.
Се+3-еСе+4 4 восстановитель Eвос=1.61 В;
O02 +4е2O-2 1 окислитель Еок=1.23 В;
E = Eок-Eвос =-0.38
Слайд 17Свойства соединений церия Ce3+.
Кислотно-основные свойства
Гидроксид в водных растворах проявляет
основной характер.
2Ce(OH)3+3H2SO4Ce2(SO4)3 + 3H2O
Ce(OH)3+NaOH;
Ce(NO3)3+3NaOH Ce(OH)3(бел.)+3NaNO3;
Получение малорастворимых солей
Церия(III)
2Ce(NO3)3+3(NH4)C2O4Ce2(C2O4)3(бел)+6NH4NO3;
2Ce(NO3)3+3Na2CO3 Ce2(CO3)3(бел)+6NaNO3;
Ce(NO3)3+Na3PO4 CePO4(бел)+3NaNO3;
Ce(NO3)3+3NaFCeF3(бел)+3NaNO3;
Слайд 18
Окислтельно-восстановительнык свойства
Ce3+ восстановитель
Переход Ce3+ + окислитель Ce4+
достаточно легко осуществим в водных растворах.
3Ce+3(OH)3 + KMn+7O4 + 2H2O
3Ce+4(OH)4 + Mn+4O2 + KOH(pН > 7)
Се+3-еСе+4 восстановитель Eвос=1.61 В; 3
Mn+7+3е Mn+4 окислитель Eок=0.6 В; 1
E = Eок-Eвос =1,01 В.
2Ce (NO3)3+NaBi+5O3+6HNO3 2Ce(NO3)4(ж.)+Bi+3(NO3)3+NaNO3+3H2O(pH<7)
Bi+5+2eBi+3 окислитель Eок=1.86 В; 1
Ce+3-eCe+4 восстановитель Eвос=1.61В; 2
E = Eок-Eвос = 0,25В.
Слайд 19Свойства Ce4+.
Кислотно - основные:
Слабые амфотерные свойства реализуются
Ce(OH)4 только при высоких температурах( при спекании с щелочью):
Ce(SO4)2(жёлт.)+4NaOHCe(OH)4(бел.)+2Na2SO4;
Ce(OH)4+NaOHводный
р-р;
Ce(OH)4 + 2NaOН t Na2CeO3 + 3H2O ;
Ce(OH)4 +2H2SO4 Ce(SO4)2 + 4H2O;
Слайд 20Окислительно-восстановительные свойстваCe(IV)
2Ce(SO4)2+2KI I2+K2SO4+Ce2(SO4)3 (pH
2
В 2I--2eI2 восстановитель Eвост=-0.54 В;
1
Ер=Еок-Евост=1.07 В;
2Ce(SO4)2+H2O2Ce2(SO4)3+O2+H2SO4
Ce+4+eCe+3 окислитель Еок=1.61 В; 2
2O-1-2eO20 восстановитель Евост=1.23 В; 1
Ер=Еок-Евост=0. 38 В.
Ионы Ce4+ сильные окислители в кислых средах:
2Ce+4(OH)4+8HCl-12Ce+3Cl3+Cl2+8H2O
Ce+4+eCe+3 окислитель Еок=1.61В; 2
2Cl-1-2eCl20 восстановитель Евост=1.36 В; 1
Ер=Еок-Евост=0,25 В;
Слайд 21Комплексообразование
Ce(C2O4)2 + 2(NH4)2C2O4 (NH4)4[Ce(C2O4)4]4-.
Ce2(C2O4)3 + (NH4)C2O4 не идёт.
ОтделениеCe
от других РЗЭ.
В основе — способность церия проявлять степень
окисления +4.
Ce(OH)3 + 3HCl CeCl3 + 3H2O.
РЗЭ(OH)3 + HCl РЗЭCl3 + 3H2O. (pH = 6,5)
2H2O+CeCl3+KMnO4+8NaOHCe(OH)4 +MnO2 +KCl+8NaCl
Слайд 22Качественные реакции на ионы церия.
Ce(NO3)3+3NH4OH Ce(OH)3(бел.)+3NH4NO3;
2Ce(OH)3+H2O22Ce(OH)4(желт.) (pH > 7);
Се+3-еСе+4 восстановитель Eвос=1.61 В;
1
H2O2+2е+2Н+НО-2+ОН-окислитель Еок=1.77 В; 1
Ер=Еок-Евост=0.16 В.
Ce(OH)4+H2O2Ce(OH)3(OOH)(оранж.)+H2O(pH > 7);
Слайд 24электронное строение
[Rn] 5f k 6d m 7s2,
где k изменяется
от 2 до 14,
а m равно 0 или 1
Различие
в энергиях 5f- и 6d-орбиталей меньше, чем 4f- и 5d-орбиталей
Слайд 26Радиусы атомов и ионов актиноидов уменьшаются с ростом порядкового номера.
По аналогии с лантаноидным, эффект называется
"актиноидное сжатие".
Слайд 27Химические свойства актиноидов
Обладают большой склонностью к комплексообразованию, особенно с
кислородсодержащими лигандами ;
В ряду легких актиноидов (от актиния до америция)
свойства элементов сильно различаются,
В ряду тяжелых актиноидов (от кюрия до лоуренсия) они в значительной степени аналогичны и похожи на свойства лантаноидов;
Слайд 28Склонность к гидролизу для каждого типа ионов M3+, M4+, MO2+
и MO22+ повышается с ростом атомного номера элемента;
В водных растворах
актиноиды образуют разнообразные ацидокомплексы, в которых часто проявляет координационное число, равное 8,
Na4[U(C2O4)4] и Na4[Th(CO3)4].
Для катионов склонность к комплексообразованию снижается в ряду
M4+ > MO22+ ≥ M3+ > MO2+,
а при замене лиганда - в рядах фторид > нитрат > хлорид > перхлорат и карбонат > оксалат > сульфат;
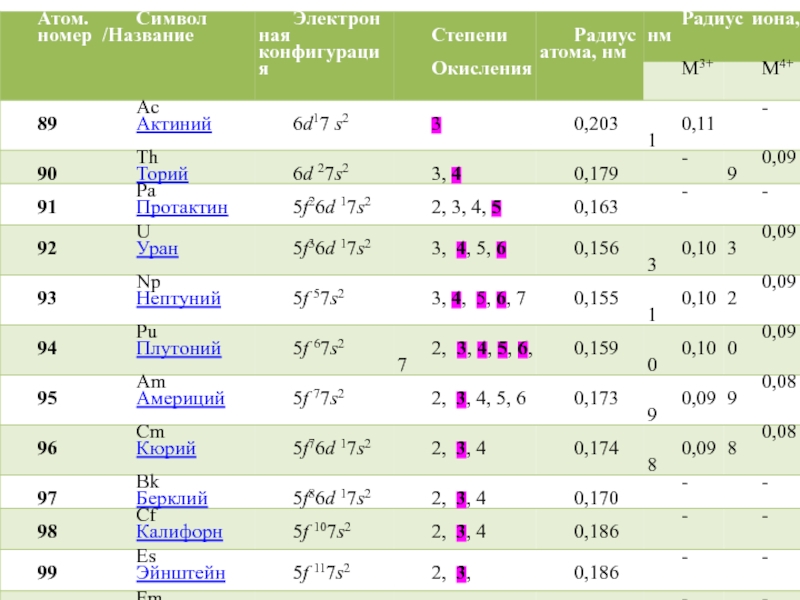
Слайд 29Свойства тория
Природный торий содержит практически один изотоп 232Th,
период полураспада
равен 1,4·1010 лет
Электронная формула 6d 2 7s2
Основная степень
окисления +4,
Слайд 30Свойства тория
Торий — активный металл, по реакционной способности близкий к
лантаноидам, но отличается от них степенью окисления
При нагревании торий реагирует
со многими неметаллами:
O2.. Н2, С, Cl2, Br2, S, N2.
Слайд 31Торий взаимодействует с азотом при 800 °C с образованием нитрида
тория ThN,
2Th + N2 2ThN
Взаимодействия тория
с углеродом
Th + C ThC
Th + 2C ThC2
карбиды разлагаются водой с образованием углеводородов.
ThC + H2O Th(OH)4 + CH4↑
ThC2 + H2O Th(OH)4 + C2H4↑
Слайд 32Взаимодействие тория с водой, кислотами
Торий - ативный восстановитель (Е о
= -1,9 В)
Торий вытесняет водород из кипящей воды
Th + 4H2O Th(OH)4 + 2H2↑
медленно растворяется в разбавленных фтороводородной, азотной или серной кислотах
Th +2H2SO4(разб) Th (SO4)2 + 2H2↑
Th + 4HF(разб) ThF4 + 2H2↑
Слайд 33Соединения тория (IV)
Th(OH)4 - имеет основной характер
Th (SO4)2 +
4NH4OH → Th (OH)4↓ +2(NH4)2SO4
Th (OH)4↓
ThO2 + 2H2O
Th (OH)4↓ + 4HCl(разб) ThCl4 + 2H2O
Th (OH)4↓ + CO2 → Th OCO3↓ + H2O
к растворимым в воде соединениям относятся нитраты, хлориды и сульфаты тория (IV)
Гидролиз солей
Th(NO3)4 + H2O ThO(NO3)2 + 2HNO3
Th(NO3)4 + 2Na2 CO3 + H2O ThO CO3 + H2CO3 + 4NaNO3
Слайд 34комплексообразование
В водных растворах торий образует комплексные соединения с КЧ=6, 8
и реже 10 или 12. Комплексообразование используют для растворения труднорастворимых
соединений тория (карбонатов, оксалатов).
ThOCO3↓ + 3Na2CO3 + H2O → Na4[Th(CO3)4] + 2NaOH
Th(C2O4)2 ↓ + 2(NH4)2C2O4 → (NH4)4[Th(C2O4)4]
Слайд 35Получение тория
минерал монацит вскрывают сернокислотным или щелочным способом
Th3(PO4)4+12NaOH
→ 3Th(OH)4↓+4Na3PO4
оксид тория ThO2 подвергают металлотермическому восстановлению кальцием в атмосфере
инертного газа:
ThO2+2Ca Th + 2CaO
электролиз расплава галогенида тория
ThF4 или ThCl4.
Слайд 37Уран
Уран — самый тяжелый из встречающихся в природе элементов
Его содержание
в земной коре составляет 3·10-4 % по массе
Он имеет три
изотопа: 99,28% природного урана составляет изотоп 238U, период полураспада которого равен 4,5·109 лет;
0,715 % – изотоп 235U с периодом полураспада 7,1·108 лет;
0,005 % – изотоп 234U с периодом полураспада 2,47·105 лет.
Изотоп 233U получен в результате ядерных реакций.
Слайд 38Электронное строение и СО урана
U 5f 36d 17s2
степени
окисления от +3 , +4, +5, +6,
наиболее устойчивыми среди
них являются степени окисления +4 и +6
в степени окисления +6 – амфотерные свойства;
Его температура плавления равна 1132 °C
Он химически активен и реагирует со многими элементами периодической системы.
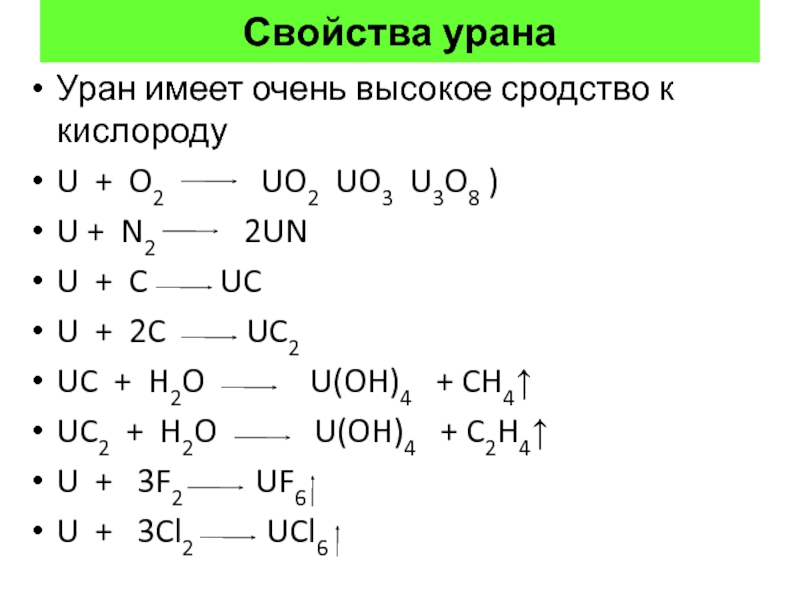
Слайд 39Свойства урана
Уран имеет очень высокое сродство к кислороду
U + O2
UO2
UO3 U3O8 )
U + N2 2UN
U + C UC
U + 2C UC2
UC + H2O U(OH)4 + CH4↑
UC2 + H2O U(OH)4 + C2H4↑
U + 3F2 UF6
U + 3Cl2 UCl6
Слайд 40Свойства U(IV)
Безводный тетрафторид получают из диоксида урана
UO2+4HF UF4↓+2H2O
восстановлением гексафторида урана различными восстановителями,
например, водородом
UF6+H2 UF4↓+2HF
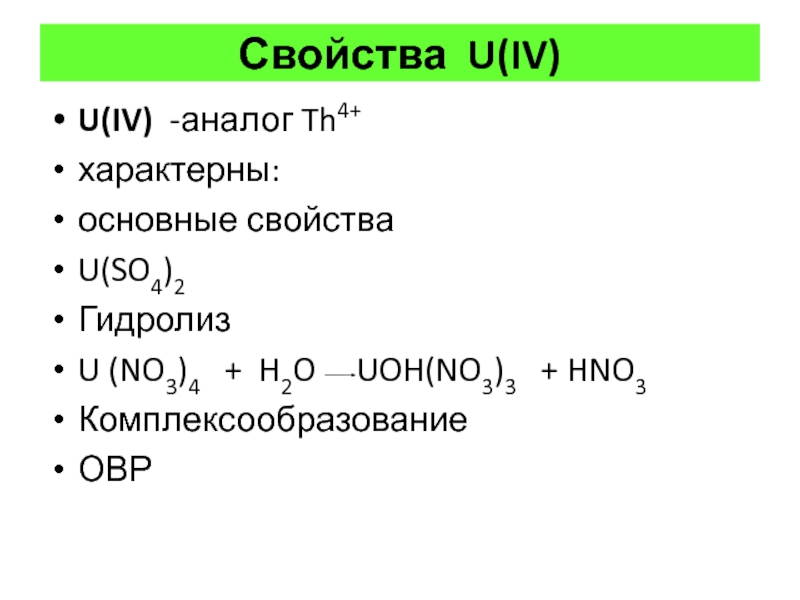
Слайд 41Свойства U(IV)
U(IV) -аналог Th4+
характерны:
основные свойства
U(SO4)2
Гидролиз
U (NO3)4 +
H2O UOH(NO3)3 + HNO3
Комплексообразование
ОВР
Слайд 42Под действием окислителей уран (IV) переходит в уран (VI)
U(SO4)2 + 2Ce(SO4)2 + 2H2O → UO2SO4 + Ce2(SO4)3
+ 2H2SO4
2U(SO4)2 + 2KMnO4 + 2H2O → 5UO2SO4 + 2MnSO4 + KHSO4 + H2SO4
Под действием восстановителей уран (IV) переходит в уран (I I I)
2U(SO4)2 + Zn + → U2(SO4)3 + ZnSO4
Слайд 43Свойства U(VI)
Гидролиз солей:
UCl6 + 2H2O →
UO2Cl2 + 4HCl
Амфотерность
при растворении в кислотах образуются соли диоксоурана
UO2(OH)2 + H2SO4 → UO2SO4 + 2H2O
при растворении в концентрированных щелочах – уранаты
UO2(OH)2 +2NaOH → Na2UO4 + 2H2O
или диуранаты
2UO2(OH)2 +2NaOH → Na2U2O7 + 3H2O
Слайд 44комплексообразование
Трикарбонатный комплекс катиона диоксоурана хорошо растворим
UO2SO4 + 3Na2CO3
→ Na4[UO2(CO3)3] + Na2 SO4
(NH4)2U2O7↓ + 6(NH4)2CO3
+ 3H2O → 2(NH4)4[UO2(CO3)3] + 6 NaOH
В карбонатных комплексах иона диоксоурана два координационных места заняты атомами кислорода
Слайд 45Окислительно-восстановительные свойства
U6+ окислитель
восстановление шестивалентного урана проводят электрохимически или
с использованием таких металлов, как железо или цинк:
UO2SO4 + Zn
+ 2H2SO4 → U(SO4)2 + ZnSO4 + 2H2O
Слайд 46Получение и очистка урана
Металлический уран получают восстановлением тетрафторида урана UF4
кальцием или магнием в инертной атмосфере:
UF4+2Ca U+2CaF2
Слайд 47 Получение урана
Для урана
известно около 200 минералов
промышленное значение имеет минерал настуран (урановая
смолка) U3O8
урановую смоляную руду, обрабатывают минеральными кислотами, например азотной или серной кислотой, в присутствии MnO2, для окисления урана(IV):
U3O8 + MnO2 + 4H2SO4 → MnSO4 + 3UO2SO4 + 4H2O
Слайд 48Карбонатная очистка
Трикарбонатный комплекс катиона диоксоурана хорошо растворим и используется в
технологии для отделения урана от металлов, образующих труднорастворимые карбонаты или
гидроксиды
UO2SO4 + 3Na2CO3 → Na4[UO2(CO3)3] + Na2 SO4
Слайд 49применение
расщепляющие материалы, к которым относятся изотопы урана 235U, 233U, плутония
239Pu и 241Pu
в природе встречается только 235U
за один акт деления
урана в расчете на 1 г ядерного топлива выделяется около 180 МэВ, что соответствует 7,4·107 кДж.










 Редкоземельные металлы – хорошие восстановители; 2РЗЭ+3СО t 3C+РЗЭ2O34РЗЭ+3СО2 t 3C+2РЗЭ2O3РЗЭ образуют комплексные соединения:Се(С2О4)2+2(NH4)2С2O4 (NH4)4[Се(С2О4)4](кч=8)](/img/thumbs/b8cfad73b3a4853986efaa52622d3a5a-800x.jpg)

![Свойства элементов III - й группы ПСЭ Cвойства церияЭлектронная конфигурация атома церия 58Се [ ] 4f 2[5s25p6]5d06s2 Cвойства церияЭлектронная конфигурация атома церия 58Се [ ] 4f 2[5s25p6]5d06s2 Церий активный металл. Церий](/img/thumbs/30ea40490513e9c12537907a6b4d1d5a-800x.jpg)





![Свойства элементов III - й группы ПСЭ КомплексообразованиеCe(C2O4)2 + 2(NH4)2C2O4 (NH4)4[Ce(C2O4)4]4-. Ce2(C2O4)3 + (NH4)C2O4 не идёт.ОтделениеCe от КомплексообразованиеCe(C2O4)2 + 2(NH4)2C2O4 (NH4)4[Ce(C2O4)4]4-. Ce2(C2O4)3 + (NH4)C2O4 не идёт.ОтделениеCe от других РЗЭ. В основе — способность](/img/thumbs/974a66fd71dec0218053421229b0c4d5-800x.jpg)


![Свойства элементов III - й группы ПСЭ электронное строение[Rn] 5f k 6d m 7s2, где k изменяется от электронное строение[Rn] 5f k 6d m 7s2, где k изменяется от 2 до 14, а m равно](/img/thumbs/ee7f5e891d9fe4259c5ea91675678c0f-800x.jpg)
















![Свойства элементов III - й группы ПСЭ комплексообразованиеТрикарбонатный комплекс катиона диоксоурана хорошо растворим UO2SO4 + 3Na2CO3 → Na4[UO2(CO3)3] комплексообразованиеТрикарбонатный комплекс катиона диоксоурана хорошо растворим UO2SO4 + 3Na2CO3 → Na4[UO2(CO3)3] + Na2](/img/thumbs/8001b21eb9e602c77b62bfc8c2a588ce-800x.jpg)


























