Слайд 1Титан и его сплавы
Кристаллическая структура и свойства титана.
Влияние примесей на
свойства титана.
Классификация примесей и легирующих элементов в титане.
Особенности структуры титановых
сплавов при деформации и термической обработке.
Литейные и деформируемые титановые сплавы.
Слайд 2История открытия и промышленного применения
Открыт в 1789 г. Клапротом.
В 1925
г. Baн Аркелем и де Бур получили иодидный титан.
В 1940
г. Кролль открыл магниетермический способ извлечения титана из руд.
В 1948 г. получена первая промышленная партия титана массой 2 т.
В 1953 г. было получено 2100 т титана;
в 1957 г. - 20000 т; в 1966 г. - 22000 т; в 1981 г – 55000 т; в 1996 г. – 66000 т.
Слайд 3Преимущества титана
распространенность в земной коре : (0,60%) четвертое место после
алюминия (8,8 %), железа (5,1%) и магния (2,1%);
небольшая плотность при
высокой удельной прочности;
необычайно высокая коррозионная стойкостью;
значительная прочность при повышенных температурах;
рабочие температуры: от –196 до 500оС, до 650 оС кратковременно.
Среди конструкционных металлов титан по распространенности занимает четвертое место, уступая лишь алюминию, железу и магнию.
Слайд 4Недостатки титана
большая склонность к водородной хрупкости и солевой коррозии;
высокая
химическая активность, в частности, активное взаимодействие с газами при повышенных
температурах и в жидком состоянии;
невысокие антифрикционные свойства (налипание);
плохая обрабатываемость резанием, сравнимую с нержавеющей сталью аустенитного класса;
трудности вовлечения отходов в производство.
Широкое применение титана сдерживается в основном высокой его стоимостью (губка – 4.500$/т, слиток – 7.000 $/т).
Слайд 5Применение титана и его сплавов (продолжение)
Судостроение: гребные винты; обшивка морских
судов, подводных лодок, торпед…
Криогенная техника.
Химическая, нефтехимическая, пищевая, электроника, ядерная техника.
Медицина:
инструмент, имплантанты.
Спорт, украшения.
Вооружения: броневые плиты, некоторые элементы боеприпасов.
Слайд 6Свойства титана
Четырехвалентный элемент, атомный номер 22.
Плотность низкотемпературной модификации 4,
505 г/см3.
Температура плавления 1668 °С.
Температура полиморфного превращения 882,5 °С.
Коэффициент линейного
расширения при 24° С 8,15 10-6 К -1 .
Удельное электросопротивление при 20° С 4510-6 Омсм.
Модуль нормальной упругости 146 ГПа.
При 0,45К титан становится сверхпроводником.
Титан – парамагнитный металл.
Слайд 7Коррозионные свойства титана
Титан — химически активный металл
обладает исключительно высоким
сопротивлением коррозии (выще нержавеющих сталей), что объясняется образованием на поверхности
металла плотной защитной окисной пленки.
реагирует с: плавиковой, соляной, серной и ортофосфорной, щавелевой, три-хлоруксусной и трифторуксусной.
стоек в тех средах, которые не разрушают защитную окисную пленку на его поверхности, и особенно в тех средах, которые способствуют ее образованию.
отличается чрезвычайно высокой коррозионной стойкостью в морской воде.
Слайд 8Коррозионные свойства титана (продолжение)
при высоких температурах активно взаимодействует с большинством
веществ, особенно с газами: кислородом, азотом, водородом, окисью углерода, двуокисью
углерода, водяным паром, аммиаком.
Титан при низких температурах абсорбирует чрезвычайно большие количества водорода. Например, при температуре 600°С и давлении 0,1 МПа титан поглощает 32000 см3/100г водорода, в то время как железо при той же температуре абсорбирует всего 1,31 см3/100г, а алюминий 0,026 см3/100г. Абсорбция водорода титаном — процесс обратимый. Вакуумный отжиг легко устраняет водород.
Слайд 9-стабилизаторы - элементы, повышающие стабильность -фазы. -стабилизаторы: Al, Ga и
In; C, O, N. (а)
- стабилизаторы - элементы, повышающие
стабильность
- фазы; две подгруппы:
1) при достаточно низкой температуре происходит эвтектоидный распад -фазы: ; эвтектоиднобразующими - стабилизаторы: Cr, Mn, Fe, Cu, Ni, Pb, Be, Co (б);
2) -твердый раствор сохраняется до комнатной температуры, не претерпевая эвтектоидного распада; изоморфные
-стабилизаторы: V, Mo, Nb, Ta (в); W (г);
Нейтральные упрочнители (мало влияют на устойчивость - и - фаз): Sn, Zr, Ge, Hf и Th.
а
б
в
г
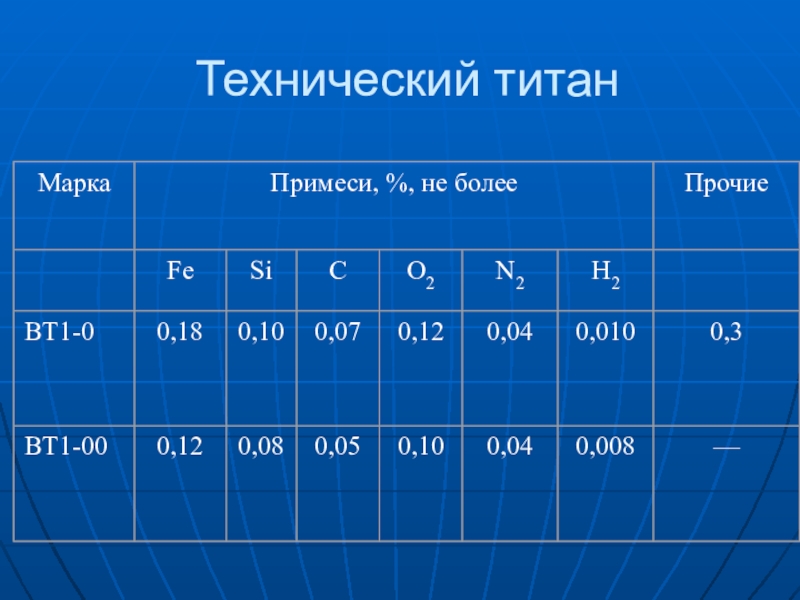
Слайд 10Влияние примесей
образующие с титаном растворы внедрения (кислород, азот, углерод, водород);
образующие
с титаном растворы замещения (железо и кремний).
примеси внедрения значительно
более сильно влияют на свойства титана, чем примеси замещения.
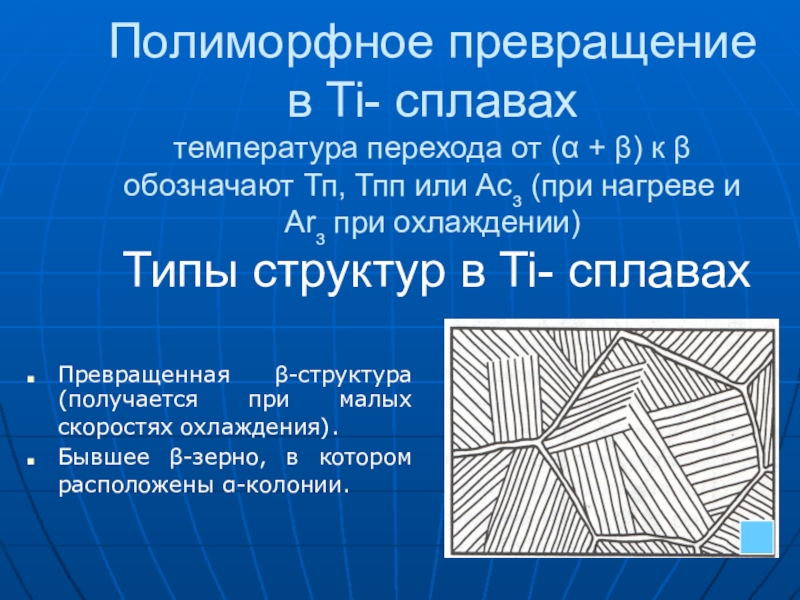
Слайд 12Полиморфное превращение в Ti- сплавах
температура перехода от ( +
) к обозначают Тп, Тпп или Асз (при нагреве
и Аrз при охлаждении)
Типы структур в Ti- сплавах
Превращенная -структура (получается при малых скоростях охлаждения).
Бывшее -зерно, в котором расположены -колонии.
Слайд 13Типы структур в Ti- сплавах
(продолжение)
Смешанная или дуплексная структура (получается
при нагреве в + область и последующем медленном охлаждении).
Состоит
из первичной -фазы и - превращенной матрицы.
Слайд 14Классификация титана и его сплавов
-Ti сплавы, структура которых представлена
-фазой;
псевдо--сплавы, структура которых представлена в основном -фазой и небольшим количеством
-фазы (не более 5%);
(+)-сплавы, структура которых представлена в основном и -фазами;
псевдо--сплавы со структурой в отожженном состоянии, представленной -фазой и большим количеством -фазы; в этих сплавах закалкой или нормализацией из -области можно легко получить однофазную -структуру;
-сплавы, структура которых представлена термодинамически стабильной -фазой.
Слайд 15Классификация Ti-сплавов по структуре в
закаленном состоянии
Сплавы мартенситного класса, структура
которых после закалки из -области представлена -или - мартенситом;
сплавы переходного класса, структура которых после закалки с температур -области представлена мартенситом () и -фазой, независимо от того образовалась в ней или нет -фаза;
-сплавы, структура которых после закалки представлена - или ()-фазами.
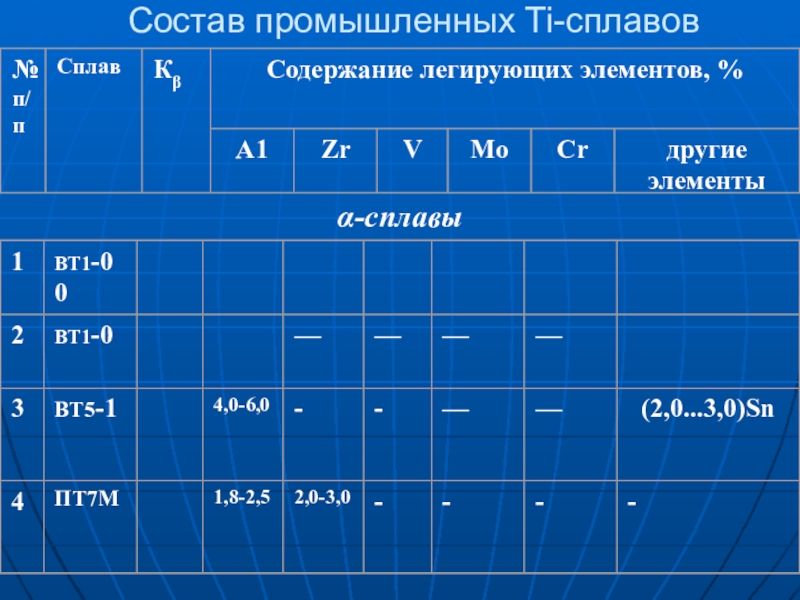
Слайд 16Состав промышленных Ti-сплавов
-сплавы
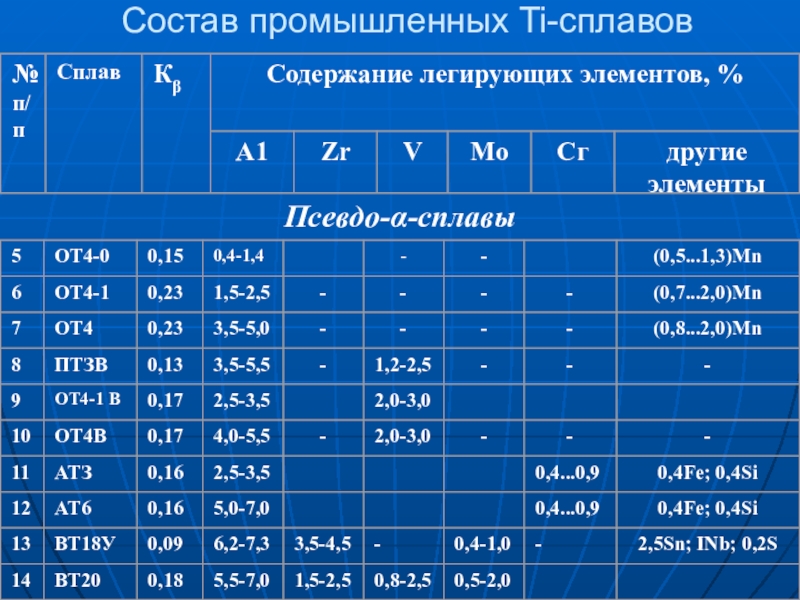
Слайд 17Состав промышленных Ti-сплавов
Псевдо--сплавы
Слайд 18Состав промышленных Ti-сплавов
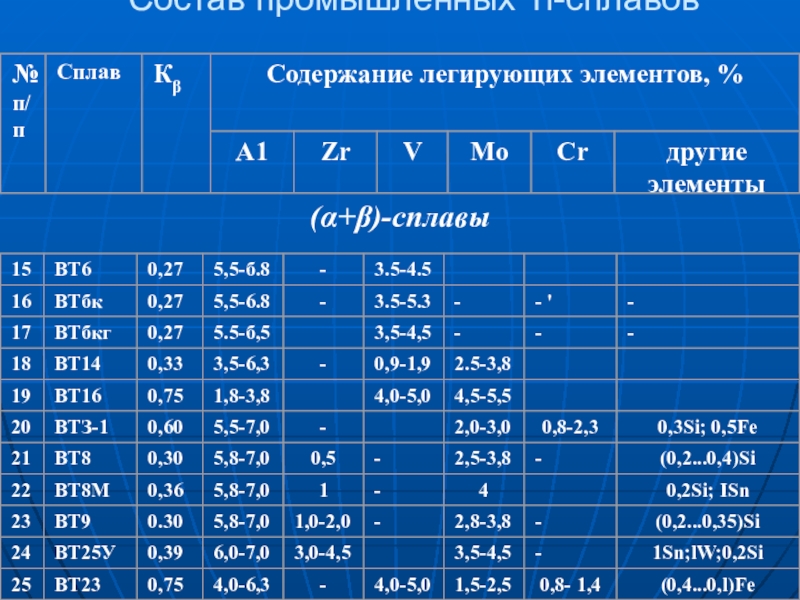
(+)-сплавы
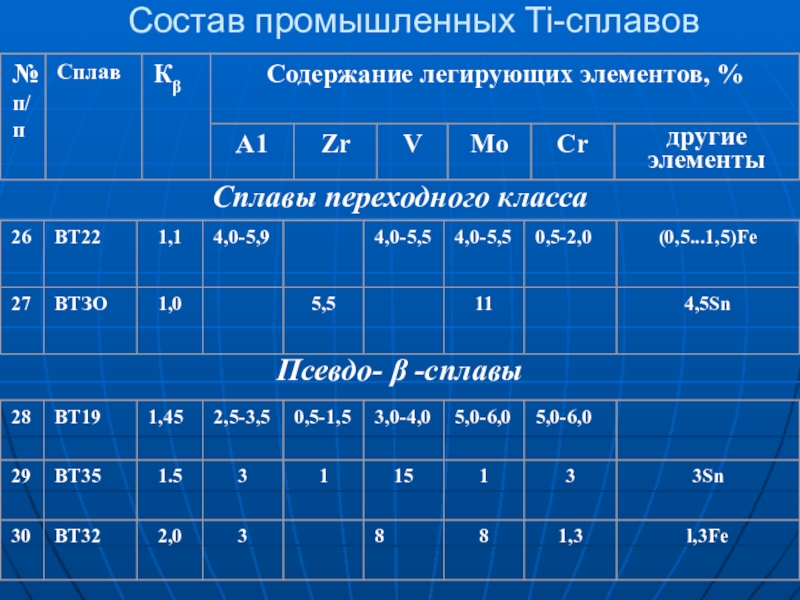
Слайд 19Состав промышленных Ti-сплавов
Сплавы переходного класса
Псевдо- -сплавы