Слайд 1Влияние ожирения на мужское репродуктивное здоровье
Князева Екатерина Сергеевна
615 группа
ek98@list.ru
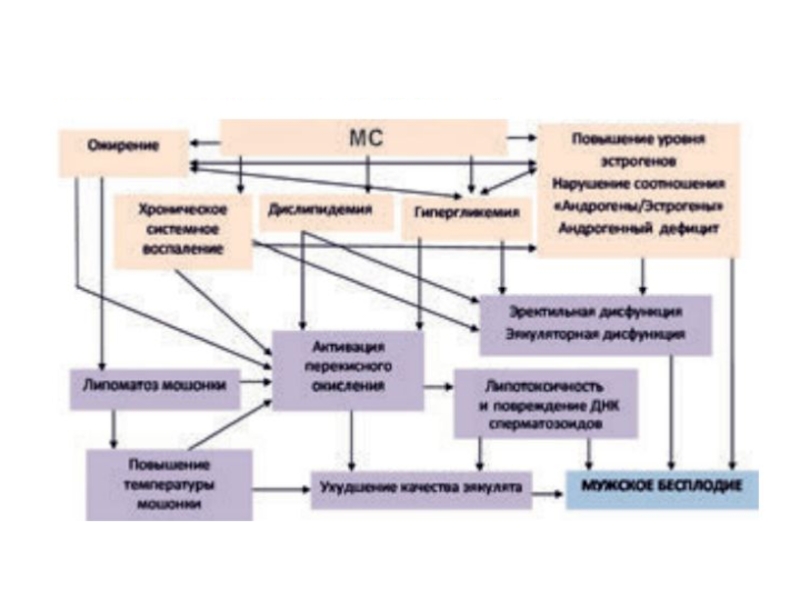
Слайд 2Метаболический синдром
МС – это сочетание абдоминального ожирения, инсулинорезистентности или СД-2,
атерогенной дислипидемии, артериальной гипертонии, нарушений системы гемостаза, эндотелиальной дисфункции и
хронического субклинического воспаления.
Ожирение и ИР/СД-2 являются ключевыми компонентами МС.
Снижение уровня тестостерона – новый патогенетически важный компонент МС у мужчин, так как частота и выраженность андрогенного дефицита у мужчин находятся в достоверной обратной связи с частотой и выраженностью ожирения и нарушений углеводного обмена (ИР и СД-2)
Слайд 3Ожирение
Ожирение – ключевой компонент МС, который имеет четкие диагностические критерии:
при окружности талии у европейского мужчины >94 см любым специалистом
должен быть поставлен диагноз «ожирение»
Код в МКБ-10 Е.66
Однако негативный вклад ожирения в патогенез мужского бесплодия до сих пор явно не дооценивается в рутинной клинической практике
Слайд 4Жировая ткань – эндокринный орган
Жировая ткань – активный, самостоятельный и
самым большой эндокринный орган, который секретирует целый ряд адипокинов
Адипокины
- биологически активные пептиды, оказывающие свое действие как локально, так и системно
В жировой ткани вырабатывается более 100 гормонов, ферментов, провоспалительных цитокинов и других биологически активных веществ, играющих разностороннюю роль в регуляции метаболизма человека
Наибольший негативный эффект жировой ткани у мужчин связывают с ее гормоном лептином
Слайд 5Лептин
Лептин («голос жировой ткани») – белок, синтезируемый и секретируемый адипоцитами
жировой ткани
Лептин регулирует потребление и расход энергии посредством влияния
на гипоталамус: воздействуя на гипоталамический центр насыщения, избыток лептина повышает тонус симпатической нервной системы, усиливает термогенез в адипоцитах, подавляет синтез инсулина, снижает транспорт глюкозы в клетку
При ожирении лептин андрогенный дефицит за счет:
снижения чувствительности андрогеновых рецепторов к тестостерону
блокады синтеза лютеинизирующего гормона в гипофизе
усиления ароматизации тестостерона в эстрадиол под влиянием ароматазы в периферических тканях (прежде всего в адипоцитах)
Слайд 6Липотоксичность
Синергизм эффектов патологических процессов ведет к глубоким нарушениям репродуктивной системы
у мужчин с ожирением: в клетках Лейдига наблюдается нарушение цепи
трансформации холестерина под влиянием цитохрома Р-450 за счет способности ФНОα и интерлейкина-1 ингибировать стероидогенез, что ведет к его угнетению
Таким образом, можно говорить о липотоксичности жировой ткани, которая, являясь фактором индукции и прогрессирования системного оксидативного стресса, приводит к митохондриальной дисфункции герминогенного эпителия у мужчин с ожирением, т. е. к формированию ОСС
Слайд 7Оксидативный стресс сперматозоидов
ОСС обусловлен гиперпродукцией в семенной плазме активных форм
кислорода (АФК) (озон, свободные радикалы, перекись водорода и т. д.)
В норме АФК присутствуют в семенной плазме и выступают как физиологические регуляторы функций сперматозоидов:
-активация акросомальной реакции
-регуляция биохимических окислительно-восстановительных реакций
-элиминация биологически чужеродных белков
Слайд 8Однако при лавинообразном и неконтролируемом увеличении концентрации АФК в семенной
плазме наблюдается обратный эффект: формируется спермальный оксидативный стресс повреждение
и дестабилизации мембран сперматозоидов, нарушение упаковки и целостности ДНК в их хромосомах, инициация апоптоза сперматозоидов нарушения их морфологии, подвижности и концентрации
Таким образом, ОСС развивается при нарушении динамического равновесия между окислителями и антиоксидантами в семенной плазме, а его частота при мужском бесплодии достигает 30–80 %
Слайд 9Скротальные нарушения
Ожирение может увеличивать скротальную температуру, что стимулирует синтез АФК
и вызывает повреждение свободными радикалами сперматозоидов с преобладанием явлений их
апоптоза
Липоматоз мошонки может быть одной из основных причин нарушения сперматогенеза у мужчин с ожирением.
При исследовании мошонки у мужчин с идиопатическим бесплодием выявили, что у тучных пациентов есть избыточное отложение жира в мошонке, которое они связали с повышением температуры в мошонке, венозным застоем и высоким расположением яичка в мошонке на фоне ожирения.
После выполнения скротальной липэктомии у большинства бесплодных мужчин с ожирением получены положительные результаты в виде улучшения морфологии и оплодотворяющей способности эякулята.
Слайд 10Тестикулярная дисфункция
Негативное влияние ожирения на тестикулярную функцию проявляется в уменьшении
уровня общего тестостерона и глобулина, связывающего половые стероиды, при этом
гормоны жировой ткани лептин, резистин и грелин играют наиболее важную роль.
P.M. Mah и G.A. Wittert (2010) приводят аналогичные данные
о том, что ожирение у мужчин достоверно ассоциируется с низким уровнем общего и свободного тестостерона крови, что, в свою очередь, повышает риск развития как ИР, так и СД-2
Слайд 11Мировые исследования
Ретроспективные исследования показали, что индекс массы тела (ИМТ)
> 25 кг/м2 у мужчин достоверно повышает частоту бесплодия по
сравнению с мужчинами, у которых ИМТ < 20 кг/м2, даже после многочисленных ранжировок по возрасту, ИМТ партнера и частоте половых актов.
Согласно данным японских исследователей, у мужчин с высоким ИМТ меньше возможность зачатия ребенка по сравнению с мужчинами с более низким ИМТ, даже после ранжировок по возрасту, липидному спектру и уровню гликированного гемоглобина HbA1c крови.
По данным перекрестного исследования QATAR, частота бесплодия у мужчин с ожирением (ИМТ > 30 кг/м2) и СД-2 оказалась более чем в 3 раза выше, чем у мужчин с нормальной массой тела (ИМТ < 25 кг/м2).
Слайд 14Список литературы
Божедомов В.А., Ушакова И.В., Спори ш Е.А. и др.
Роль гиперпродукции
активных форм кислорода в мужском бесплодии и возможности антиоксидантной
терапии (обзор литературы). Consilium Medicum 2012;7:51–5.
2. Тюзиков И.А., Калинченко С.Ю., Марто в А.Г. Роль коррекции метаболического статуса при репродуктивных нарушениях у мужчин. Материалы X Всероссийского Форума с международным участием «Мужское здоровье и долголетие». М., 2012. С. 95–6. 60.
3. Аляев Ю.Г., Алленов С.Н., Кулаков а Е.В. и др. Стресс и инфертильность: психологические аспекты бесплодия. Материалы IV Конгресса «Мужское здоровье». М., 2008. С. 198–9.
4. Fujii J., Tsunoda S. Redox regulation of fertilisation and the spermatogenic process. Asian J Androl 2011;13(3):420–3.
5. Sarkar O., Bahrainwala J., Chandrasekaran S. et al. Impact of inflammation on male fertility. Front Biosci (Elite Ed) 2011;3:89–95.
6. Alberti G. Introduction to the metabolic syndrome. Eur Heart J 2005; 7(Suppl D):D3–5.