Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Введение в специальность
Содержание
- 1. Введение в специальность
- 2. Введение
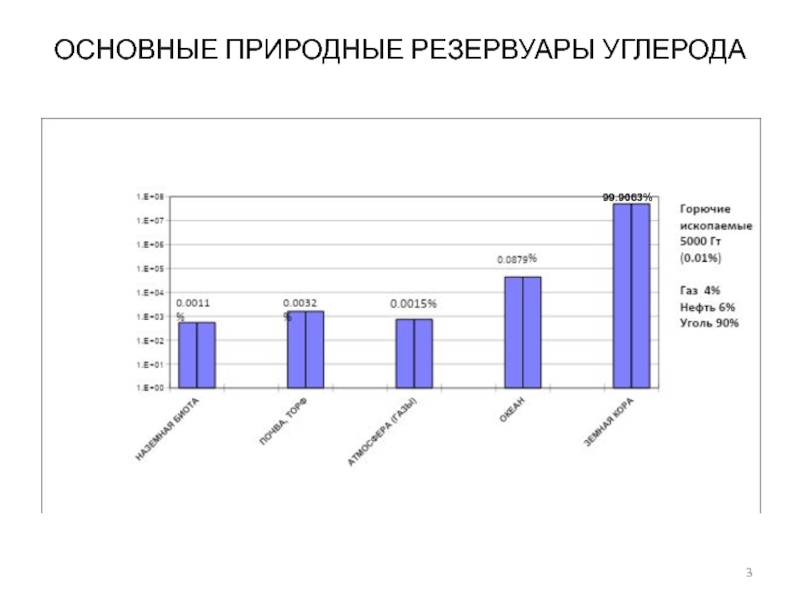
- 3. ОСНОВНЫЕ ПРИРОДНЫЕ РЕЗЕРВУАРЫ УГЛЕРОДА99.9063%
- 4. Часть 1 Основные положения химии соединений углерода
- 5. Валентные состояния атома углеродаГраничные поверхности s-, p-
- 6. Валентные состояния атома углеродаСхема электронного строения молекулы
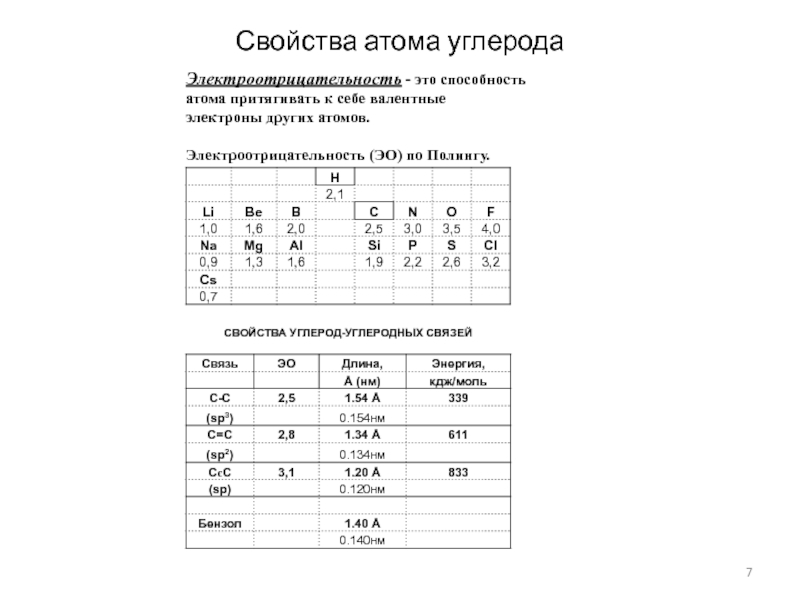
- 7. Свойства атома углерода
- 8. Аллотропные формы углеродаa) Алмаз sp3; b) графит
- 9. Аллотропные формы углеродаНано-почки
- 10. Аллотропные формы углеродаГрафен (sp2) является двумерным кристаллом,
- 11. Аллотропные формы углеродаФуллерен С60 Фуллерен С60 в кристаллической форме Чистый фуллерен С60 в растворе толуола
- 12. ИзомерияСтруктурная изомерияПространственная изомерияЗеркальная изомерияИзомерия углеродного скелетаГеометрическая (цис-, транс) изомерияМетамерияИзомерия положения
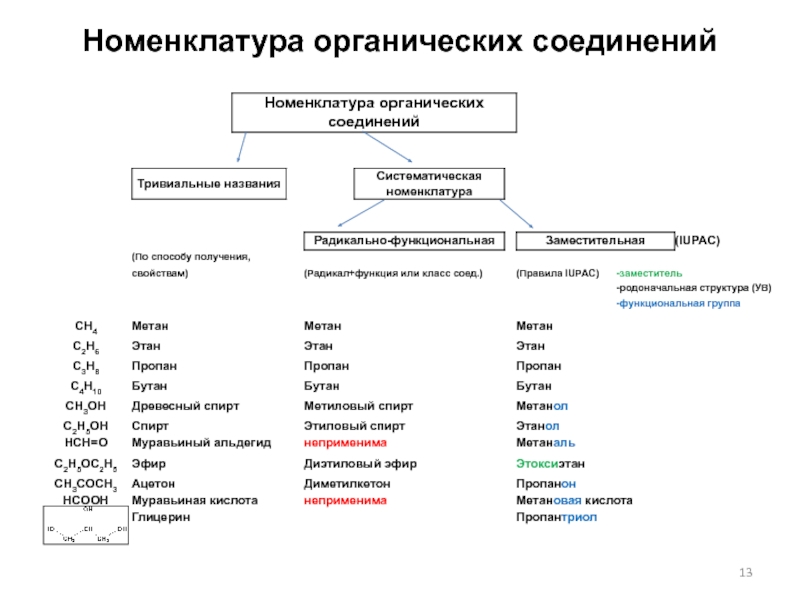
- 13. Номенклатура органических соединений
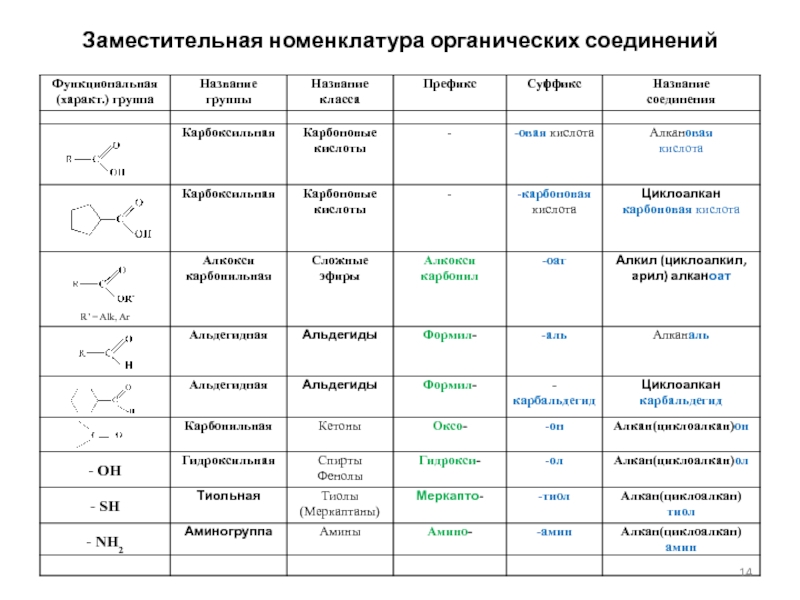
- 14. Заместительная номенклатура органических соединений
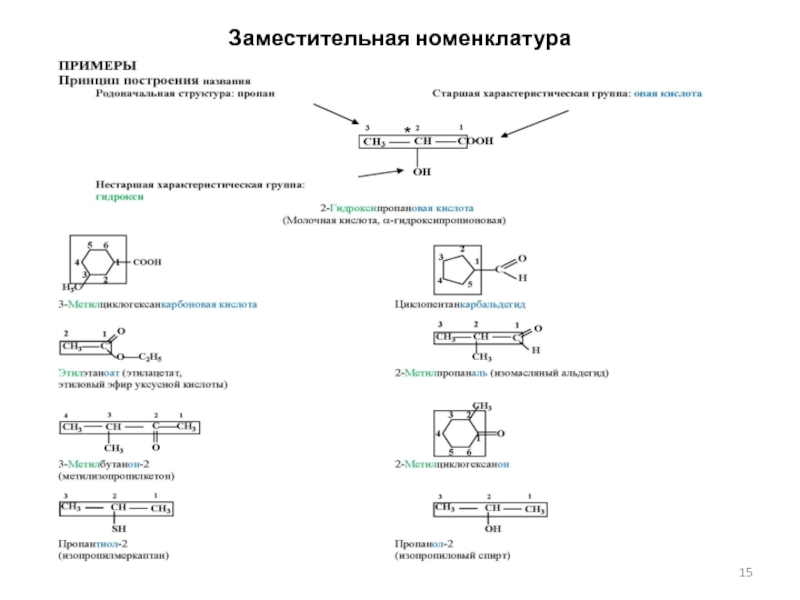
- 15. Заместительная номенклатура*
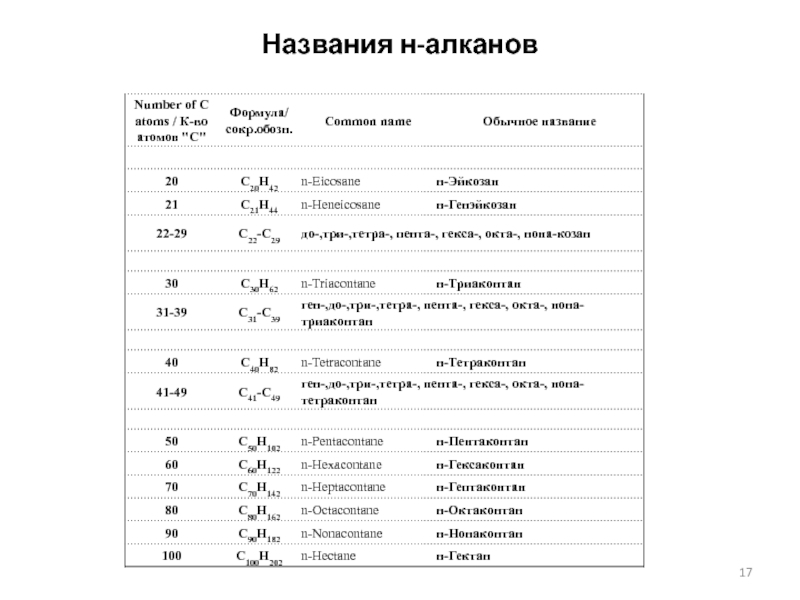
- 16. Названия н-алканов
- 17. Названия н-алканов
- 18. Наиболее употребительные радикалы
- 19. Часть 2 Углеводороды предельные и ароматические
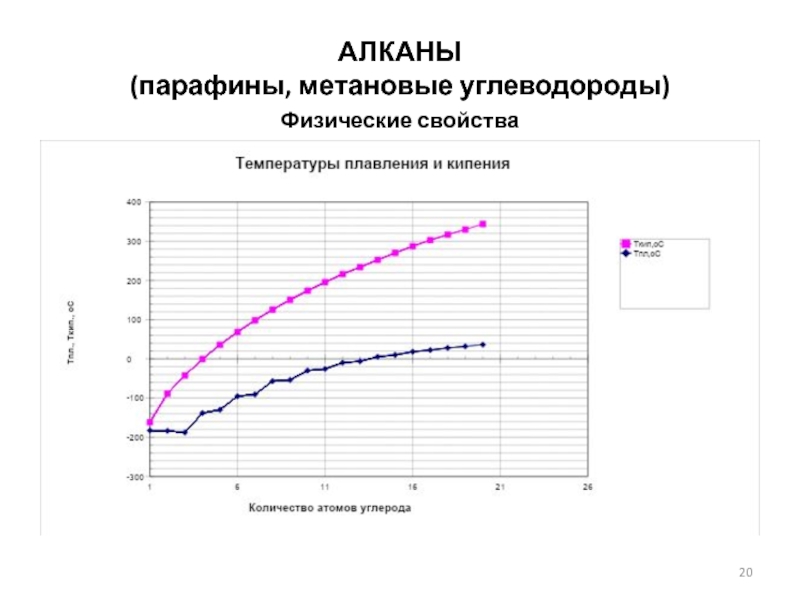
- 20. АЛКАНЫ (парафины, метановые углеводороды) Физические свойства
- 21. Физические свойства алкановГОМОЛОГИЧЕСКИЙ РЯД , последовательность орг.
- 22. Измерение плотности (ручной метод)Пикнометр для жидкостейПикнометр газовыйАреометрыАреометрТермостатирующая
- 23. Физические свойства алканов
- 24. Газовые гидраты (водные клатраты, нестехиометрические соединения)Структура
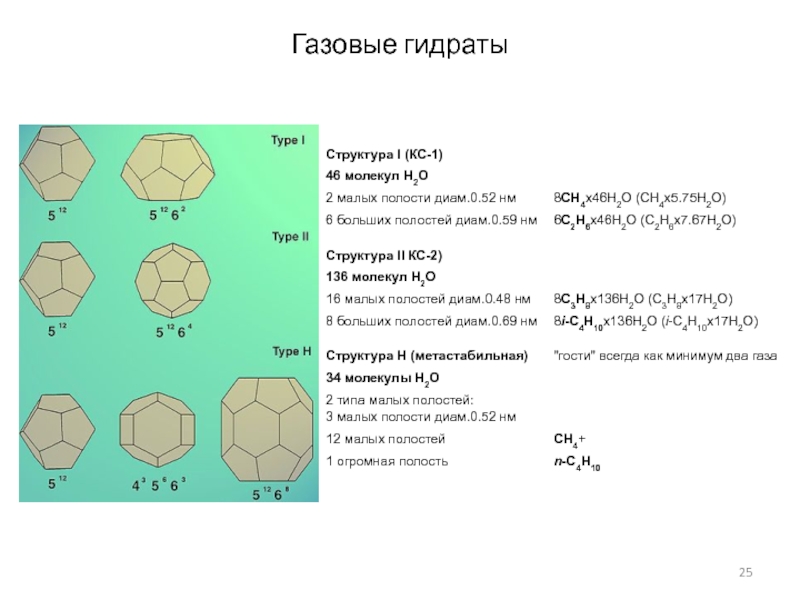
- 25. Газовые гидраты
- 26. Соединения включения алканов с мочевиной (туннельного типа)Внутри
- 27. Соединения включения алканов с мочевиной и
- 28. Некоторые гомологические серии алкановизо- и антеизо-алканы
- 29. Некоторые гомологические серииИзопреноидные алканы (изопренаны) регулярныеОбразование из фитола(E)-3,7,11,15-tetramethylhexadec-2-en-1-ol
- 30. Основные изопреноиды *
- 31. Способы пространственного изображения молекулКонформация (от лат. conformatio
- 32. Конформации этана 0° 60° 120° 180°
- 33. Конформации этана, бутана, пентанаВращение в этане свободноеПри
- 34. Циклоалканы (циклопарафины, цикланы) [полиметилены – моноциклические циклоалканы
- 35. Конформации циклобутана, циклопентана, циклогексанаКонформационные формы молекул циклобутана
- 36. Конформации циклогексанаКонформации шестичленных циклов на примере циклогексана:1
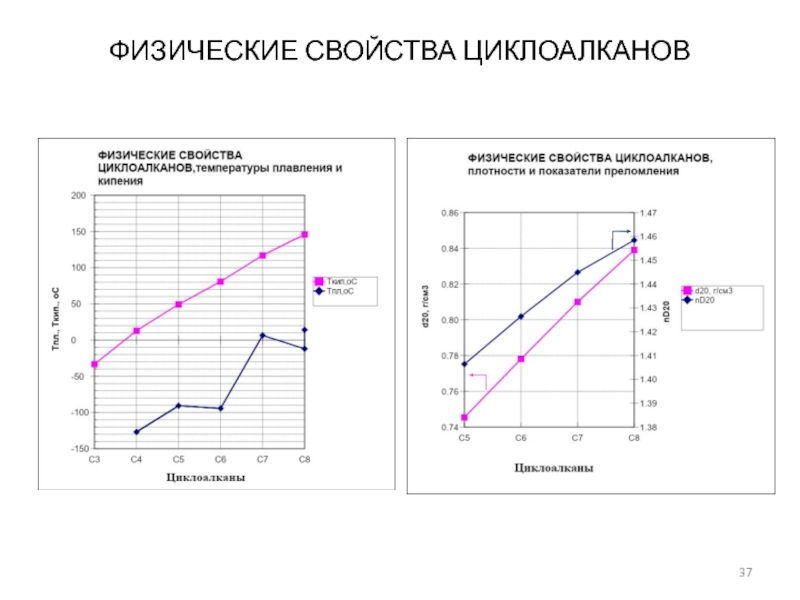
- 37. ФИЗИЧЕСКИЕ СВОЙСТВА ЦИКЛОАЛКАНОВ
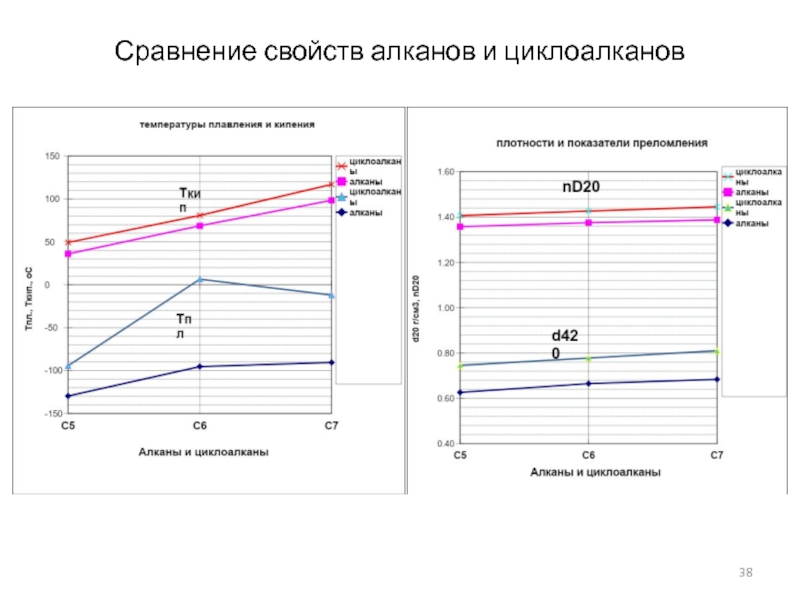
- 38. Сравнение свойств алканов и циклоалканов
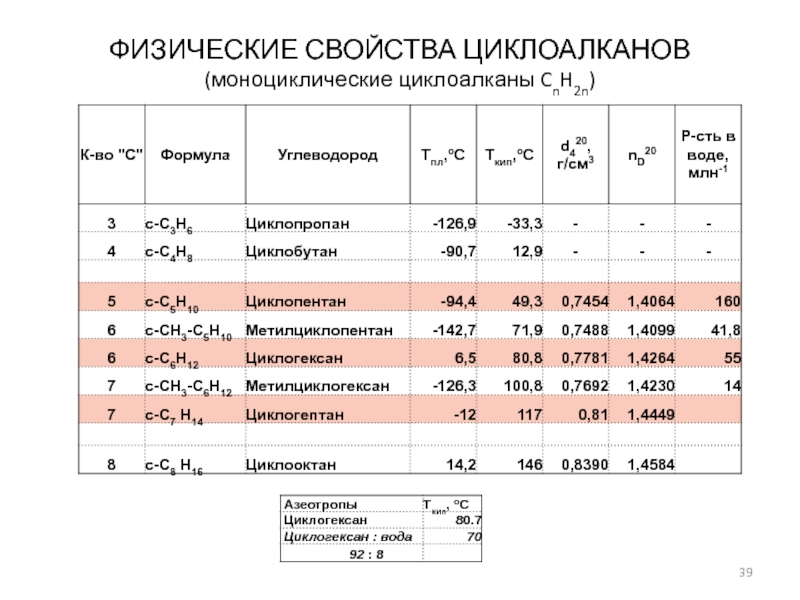
- 39. ФИЗИЧЕСКИЕ СВОЙСТВА ЦИКЛОАЛКАНОВ (моноциклические циклоалканы CnH2n)
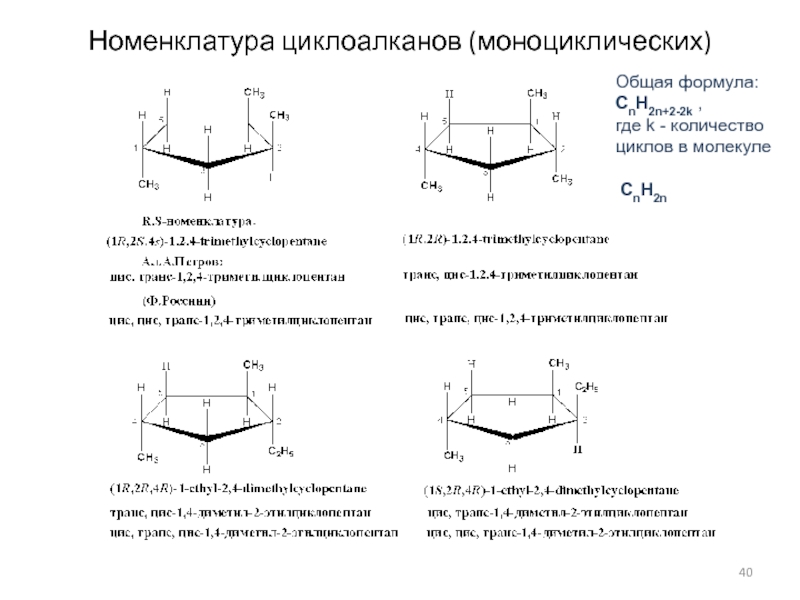
- 40. Номенклатура циклоалканов (моноциклических) Общая формула:CnH2n+2-2k ,где k - количествоциклов в молекуле CnH2n
- 41. R,S-номенклатураСтаршинство заместителей в порядке убывания: 1, 2, 3, 4Rectus (вправо), Sinister (влево)
- 42. Бициклические нафтены с конденсированными циклами
- 43. Бициклические нафтены с конденсированными цикламиПенталаны C8H14 (бицикло [3.3.0] октаны)Общая формула:CnH2n-2
- 44. Бициклические нафтены с конденсированными цикламиГидринданы C9H16 (бицикло [4.3.0] нонаны)Общая формула:CnH2n-2
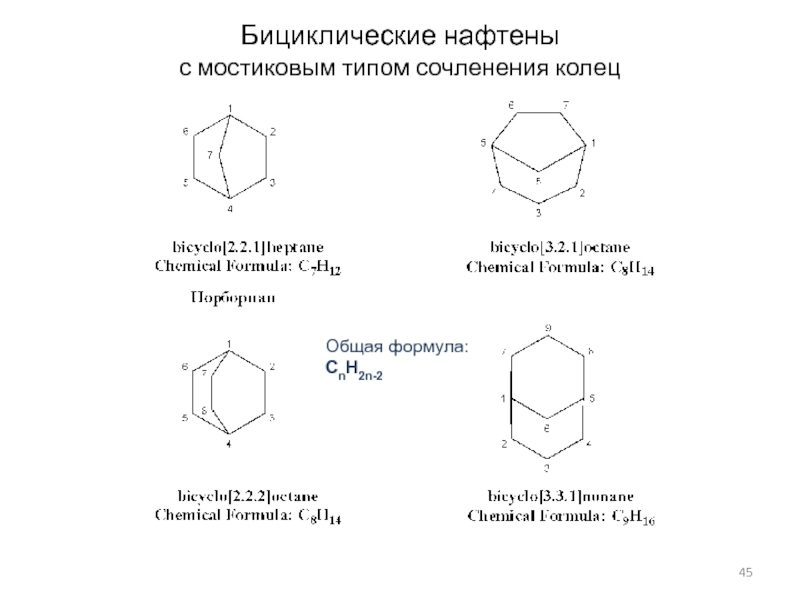
- 45. Бициклические нафтены с мостиковым типом сочленения колецОбщая формула:CnH2n-2
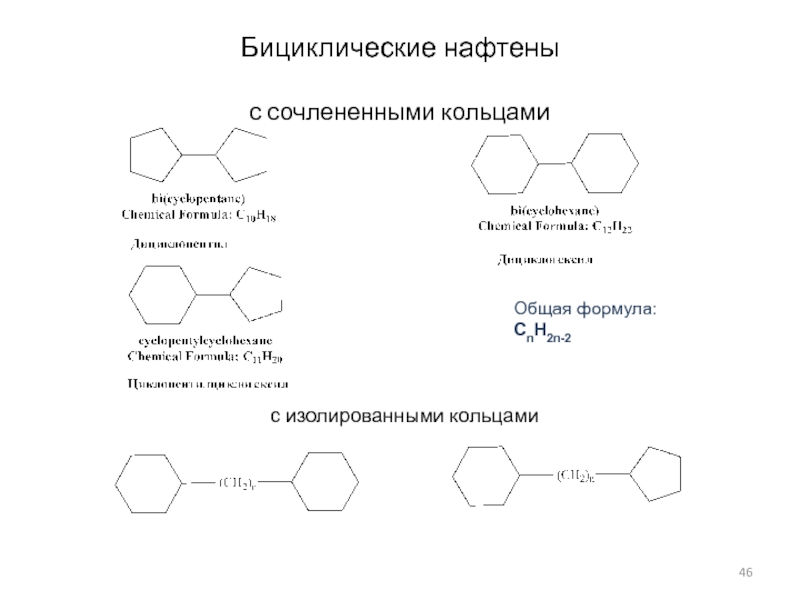
- 46. Бициклические нафтены с сочлененными кольцамиОбщая формула:CnH2n-2с изолированными кольцами
- 47. Трициклические нафтеныМостикового типаОбщая формула:CnH2n+2-2k ,где k - количествоциклов в молекуле CnH2n-4
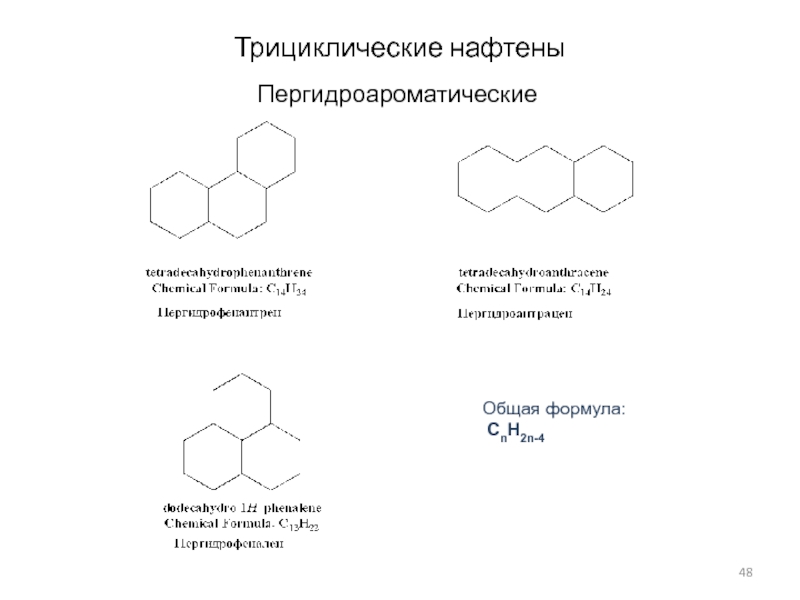
- 48. Трициклические нафтеныПергидроароматическиеОбщая формула: CnH2n-4
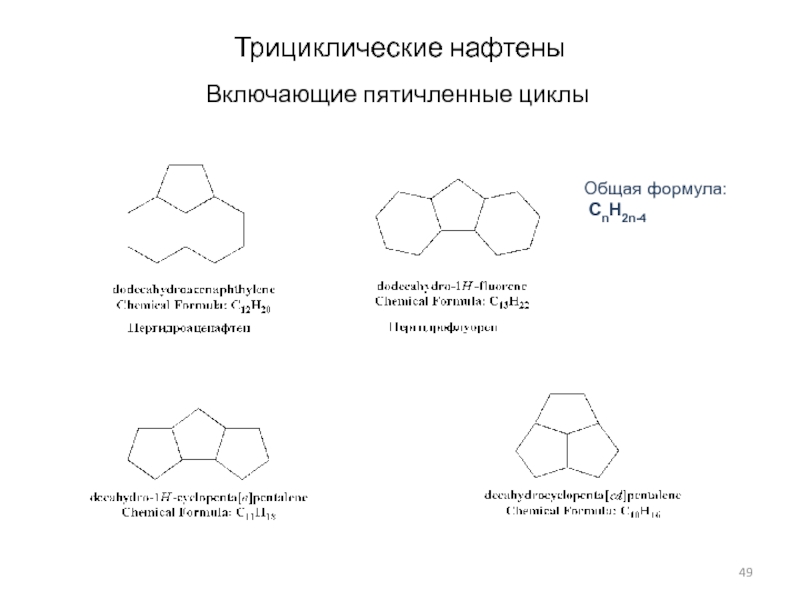
- 49. Трициклические нафтеныВключающие пятичленные циклыОбщая формула: CnH2n-4
- 50. Полициклические нафтены Тетрациклические
- 51. Стераны Cholestane
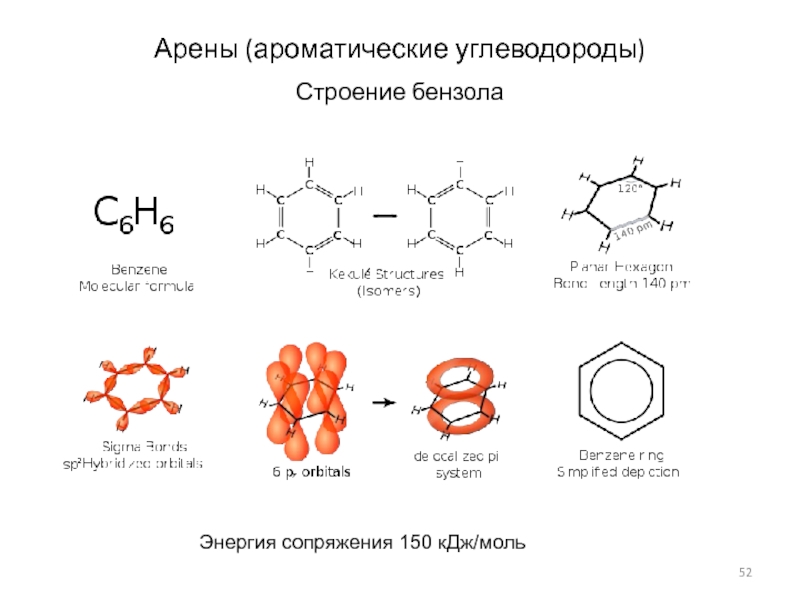
- 52. Арены (ароматические углеводороды)Строение бензолаЭнергия сопряжения 150 кДж/моль
- 53. Предлагаемые формулы для бензола Claus
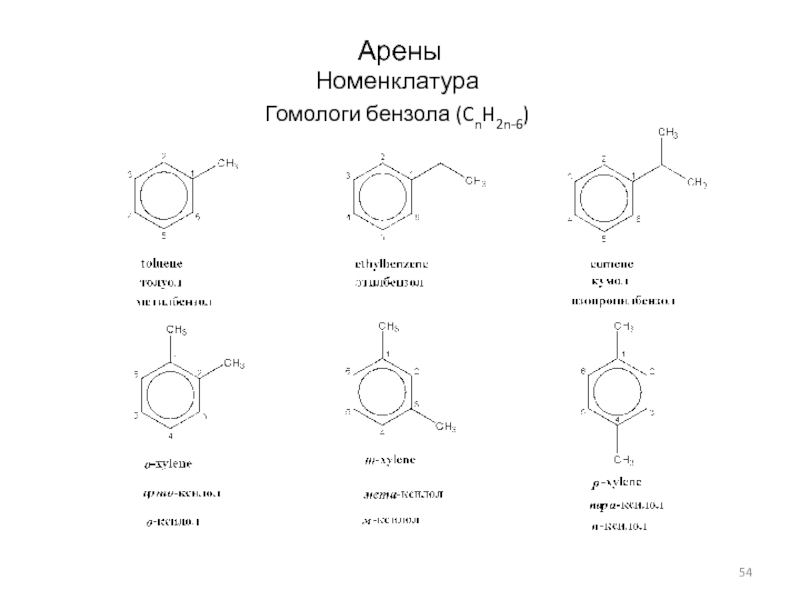
- 54. АреныНоменклатураГомологи бензола (CnH2n-6)
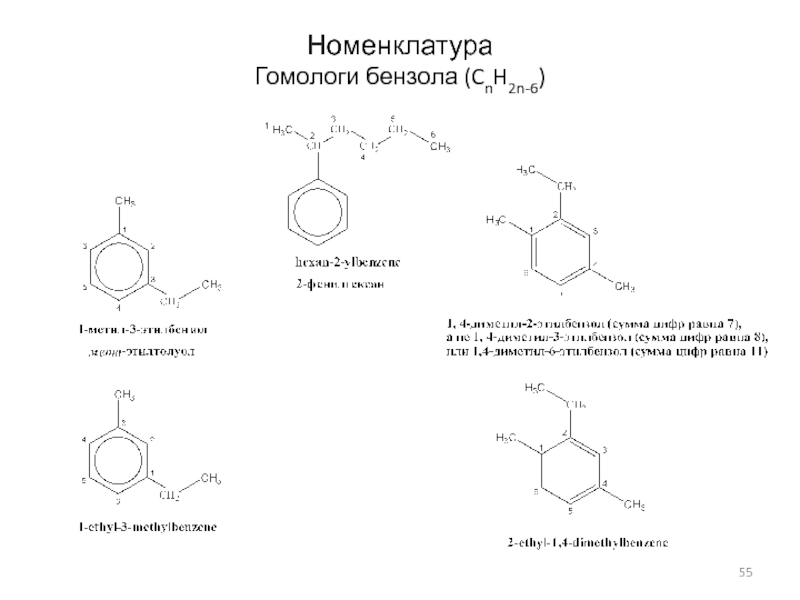
- 55. Номенклатура Гомологи бензола (CnH2n-6)
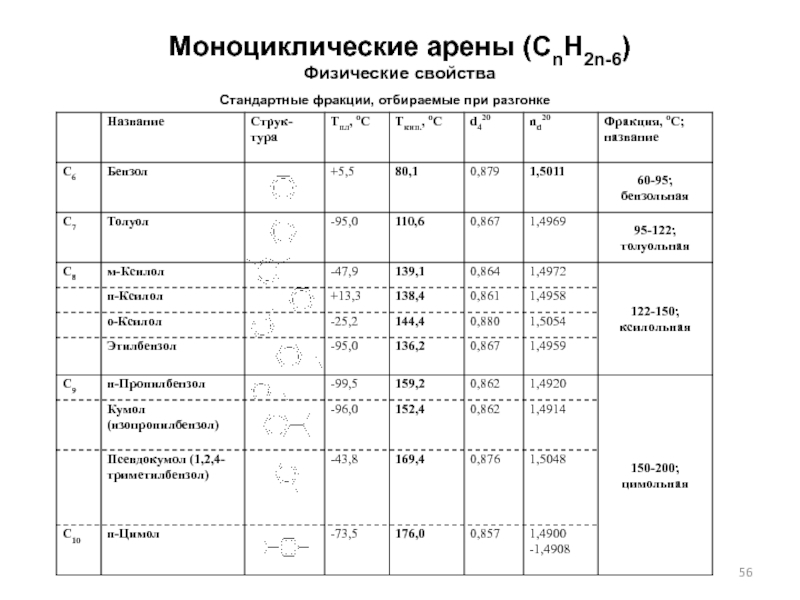
- 56. Моноциклические арены (CnH2n-6) Физические свойстваСтандартные фракции, отбираемые при разгонке
- 57. Определение группового углеводородного состава нефтяных фракций
- 58. Азеотропы с водой Люминесценция
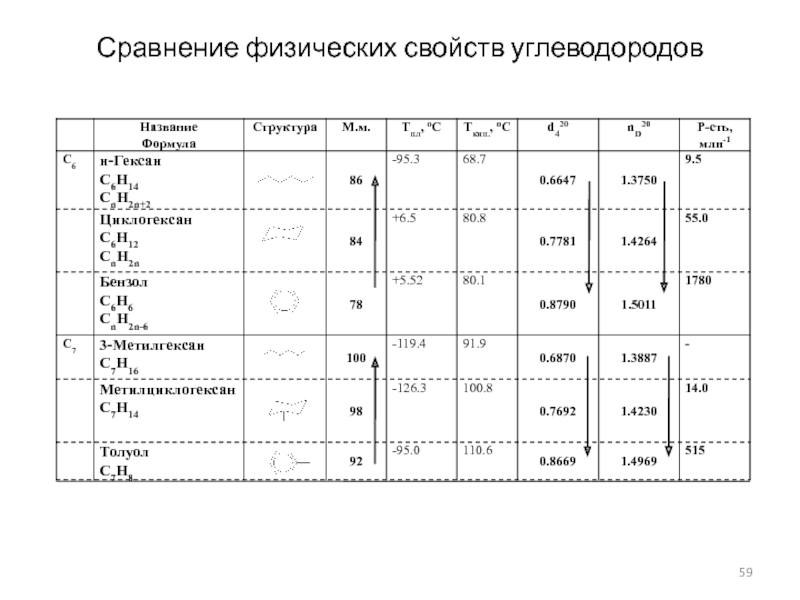
- 59. Сравнение физических свойств углеводородов
- 60. Структурно-групповой анализ керосиновых, масляных и смолистых фракций
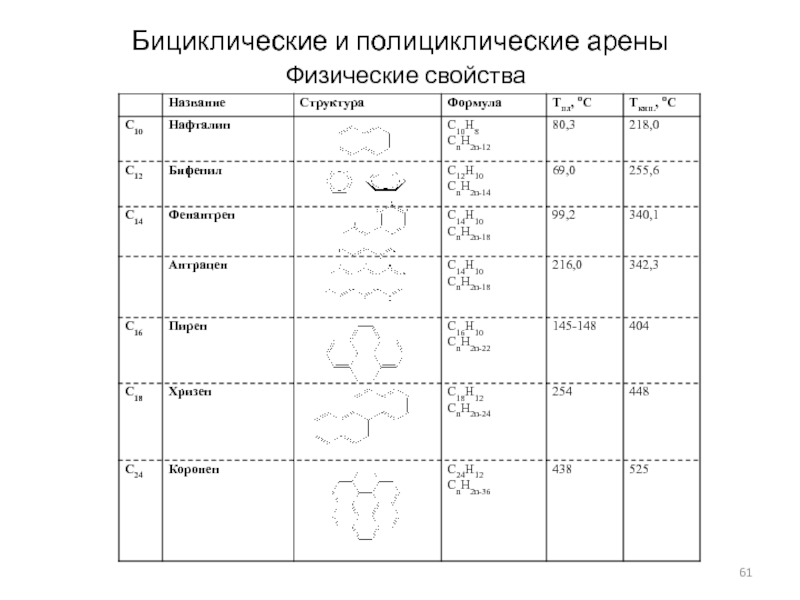
- 61. Бициклические и полициклические ареныФизические свойства
- 62. Нафталин
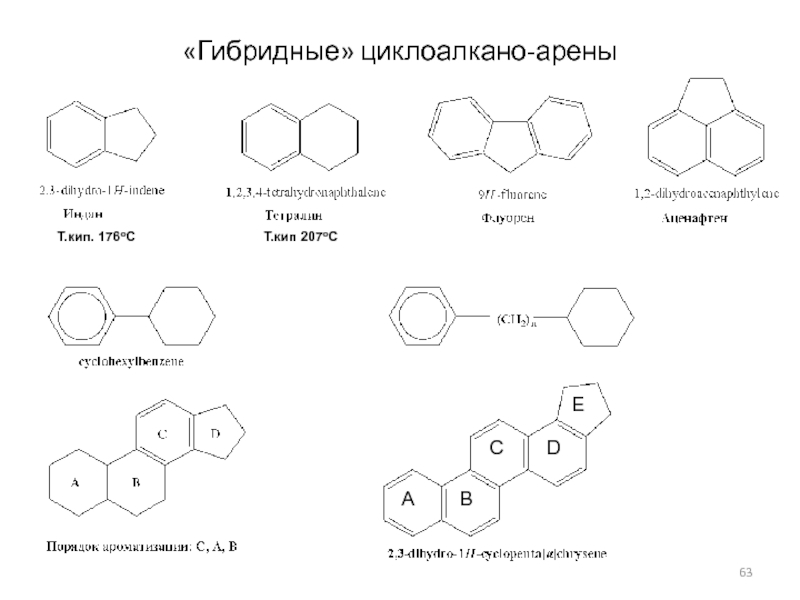
- 63. «Гибридные» циклоалкано-арены ABCDEТ.кип 207оСТ.кип. 176оС
- 64. Реакции ароматических соединенийРеакции замещенияАлкилирование олефинамиСульфированиеХлорирование
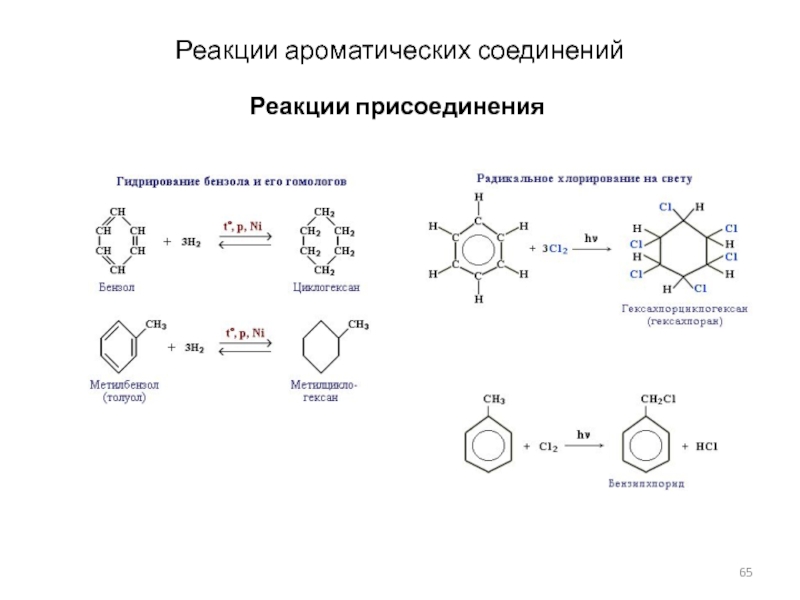
- 65. Реакции присоединенияРеакции ароматических соединений
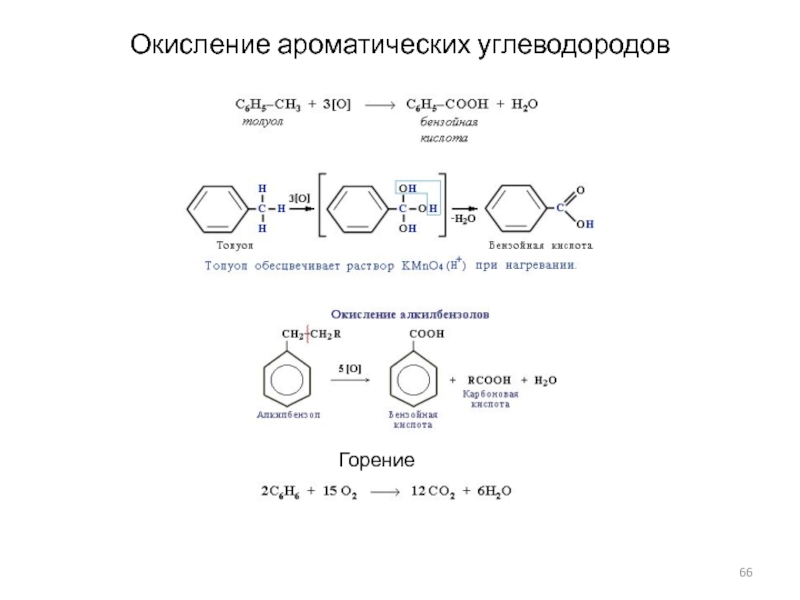
- 66. Окисление ароматических углеводородов Горение
- 67. Правила ориентации в бензольном кольце В молекуле
- 68. Правила ориентации в бензольном кольцеI. Заместители, обладающие
- 69. Правила ориентации в бензольном кольцеII. Заместители, обладающие
- 70. Правила ориентации в бензольном кольце
- 71. Хроматограмма nC5-nC8
- 72. Хроматограмма nC9-nC35nC17PrnC18PhnC20nC9nC11nC13nC30
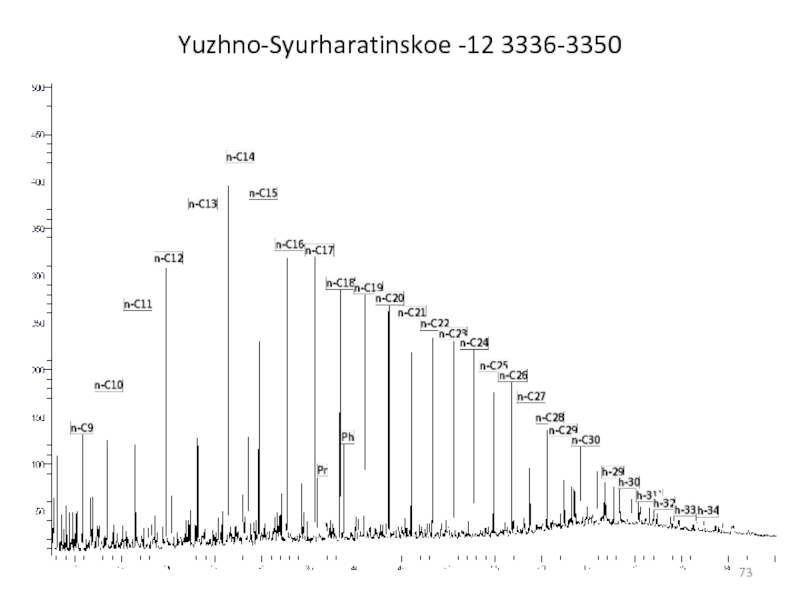
- 73. Yuzhno-Syurharatinskoe -12 3336-3350
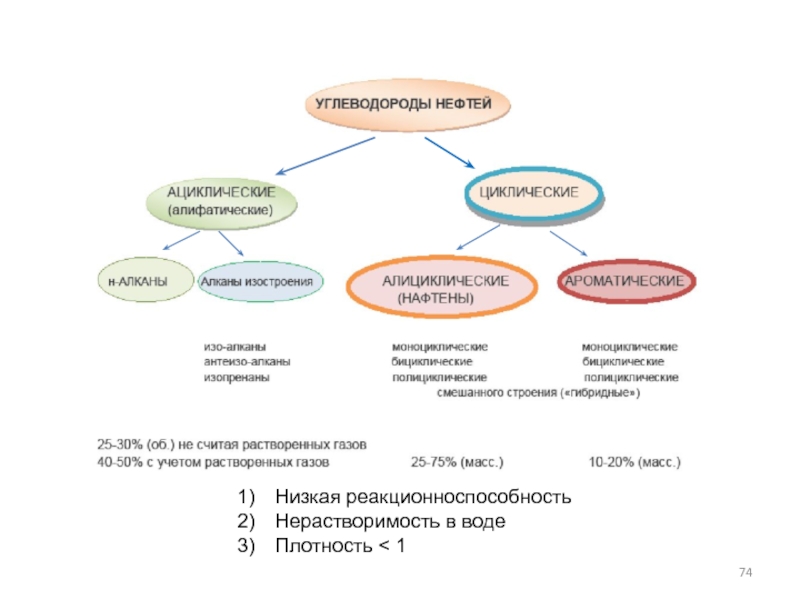
- 74. Низкая реакционноспособностьНерастворимость в водеПлотность < 1
- 75. Геохимические типы нефтей, биодеградация Биодеградация нефтей (окисление
- 76. Часть 4 Некоторые ароматические гетероциклы
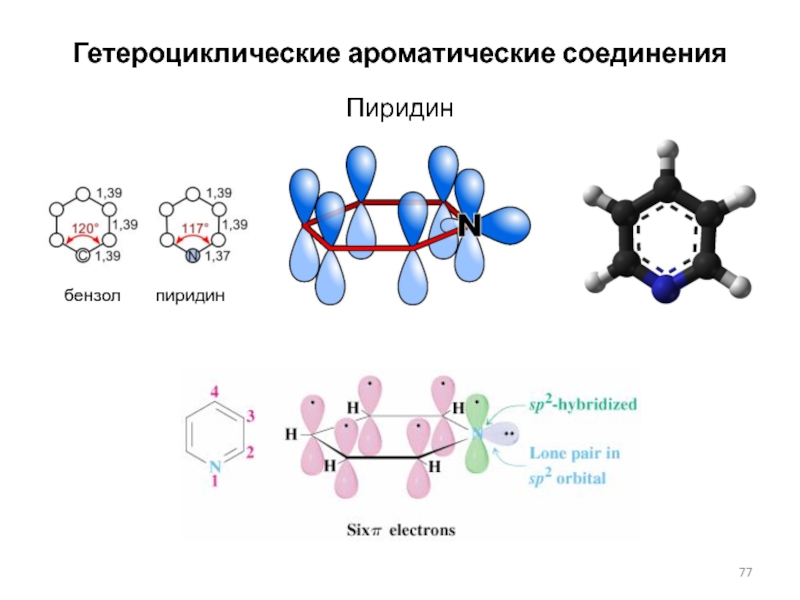
- 77. Гетероциклические ароматические соединенияПиридинбензол пиридин
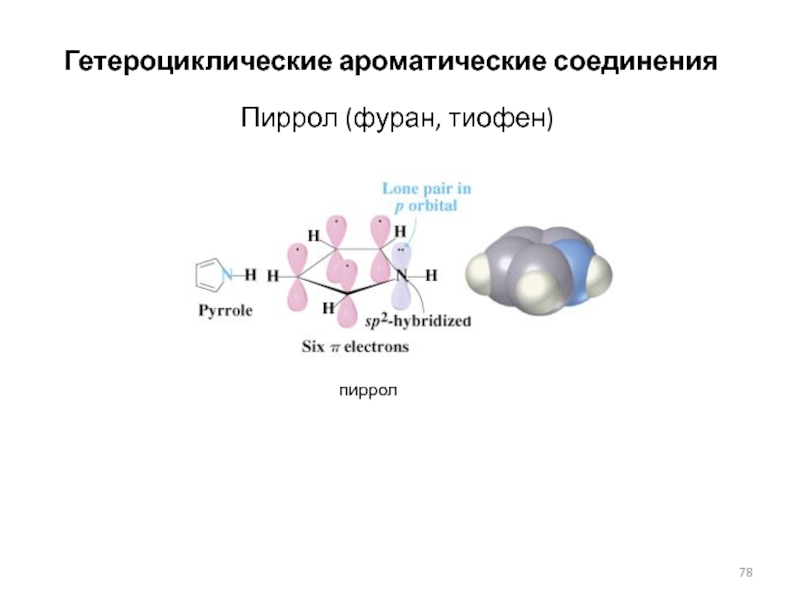
- 78. Пиррол (фуран, тиофен) пирролГетероциклические ароматические соединения
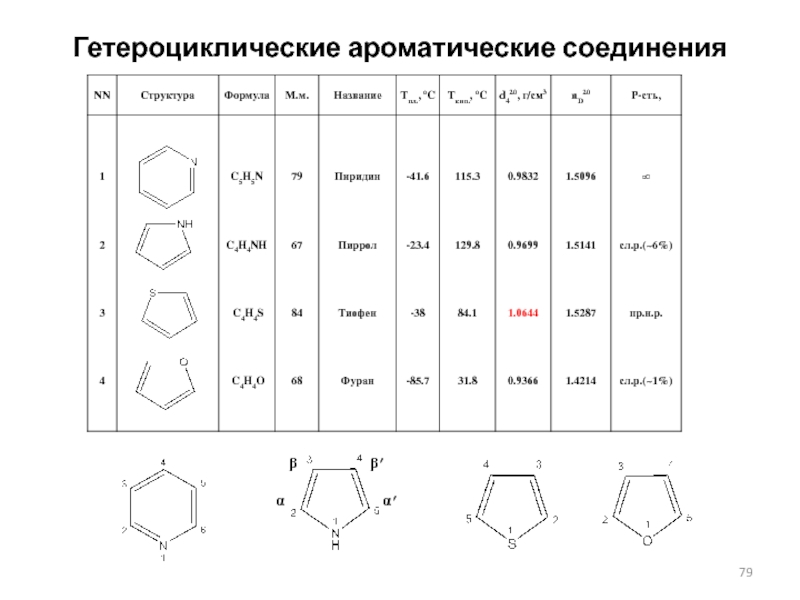
- 79. Гетероциклические ароматические соединения aba’b’
- 80. Некоторые реакции гетероцикловВзаимопревращения пятичленных гетероциклов (Ю.К.Юрьев)(T ~400oC, катализатор Al2O3)пирролпирролнатрийКислотные свойства NH-группы пирролаОсновные свойства N пиридина
- 81. Некоторые реакции гетероцикловСульфирование тиофена (замещение)тиофентиофен-2-сульфокислотаГидрирование гетероциклов (присоединение)X
- 82. Гетероциклы в нефтях тиофены
- 83. Гетероциклы в нефтяхАзотистые основанияCH3 пиридины
- 84. ХЛОРОФИЛЛХЛОРОФИ́ЛЛ (от греч. χλωρός, «зелёный» и φύλλον,
- 85. Хлорофилл (от греч. chloros - зеленый и phyllon — лист)
- 86. Ядро хлорофилла26 p-электронов: 11 двойных связей +
- 87. Структура хлорофилла BCDAE
- 88. Радикалы R4 в хлорофиллах a, b, d, e Хлорофиллыa, b, dБактерио-хлорофилл eБактерио-xлорофиллыa, b
- 89. Хлорофиллы a, b, dХлорофилл aХлорофилл bХлорофилл dФитилФитилФитилРаспространение:цианобактерииназемные растенияповсеместноC55H72O5N4MgC55H70O6N4MgC54H70O6N4Mg
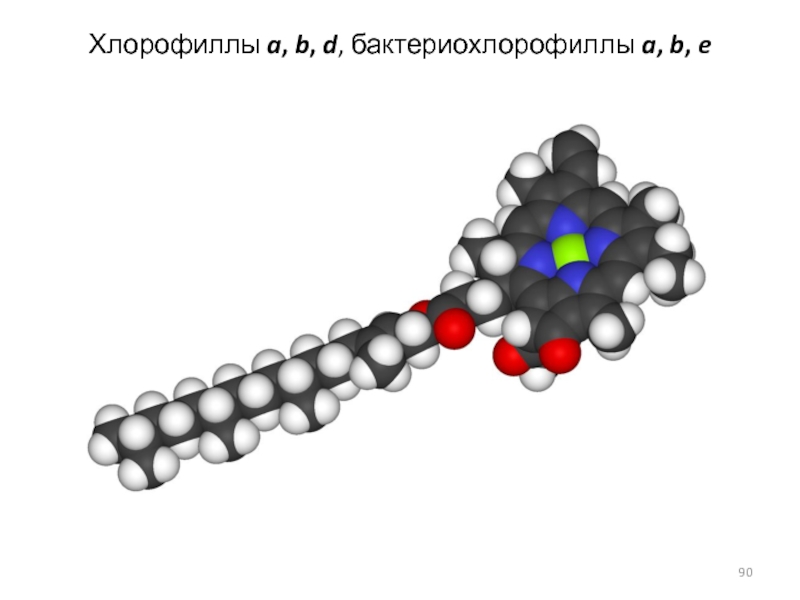
- 90. Хлорофиллы a, b, d, бактериохлорофиллы a, b, e
- 91. Хлорофиллы cХлорофилл c1Хлорофилл c2различные водоросли (бурые, диатомовые)C35H30O5N4MgC35H28O5N4Mg
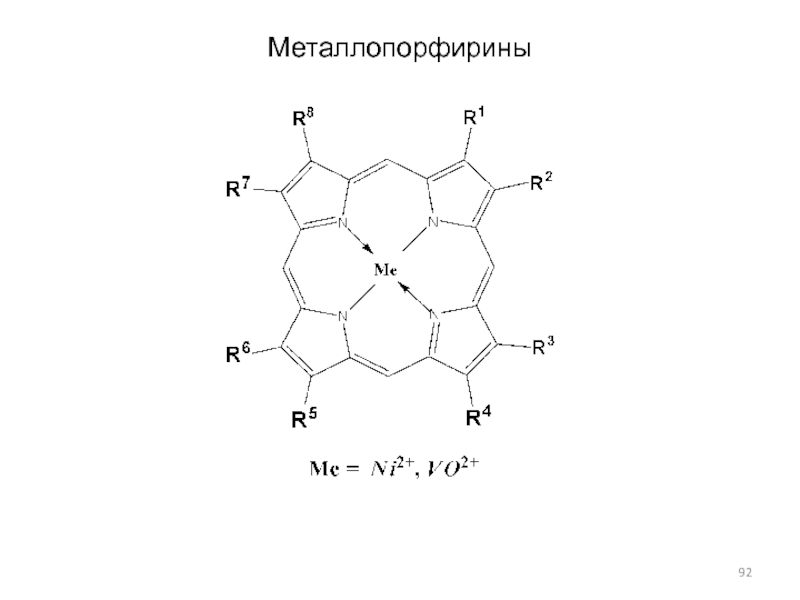
- 92. Металлопорфирины
- 93. Часть 5 Непредельные углеводороды
- 94. Каротин
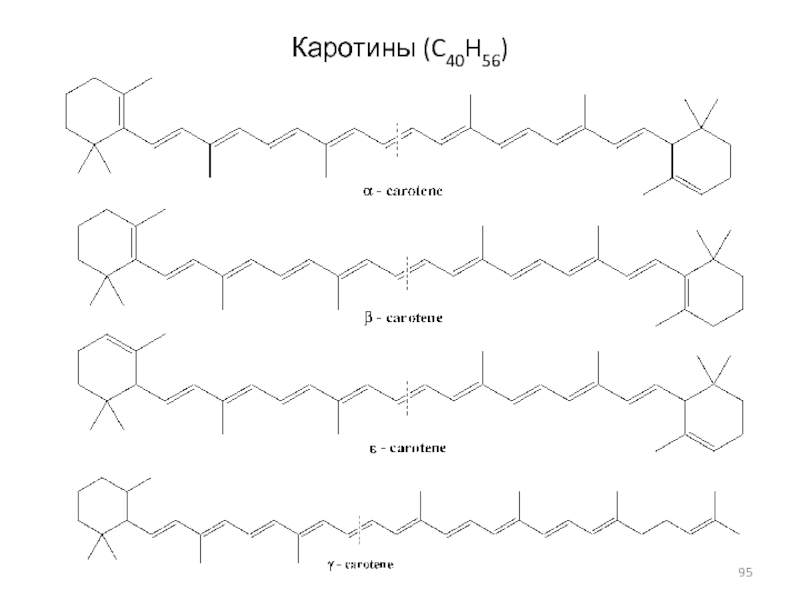
- 95. Каротины (C40H56)
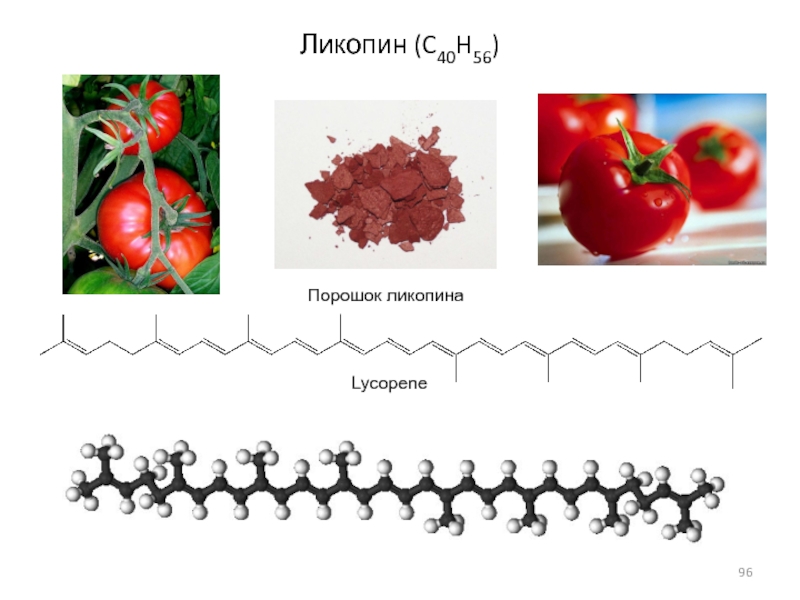
- 96. Ликопин (C40H56)Порошок ликопинаLycopene
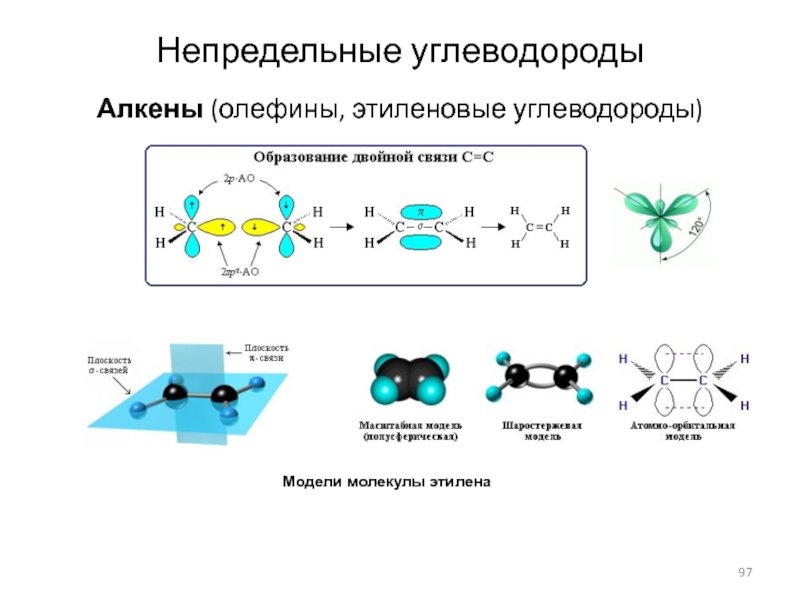
- 97. Непредельные углеводородыАлкены (олефины, этиленовые углеводороды) Модели молекулы этилена
- 98. Алкены (CnH2n) * Значения измерены при температуре кипения.Температуры
- 99. Изомерия и номенклатура алкенов (на примере бутенов)1. Структурная2. Изомерия положения двойной связибутен-12-метилпропен-1(изобутилен)бутен-1бутен-2[1][2]
- 100. Изомерия и номенклатура алкенов (на примере
- 101. Номенклатура алкенов 4. За основу названия берется
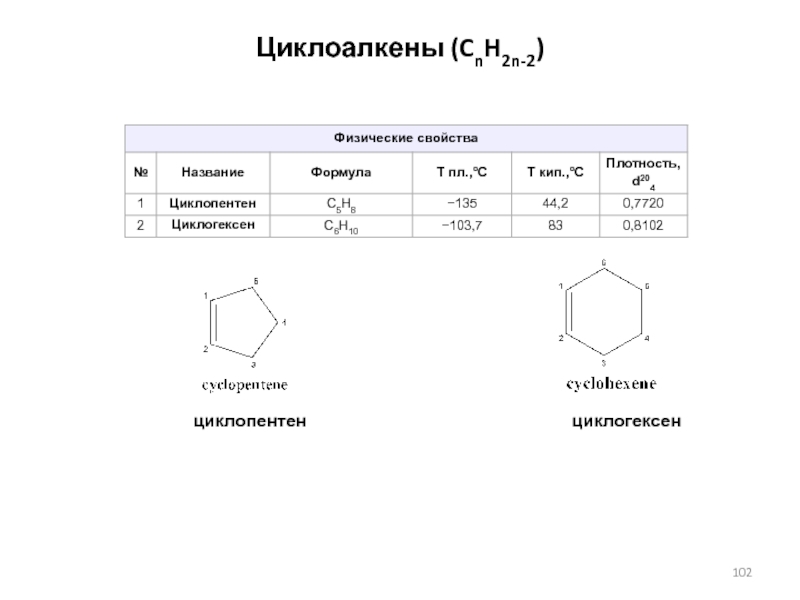
- 102. Циклоалкены (CnH2n-2)
- 103. Номенклатура циклоалкеновЗа основу названия берется название циклоалкана,
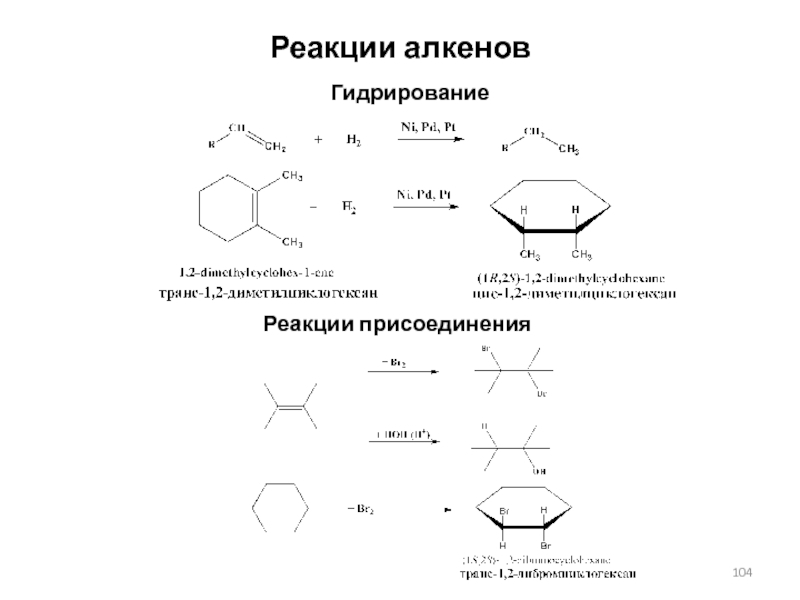
- 104. Реакции алкеновРеакции присоединенияГидрирование
- 105. Реакции присоединения Правило МарковниковаВ реакциях присоединения полярных
- 106. Реакции присоединения Правило Марковникова
- 107. Реакции присоединенияизобутилен
- 108. Реакции присоединения Присоединение сероводородаПрисоединение меркаптановпропилен
- 109. Димеризация (изобутилен)Димеризация алкенов – образование димера (удвоенной
- 110. Димеризация (пропилен) пропилен
- 111. «Необратимый» катализ(Н.Д.Зелинский, 1911 г.)Каталитическое диспропорционирование углеводородов ряда
- 112. «Необратимый» катализ лимонен
- 113. Реакции алкеновРеакции карбонилированиягидроформилированиегидрокарбоксилированиегидрокарбометоксилированиеОкислениепропандиол-1,2Горение
- 114. Алкадиены (диены) (CnH2n-2)Классификация1. Диены с кумулированными связями
- 115. АлкадиеныСопряженные диеныπ-Электроны двойных связей образуют единое π-электронное облако (сопряженную систему) и делокализованы между всеми атомами углерода
- 116. Номенклатура алкадиеновЗа основу названия берется название алкана,
- 117. Номенклатура циклоалкадиеновЗа основу названия берется название циклоалкана,
- 118. Алкадиены
- 119. Реакции 1,3-диенов1,4-присоединение80%20%Правило Марковникова и правило Тиле
- 120. Реакция Дильса-Альдера (Нобелевская премия в 1950 г.)
- 121. Реакция Дильса-Альдера (1,4-циклоприсоединение)«Необратимый» катализДиен+диенофилРеакции 1,3-диенов (3 CnH2n-4
- 122. Полимеризация Реакции 1,3-диеновизопренНатуральный каучук (1,4-цис-полиизопрен)Натуральный каучук –
- 123. Полимеризация Реакции 1,3-диеновГуттаперча (до 90 % 1,4-транс-полиизопрена)(отвердевший
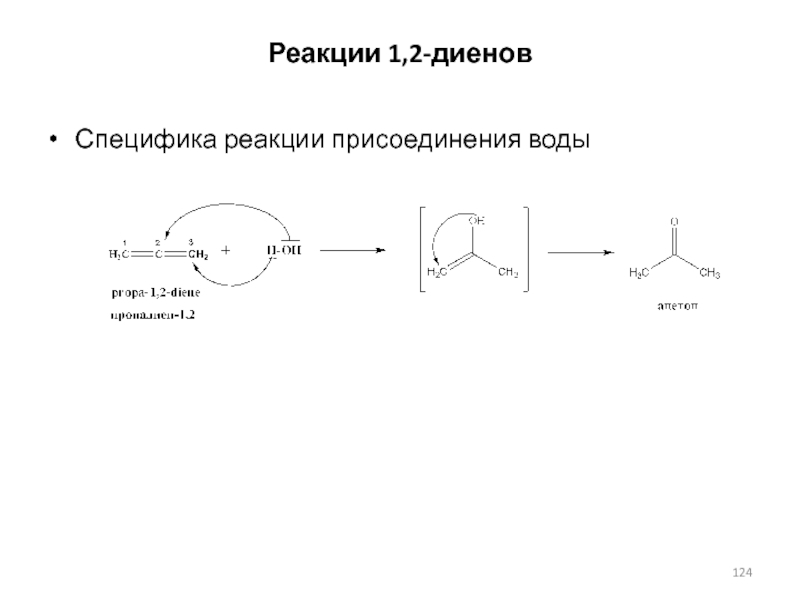
- 124. Реакции 1,2-диеновСпецифика реакции присоединения воды
- 125. ТерпеныПолиизопреновые структуры с невысокой степенью полимеризации содержатся
- 126. ТерпеныТерпены классифицируют по числу изопреновых звеньев, образующих
- 127. ТерпеныСемитерпены C5H8;
- 128. ТерпеныМонотерпены (терпены) C10H16, монотерпеноиды
- 129. ТерпеныСесквитерпены (полуторатерпены) C15H24, сесквитерпеноидыДитерпены C20H32,
- 130. ТерпеныТритерпены, C30H48, (C10H16)3;
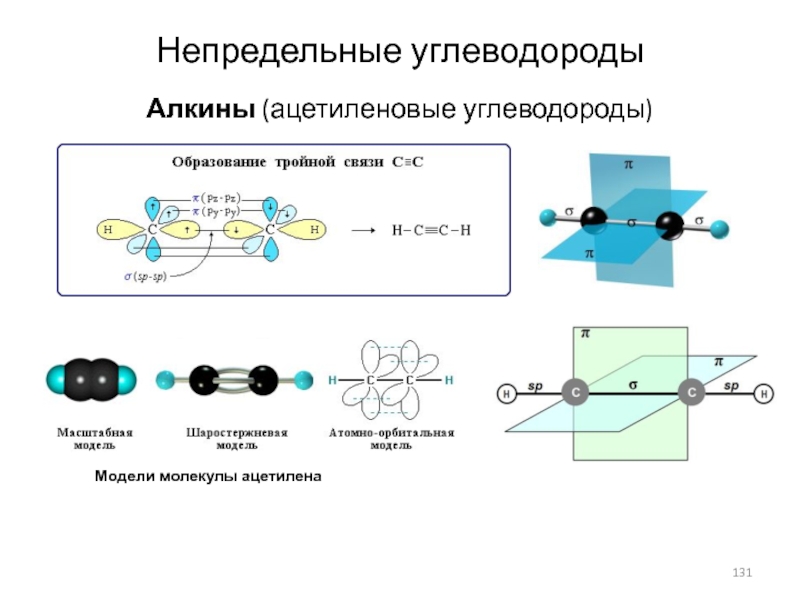
- 131. Непредельные углеводородыАлкины (ацетиленовые углеводороды) Модели молекулы ацетилена
- 132. Изомерия и номенклатура алкинов (CnH2n-2)Структурная изомерияИзомерия положения
- 133. Номенклатура алкинов1. За основу названия берется название
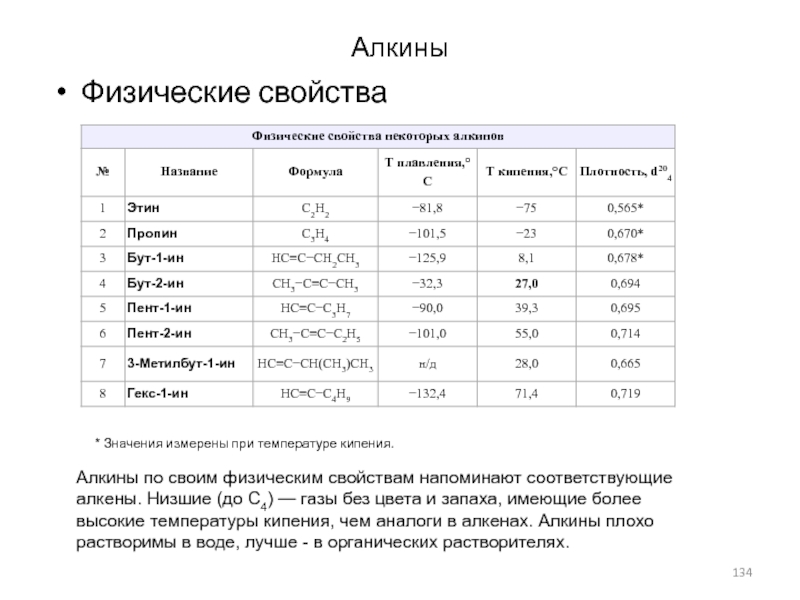
- 134. АлкиныФизические свойства* Значения измерены при температуре кипения.Алкины
- 135. Взаимодействие карбидов металлов с водой
- 136. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Введение в специальность
Геологический факультет МГУ
им. М.В.Ломоносова
Кафедра геологии и геохимии горючих
ископаемых
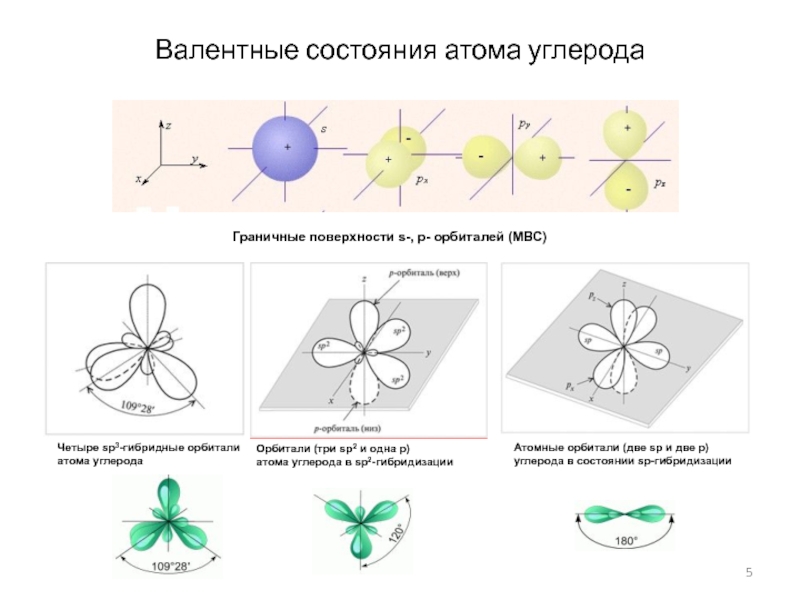
Слайд 5Валентные состояния атома углерода
Граничные поверхности s-, p- орбиталей (МВС)
Четыре sp3-гибридные
орбитали
атома углерода
Орбитали (три sp2 и одна р)
атома углерода в sp2-гибридизации
Атомные
орбитали (две sp и две р)углерода в состоянии sp-гибридизации
Слайд 6Валентные состояния атома углерода
Схема электронного строения молекулы метана
Образование молекулы
этана перерекрыванием двух гибридных электронных облаков атомов углерода
Модели молекулы этилена
Модели
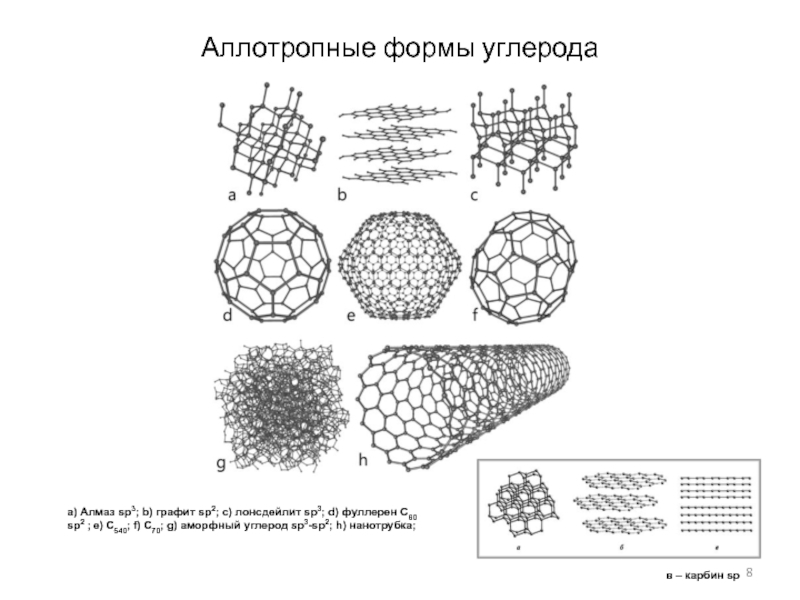
молекулы ацетиленаСлайд 8Аллотропные формы углерода
a) Алмаз sp3; b) графит sp2; c) лонсдейлит
sp3; d) фуллерен С60 sp2 ; e) С540; f) С70;
g) аморфный углерод sp3-sp2; h) нанотрубка;в – карбин sp
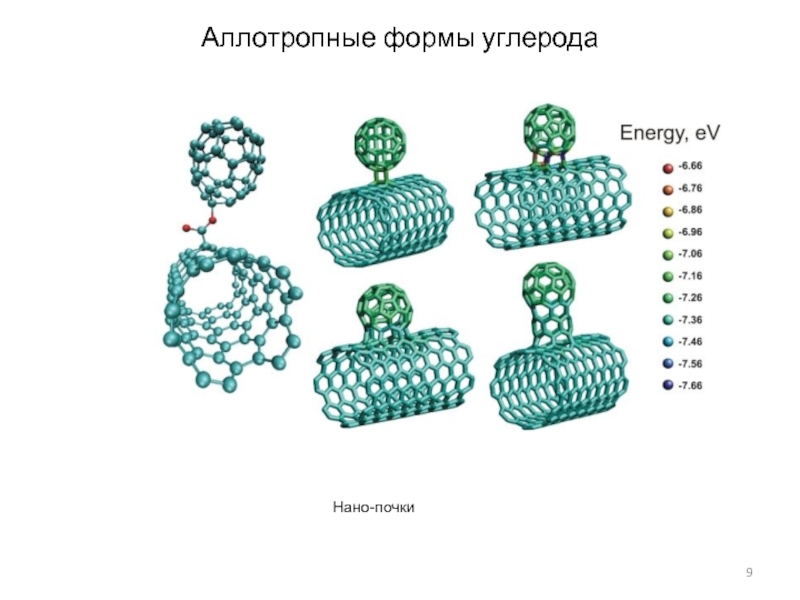
Слайд 10Аллотропные формы углерода
Графен (sp2) является двумерным кристаллом, состоящим из одиночного
слоя атомов углерода, собранных в гексагональную решётку
Слайд 11Аллотропные формы углерода
Фуллерен С60
Фуллерен С60 в кристаллической форме
Чистый
фуллерен С60 в растворе толуола
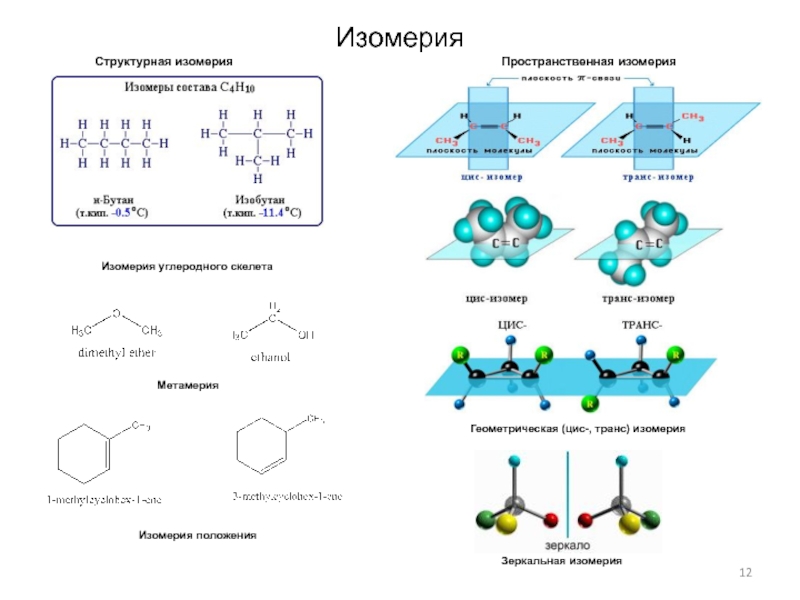
Слайд 12Изомерия
Структурная изомерия
Пространственная изомерия
Зеркальная изомерия
Изомерия углеродного скелета
Геометрическая (цис-, транс) изомерия
Метамерия
Изомерия положения
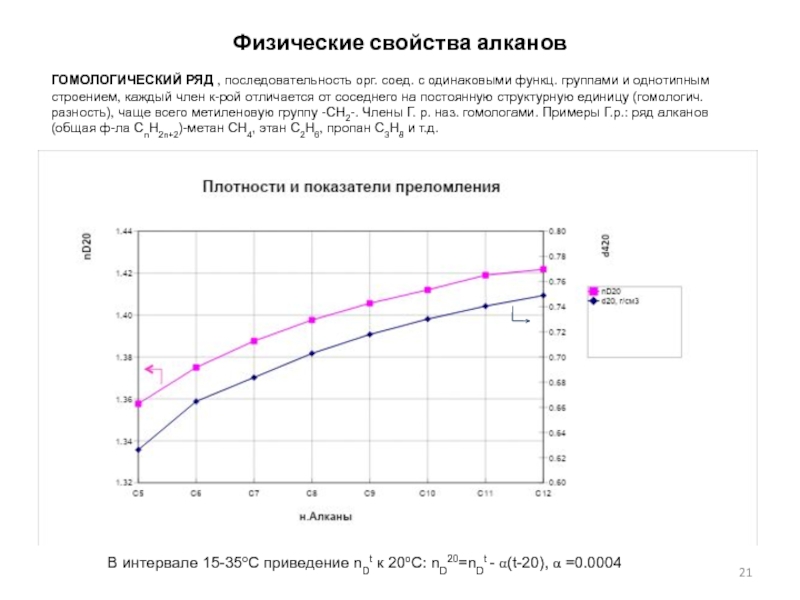
Слайд 21Физические свойства алканов
ГОМОЛОГИЧЕСКИЙ РЯД , последовательность орг. соед. с одинаковыми
функц. группами и однотипным строением, каждый член к-рой отличается от
соседнего на постоянную структурную единицу (гомологич. разность), чаще всего метиленовую группу -СН2-. Члены Г. р. наз. гомологами. Примеры Г.р.: ряд алканов (общая ф-ла СnН2n+2)-метан СН4, этан С2Н6, пропан С3Н8 и т.д.В интервале 15-35оС приведение nDt к 20оС: nD20=nDt - a(t-20), a =0.0004
Слайд 22Измерение плотности (ручной метод)
Пикнометр для жидкостей
Пикнометр газовый
Ареометры
Ареометр
Термостатирующая баня для определения
плотности, на 4 позиции
Для газов:
d ~ M.m./22,4 [g/L]
Для жидкостей в
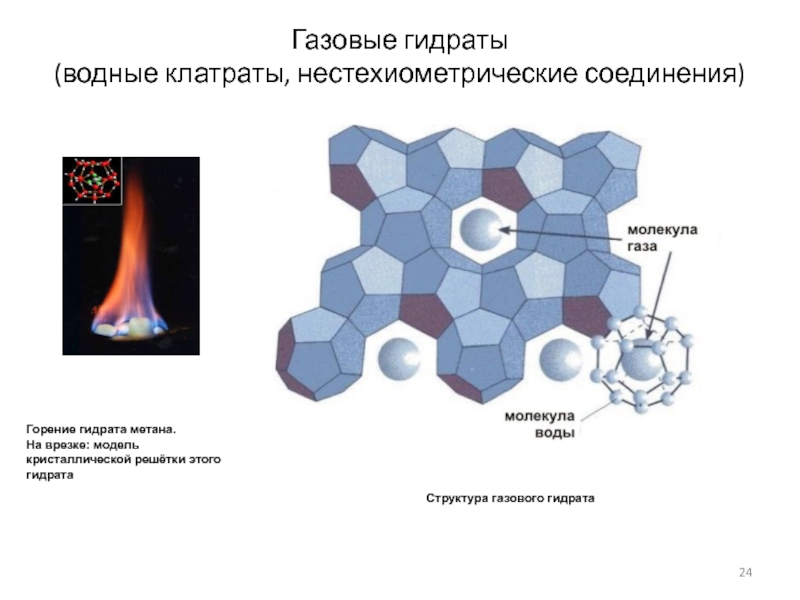
интервале 20-50оС приведение d к 20оС: плотность d420 = d4t +g(t-20), g- табличн.знач. Слайд 24Газовые гидраты
(водные клатраты, нестехиометрические соединения)
Структура газового гидрата
Горение гидрата метана.
На
врезке: модель кристаллической решётки этого гидрата
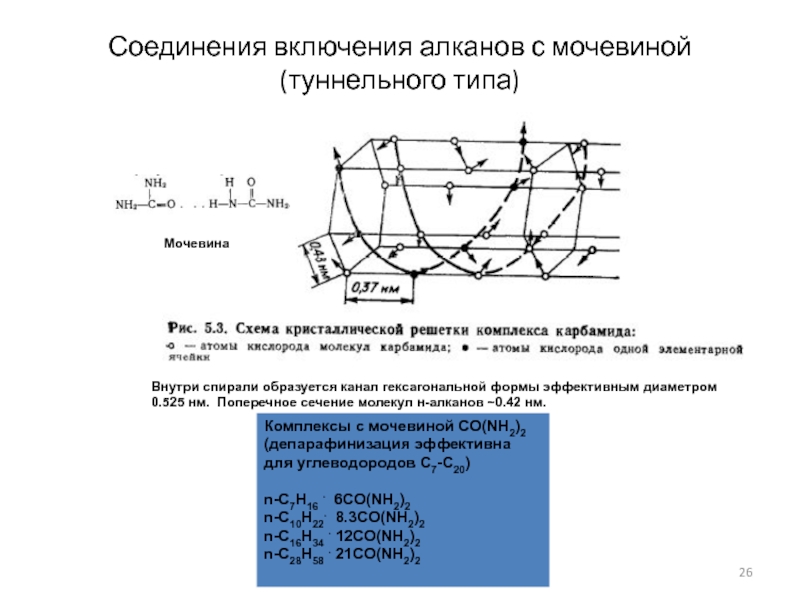
Слайд 26Соединения включения алканов с мочевиной
(туннельного типа)
Внутри спирали образуется канал гексагональной
формы эффективным диаметром 0.525 нм. Поперечное сечение молекул н-алканов ~0.42
нм.Мочевина
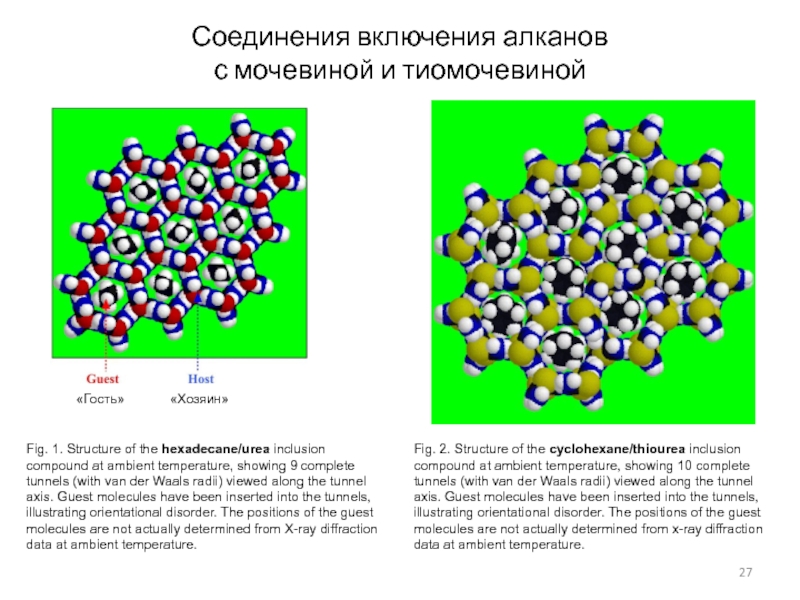
Слайд 27Соединения включения алканов
с мочевиной и тиомочевиной
Fig. 1. Structure of
the hexadecane/urea inclusion compound at ambient temperature, showing 9 complete
tunnels (with van der Waals radii) viewed along the tunnel axis. Guest molecules have been inserted into the tunnels, illustrating orientational disorder. The positions of the guest molecules are not actually determined from X-ray diffraction data at ambient temperature.Fig. 2. Structure of the cyclohexane/thiourea inclusion compound at ambient temperature, showing 10 complete tunnels (with van der Waals radii) viewed along the tunnel axis. Guest molecules have been inserted into the tunnels, illustrating orientational disorder. The positions of the guest molecules are not actually determined from x-ray diffraction data at ambient temperature.
«Гость»
«Хозяин»
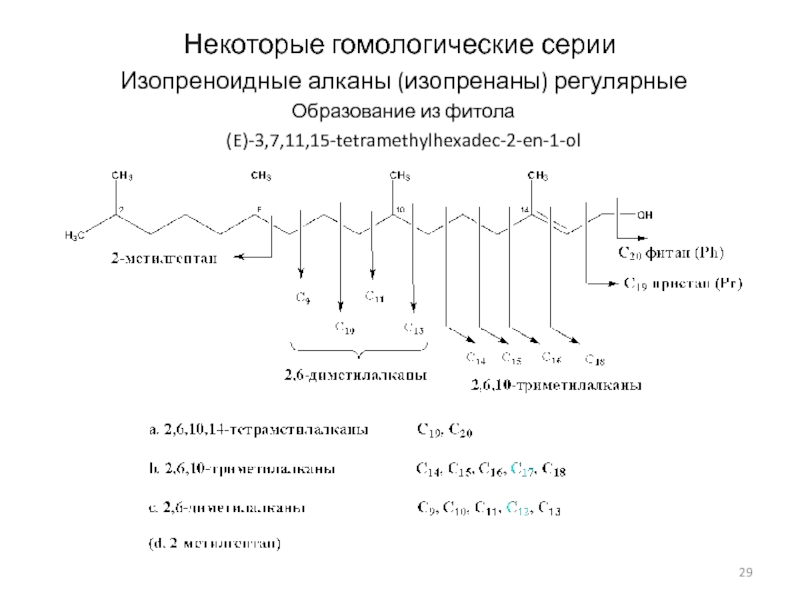
Слайд 29Некоторые гомологические серии
Изопреноидные алканы (изопренаны) регулярные
Образование из фитола
(E)-3,7,11,15-tetramethylhexadec-2-en-1-ol
Слайд 31Способы пространственного изображения молекул
Конформация (от лат. conformatio — форма, построение,
расположение) молекул, геометрические формы, которые могут принимать молекулы органических соединений
при вращении атомов или групп атомов (заместителей) вокруг простых связей при сохранении неизменными порядка химической связи атомов (химического строения), длины связей и валентных углов. Молекулы, отличающиеся только своими К., называются конформерами, или поворотными изомерами.Newman
Projection
Sawhorse
Projection
Model
Проекция
«лесопильные козлы»
Проекция
Ньюмена
Шаростержневая модель
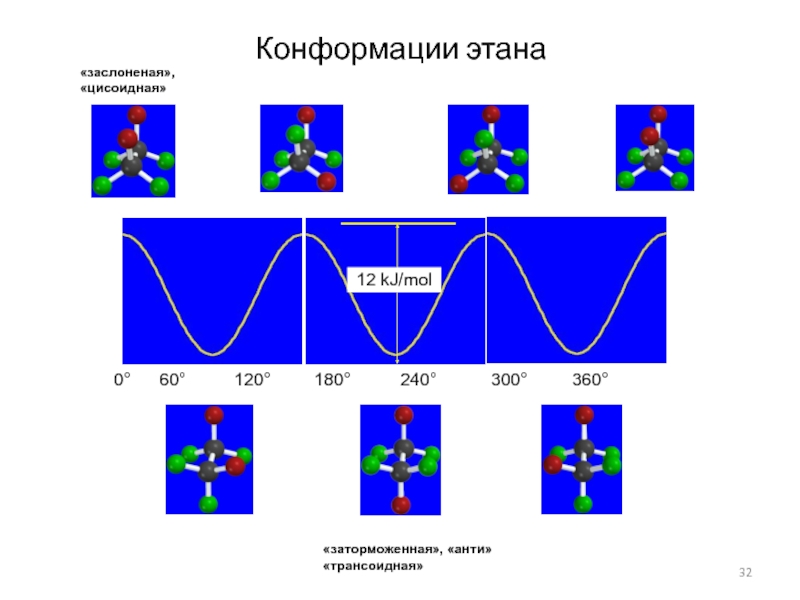
Слайд 32Конформации этана
0° 60° 120° 180°
240° 300°
360°12 kJ/mol
«заторможенная», «анти»
«трансоидная»
«заслоненая»,
«цисоидная»
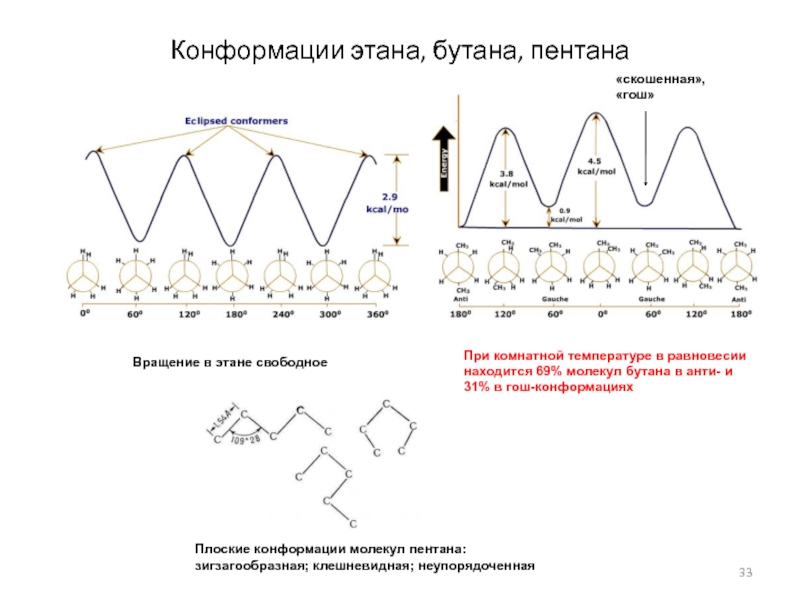
Слайд 33Конформации этана, бутана, пентана
Вращение в этане свободное
При комнатной температуре в
равновесии находится 69% молекул бутана в анти- и 31% в
гош-конформацияхПлоские конформации молекул пентана:
зигзагообразная; клешневидная; неупорядоченная
«скошенная»,
«гош»
Слайд 34Циклоалканы (циклопарафины, цикланы) [полиметилены – моноциклические циклоалканы (CH2)n] [нафтены – циклоалканы,
содержащие пяти- и шестичленные циклы]
ТИПЫ НАПРЯЖЕНИЯ В ЦИКЛАХ. 1) УГЛОВОЕ
(только малые),
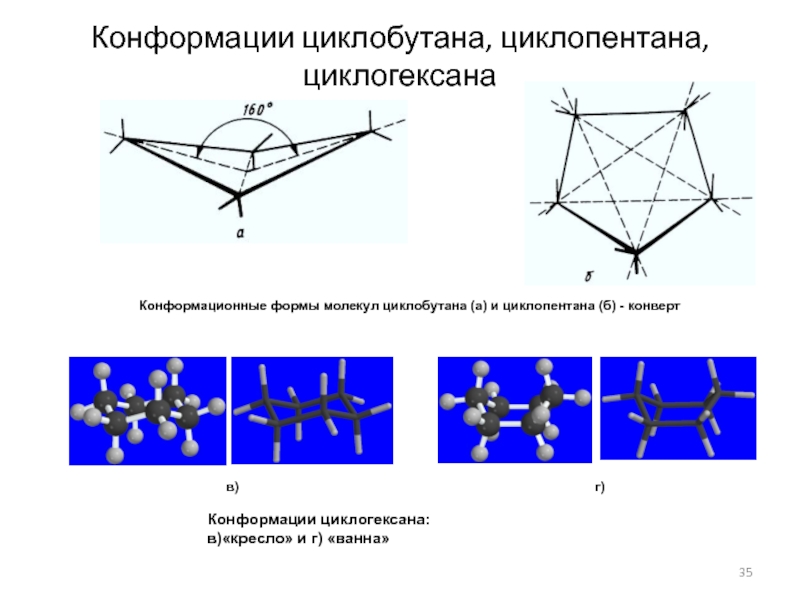
2) ТОРСИОННОЕ (заслоненное), ТРАНСАННУЛЯРНОЕ (в средних циклах). Слайд 35Конформации циклобутана, циклопентана, циклогексана
Конформационные формы молекул циклобутана (а) и циклопентана
(б) - конверт
Конформации циклогексана:
в)«кресло» и г) «ванна»
в)
г)
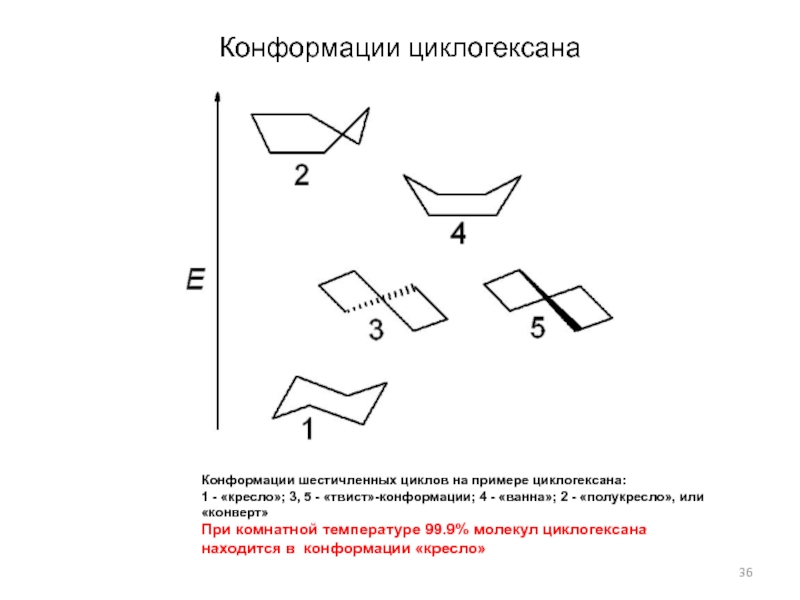
Слайд 36Конформации циклогексана
Конформации шестичленных циклов на примере циклогексана:
1 - «кресло»; 3,
5 - «твист»-конформации; 4 - «ванна»; 2 - «полукресло», или
«конверт»При комнатной температуре 99.9% молекул циклогексана находится в конформации «кресло»
Слайд 40Номенклатура циклоалканов (моноциклических)
Общая формула:
CnH2n+2-2k ,
где k - количество
циклов в
молекуле
CnH2n
Слайд 41R,S-номенклатура
Старшинство заместителей в порядке убывания:
1, 2, 3, 4
Rectus (вправо),
Sinister (влево)
Слайд 42
Бициклические нафтены
с конденсированными циклами
Декалины C10H18 (бицикло [4.4.0] деканы)
Общая
формула:
CnH2n+2-2k ,
где k - количество
циклов в молекуле
CnH2n-2
Слайд 43Бициклические нафтены
с конденсированными циклами
Пенталаны C8H14 (бицикло [3.3.0] октаны)
Общая формула:
CnH2n-2
Слайд 44Бициклические нафтены
с конденсированными циклами
Гидринданы C9H16 (бицикло [4.3.0] нонаны)
Общая формула:
CnH2n-2
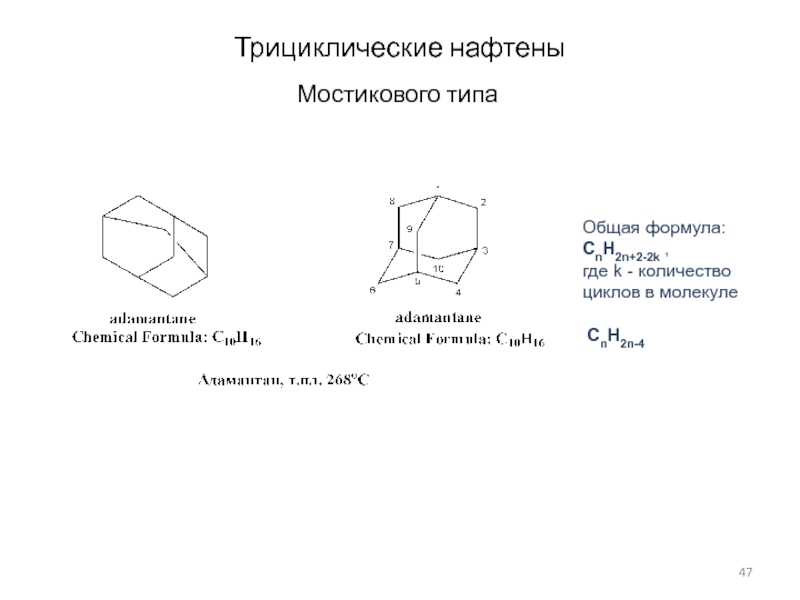
Слайд 47Трициклические нафтены
Мостикового типа
Общая формула:
CnH2n+2-2k ,
где k - количество
циклов в молекуле
CnH2n-4
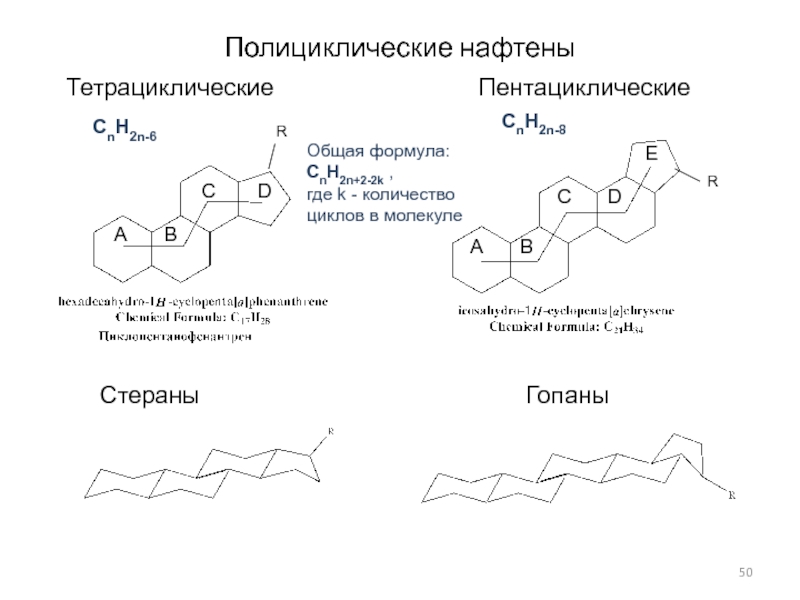
Слайд 50Полициклические нафтены
Тетрациклические
Пентациклические
Стераны Гопаны
R
R
Общая формула:
CnH2n+2-2k ,
где k - количество
циклов в молекуле
CnH2n-6
CnH2n-8
A
B
C
D
A
B
D
C
E
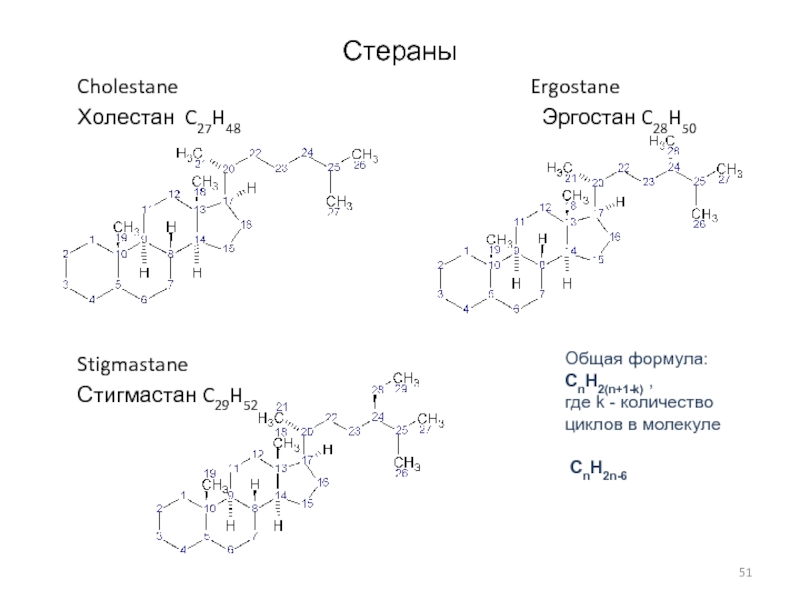
Слайд 51Стераны
Cholestane
Ergostane
Холестан C27H48 Эргостан C28H50
Stigmastane
Стигмастан C29H52
Общая формула:
CnH2(n+1-k) ,
где k - количество
циклов в молекуле
CnH2n-6
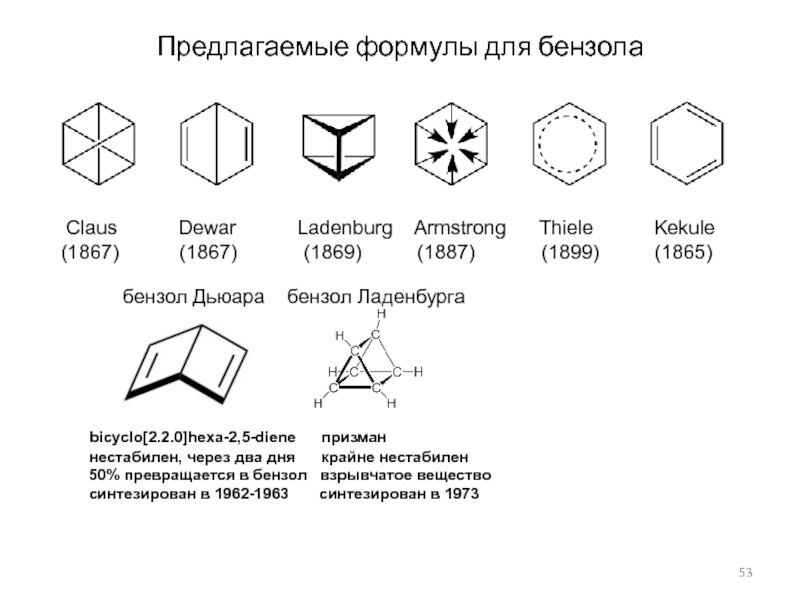
Слайд 53Предлагаемые формулы для бензола
Claus
Dewar Ladenburg Armstrong
Thiele Kekule(1867) (1867) (1869) (1887) (1899) (1865)
бензол Дьюара бензол Ладенбурга
bicyclo[2.2.0]hexa-2,5-diene призман
нестабилен, через два дня крайне нестабилен
50% превращается в бензол взрывчатое вещество
синтезирован в 1962-1963 синтезирован в 1973
Слайд 56Моноциклические арены (CnH2n-6)
Физические свойства
Стандартные фракции, отбираемые при разгонке
Слайд 57
Определение группового углеводородного состава нефтяных фракций (до 200о) методом
анилиновых точек
Арены
X=K(t-t0), где
X - содержание ароматических УВ во фракции, вес.%;
K
- коэффициент, показывающий количество аром. УВ, соответствующее понижению анилиновой точки смеси насыщенных УВ на 1оС;t - максимальная анилиновая точка фракции после удаления аром. УВ, оС ;
t0 - максимальная анилиновая точка исходной фракции, оС.
(ГОСТ 12329, ASTM D611)
Нафтены
Для фракций до 150оС
X1=K1(t1-t) /d420, где
X1 - содержание нафтеновых УВ в деароматизированной фракции, вес.%;
K 1 – анилиновый коэффициент для нафтеновых УВ;
t1 – средняя максимальная анилиновая точка чистых парафиновых УВ, оС.
d420 - Плотность деароматизированной фракции
Для фракций выше 150оС
X1=K1(t1-t)
Содержание нафтеновых УВ (вес.%) на исходную фракцию (X2):
X2=X1(100-X)/100
Парафины
Содержание парафиновых УВ, вес.%:
X3=100-(X+X2)
K, K1, t1 –
табличные
данные
Олеум
H2SO4·xSO3
или H2S2O7
Слайд 60Структурно-групповой анализ керосиновых, масляных и смолистых фракций нефтей
Метод позволяет найти
долю атомов углерода (%), содержащихся:
в ароматических кольцах СА, нафтеновых кольцах
Сн и в парафиновых цепях Сп.СА+Сн+Сп = 100 %; n и d определяются при 20оС для жидких фракций и при 70оС для твердых.
Недостатком метода n—d—M является допущение, что все кольца в среднем содержат шесть атомов углерода. Кроме того, принимается, что если число колец в молекуле больше одного, то все кольца в ней находятся в катаконденсированном состоянии. Таким образом, предполагается, что при каждом дополнительном кольце привносятся четыре атома углерода.
Применимость метода доказана для масляных фракций, содержащих до 75 % углерода в кольцевых структурах — ароматических и нафтеновых (при условии, что процентное содержание углерода в ароматических структурах не превышает более чем в 1,5 раза содержание его в нафтеновых, а число колец в молекуле не превышает четырех, из которых не более половины ароматические).
По уравнениям или номограммам находят:
СА , Скол - процентное содержание углерода в ароматических и кольчатых структурах (ароматических+нафтеновых)
КА - среднее число ароматических колец в молекуле
Ко – общее число колец (ароматических+нафтеновых)
Сн=Скол-СА; Сп=100-Скол; среднее число нафтеновых колец в молекуле Кн=Ко-КА
(ASTM D3238)
Метод n-d-M:
метод дает возможность составить представление о «средней» молекуле данной фракции и определять распределение углерода и содержание колец в УВ нефтяных фракций, кипящих выше 200 °С и не содержащих непредельных соединений.
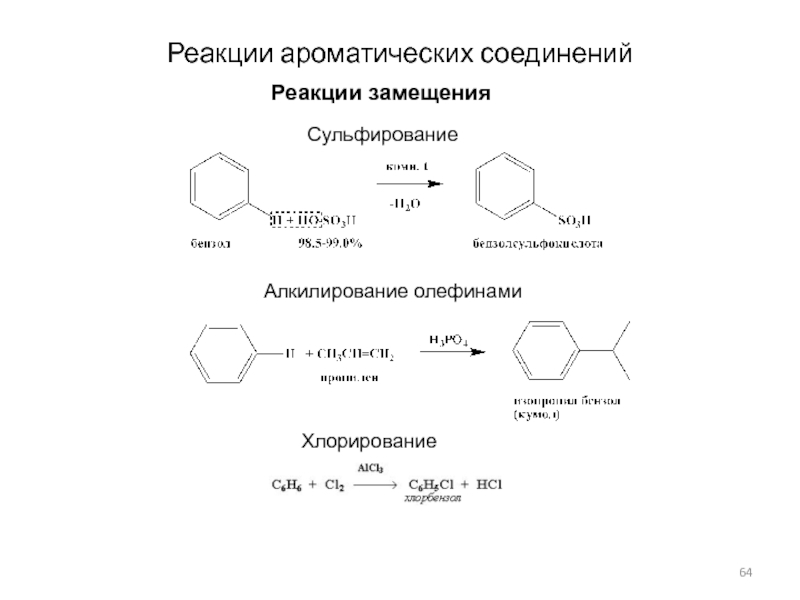
Слайд 64Реакции ароматических соединений
Реакции замещения
Алкилирование олефинами
Сульфирование
Хлорирование
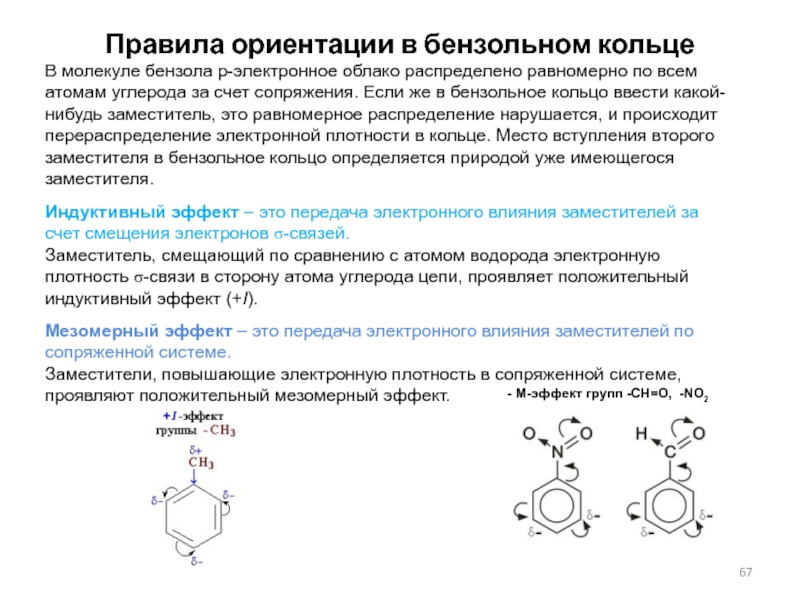
Слайд 67Правила ориентации в бензольном кольце
В молекуле бензола p-электронное облако
распределено равномерно по всем атомам углерода за счет сопряжения. Если
же в бензольное кольцо ввести какой-нибудь заместитель, это равномерное распределение нарушается, и происходит перераспределение электронной плотности в кольце. Место вступления второго заместителя в бензольное кольцо определяется природой уже имеющегося заместителя.Индуктивный эффект – это передача электронного влияния заместителей за счет смещения электронов s-связей.
Заместитель, смещающий по сравнению с атомом водорода электронную плотность s-связи в сторону атома углерода цепи, проявляет положительный индуктивный эффект (+I).
Мезомерный эффект – это передача электронного влияния заместителей по сопряженной системе.
Заместители, повышающие электронную плотность в сопряженной системе, проявляют положительный мезомерный эффект.
- M-эффект групп -СН=О, -NO2
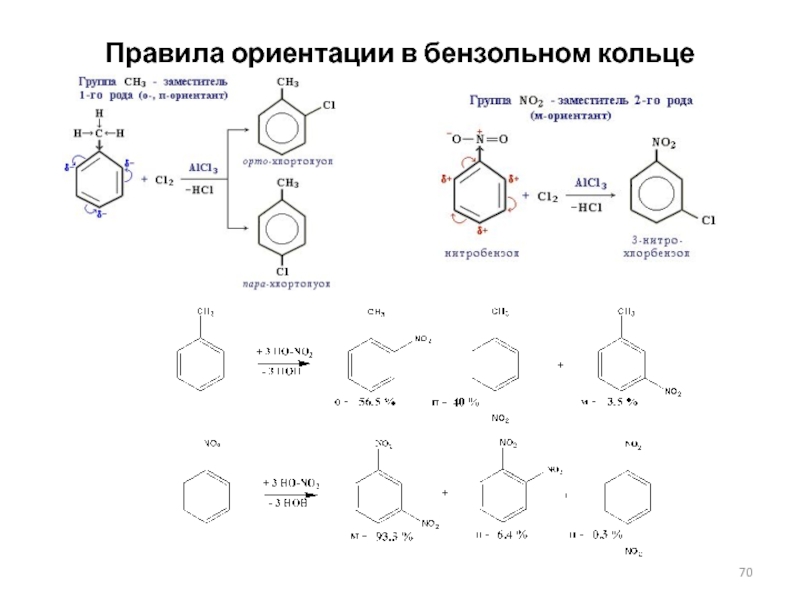
Слайд 68Правила ориентации в бензольном кольце
I. Заместители, обладающие +I-эффектом или +M-эффектом,
способствуют электрофильному замещению в орто- и пара-положения бензольного кольца и
называются заместителями (ориентантами) первого рода.-СН3 (R-) -ОН (-OR) -NH2 -CI (-F,-Вr,-I)
+I +M,-I +M,-I +М,-I
Ориентанты 1-го рода, повышая электронную плотность в бензольном кольце, увеличивают его активность в реакциях электрофильного замещения по сравнению с незамещенным бензолом.
Особое место среди ориентантов 1-го рода занимают галогены .
Являясь орто-пара-ориентантами, они замедляют электрофильное замещение. Причина - сильный –I-эффект электроотрицательных атомов галогенов, понижащий электронную плотность в кольце.
Слайд 69Правила ориентации в бензольном кольце
II. Заместители, обладающие -I-эффектом или -
M-эффектом, направляют электрофильное замещение в мета-положения бензольного кольца и называются
заместителями (ориентантами) второго рода:-S03H -ССl3 -СООН -СН=О -NO2
-М -I -М, -I -М, -I -M, –I
Ориентанты 2-го рода уменьшают электронную плотность в бензольном кольце, особенно в орто- и пара-положениях. Поэтому электрофил атакует атомы углерода не в этих положениях, а в мета-положении, где электронная плотность несколько выше.
Все ориентанты 2-го рода, уменьшая в целом электронную плотность в бензольном кольце, снижают его активность в реакциях электрофильного замещения.
Слайд 75Геохимические типы нефтей, биодеградация
Биодеградация нефтей (окисление микроорганизмами, биологическое окисление,
биологическая эволюция)
Биологическая эволюция:
А1 А2
Б2 Б1Условия (зависят от глубины залегания):
T , Влага
Аэробные и анаэробные условия
Порядок биодеградации:
н-алканы (в первую очередь С12-С18)
изо-, антеизо-алканы
изопренаны (в последнюю очередь пристан и фитан)
моноциклические нафтены
стераны, гопаны
ароматические УВ
Хемофоссилии (биометки, биомаркеры)
- соединения, сохранившие явную
структурную связь с исходными с
исходными биомолекулами.
А1 ~2000м, 90оС
А2 ~1200м, 40оС
Б2 ~1200м, 40оС
Б1 ~1200м, 40оС
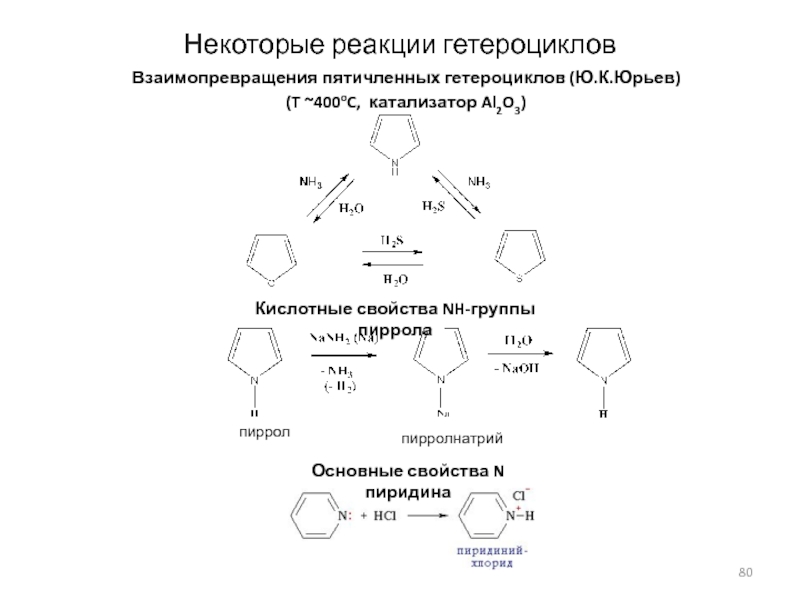
Слайд 80Некоторые реакции гетероциклов
Взаимопревращения пятичленных гетероциклов (Ю.К.Юрьев)
(T ~400oC, катализатор Al2O3)
пиррол
пирролнатрий
Кислотные свойства
NH-группы пиррола
Основные свойства N пиридина
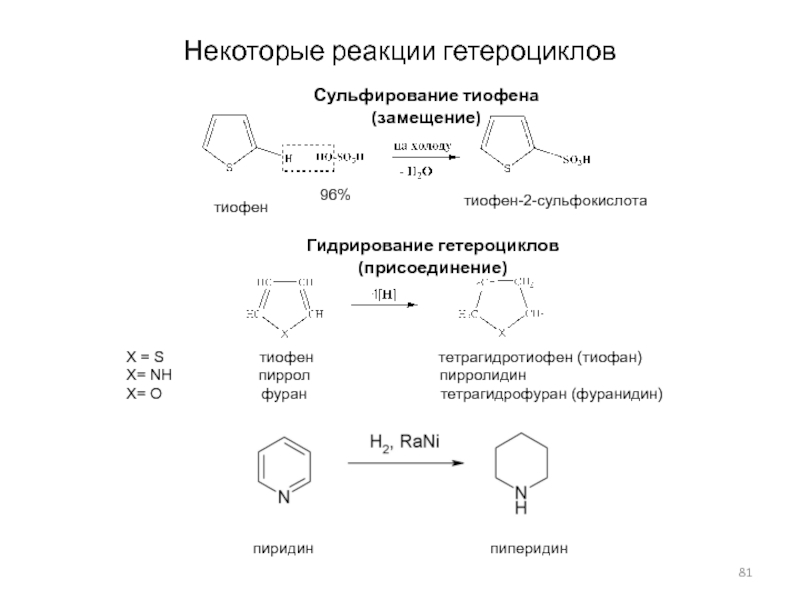
Слайд 81Некоторые реакции гетероциклов
Сульфирование тиофена (замещение)
тиофен
тиофен-2-сульфокислота
Гидрирование гетероциклов (присоединение)
X = S
тиофен
тетрагидротиофен (тиофан)X= NH пиррол пирролидин
X= O фуран тетрагидрофуран (фуранидин)
пиридин пиперидин
96%
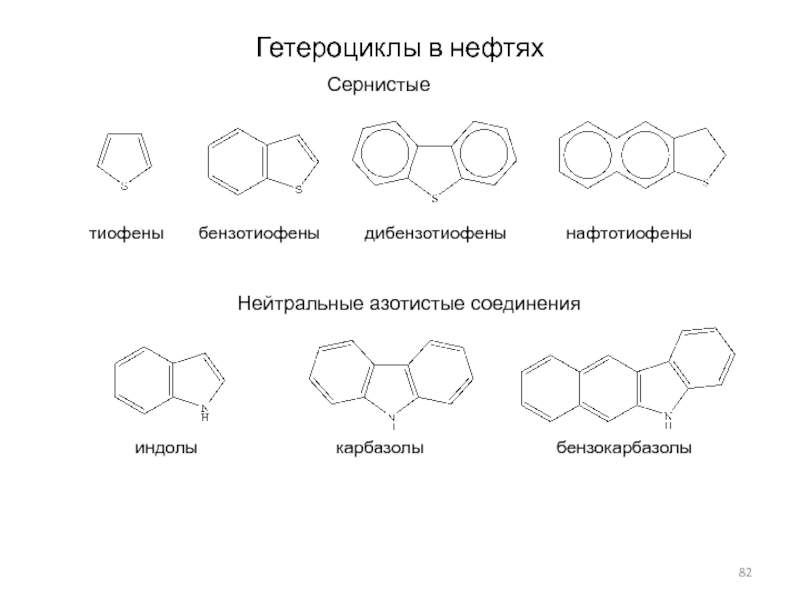
Слайд 82Гетероциклы в нефтях
тиофены бензотиофены
дибензотиофены нафтотиофены
индолы карбазолы бензокарбазолыСернистые
Нейтральные азотистые соединения
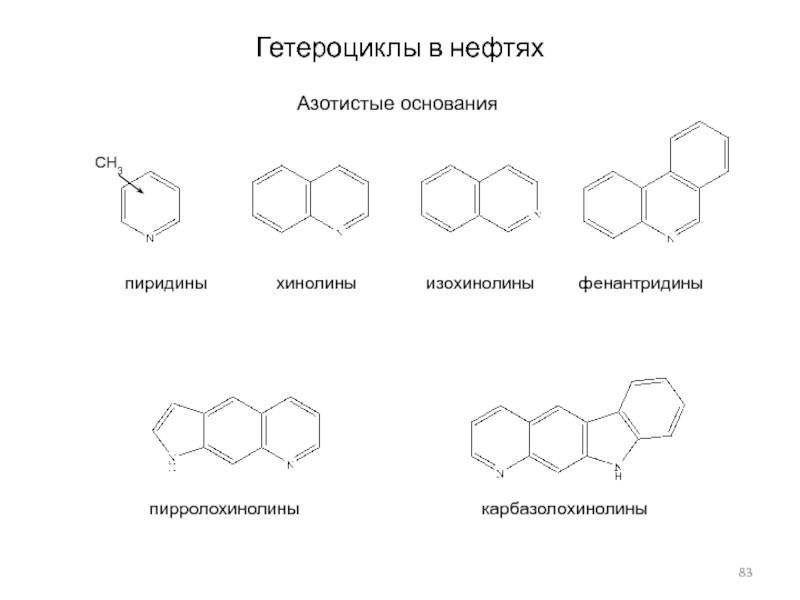
Слайд 83Гетероциклы в нефтях
Азотистые основания
CH3
пиридины
хинолины изохинолины
фенантридины пирролохинолины карбазолохинолины
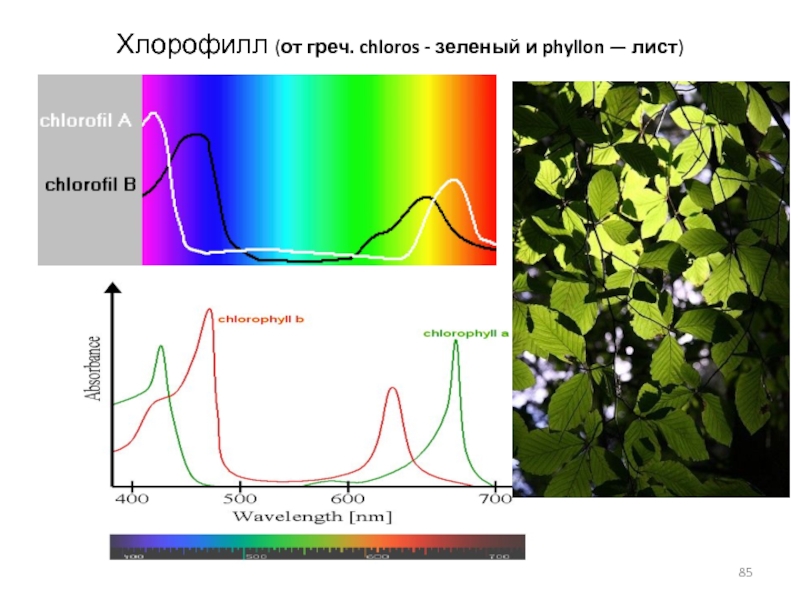
Слайд 84ХЛОРОФИЛЛ
ХЛОРОФИ́ЛЛ (от греч. χλωρός, «зелёный» и φύλλον, «лист») — зелёный
пигмент, обусловливающий окраску ХЛОРОПЛАСТОВ - особых клеточных структур - растений
в зелёный цвет, в хлоропластах он связан с белками и липидами этих структур. При его участии осуществляется процесс фотосинтеза. По химическому строению хлорофиллы — магниевые комплексы различных тетрапирролов. Хлорофиллы имеют порфириновое строение и структурно близки гему.ХЛОРОПЛА́СТЫ (от греч. «chloros» — зеленый и «plastos» - вылепленный, образованный), внутриклеточные органоиды растительной клетки, в которых осуществляется фотосинтез; окрашены в зеленый цвет (в них присутствует хлорофилл).
Реакция фотосинтеза:
6 CO2 (газ) + 12 H2O18 (ж) C6H12O6 + 6 O218 + 6 H2O
фотон
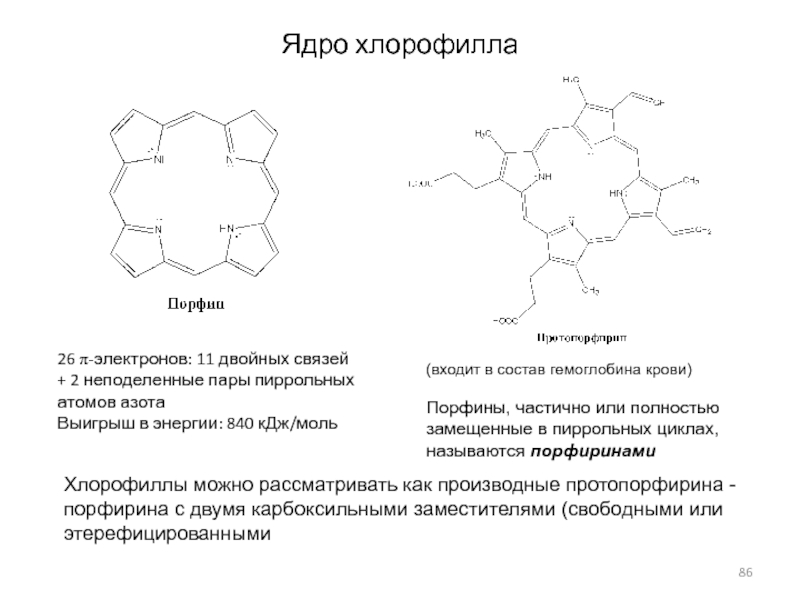
Слайд 86Ядро хлорофилла
26 p-электронов: 11 двойных связей + 2 неподеленные пары
пиррольных атомов азота
Выигрыш в энергии: 840 кДж/моль
(входит в состав гемоглобина
крови)Порфины, частично или полностью
замещенные в пиррольных циклах,
называются порфиринами
Хлорофиллы можно рассматривать как производные протопорфирина - порфирина с двумя карбоксильными заместителями (свободными или этерефицированными
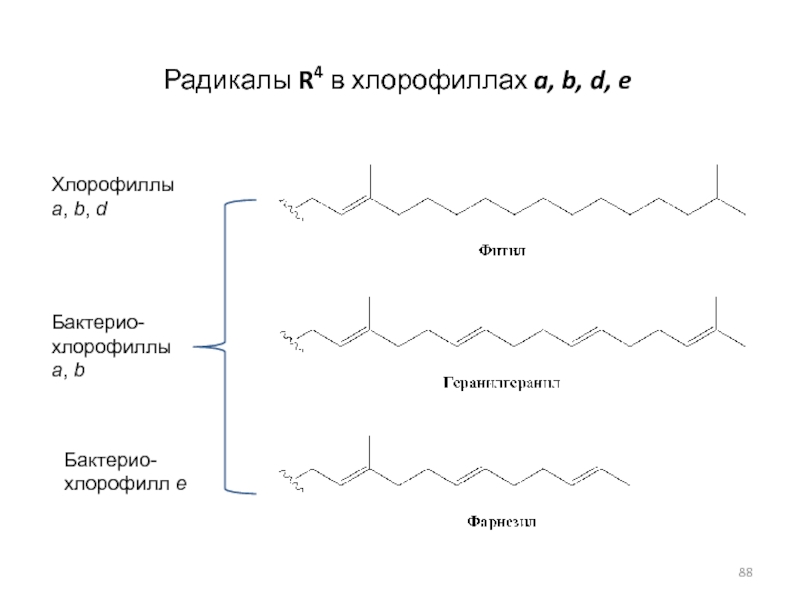
Слайд 88Радикалы R4 в хлорофиллах a, b, d, e
Хлорофиллы
a, b,
d
Бактерио-
хлорофилл e
Бактерио-
xлорофиллы
a, b
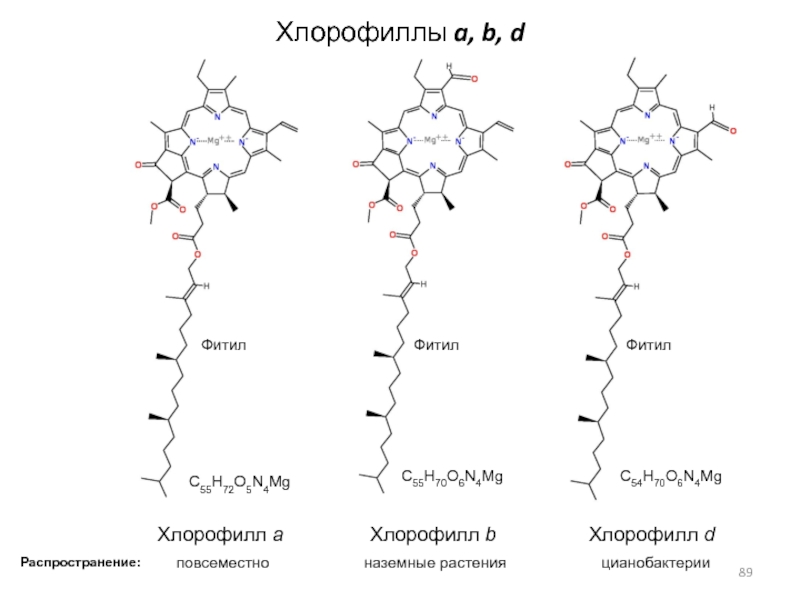
Слайд 89Хлорофиллы a, b, d
Хлорофилл a
Хлорофилл b
Хлорофилл d
Фитил
Фитил
Фитил
Распространение:
цианобактерии
наземные растения
повсеместно
C55H72O5N4Mg
C55H70O6N4Mg
C54H70O6N4Mg
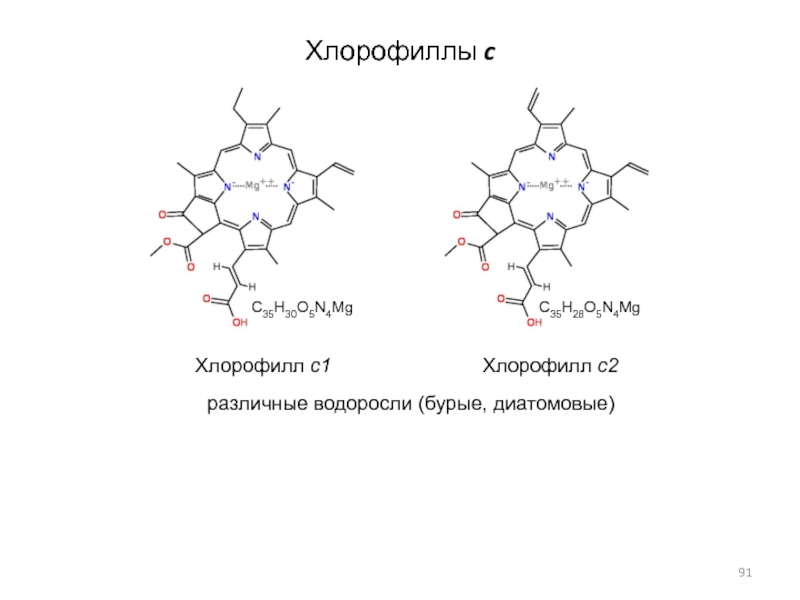
Слайд 91Хлорофиллы c
Хлорофилл c1
Хлорофилл c2
различные водоросли (бурые, диатомовые)
C35H30O5N4Mg
C35H28O5N4Mg
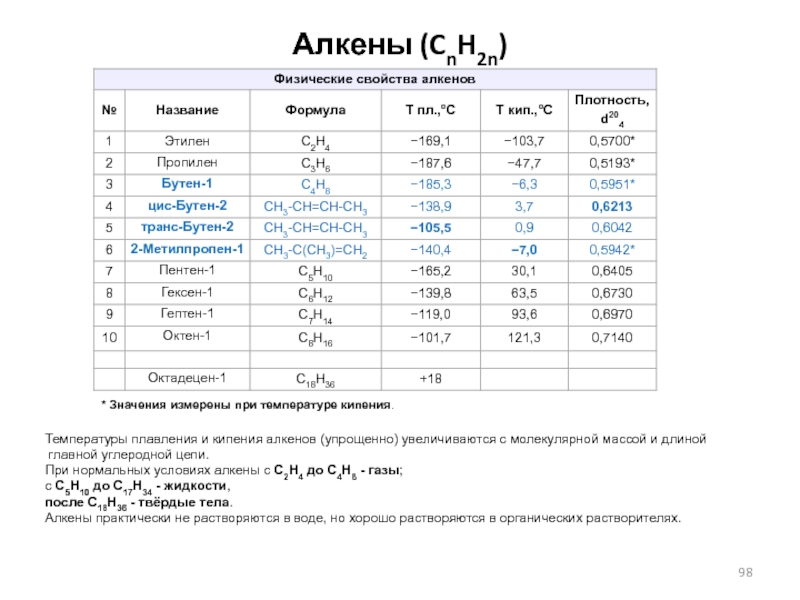
Слайд 98Алкены (CnH2n)
* Значения измерены при температуре кипения.
Температуры плавления и кипения
алкенов (упрощенно) увеличиваются с молекулярной массой и длиной
главной углеродной
цепи. При нормальных условиях алкены с C2H4 до C4H8 - газы;
с C5H10 до C17H34 - жидкости,
после C18H36 - твёрдые тела.
Алкены практически не растворяются в воде, но хорошо растворяются в органических растворителях.
Слайд 99Изомерия и номенклатура алкенов
(на примере бутенов)
1. Структурная
2. Изомерия положения двойной
связи
бутен-1
2-метилпропен-1
(изобутилен)
бутен-1
бутен-2
[1]
[2]
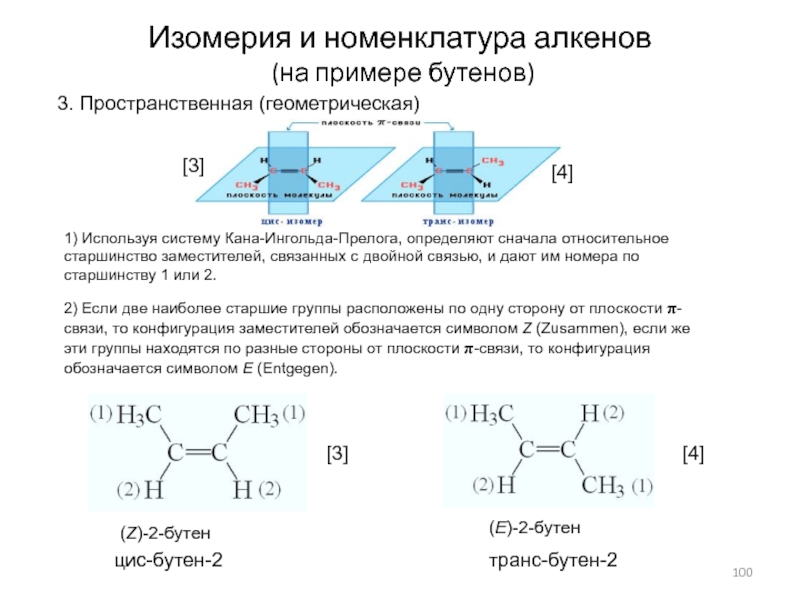
Слайд 100Изомерия и номенклатура алкенов
(на примере бутенов)
1) Используя систему Кана-Ингольда-Прелога,
определяют сначала относительное старшинство заместителей, связанных с двойной связью, и
дают им номера по старшинству 1 или 2.2) Если две наиболее старшие группы расположены по одну сторону от плоскости p-связи, то конфигурация заместителей обозначается символом Z (Zusammen), если же эти группы находятся по разные стороны от плоскости p-связи, то конфигурация обозначается символом Е (Entgegen).
(Е)-2-бутен
(Z)-2-бутен
транс-бутен-2
цис-бутен-2
3. Пространственная (геометрическая)
[3]
[4]
[3]
[4]
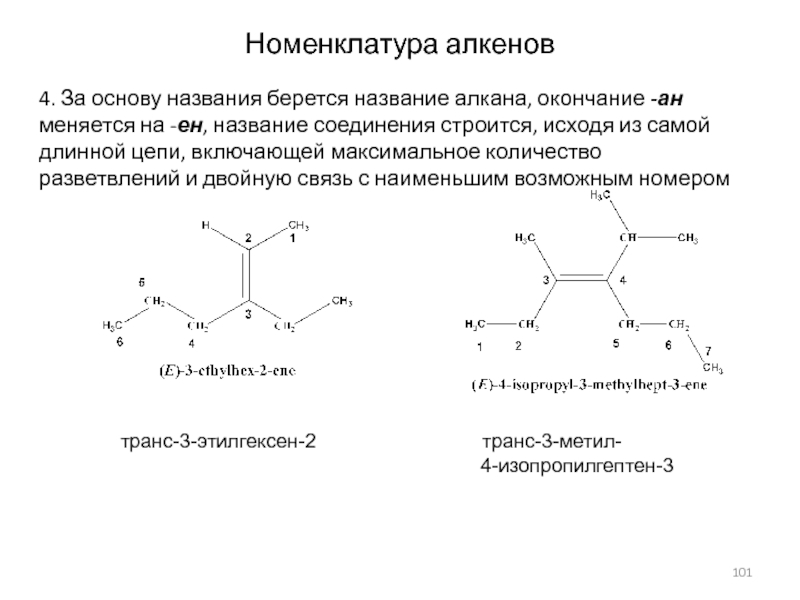
Слайд 101Номенклатура алкенов
4. За основу названия берется название алкана, окончание -ан
меняется на -ен, название соединения строится, исходя из самой длинной
цепи, включающей максимальное количество разветвлений и двойную связь с наименьшим возможным номером транс-3-этилгексен-2 транс-3-метил-
4-изопропилгептен-3
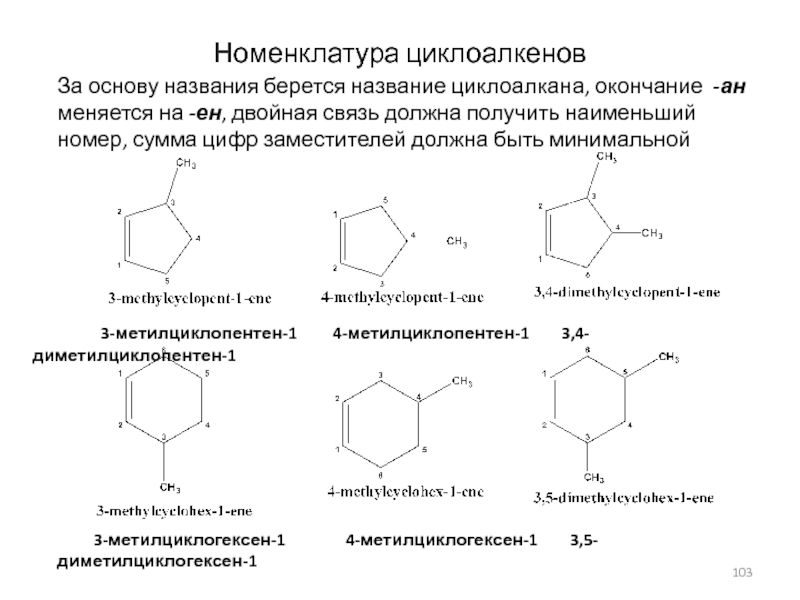
Слайд 103Номенклатура циклоалкенов
За основу названия берется название циклоалкана, окончание -ан меняется
на -ен, двойная связь должна получить наименьший номер, сумма цифр
заместителей должна быть минимальной 3-метилциклопентен-1 4-метилциклопентен-1 3,4-диметилциклопентен-1
3-метилциклогексен-1 4-метилциклогексен-1 3,5-диметилциклогексен-1
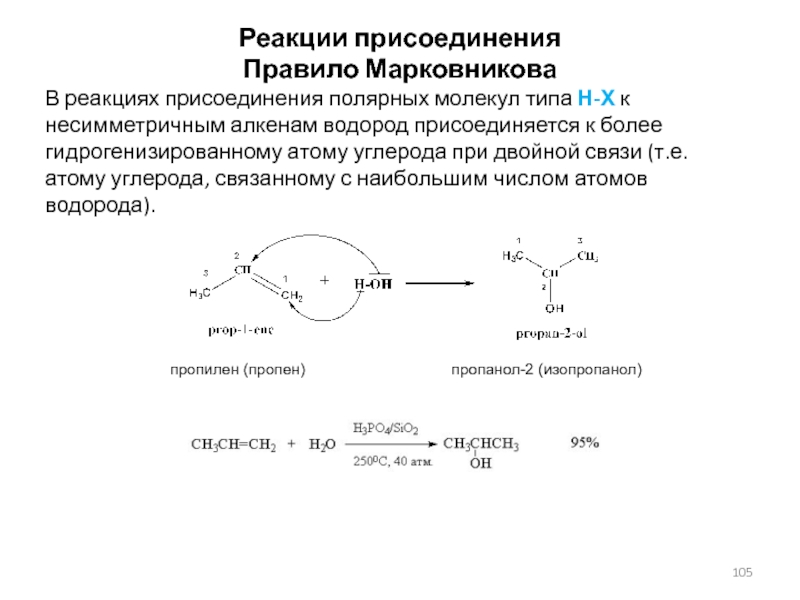
Слайд 105Реакции присоединения
Правило Марковникова
В реакциях присоединения полярных молекул типа Н-Х к
несимметричным алкенам водород присоединяется к более гидрогенизированному атому углерода при
двойной связи (т.е. атому углерода, связанному с наибольшим числом атомов водорода).пропилен (пропен) пропанол-2 (изопропанол)
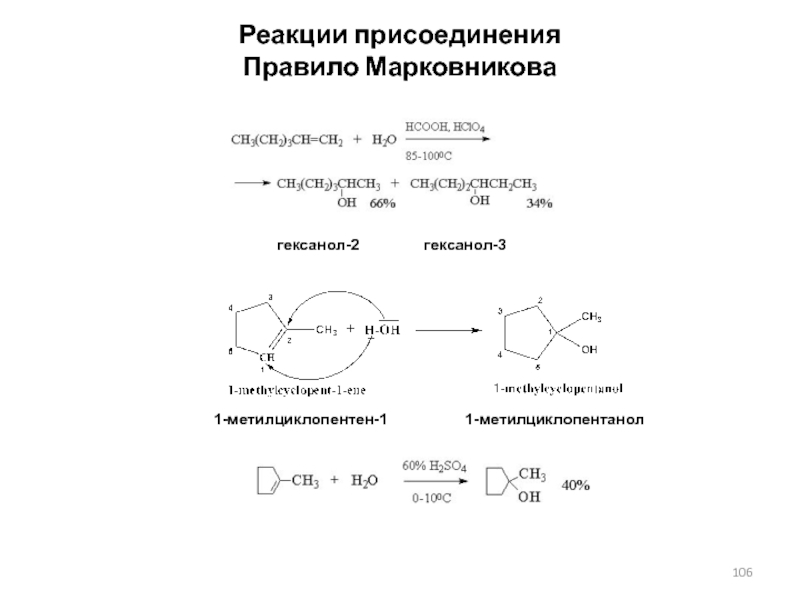
Слайд 106Реакции присоединения
Правило Марковникова
гексанол-2
гексанол-3
1-метилциклопентен-1
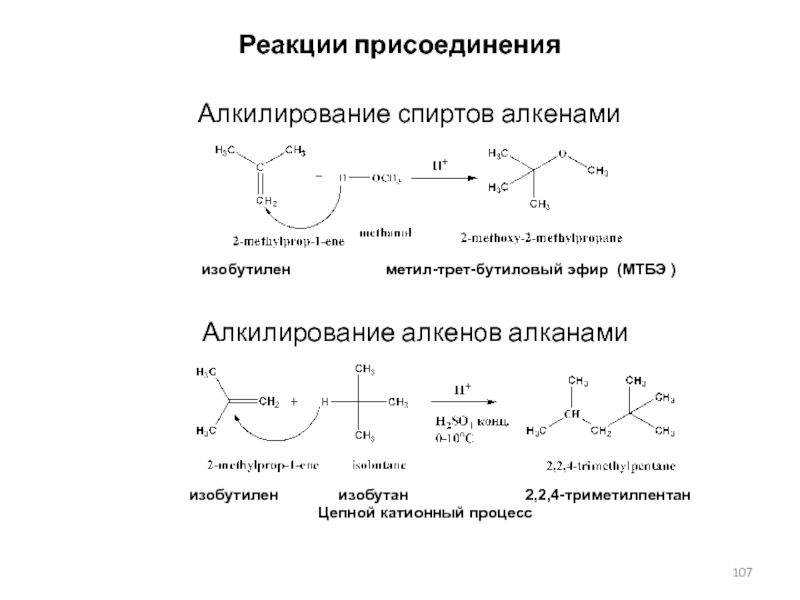
1-метилциклопентанолСлайд 107Реакции присоединения
изобутилен
метил-трет-бутиловый эфир (МТБЭ )
Алкилирование спиртов алкенами
Алкилирование алкенов алканами
изобутилен изобутан 2,2,4-триметилпентан
Цепной катионный процесс
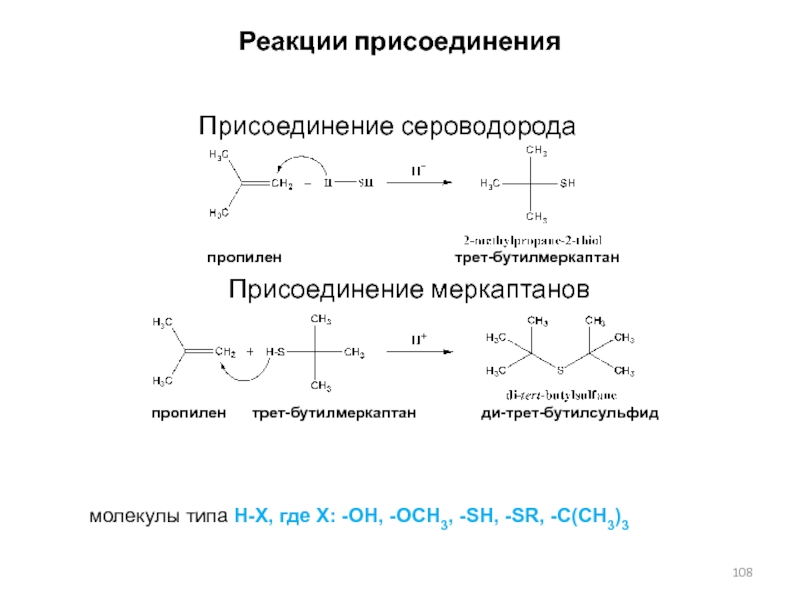
Слайд 108Реакции присоединения
Присоединение сероводорода
Присоединение меркаптанов
пропилен
трет-бутилмеркаптан
пропилен трет-бутилмеркаптан ди-трет-бутилсульфид
молекулы типа Н-Х, где X: -OH, -OCH3, -SH, -SR, -C(CH3)3
Слайд 109Димеризация (изобутилен)
Димеризация алкенов – образование димера (удвоенной молекулы) в результате
реакции присоединения. В присутствии минеральной кислоты (донора протона Н+) происходит
присоединение протона по двойной связи молекулы алкена. При этом образуется карбокатион:Этот карбокатион присоединяется к следующей молекуле алкена с образованием "димерного карбокатиона":
"Димерный карбокатион" стабилизируется путем выброса протона, что приводит к продуктам димеризации алкена – смеси изомерных диизобутиленов (2,4,4-триметипентена-2 и 2,4,4-триметилпентена-1):
60% H2SO4 ,70oC
- 20%
- 80%
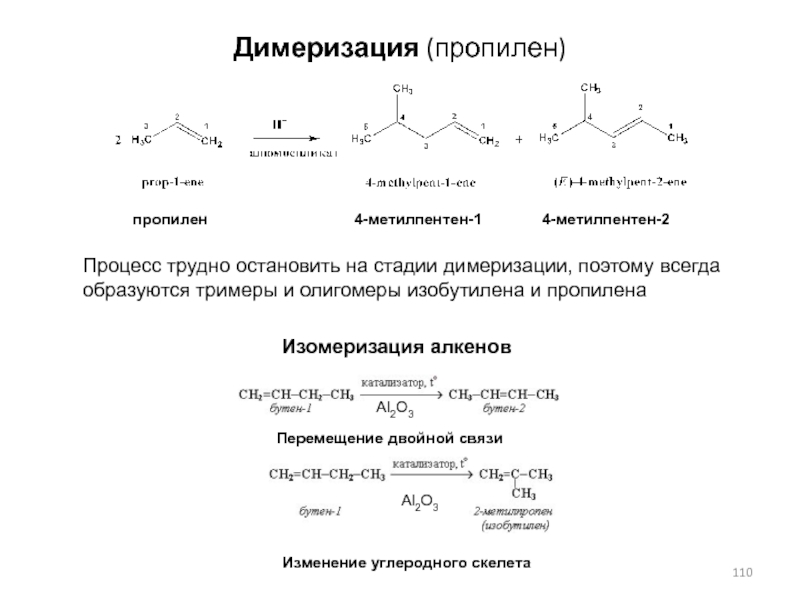
Слайд 110Димеризация (пропилен)
пропилен
4-метилпентен-1 4-метилпентен-2
Процесс трудно остановить на стадии димеризации, поэтому всегда образуются тримеры и олигомеры изобутилена и пропилена
Изомеризация алкенов
Al2O3
Al2O3
Перемещение двойной связи
Изменение углеродного скелета
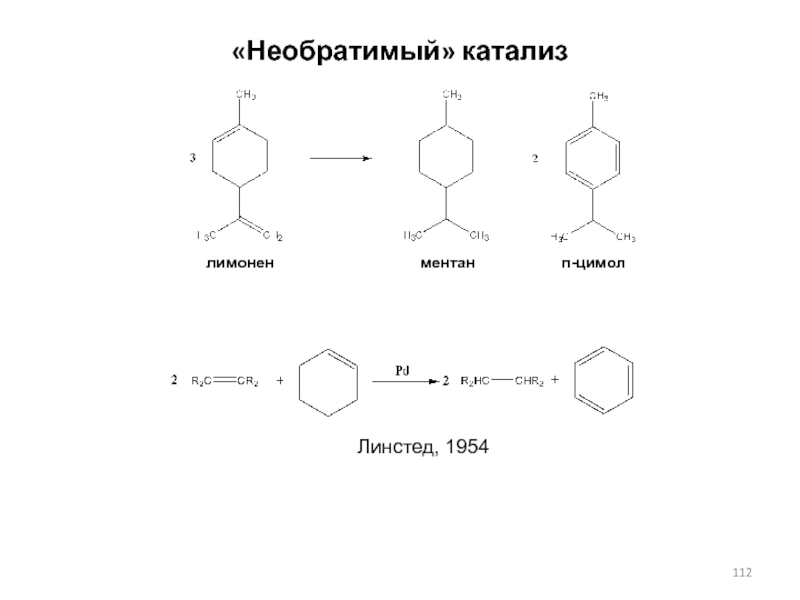
Слайд 111«Необратимый» катализ
(Н.Д.Зелинский, 1911 г.)
Каталитическое диспропорционирование углеводородов ряда циклогексена
с образованием соответствующих
производных бензола и циклогексана
(перераспределение водорода , дисмутация)
циклогексилацетилен
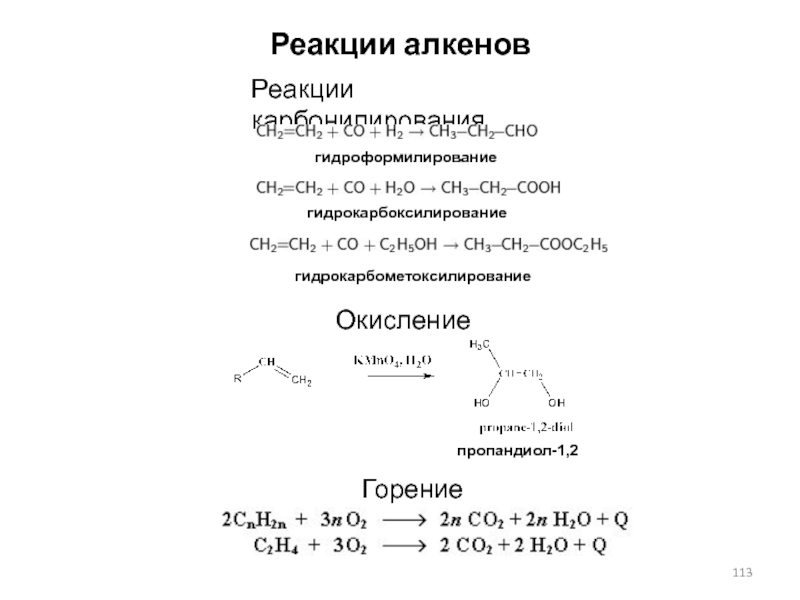
Слайд 113Реакции алкенов
Реакции карбонилирования
гидроформилирование
гидрокарбоксилирование
гидрокарбометоксилирование
Окисление
пропандиол-1,2
Горение
Слайд 114Алкадиены (диены) (CnH2n-2)
Классификация
1. Диены с кумулированными связями (аллены,
замещённые производные пропадиена-1,2
H2C=C=CH2)
2. Сопряжённые диены, или 1,3-диены
(замещённые производные бутадиена-1,3 CH2=CH–CH=CH2)
3. Изолированные диены,
в которых двойные связи располагаются через две и более простых связи С–С.дивинил
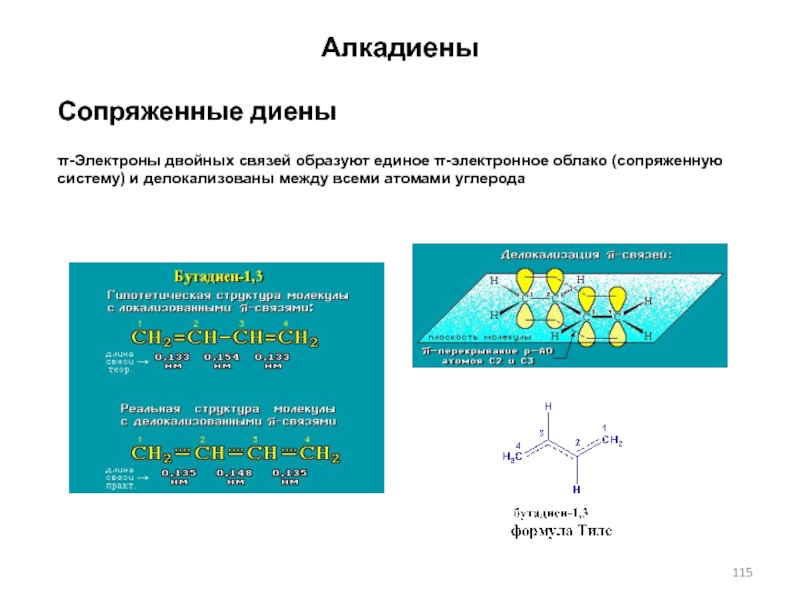
Слайд 115Алкадиены
Сопряженные диены
π-Электроны двойных связей образуют единое π-электронное облако (сопряженную систему)
и делокализованы между всеми атомами углерода
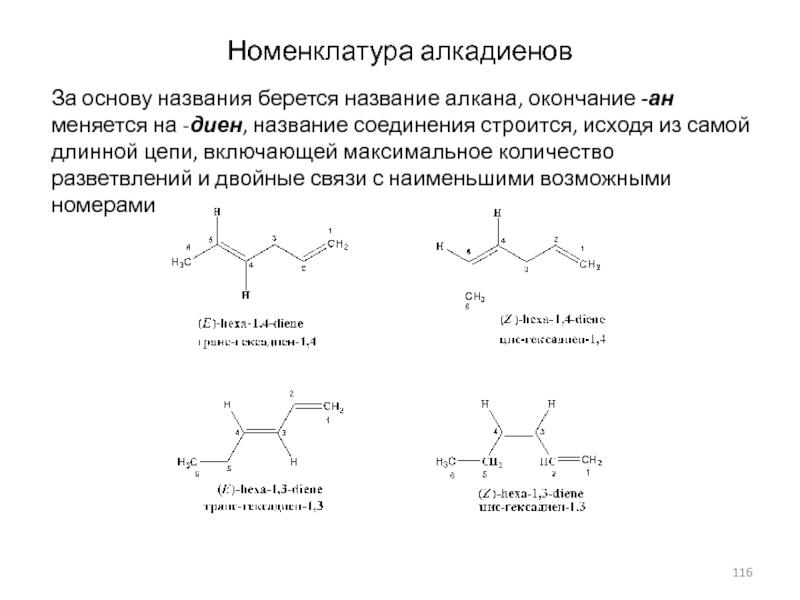
Слайд 116Номенклатура алкадиенов
За основу названия берется название алкана, окончание -ан меняется
на -диен, название соединения строится, исходя из самой длинной цепи,
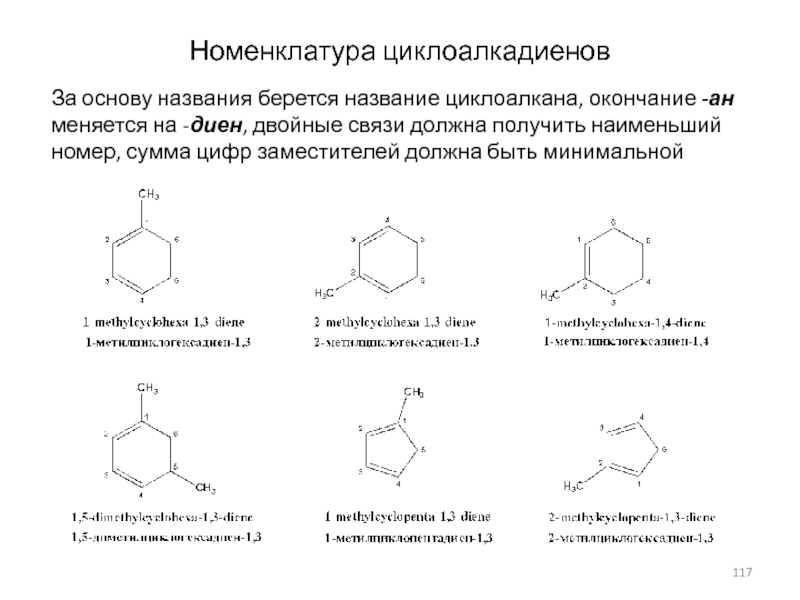
включающей максимальное количество разветвлений и двойные связи с наименьшими возможными номерамиСлайд 117Номенклатура циклоалкадиенов
За основу названия берется название циклоалкана, окончание -ан меняется
на -диен, двойные связи должна получить наименьший номер, сумма цифр
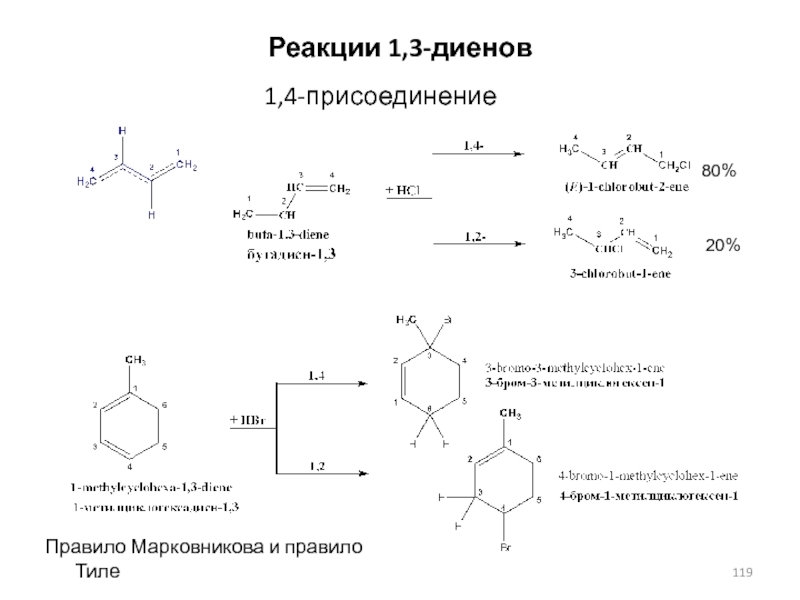
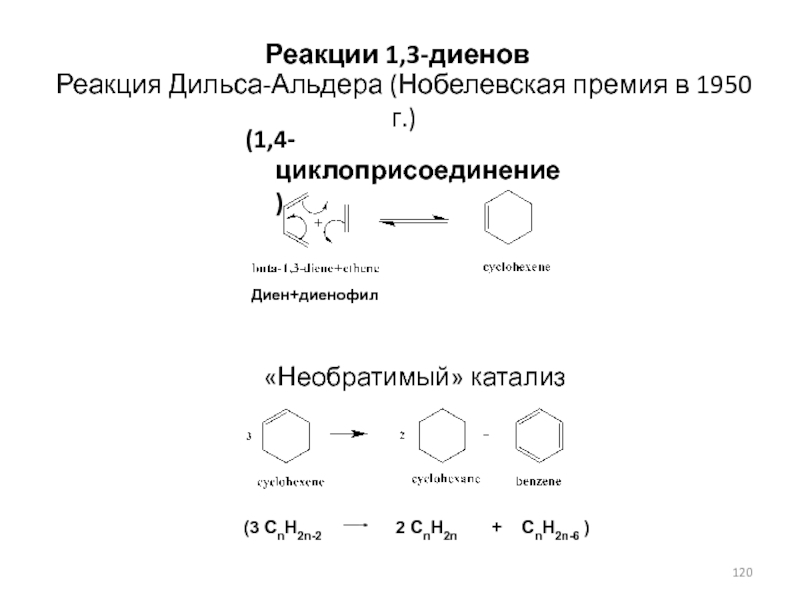
заместителей должна быть минимальнойСлайд 120Реакция Дильса-Альдера (Нобелевская премия в 1950 г.)
(3 CnH2n-2
2 CnH2n
+ CnH2n-6 )(1,4-циклоприсоединение)
«Необратимый» катализ
Диен+диенофил
Реакции 1,3-диенов
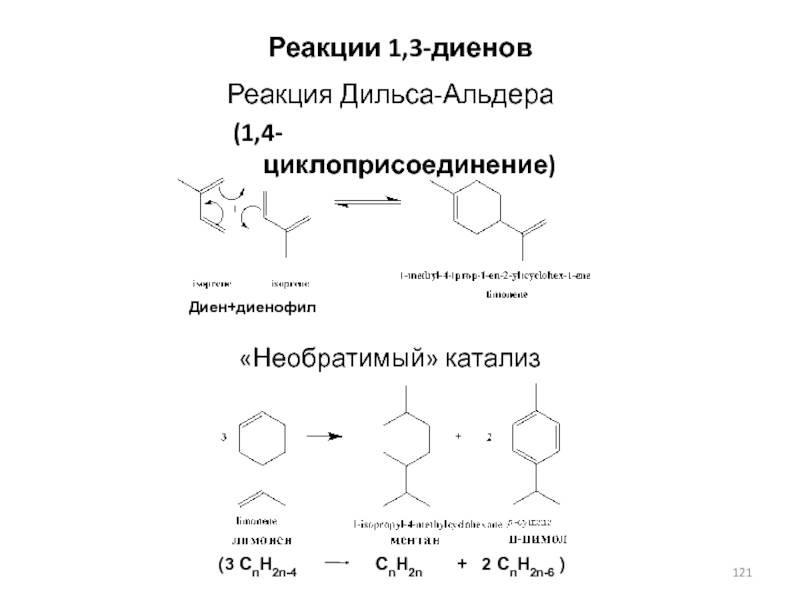
Слайд 121Реакция Дильса-Альдера
(1,4-циклоприсоединение)
«Необратимый» катализ
Диен+диенофил
Реакции 1,3-диенов
(3 CnH2n-4
CnH2n +
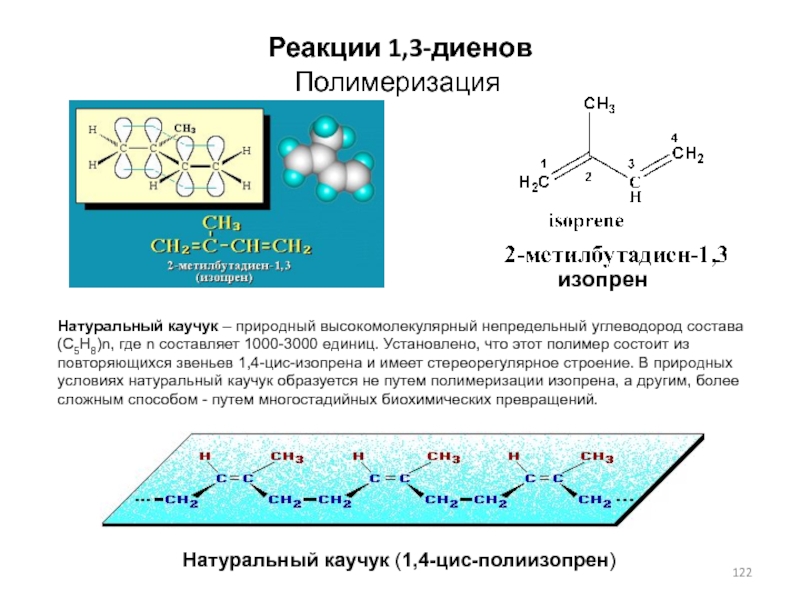
2 CnH2n-6 )Слайд 122Полимеризация
Реакции 1,3-диенов
изопрен
Натуральный каучук (1,4-цис-полиизопрен)
Натуральный каучук – природный высокомолекулярный непредельный
углеводород состава (С5Н8)n, где n составляет 1000-3000 единиц. Установлено, что
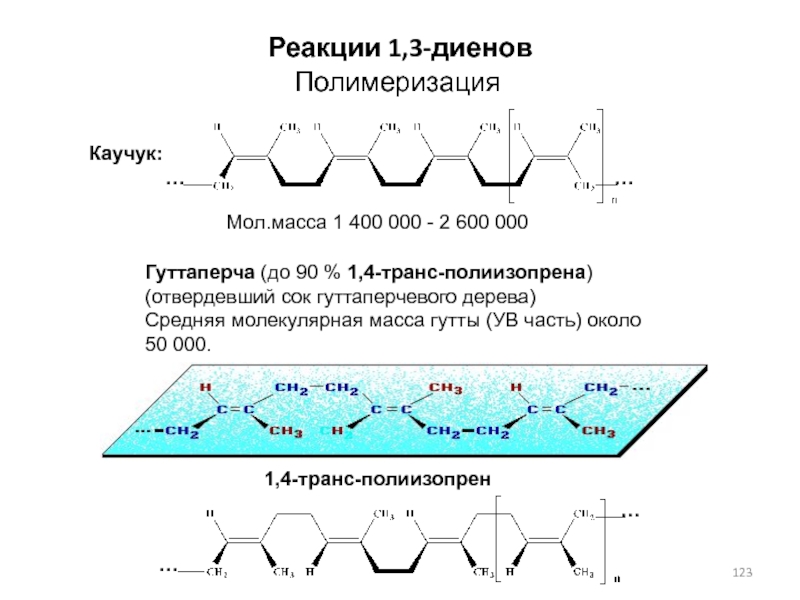
этот полимер состоит из повторяющихся звеньев 1,4-цис-изопрена и имеет стереорегулярное строение. В природных условиях натуральный каучук образуется не путем полимеризации изопрена, а другим, более сложным способом - путем многостадийных биохимических превращений.Слайд 123Полимеризация
Реакции 1,3-диенов
Гуттаперча (до 90 % 1,4-транс-полиизопрена)
(отвердевший сок гуттаперчевого дерева)
Средняя
молекулярная масса гутты (УВ часть) около 50 000.
Каучук:
1,4-транс-полиизопрен
Мол.масса 1 400
000 - 2 600 000…
…
…
…
Слайд 125Терпены
Полиизопреновые структуры с невысокой степенью полимеризации содержатся в смоле хвойных
деревьев, в эфирных маслах растений (герани, розы, лаванды, лимона и
др.), входят в состав некоторых липидов.Много терпенов выделяется из хвойной смолы например сосны.
Терпе́ны - класс углеводородов - продуктов биосинтеза общей формулы (C5H8)n, с углеродным скелетом, формально являющихся производным (олигомером) изопрена. В больших количествах терпены содержатся в растениях семейства хвойные, во многих эфирных маслах. Терпены - основной компонент смол и бальзамов, так, скипидар получают из живицы. Название «Терпены» происходит от лат. «Oleum Terepinthinae» — скипидар.
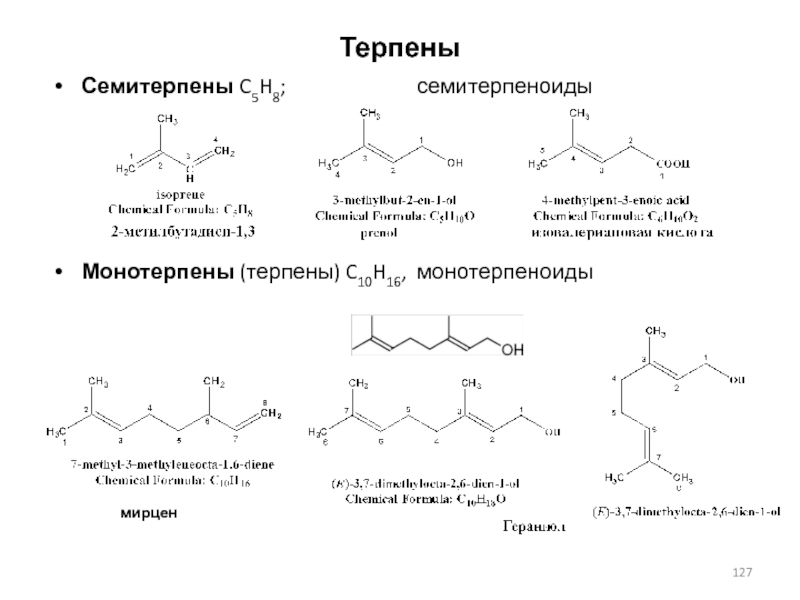
Слайд 126Терпены
Терпены классифицируют по числу изопреновых звеньев, образующих углеродный скелет молекулы
Семитерпены
C5H8;
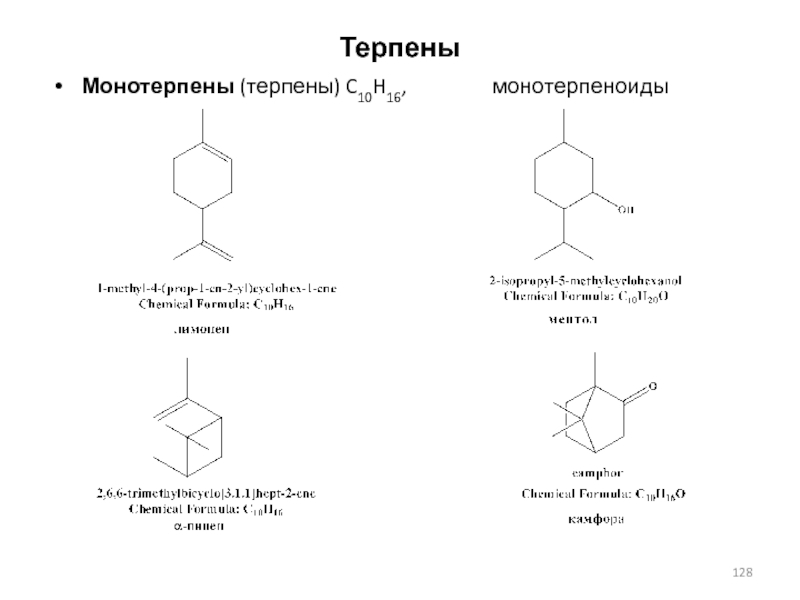
Монотерпены (терпены) C10H16,
Сесквитерпены (полуторатерпены) C15H24,
Дитерпены C20H32, (C10H16)2;
Тритерпены, C30H48, (C10H16)3;
Тетратерпены C40H64,
(C10H16)4;Политерпены (C5H8)n, где n > 8.
Сами углеводороды называют терпеновыми углеводородами (терпенами), а их кислородсодержащие производные – терпеноидами.
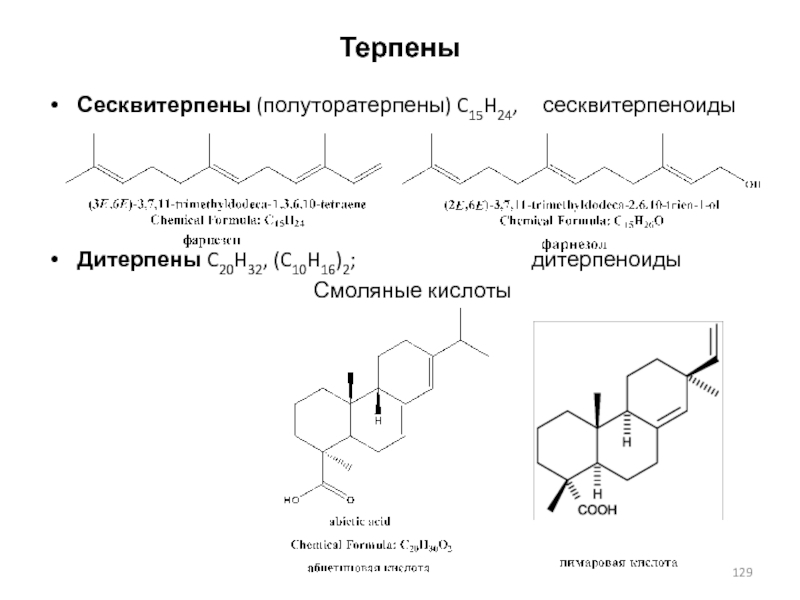
Слайд 129Терпены
Сесквитерпены (полуторатерпены) C15H24, сесквитерпеноиды
Дитерпены C20H32, (C10H16)2;
дитерпеноиды
Смоляные кислоты
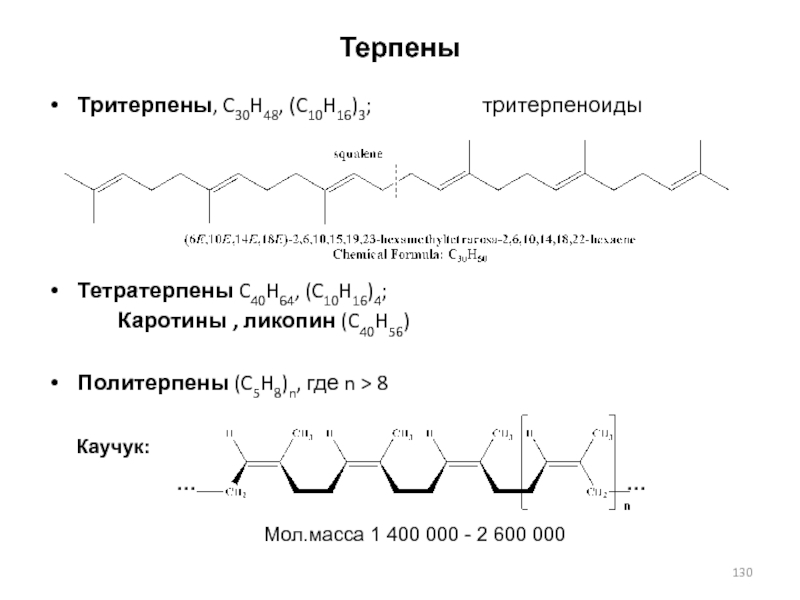
Слайд 130Терпены
Тритерпены, C30H48, (C10H16)3;
тритерпеноиды
Тетратерпены C40H64, (C10H16)4;
Каротины , ликопин (C40H56)Политерпены (C5H8)n, где n > 8
Каучук:
Мол.масса 1 400 000 - 2 600 000
…
…
Слайд 132Изомерия и номенклатура алкинов (CnH2n-2)
Структурная изомерия
Изомерия положения тройной связи (начиная
с С4Н6):
Изомерия углеродного скелета (начиная с С5Н8):
Межклассовая изомерия с алкадиенами
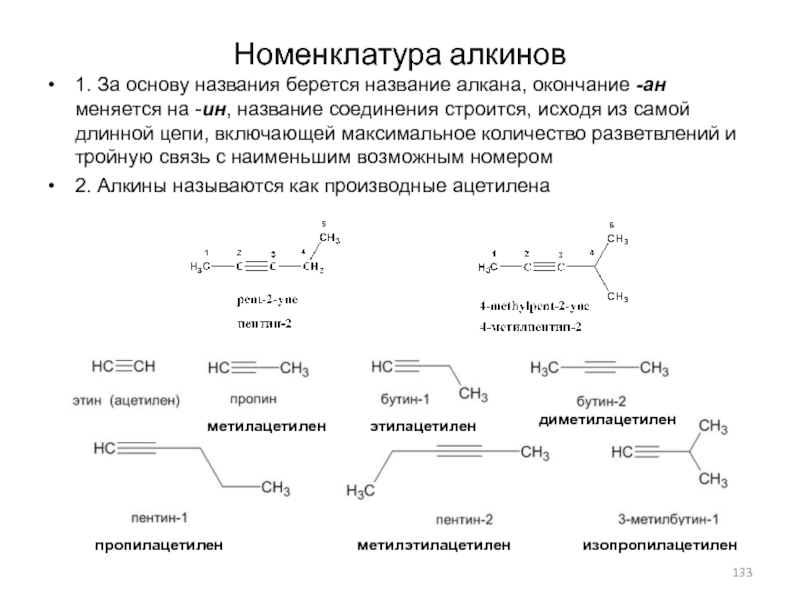
и циклоалкенами, начиная с С4Н6:Слайд 133Номенклатура алкинов
1. За основу названия берется название алкана, окончание -ан
меняется на -ин, название соединения строится, исходя из самой длинной
цепи, включающей максимальное количество разветвлений и тройную связь с наименьшим возможным номером2. Алкины называются как производные ацетилена
метилацетилен
этилацетилен
диметилацетилен
изопропилацетилен
пропилацетилен
метилэтилацетилен














![Введение в специальность Циклоалканы (циклопарафины, цикланы) [полиметилены – моноциклические циклоалканы (CH2)n] [нафтены – циклоалканы, Циклоалканы (циклопарафины, цикланы) [полиметилены – моноциклические циклоалканы (CH2)n] [нафтены – циклоалканы, содержащие пяти- и шестичленные циклы]ТИПЫ](/img/thumbs/eed67add75550a9c7df6bcc08a848ff3-800x.jpg)

![Введение в специальность Бициклические нафтены с конденсированными циклами Декалины C10H18 (бицикло [4.4.0] деканы)Общая Бициклические нафтены с конденсированными циклами Декалины C10H18 (бицикло [4.4.0] деканы)Общая формула:CnH2n+2-2k ,где k -](/img/thumbs/faf225f834916ad5dfcb20d89c921e1a-800x.jpg)
![Введение в специальность Бициклические нафтены с конденсированными цикламиПенталаны C8H14 (бицикло [3.3.0] октаны)Общая формула:CnH2n-2 Бициклические нафтены с конденсированными цикламиПенталаны C8H14 (бицикло [3.3.0] октаны)Общая формула:CnH2n-2](/img/thumbs/5cd280ee2158414b172440a14da43bfb-800x.jpg)
![Введение в специальность Бициклические нафтены с конденсированными цикламиГидринданы C9H16 (бицикло [4.3.0] нонаны)Общая формула:CnH2n-2 Бициклические нафтены с конденсированными цикламиГидринданы C9H16 (бицикло [4.3.0] нонаны)Общая формула:CnH2n-2](/img/thumbs/336ca0bb13becde7803c7f505fdf5530-800x.jpg)














![Введение в специальность Изомерия и номенклатура алкенов (на примере бутенов)1. Структурная2. Изомерия положения двойной связибутен-12-метилпропен-1(изобутилен)бутен-1бутен-2[1][2] Изомерия и номенклатура алкенов (на примере бутенов)1. Структурная2. Изомерия положения двойной связибутен-12-метилпропен-1(изобутилен)бутен-1бутен-2[1][2]](/img/thumbs/a56ce9b5d5eebfb357aac498ab872534-800x.jpg)