Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация к уроку: Структура таблицы химических элементов.
Содержание
- 1. Презентация к уроку: Структура таблицы химических элементов.
- 2. Цитата: Человек образованный - тот, кто
- 3. Информация об элементеСимвол элемента- условное обозначениеПорядковый номер-
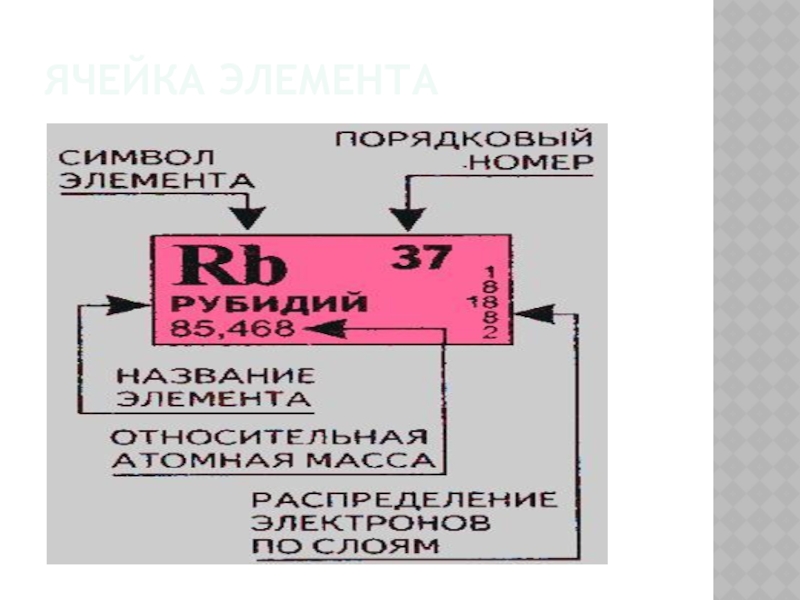
- 4. Ячейка элемента
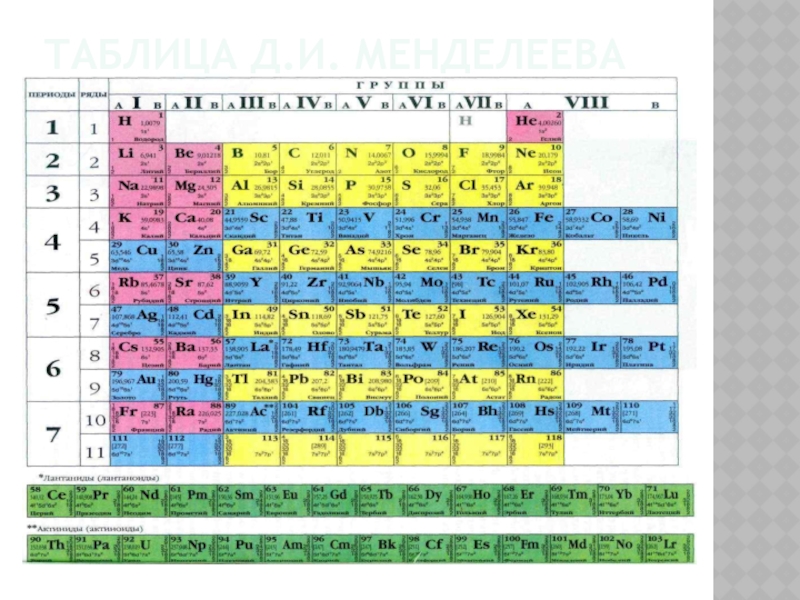
- 5. Таблица Д.И. Менделеева
- 6. Тема урокаСтруктура таблицы химических элементов
- 7. Создатель таблицы
- 8. Период- горизонтальный ряд химических элементов.Малые периоды -1, 2, 3Большие периоды-4,5,6,7
- 9. Группа- вертикальный столбик элементов с похожими свойствамиГруппаГлавная
- 10. Найдите элемент1 период, VIII гр., главная подгруппа—He3
- 11. Относительная атомная массаАr- а.е.мФизическая величина, которая показывает
- 12. Примеры относительных атомных массАr (Fe)= 55,8 =56 а.е.мАr (Li)= 6,9= 7 а.е.мАr (С)= 12,1= 12 а.е.м
- 13. Определите место положение элемента и его АrФторНатрийАргентумСераМедьХлор
- 14. Кроссворд
- 15. Скачать презентанцию
Цитата: Человек образованный - тот, кто знает где найти то, чего он не знает. ГЕОРГ ЗИММЕЛЬ
Слайды и текст этой презентации
Слайд 3Информация об элементе
Символ элемента-
условное обозначение
Порядковый номер-
заряд ядра
Количество протонов
Пренадлежность
к Металлам или Неметаллам
По диагонали от В до Аt
Слайд 8Период- горизонтальный ряд химических элементов.
Малые периоды -1, 2, 3
Большие периоды-4,5,6,7
Слайд 9Группа- вертикальный столбик элементов с похожими свойствами
Группа
Главная
Побочная
Розовый,
Желтый
СинийСлайд 10Найдите элемент
1 период, VIII гр., главная подгруппа—
He
3 период, V гр.,
главная подгруппа---
P
4 период, II гр., побочная подгруппа—
Zn
4 период, VI гр.,
побочная подгруппа-Cr