Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Реакции замещения 8 класс
Содержание
- 1. Реакции замещения 8 класс
- 2. Цель:изучение нового типа химических реакций – реакциями
- 3. «Химия не должна ограничиваться одним изучением изменений
- 4. Опыт английского химика Г. КавендишаНальем в пробирку
- 5. Составим уравнение реакции цинка с соляной
- 6. Zn + H2SO4 → ZnSO4 +H2 ↑
- 7. Вытеснительный ряд активности металлов Металлы, расположенные в
- 8. Узнали, что такое реакции замещения и какие
- 9. Домашнее задание§32 упр. №№1-2, стр. 187
- 10. Источники информации Габриелян О.С. Химия. 8 класс.
- 11. Скачать презентанцию
Цель:изучение нового типа химических реакций – реакциями замещения. Задачи: познакомить учащихся с рядом активности металлов, составленным русским химиком Н.Н. Бекетовым; показать с помощью лабораторных опытов, как ряд активности металлов можно использовать
Слайды и текст этой презентации
Слайд 2Цель:
изучение нового типа химических реакций – реакциями замещения.
Задачи:
познакомить
учащихся с рядом активности металлов, составленным русским химиком Н.Н. Бекетовым;
показать с помощью лабораторных опытов, как ряд активности металлов можно использовать для прогнозирования возможности протекания реакций вытеснения одних металлов из растворов их солей другими;
расширить знания о влиянии природы веществ на интенсивность протекания реакции.
Слайд 3«Химия не должна ограничиваться одним изучением изменений в составе тел,
потому что одним этим путем нельзя решить основного вопроса химии
о причине химических реакций»Д.И. Менделеев
Слайд 4Опыт английского химика Г. Кавендиша
Нальем в пробирку 2-3 мл соляной
кислоты и опустим в неё 2-3 гранулы цинка.
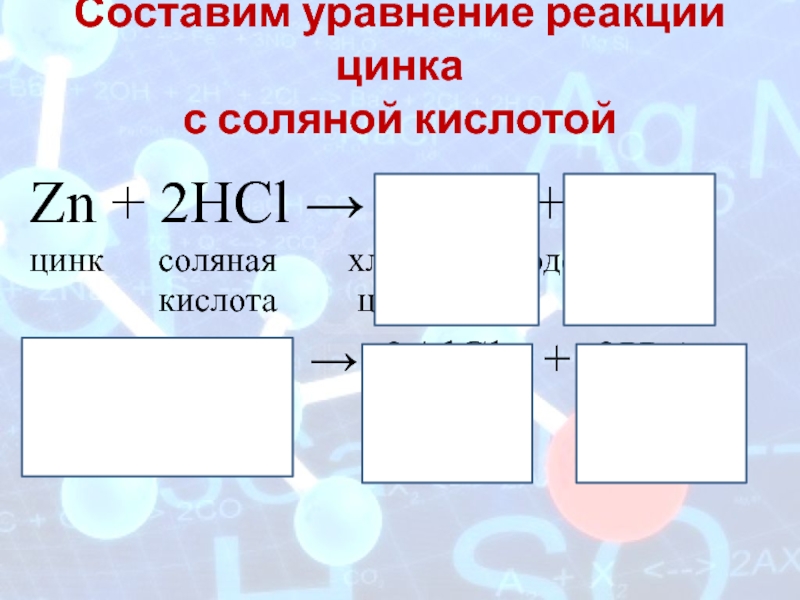
Слайд 5Составим уравнение реакции цинка
с соляной кислотой
Zn + 2HCl →
ZnCl2 +H2 ↑
цинк соляная
хлорид водород кислота цинка
2Al + 6HCl → 2AlCl3 + 3H2↑
алюми- соляная хлорид водород
ний кислота алюминия
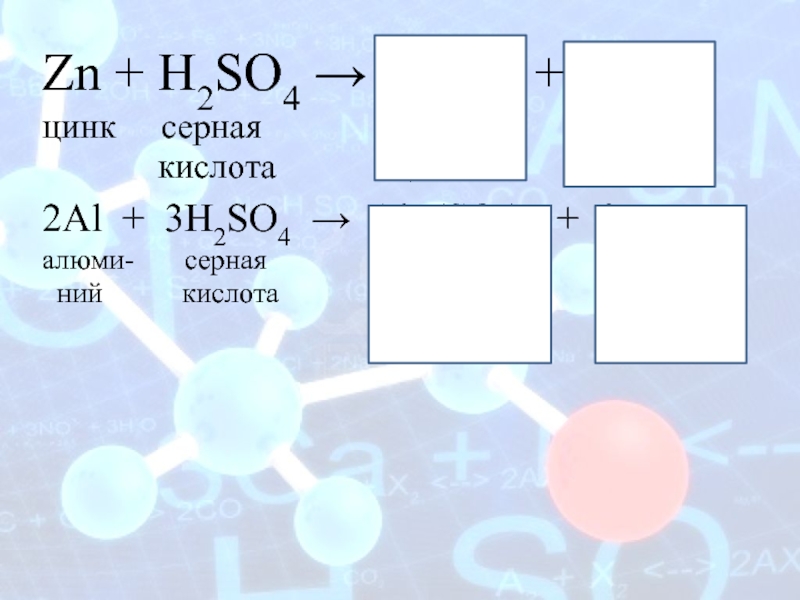
Слайд 6Zn + H2SO4 → ZnSO4 +H2 ↑
цинк
серная сульфат
водородкислота цинка
2Al + 3H2SO4 → Al2 (SO4)3 + 3H2↑
алюми- серная сульфат водород
ний кислота алюминия
Слайд 7Вытеснительный ряд активности металлов
Металлы, расположенные в ряду активности левее
водорода, способны вытеснять его из растворов кислот (за исключением азотной
кислоты). Металлы, расположенные в ряду активности правее водорода, не вытесняют его из растворов кислотСлайд 8Узнали, что такое реакции замещения и какие условия необходимы для
их осуществления.
Познакомились с рядом активности металлов Н.Н. Бекетова.
Пополнили
свои знания о влиянии природы веществ на интенсивность протекания реакции. Какая новые знания были получены вами сегодня?
Подведение итогов