Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Абсолютная температура как мера средней кинетической энергии частиц
Содержание
- 1. Абсолютная температура как мера средней кинетической энергии частиц
- 2. План занятияМикро- и макроскопические параметрыОсновное уравнение МКТ
- 3. Микроскопические параметры — характеристики состояния молекул, из
- 4. Идеальный газ – газ, состоящий из молекул,
- 5. Основное уравнение МКТЧисло ударов молекул ~ концентрации
- 6. Тепловое равновесие - состояние тел, при котором
- 7. Температура тела — мера средней кинетической энергии
- 8. Абсолютный нуль температуры – температура, при которой
- 9. Средняя кинетическая энергия хаотичного поступательного движения молекул
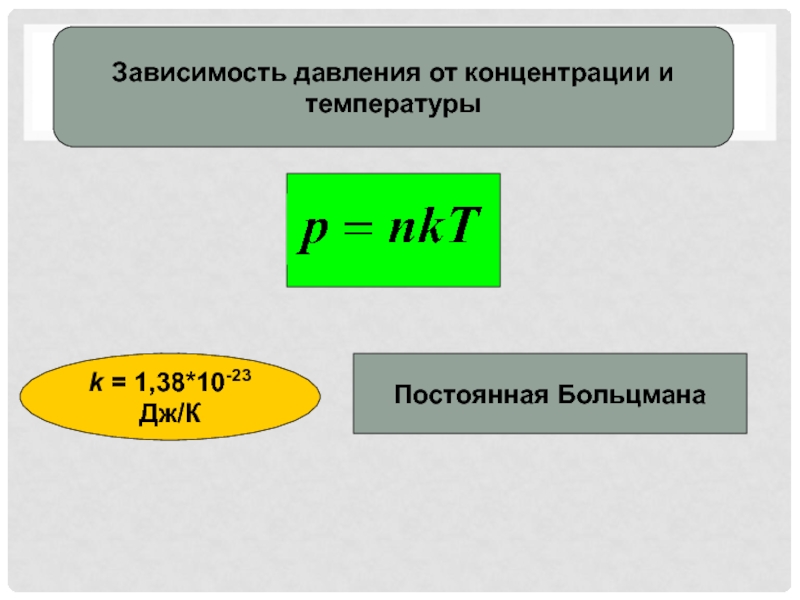
- 10. Зависимость давления от концентрации и температурыk = 1,38*10-23 Дж/КПостоянная Больцмана
- 11. Наиболее вероятнаяСредняя арифметическаяСредняя квадратичнаяРаспределение молекул газа по
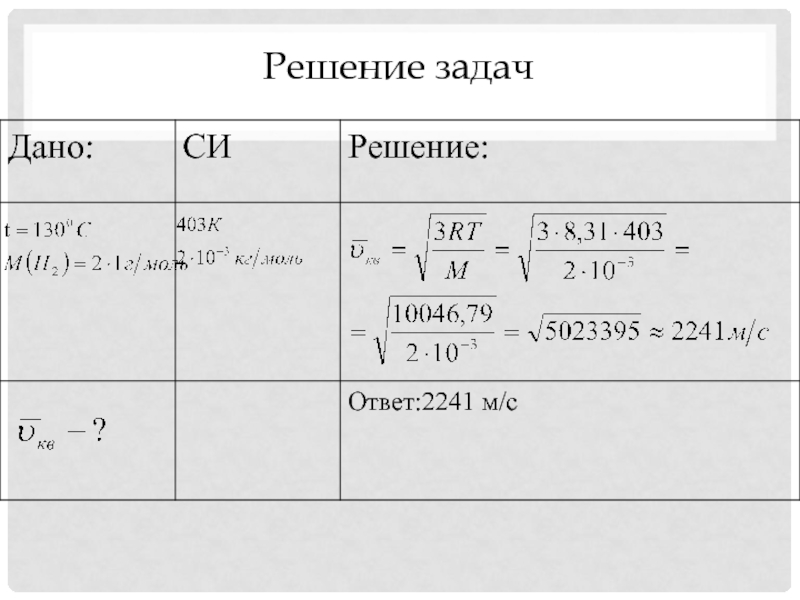
- 12. Решение задач
- 13. Вывод уравнения состояния идеального газаУниверсальная газовая постояннаяУравнение Менделеева-Клапейрона
- 14. если m=const и M=const, то …Уравнение КлапейронаГазовый
- 15. Соотношение было открыто в 1662 г. Робертом
- 16. Дыхание можно объяснить так: межреберные мышцы и
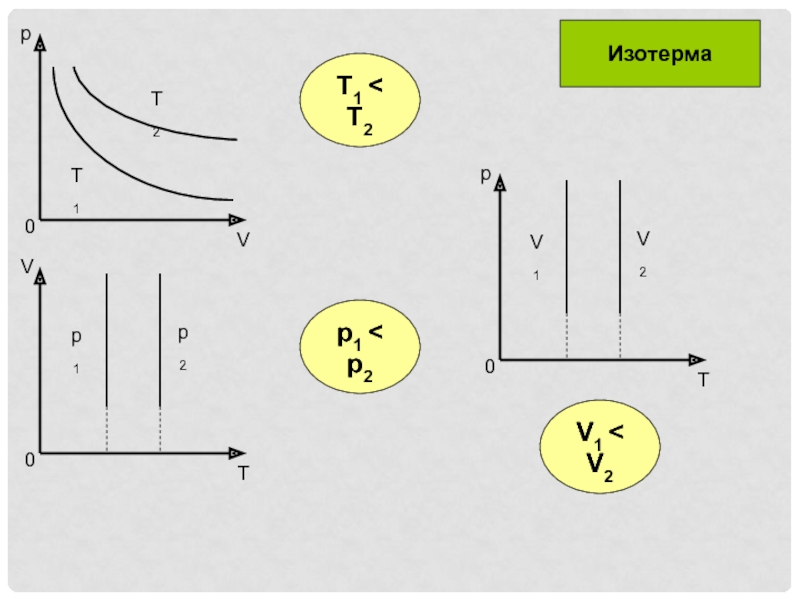
- 17. T1 < T2p1 < p2V1 < V2Изотерма
- 18. Равновесное состояние - состояние, при котором температура
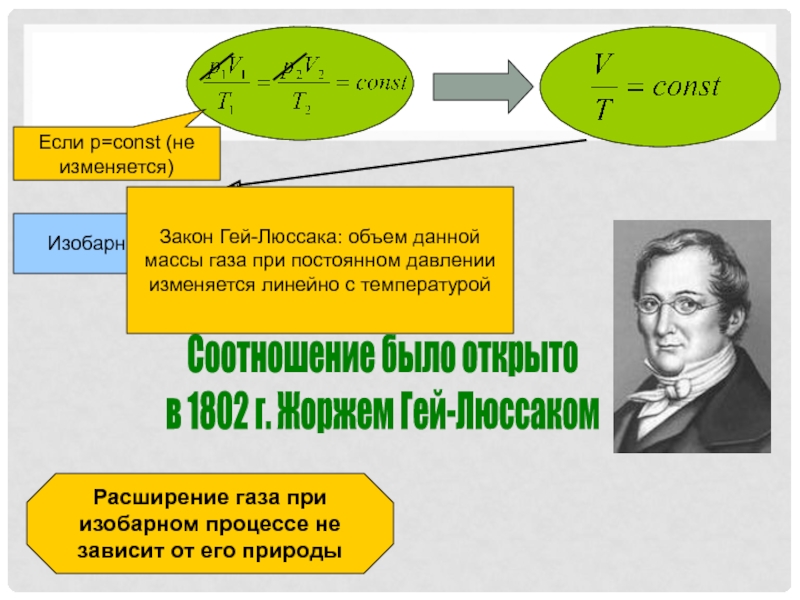
- 19. Соотношение было открыто в 1802 г. Жоржем
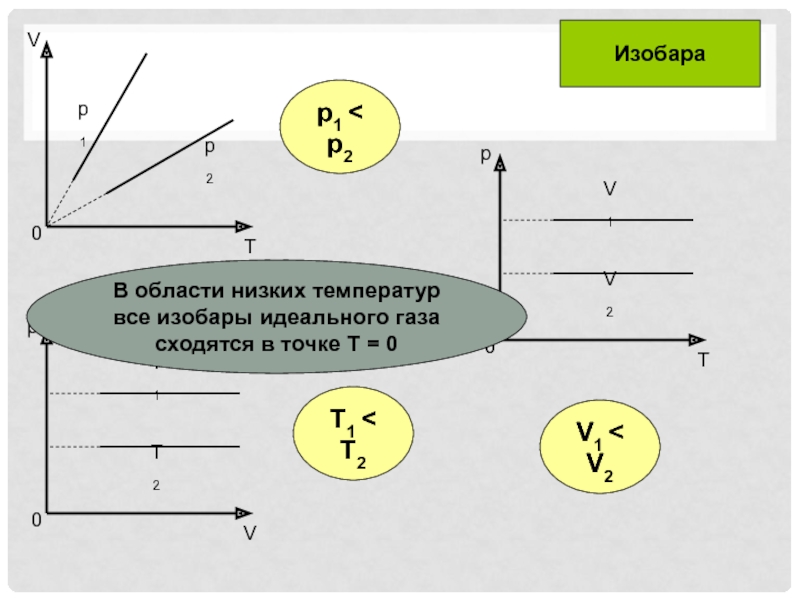
- 20. T1 < T2p1 < p2V1 < V2ИзобараВ
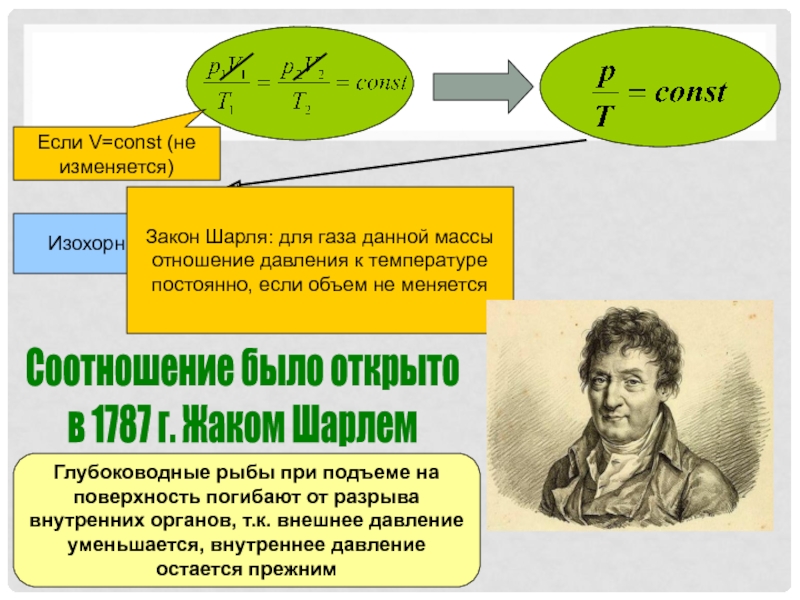
- 21. Соотношение было открыто в 1787 г. Жаком
- 22. T1 < T2p1 < p2V1 < V2ИзохораДавление идеального газа при абсолютном нуле равно 0
- 23. Слайд 23
- 24. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2План занятия
Микро- и макроскопические параметры
Основное уравнение МКТ идеального газа
Абсолютная температура
как мера средней кинетической энергии частиц
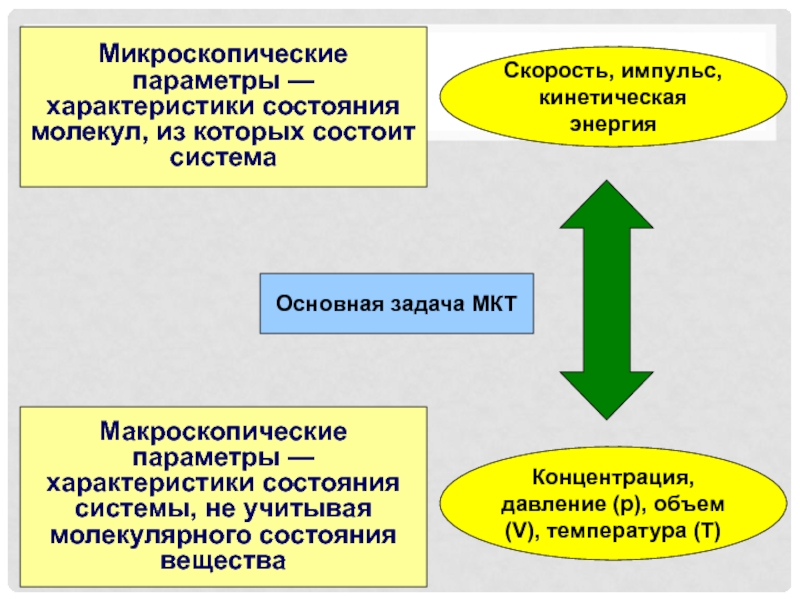
Слайд 3Микроскопические параметры — характеристики состояния молекул, из которых состоит система
Скорость,
импульс, кинетическая энергия
Макроскопические параметры — характеристики состояния системы, не учитывая
молекулярного состояния веществаКонцентрация, давление (p), объем (V), температура (T)
Основная задача МКТ
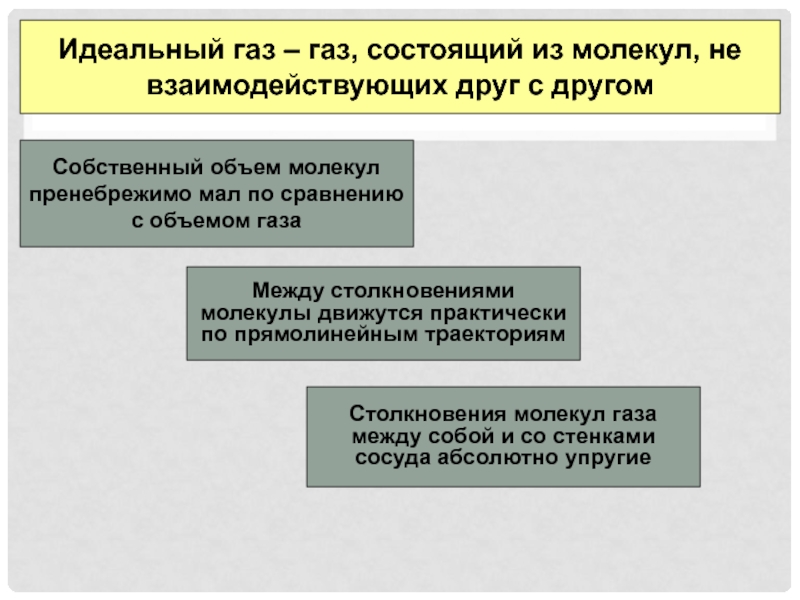
Слайд 4Идеальный газ – газ, состоящий из молекул, не взаимодействующих друг
с другом
Собственный объем молекул пренебрежимо мал по сравнению с объемом
газаМежду столкновениями молекулы движутся практически по прямолинейным траекториям
Столкновения молекул газа между собой и со стенками сосуда абсолютно упругие
Слайд 5Основное уравнение МКТ
Число ударов молекул ~ концентрации частиц
Интенсивность каждого удара
определяется средней Ek
Концентрация молекул – число молекул в 1 м3
Уравнение
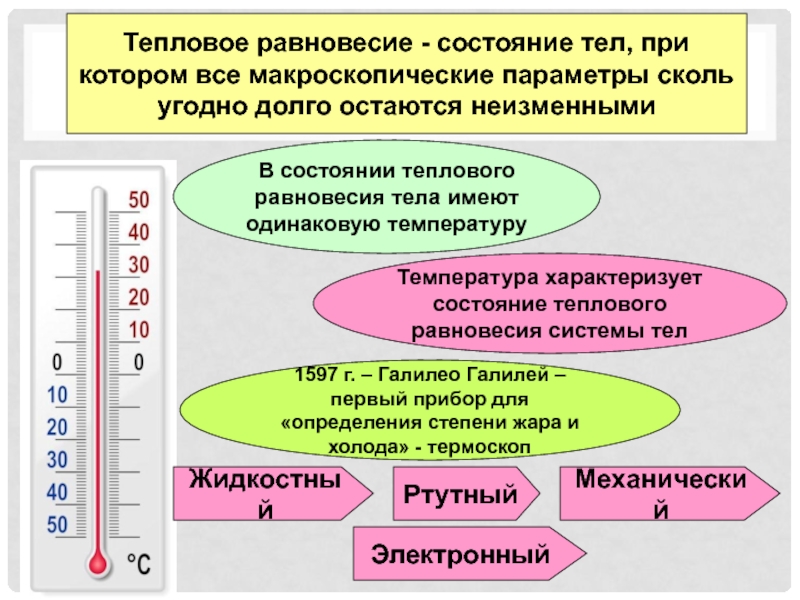
КлаузиусаСлайд 6Тепловое равновесие - состояние тел, при котором все макроскопические параметры
сколь угодно долго остаются неизменными
Температура характеризует состояние теплового равновесия системы
тел 1597 г. – Галилео Галилей – первый прибор для «определения степени жара и холода» - термоскоп
В состоянии теплового равновесия тела имеют одинаковую температуру
Жидкостный
Ртутный
Механический
Электронный
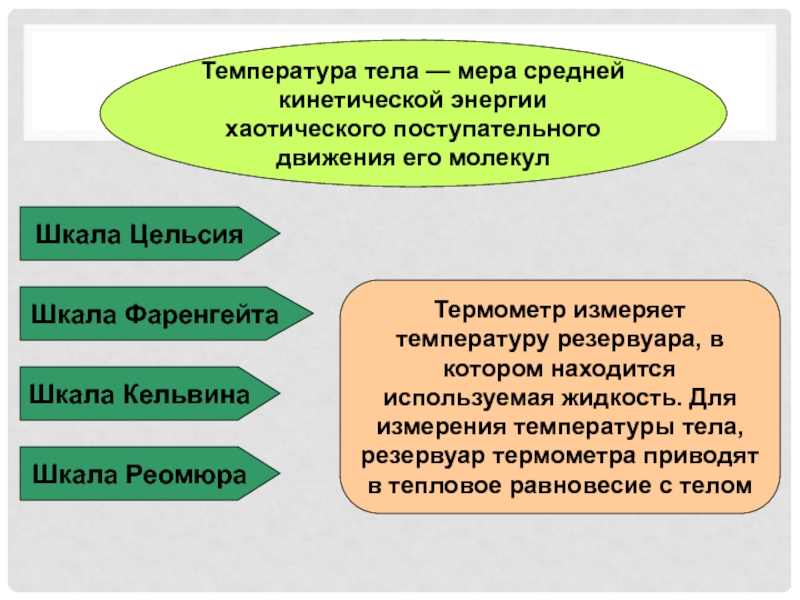
Слайд 7Температура тела — мера средней кинетической энергии хаотического поступательного движения
его молекул
Шкала Кельвина
Шкала Цельсия
Шкала Фаренгейта
Шкала Реомюра
Термометр измеряет температуру резервуара, в
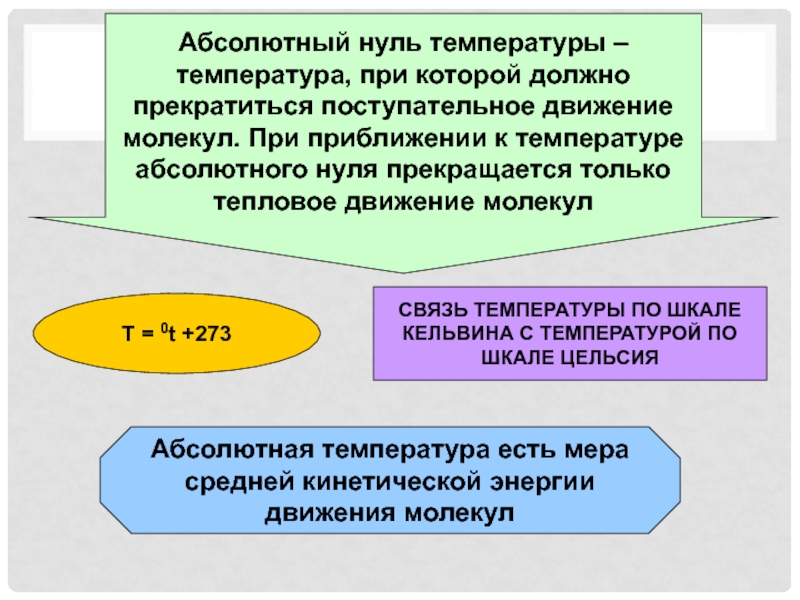
котором находится используемая жидкость. Для измерения температуры тела, резервуар термометра приводят в тепловое равновесие с теломСлайд 8Абсолютный нуль температуры – температура, при которой должно прекратиться поступательное
движение молекул. При приближении к температуре абсолютного нуля прекращается только
тепловое движение молекулT = 0t +273
СВЯЗЬ ТЕМПЕРАТУРЫ ПО ШКАЛЕ КЕЛЬВИНА С ТЕМПЕРАТУРОЙ ПО ШКАЛЕ ЦЕЛЬСИЯ
Абсолютная температура есть мера средней кинетической энергии движения молекул
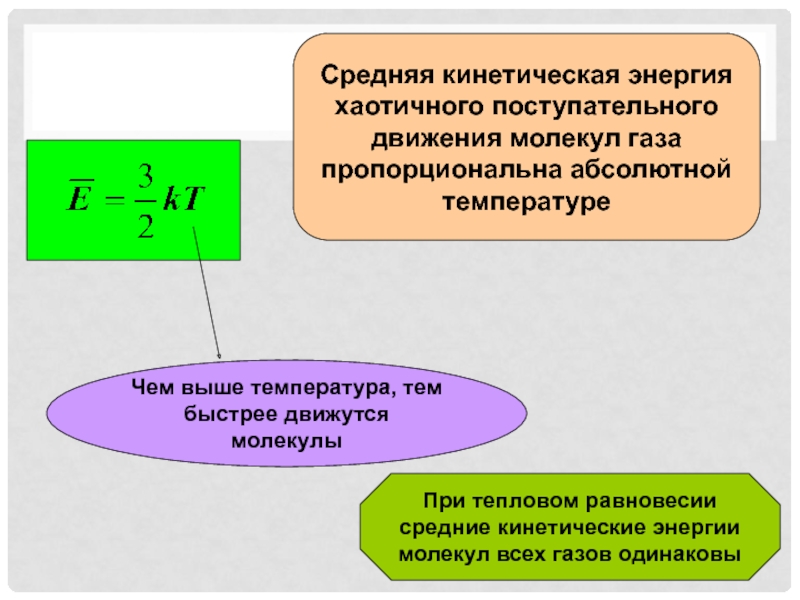
Слайд 9Средняя кинетическая энергия хаотичного поступательного движения молекул газа пропорциональна абсолютной
температуре
При тепловом равновесии средние кинетические энергии молекул всех газов одинаковы
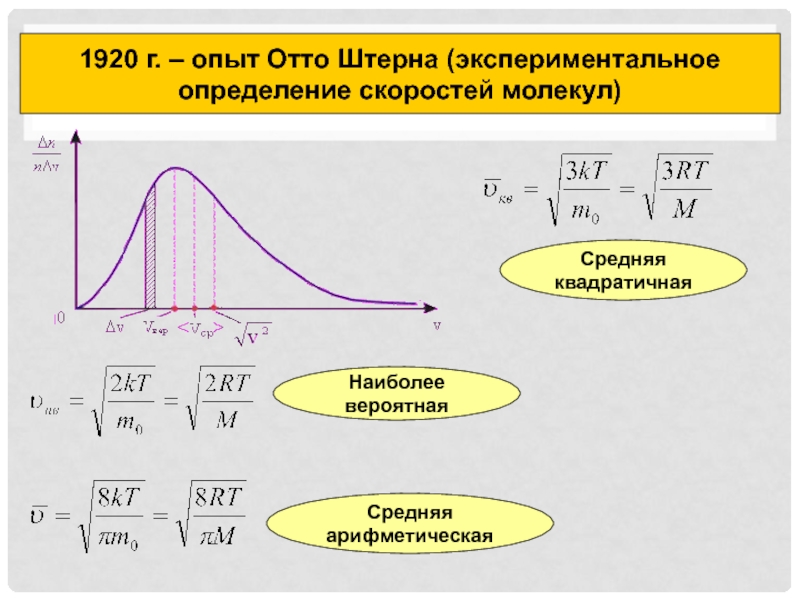
Слайд 11Наиболее вероятная
Средняя арифметическая
Средняя квадратичная
Распределение молекул газа по скоростям
1920 г. –
опыт Отто Штерна (экспериментальное определение скоростей молекул)
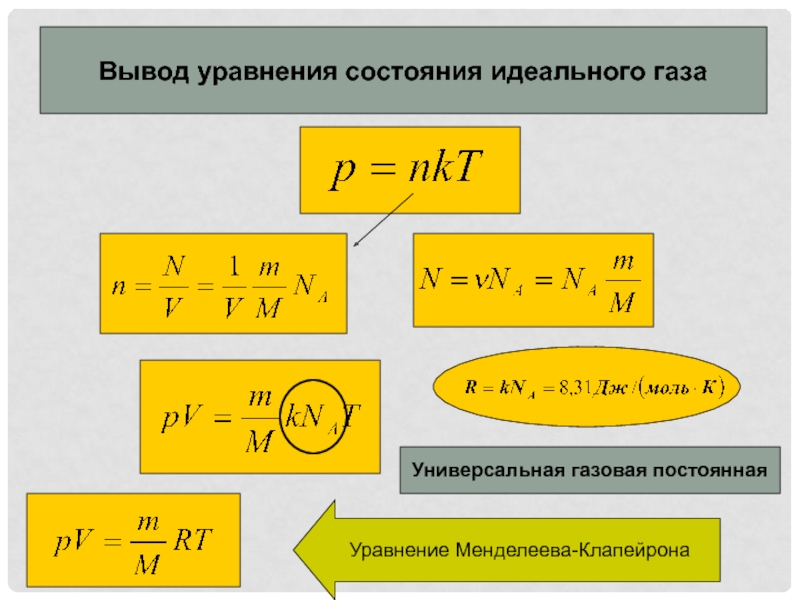
Слайд 13Вывод уравнения состояния идеального газа
Универсальная газовая постоянная
Уравнение Менделеева-Клапейрона
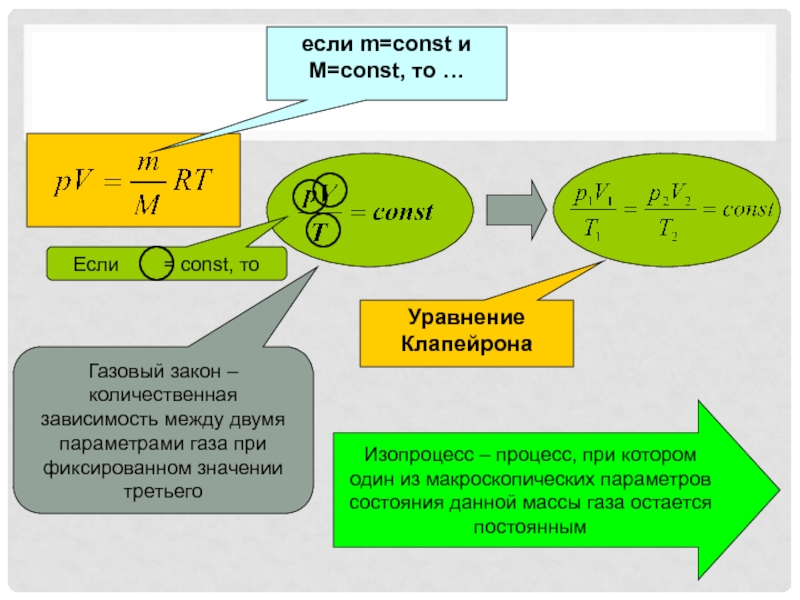
Слайд 14если m=const и M=const, то …
Уравнение Клапейрона
Газовый закон – количественная
зависимость между двумя параметрами газа при фиксированном значении третьего
Изопроцесс –
процесс, при котором один из макроскопических параметров состояния данной массы газа остается постояннымСлайд 15Соотношение было открыто
в 1662 г. Робертом Бойлем
Переоткрыто в 1676
г. Эдмоном Мариоттом
Если T=const (не изменяется)
Изотермический процесс
При изотермическом процессе плотность
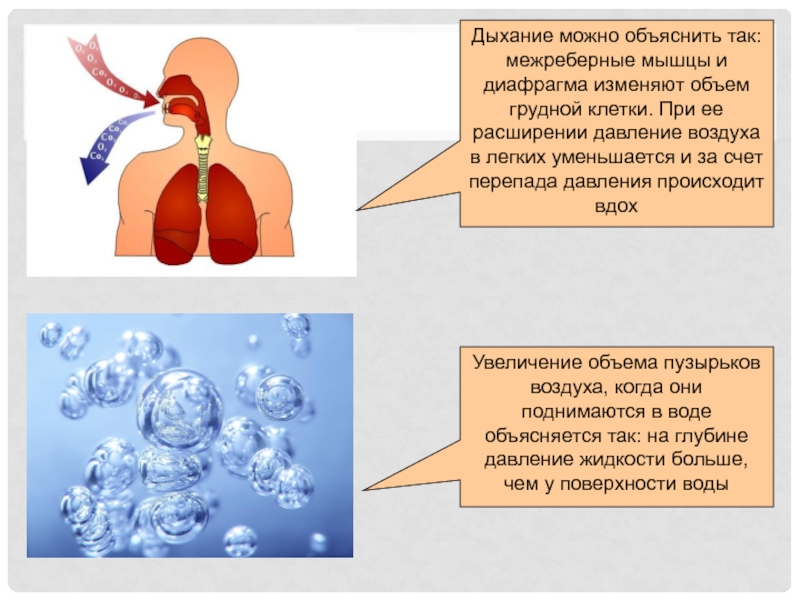
газа изменяется прямо пропорционально давлениюСлайд 16Дыхание можно объяснить так: межреберные мышцы и диафрагма изменяют объем
грудной клетки. При ее расширении давление воздуха в легких уменьшается
и за счет перепада давления происходит вдохУвеличение объема пузырьков воздуха, когда они поднимаются в воде объясняется так: на глубине давление жидкости больше, чем у поверхности воды