Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Алканы
Содержание
- 1. Алканы
- 2. Определение алкановЭто предельные углеводороды, в молекулах которых все атомы связаны одинарными связами
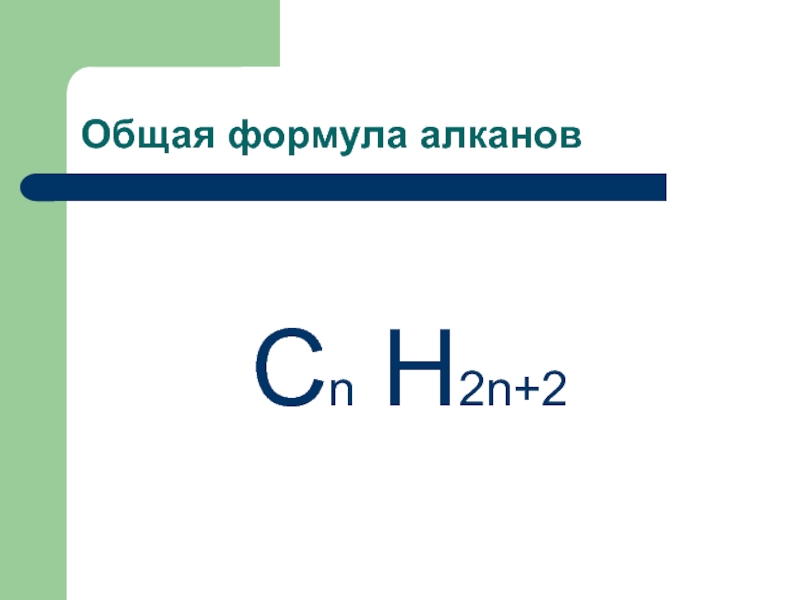
- 3. Общая формула алкановСn H2n+2
- 4. Гомологический рядСН4 метан
- 5. Название радикаловCH3 метилC2H5
- 6. Физические свойстваС1 – С4 – газы, С5
- 7. Строение алкановМолекула первого члена гомологического ряда алканов
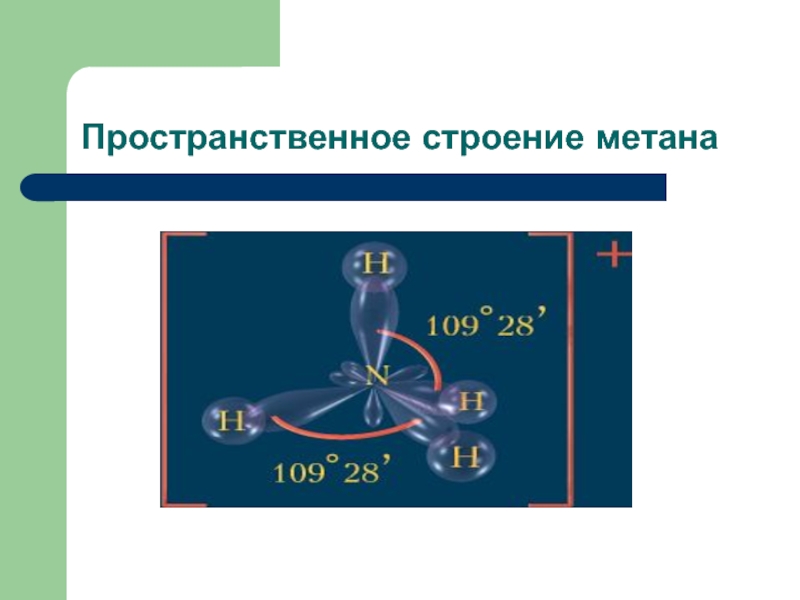
- 8. Пространственное строение метана
- 9. Виды изомерииСтруктурная
- 10. Алгоритм составления названия алканов 1.В структурной формуле
- 11. Дать название алканам
- 12. Дать название алканам 1
- 13. Составления названия алканов. 7
- 14. Получение алканов.Получение метана 1.В п р
- 15. Получение метана В л а б о
- 16. Получение гомологов метана.
- 17. Получение гомологов метана.В л а б о
- 18. ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ. НАХОЖДЕНИЕ В ПРИРОДЕ.МЕТАН –
- 19. ЭТАН, ПРОПАН И БУТАН входят в состав
- 20. Скачать презентанцию
Определение алкановЭто предельные углеводороды, в молекулах которых все атомы связаны одинарными связами
Слайды и текст этой презентации
Слайд 2Определение алканов
Это предельные углеводороды, в молекулах которых все атомы связаны
одинарными связами
Слайд 4Гомологический ряд
СН4 метан
С2Н6 этан
С3Н8 пропан С4Н10 бутан
С5Н12 пентан С6Н14 гексан
С7Н16 гептан С8Н18 октан
С9Н20 нонан С10Н22 декан
Слайд 6Физические свойства
С1 – С4 – газы,
С5 –С15 – жидкости,
С16
- ∞ -твердые вещества
Газы и твердые алканы запаха
не имеют, жидкие имеют бензиновый запах. Легче воды. Плохо растворимы в воде Слайд 7Строение алканов
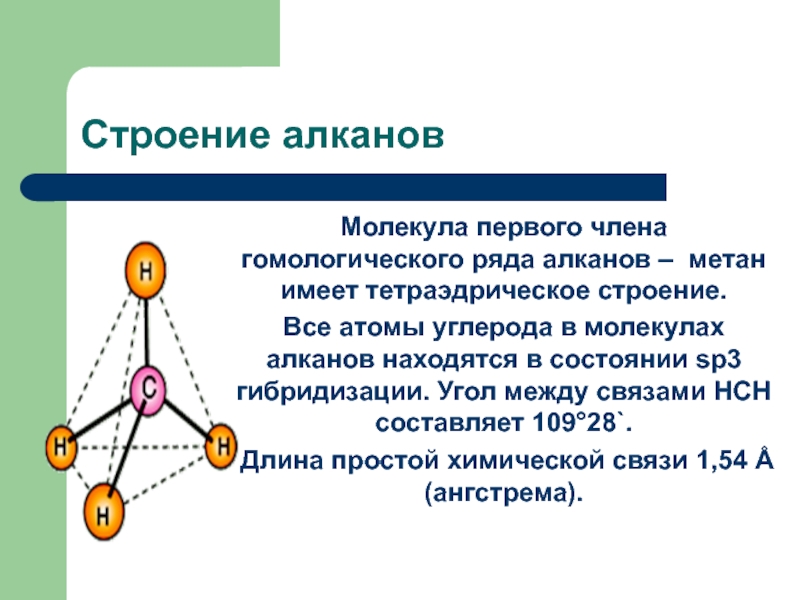
Молекула первого члена гомологического ряда алканов – метан имеет
тетраэдрическое строение.
Все атомы углерода в молекулах алканов находятся в состоянии
sp3 гибридизации. Угол между связами HCH составляет 109°28`.Длина простой химической связи 1,54 Å (ангстрема).
Слайд 9Виды изомерии
Структурная
Углеродного скелета
Положения кратной связи
Положения функциональной группыМежклассовая
Слайд 10Алгоритм составления названия алканов
1.В структурной формуле выбирают самую длинную
цепь атомов углерода (главную цепь)
2.Атомы углерода главной цепи нумеруют, начиная
с того конца, к которому ближе разветвление (радикал)3.В начале названия перечисляют радикалы и другие заместители с указанием номеров атомов углерода ,с которыми они связаны. Если в молекуле присутствует несколько одинаковых радикалов (два, три, четыре и т. д) то цифрой указывают место каждого из них в главной цепи и перед их названием ставят соответственно частицы ди-, три-, тетра- и т.д.
4.Основой названия служит наименование предельного углеводорода с тем же числом атомов углерода, что и в главной цепи.
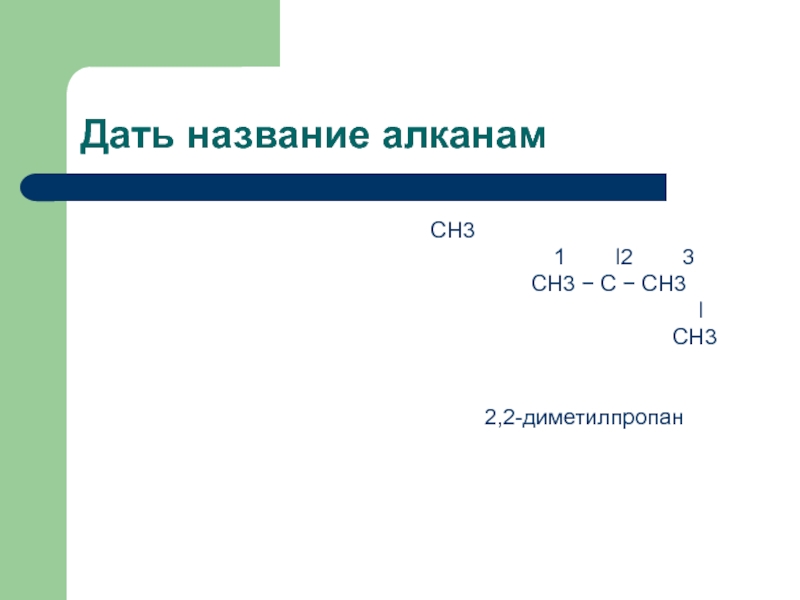
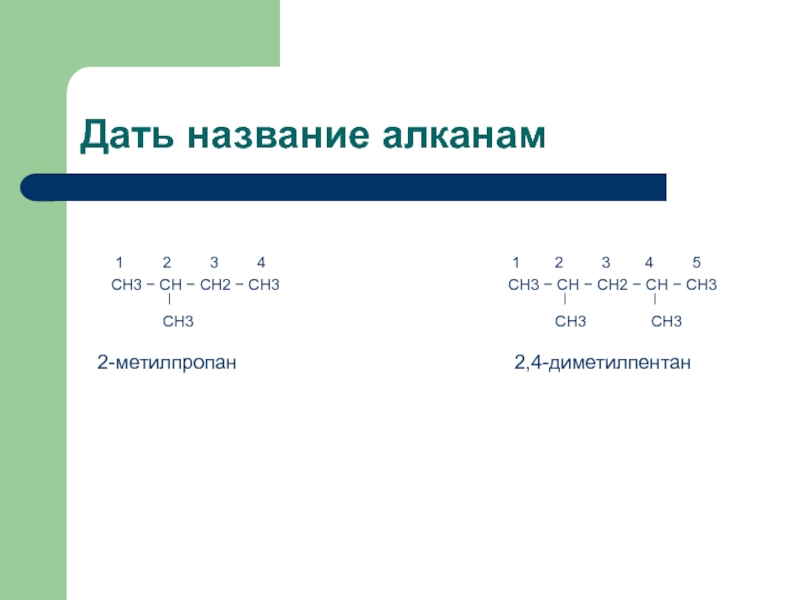
Слайд 12Дать название алканам
1
2 3
4 1 2 3 4 5CH3 − CH − CH2 − CH3 CH3 − CH − CH2 − CH − CH3
ǀ ǀ ǀ
CH3 CH3 CH3
2-метилпропан 2,4-диметилпентан
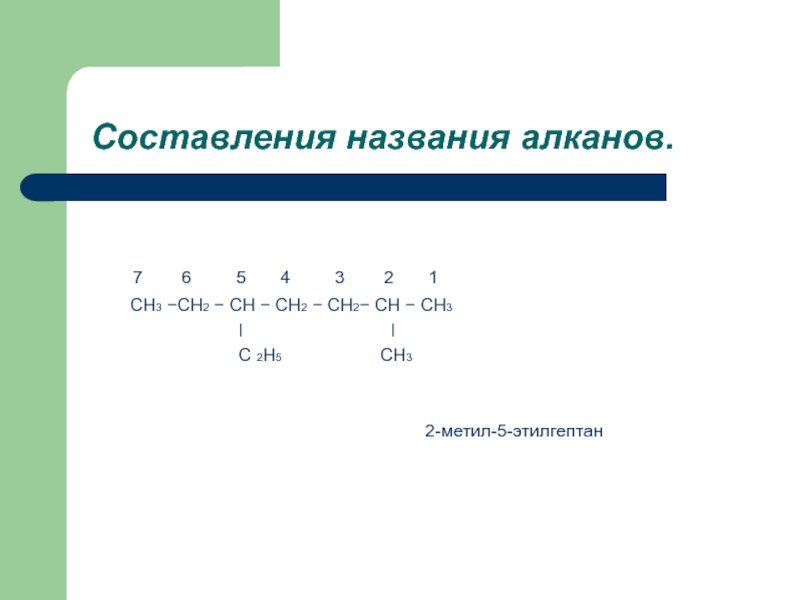
Слайд 13 Составления названия алканов.
7
6 5 4
3 2 1CH3 −CH2 − CH − CH2 − CH2− CH − CH3
ǀ ǀ
C 2H5 CH3
2-метил-5-этилгептан
Слайд 14Получение алканов.
Получение метана
1.В п р о м
ы ш л е н н о с т и:
а)из природного газаб)синтез из оксида углерода (II) и водорода
Ni,300˚C
CO + 3H2 → CH4 ↑ +H2O
Слайд 15Получение метана
В л а б о р а т
о р и и
а)гидролиз карбида алюминияAl4C3 +12H2O → 3CH4 ↑ +4Al(OH)3
б )сплавление солей уксусной кислоты со щелочами
CH3COONa +NaOH (т) → CH4 ↑ +Na2CO3
Слайд 16Получение гомологов метана.
В п
р о м ы ш л е н н о
с т иа) из природного сырья (нефть, газ, горный воск)
б) синтез из оксида углерода (II) и водорода
Слайд 17Получение гомологов метана.
В л а б о р а т
о р и и
а)каталитическое
гидрирование непредельных углеводородов (алкенов,алкинов)Pt
CnH2n + H2 → CnH2n+2
Ni,150˚C
CnH2n-2 + 2H2 → CnH2n+2
б) взаимодействие галогеноалканов с натрием (реакция Вюрца)
2R−Br +Na → R−R + 2NaBr
2CH3Br + Na → CH3 − CH3 +2NaBr