Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Атом - сложная частица
Содержание
- 1. Атом - сложная частица
- 2. Цели и задачиПознакомить учащихся с эволюцией научных
- 3. Представления о строении атомаАтом – «неделимая» частица
- 4. СЛОВО «АТОМ» ПРИДУМАЛ БОЛЕЕ 2500 ЛЕТ НАЗАД
- 5. Представления о строении атома Классическая теория строения
- 6. МОДЕЛЬ АТОМА ТОМСОНААтом, по мысли Дж. Томсона,
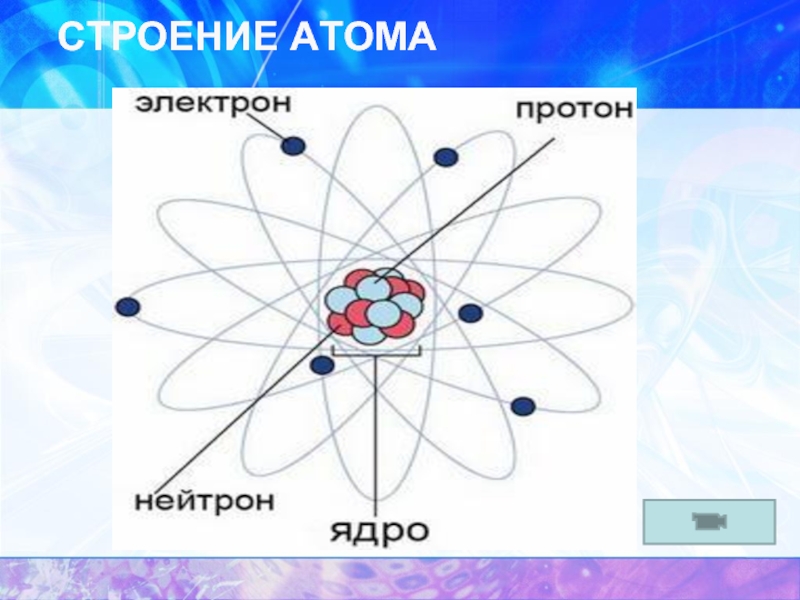
- 7. СТРОЕНИЕ АТОМА
- 8. Постулаты Н. Бораэлектроны в атоме вращаются по
- 9. Современная квантовая модель Н. Бор - создатель
- 10. Современная модель атома
- 11. СТРОЕНИЕ АТОМА
- 12. СТРОЕНИЕ АТОМАпротонынейтроныэлектроныатомядроэлектроннаяоболочка
- 13. Z – порядковый номер
- 14. Число p
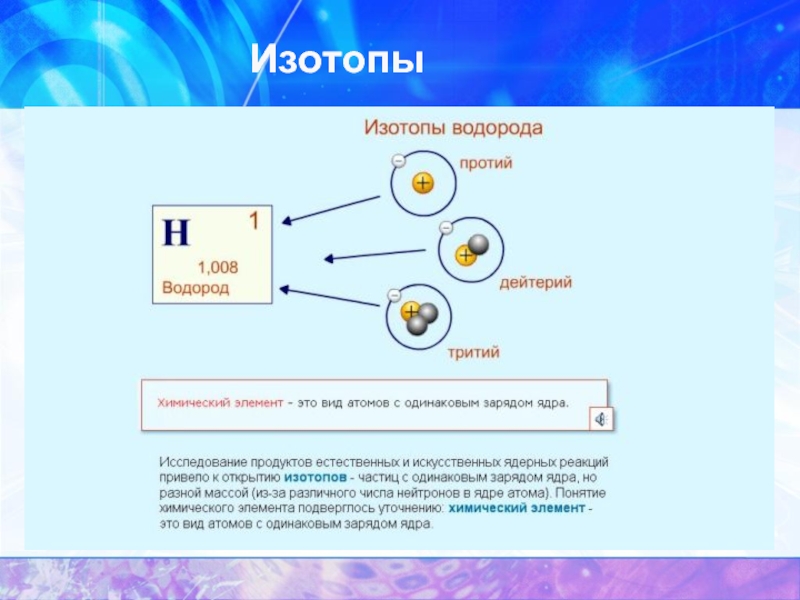
- 15. Изотопы
- 16. Нуклиды - различные виды атомов.Нуклиды характеризуются массовым
- 17. Задание 1. Запишите для 2-3элементов (по вашему
- 18. Задание 2. Выполните следующие упражнения Назовите элемент,
- 19. Задание 3. Определить состав изотопов 35Cl и 37Cl 28Si , 29Si, 30Si 39Ar, 40ArПроверяем знания
- 20. «Строение атома», презентация автор Беземская И.В. учитель химии МОУ «СОШ №2 п.Сенной Вольского района Саратовской области»http://ru.wikipedia.org/wiki/http://www.chem.msu.su/rus/teaching/
- 21. Скачать презентанцию
Цели и задачиПознакомить учащихся с эволюцией научных взглядов на строение атомаПоказать взаимодействие наук физики и химии
Слайды и текст этой презентации
Слайд 3Представления о строении атома
Атом – «неделимая» частица химического элемента
Доказательства сложности
строения атома
Открытие катодных лучей (1897г., Дж. Томсон)
Открытие рентгеновских лучей (1895г.,
К. Рентген),явления фотоэффекта 1889 г., А.Г. Столетов)
3.Открытие радиактивности (1896 г.,А. Беккерель) и её изучение
(1897-1903 гг., супруги М. Склодовская- Кюри и П. Кюри)
Слайд 4СЛОВО «АТОМ» ПРИДУМАЛ БОЛЕЕ 2500 ЛЕТ НАЗАД ДРЕВНЕГРЕЧЕСКИЙ ФИЛОСОФ ДЕМОКРИТ
АТОМ
– ЭТО МЕЛЬЧАЙШАЯ ХИМИЧЕСКИ НЕДЕЛИМАЯ ЧАСТИЦА ВЕЩЕСТВА
Слайд 5Представления о строении атома
Классическая теория строения атома
Модели строения атома:
1.
«Пудинг с изюмом» (1902-1904 гг.,Дж. Томсон и В. Кельвин
2. Планетарная
модель (1907г., Э. Резерфорд)3. Модель Бора (1913)
Современные представления
о строении атома
на основе квантовой механики
Слайд 6МОДЕЛЬ АТОМА ТОМСОНА
Атом, по мысли Дж. Томсона, очень похож на
пудинг с изюмом: электроны, как "изюминки", а "каша" - положительно
заряженное вещество атома .Джозеф Джон ТОМСОН
Слайд 8Постулаты Н. Бора
электроны в атоме вращаются по строго определённым замкнутым
орбитам, не испуская и не поглощая энергии;
при переходе электронов
содной орбиты на другую
происходит поглощение
или выделение энергии.
Слайд 9Современная квантовая модель
Н. Бор - создатель первой квантовой теории
атомаН. Бор - создатель первой квантовой теории атома и активный
участник разработки основ квантовой механикиН. Бор - создатель первой квантовой теории атома и активный участник разработки основ квантовой механики. Также он внёс значительный вклад в развитие теории атомного ядраН. Бор - создатель первой квантовой теории атома и активный участник разработки основ квантовой механики. Также он внёс значительный вклад в развитие теории атомного ядра и ядерных реакций, процессов взаимодействия элементарных частиц со средой.Электрон имеет двойственную (корпускулярно-волновую природу) -28 -19
Масса = 9,1*10 г ; заряд =1,6*10 Кл
Движущийся электрон обладает свойствами волны (способность к дифракции интерференции)
Слайд 14
Число p Z p =
Z (порядковому номеру химического элемента)
Число ē
Z ē = Z (порядковому номеру химического элемента)Число n N = A – Z (массовое число минус порядковый номер химического элемента)
+
+
о
Слайд 16Нуклиды -
различные виды атомов.
Нуклиды характеризуются массовым числом А и
зарядом ядра Z.
Изотопы - нуклиды с одинаковыми Z, но разными
АИзобары – нуклиды с разными Z, но одинаковыми А
Слайд 17Задание 1. Запишите для 2-3
элементов (по вашему выбору).
Элемент
Порядковый номер
Относительная
атомная масса
Заряд ядра атома
Число протонов
Число нейтронов
Число электронов
Проверяем знания
Слайд 18Задание 2. Выполните следующие упражнения
Назовите элемент, содержащий 23 протона.
Назовите
элементы II периода, содержащие 8 нейтронов и запишите их.
Назовите
и запишите символы элементов, в которых сумма протонов и нейтронов равна 40.В ядре атома химического элемента А содержится 11 протонов и 12 нейтронов, а в ядре атома химического элемента В – 12 протонов и 12 нейтронов.
Определите, являются ли они:
а) изотопами одного элемента;
б) атомами двух химических элементов, у которых одинаковое массовое число;
в) атомами двух разных элементов, находящихся в периодической системе рядом.
Проверяем знания
Слайд 19Задание 3. Определить состав изотопов
35Cl и 37Cl
28Si , 29Si,
30Si
39Ar, 40Ar
Проверяем знания
Слайд 20
«Строение атома», презентация автор Беземская И.В. учитель химии МОУ «СОШ
№2 п.Сенной Вольского района Саратовской области»
http://ru.wikipedia.org/wiki/
http://www.chem.msu.su/rus/teaching/
Теги