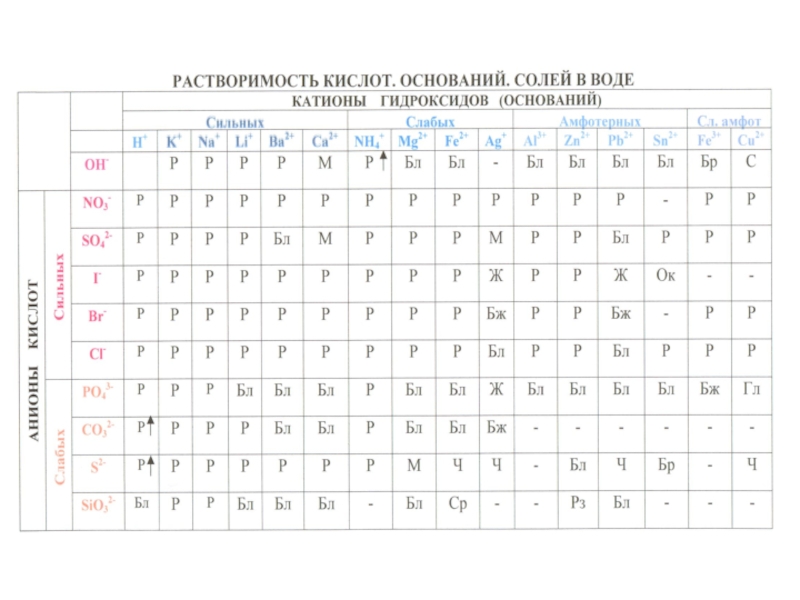
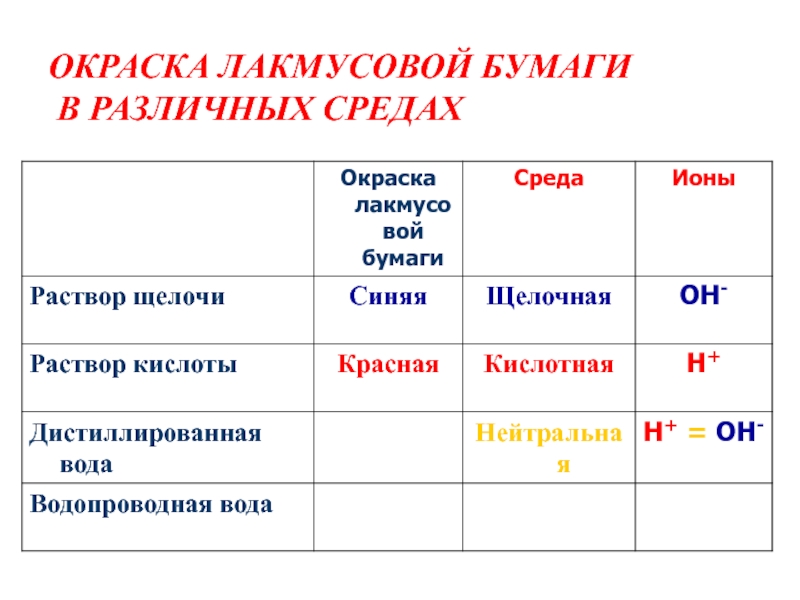
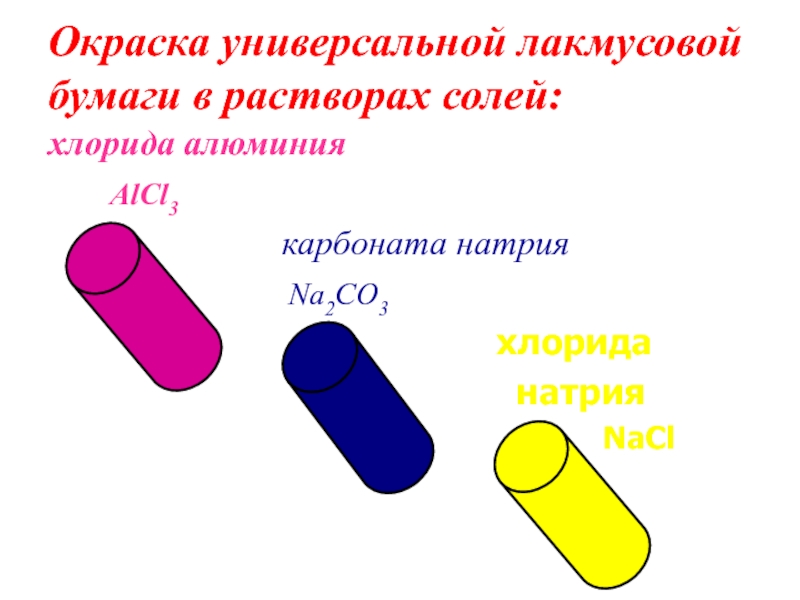
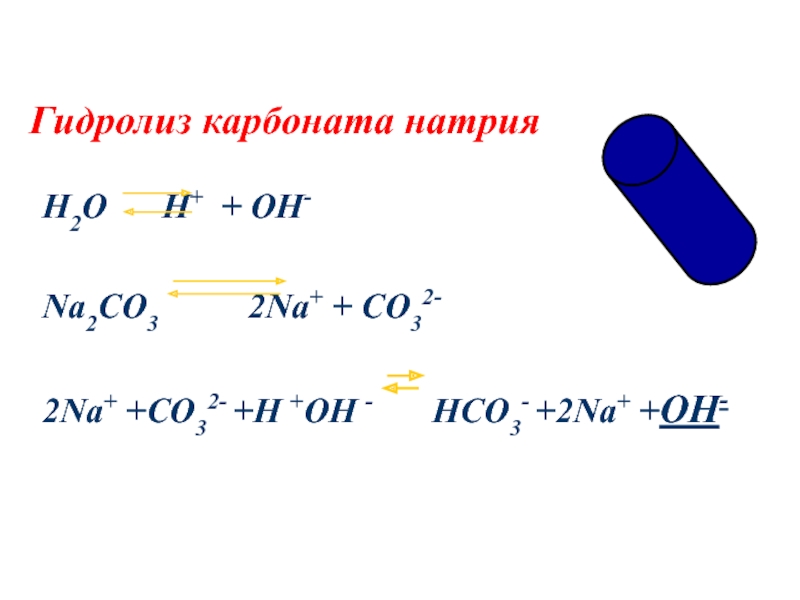
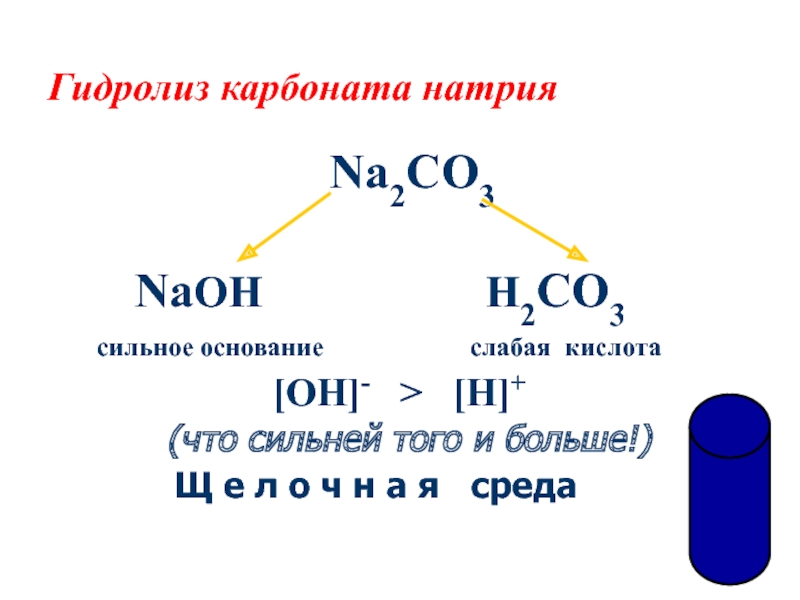
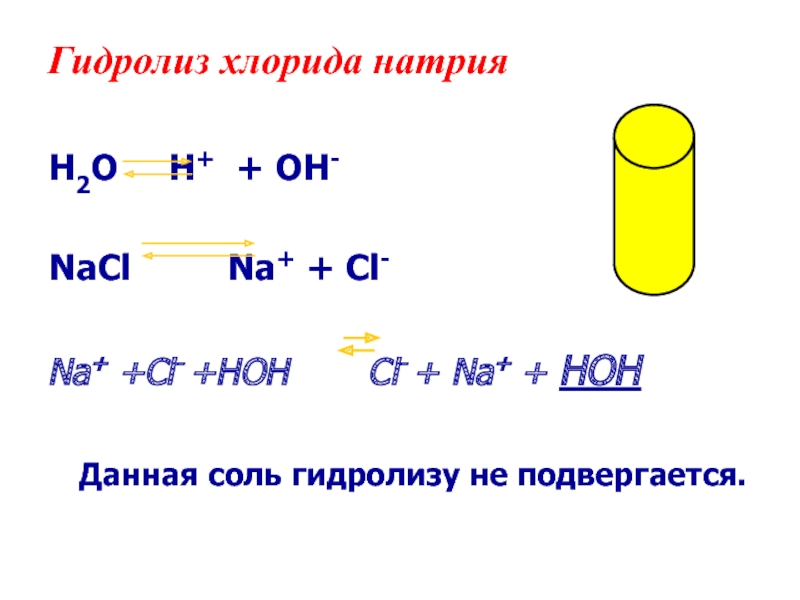
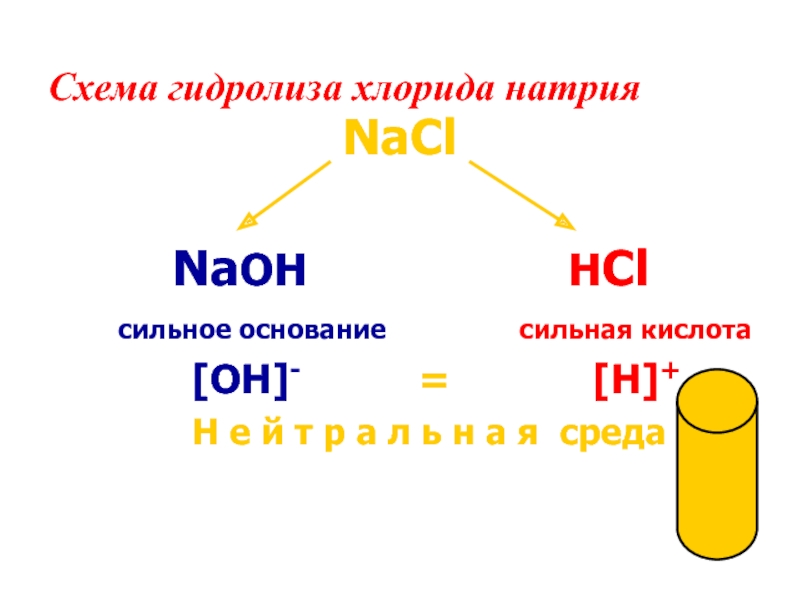
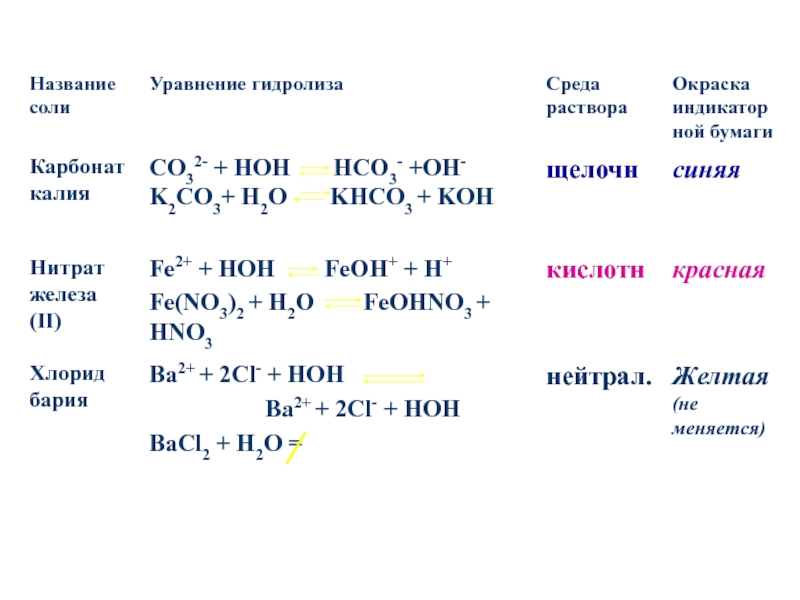
в водных растворах солей
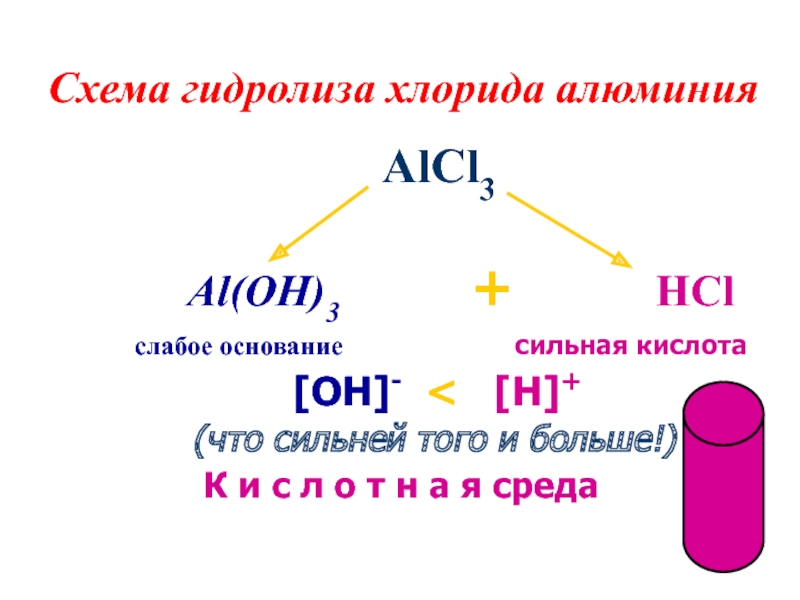
записывать уравнения реакций гидролиза
предсказывать
и объяснять изменение кислотности среды и образование кислых и основных солей в этом процессепознакомиться с ролью гидролиза солей в природе, хозяйственной деятельности и повседневной жизни человека.