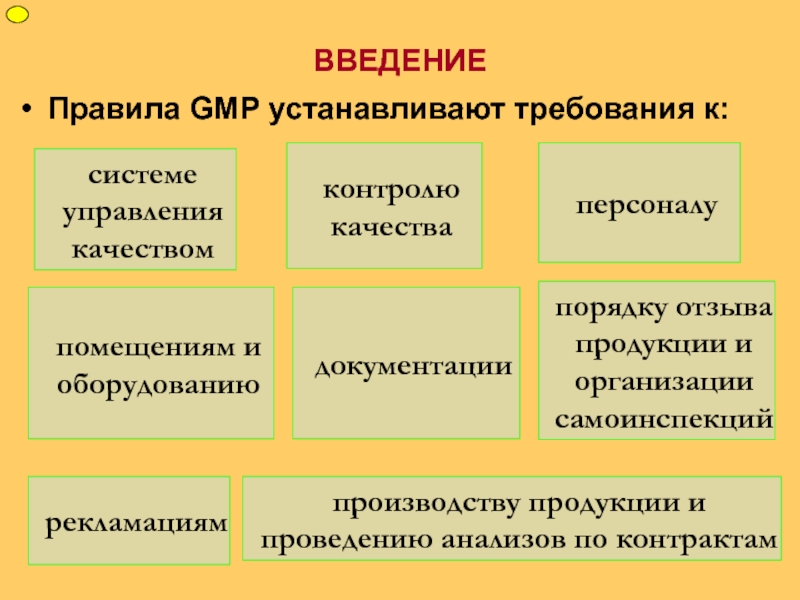
персонала с учетом особенностей конкретного производства. Правила должны содержать инструкции,
регламентирующие требования к состоянию здоровья, соблюдению гигиены и порядку ношения одежды. Инструкции должны соблюдать все сотрудники, которые связаны с нахождением в производственных помещениях и помещениях контроля качества. Руководство предприятия несет ответственность за выполнение персоналом правил гигиены и организацию необходимого обучения.
2.14. Все лица, принимаемые на работу, должны проходить медицинский осмотр. На предприятии должны быть инструкции с перечнем показателей состояния здоровья, которые могут оказать влияние на качество продукции. В случаях, связанных с производственной необходимостью или состоянием здоровья, сотрудники должны проходить повторный медицинский осмотр.
2.15. Лица с инфекционными заболеваниями и повреждениями на открытых участках тела не допускаются к производству лекарственных средств.
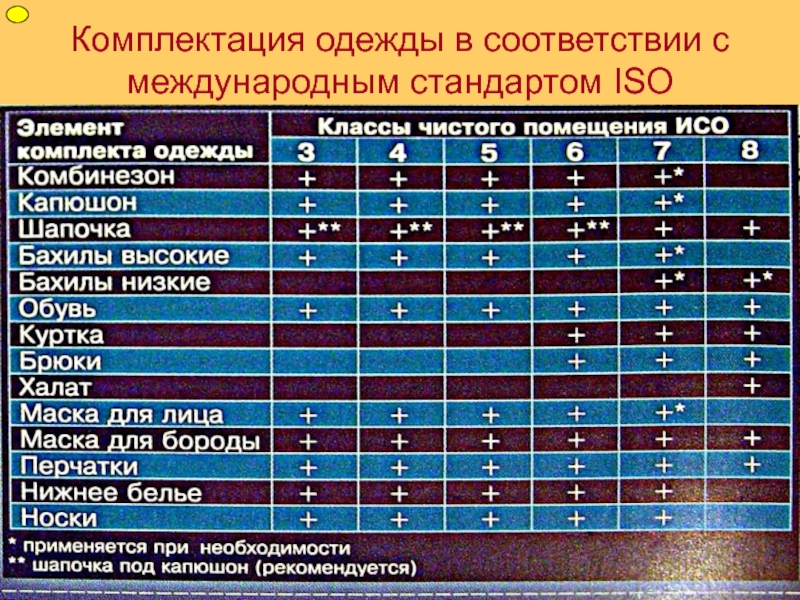
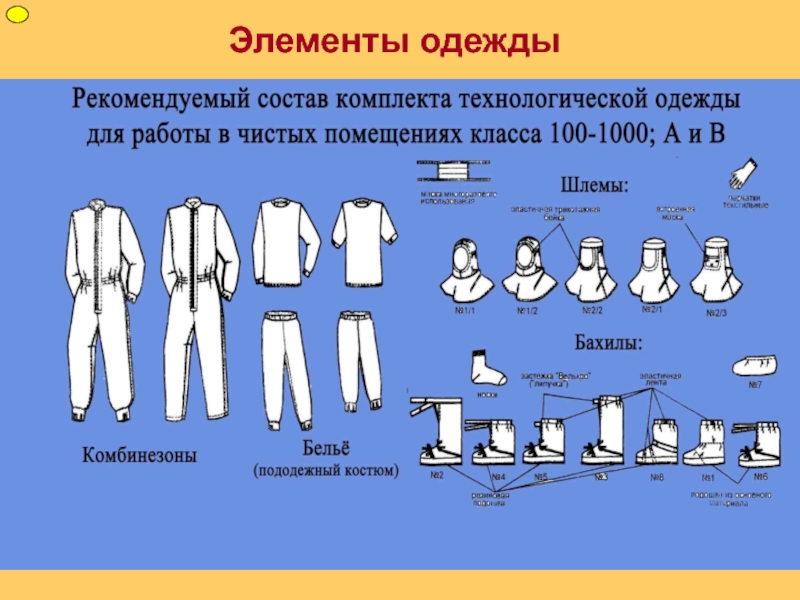
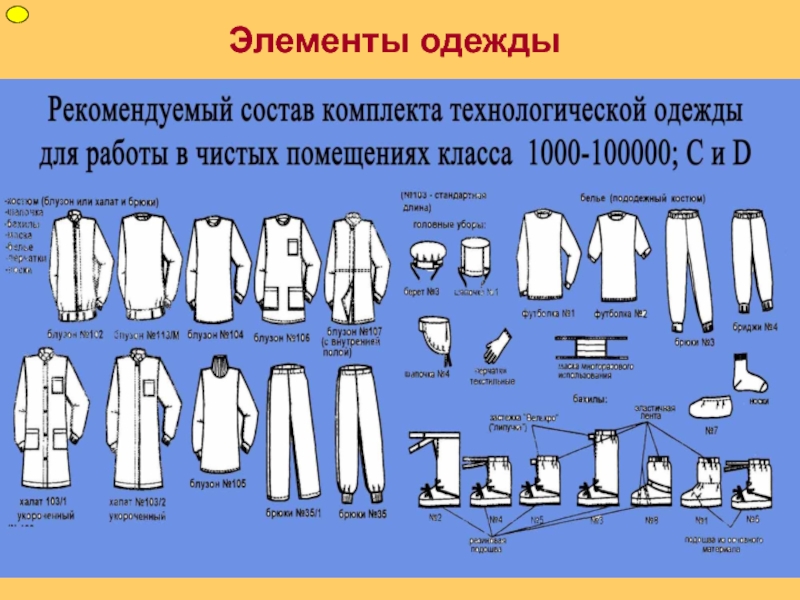
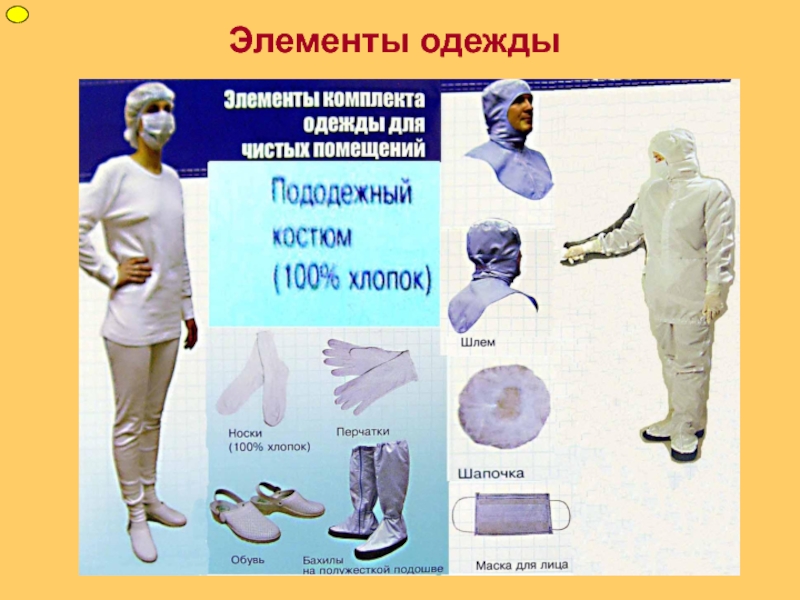
2.16. Одежда входящего в производственные помещения должна соответствовать назначению этого помещения.
2.17. В производственных и складских зонах запрещаются курение, прием пищи или питье, жевание резинки, а также хранение пищевых продуктов, напитков, табачных изделий и личных лекарственных средств. Не допускается любая деятельность, нарушающая правила гигиены в производственных помещениях или других местах, которая может оказать отрицательное влияние на качество продукции.
2.18. Непосредственный контакт операторов с открытой продукцией или любыми деталями оборудования, контактирующими с продукцией, не допускается.
2.19. Персонал должен пройти инструктаж по правилам мытья рук.
2.20. Специальные требования, относящиеся к производству отдельных видов продукции, например стерильных препаратов, даны в Приложениях к настоящему стандарту.
ФУП