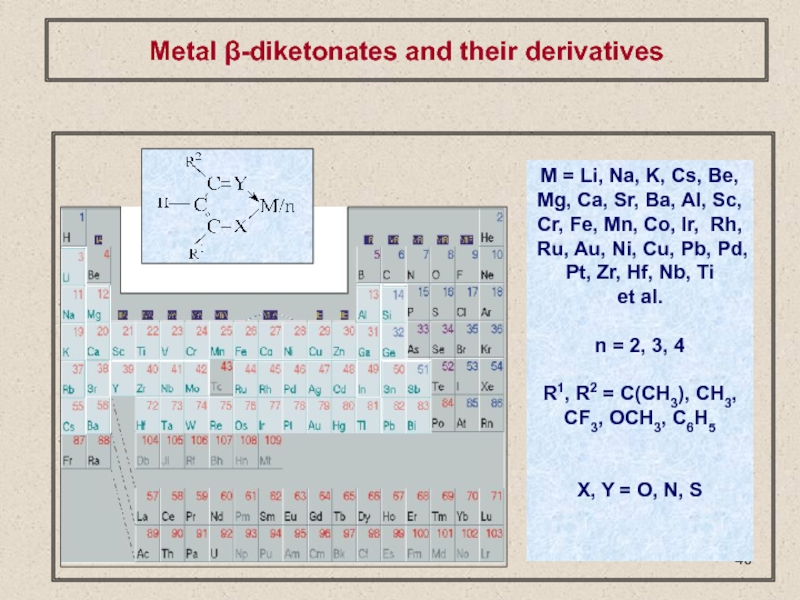
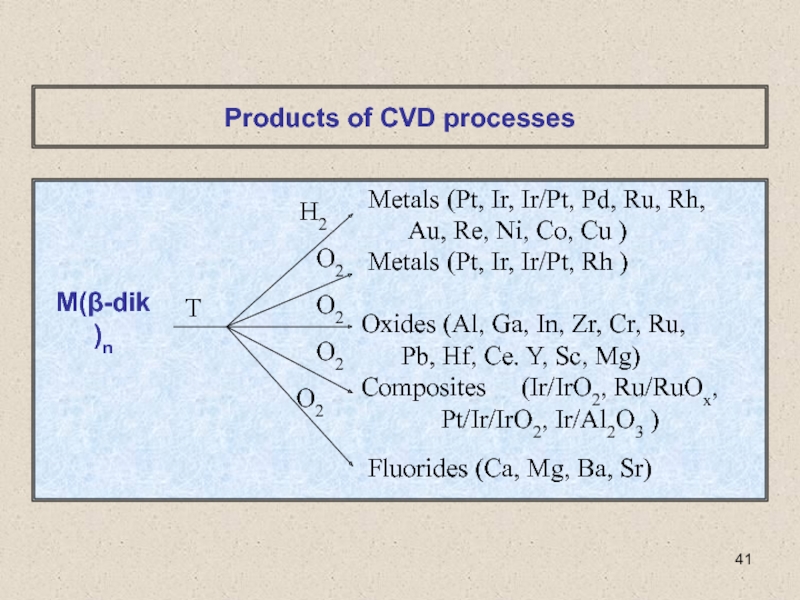
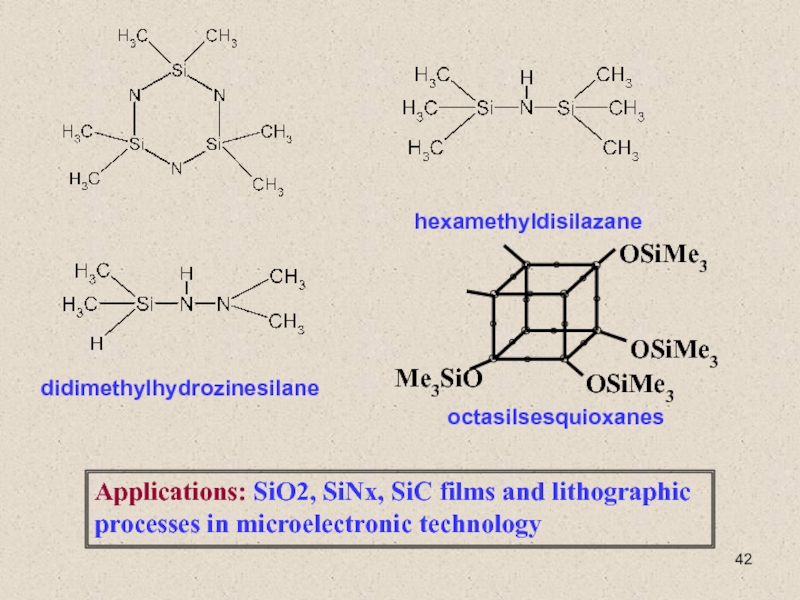
Слайд 1Химическое осаждение из газовой фазы
CVD – Chemical Vapour Deposition
Слайд 2Применение процессов CVD
покрытия: износостойкие, коррозионно-стойкие, высокотемпературные, защитные
в микроэлектронике (твердотельные интегральные
схемы - полупроводники, диэлектрики, металлы)
оптические покрытия
композиты (керамические матричные композиты углерод-углерод,
углерод-карбид кремния)
производство порошков
катализ
реставрация, декоративные покрытия
Слайд 3
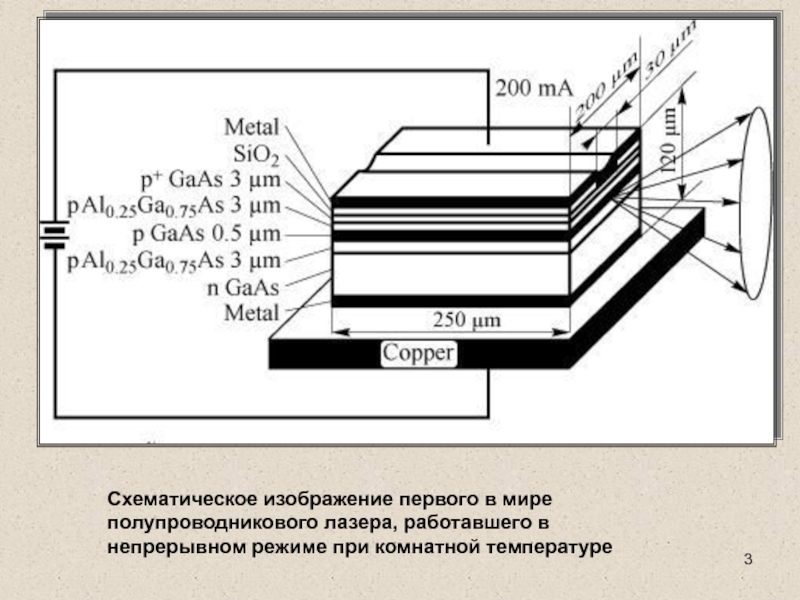
Схематическое изображение первого в мире полупроводникового лазера, работавшего в непрерывном
режиме при комнатной температуре
Слайд 4Преимущества CVD метода
универсальность (почти любой состав пленок),
огромный выбор исходных
веществ, можно получить пленки многих элементов и соединений,
получение тугоплавких покрытий
(процесс идет при Т < Тпл),
подложка может быть сложной формы: возможность нанесения однородных по составу и толщине одно- и двухсторонних пленок на детали сложной, непланарной конфигурации и большой площади, включая непрерывное напыление пленки на длинномерный металлический носитель-ленту,
возможность достижения высоких скоростей осаждения при сохранении высокого качества пленки,
отсутствие растворителя (примеси в пленке),
высокая чистота синтезированных материалов (99.99-99.999%)
Слайд 5Преимущества CVD метода
переход от высоковакуумной аппаратуры к проточным установкам, функционирующим
при давлениях 10-3-1 атм., простота и дешевизна оборудования в сравнении
с физическими методами,
гибкость процесса на этапе отладки технологического режима, в первую очередь за счет плавного изменения состава паровой фазы.
Слайд 6
проблема выбора подложек
управление стехиометрией пленки (температура подложки, парциальное
давление исходных веществ, несколько источников)
целенаправленный поиск веществ с высокой
и воспроизводимой летучестью
создание оптимальной морфологии пленки
Недостатки метода CVD
Слайд 7Химическое осаждение из газовой фазы (процессы CVD)
Сущность процессов химического
осаждения из газовой фазы состоит в получении веществ в твердом
состоянии за счет химических превращений реагентов, одновременно подаваемых в реакционный объем и находящихся в газообразном состоянии.
В результате протекания процессов CVD твердое вещество может получаться однофазным (чистые элементы, химические соединения стехиометрического состава, растворы) или многофазным (композиционные материалы, состоящие из смеси кристаллических и/или аморфных фаз).
Наиболее часто получаемое твердое вещество осаждается в виде покрытий или тонких пленок на помещенных в реакционную зону (зона осаждения) объектах, также получают объемные моно- или поликристаллические образования, продукты в порошкообразном или нитевидном состояниях.
Слайд 8Химическое осаждение из газовой фазы (процессы CVD)
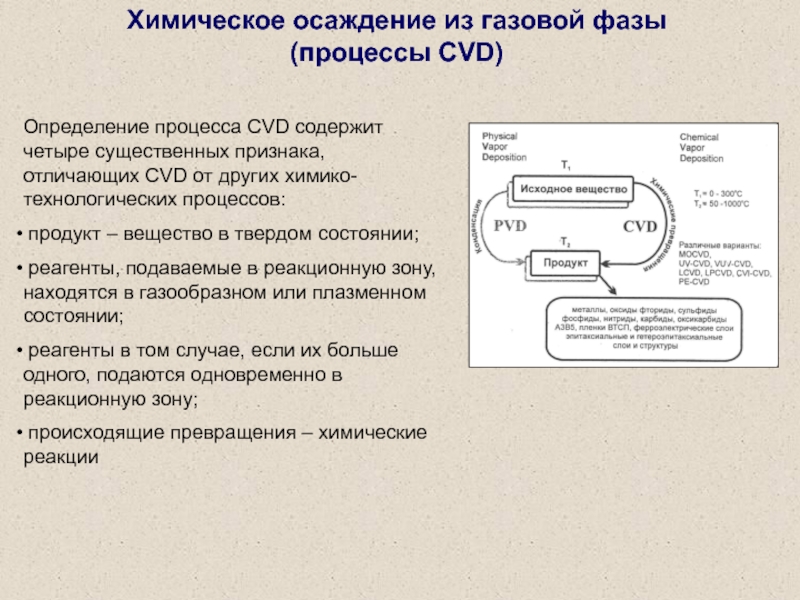
Определение процесса CVD
содержит четыре существенных признака, отличающих CVD от других химико-технологических процессов:
продукт – вещество в твердом состоянии;
реагенты, подаваемые в реакционную зону, находятся в газообразном или плазменном состоянии;
реагенты в том случае, если их больше одного, подаются одновременно в реакционную зону;
происходящие превращения – химические реакции
Слайд 9Химическое осаждение из газовой фазы (процессы CVD)
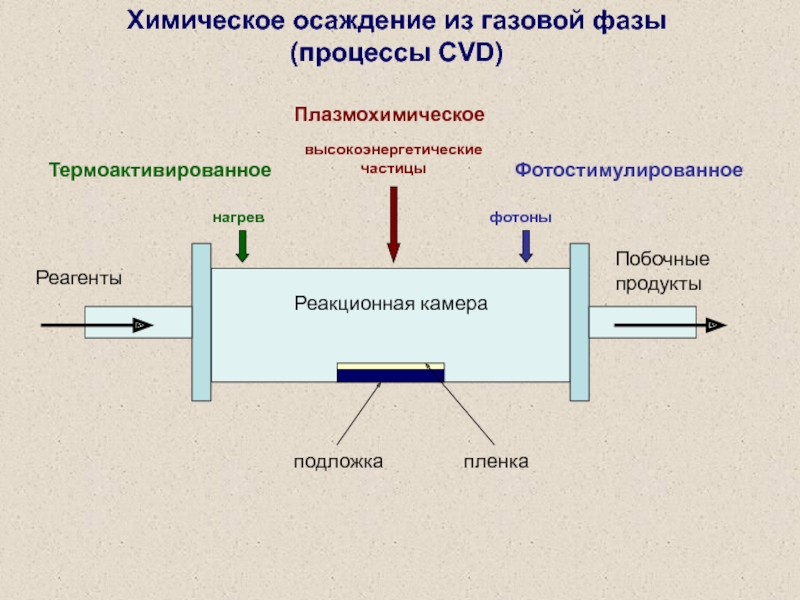
Термоактивированное
нагрев
Плазмохимическое
высокоэнергетические частицы
Фотостимулированное
фотоны
подложка
пленка
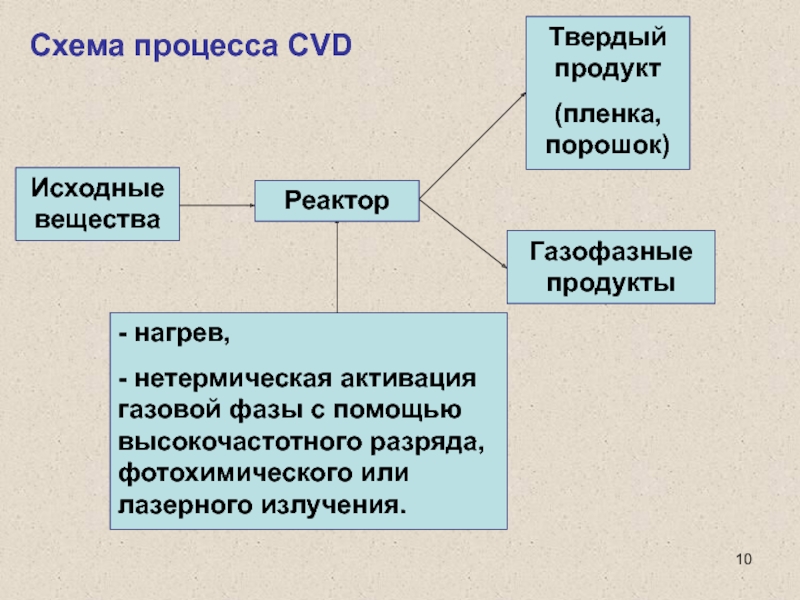
Слайд 10Схема процесса CVD
- нагрев,
- нетермическая активация газовой фазы с
помощью высокочастотного разряда, фотохимического или лазерного излучения.
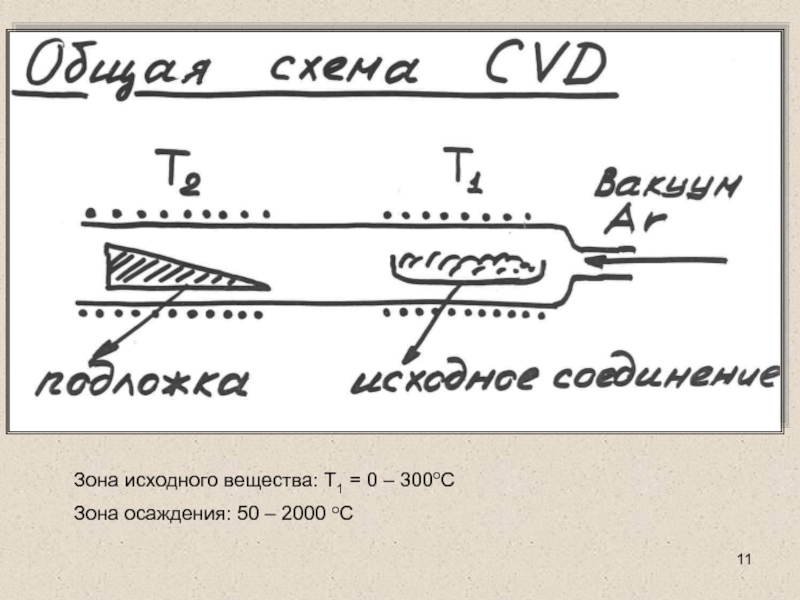
Слайд 11Зона исходного вещества: Т1 = 0 – 300оС
Зона осаждения: 50
– 2000 оС
Слайд 12Процессы CVD используют для получения следующих материалов:
-Элементы
Металлы и сплавы
Карбиды
Нитриды
Бориды
Оксиды
Интерметаллические соединения
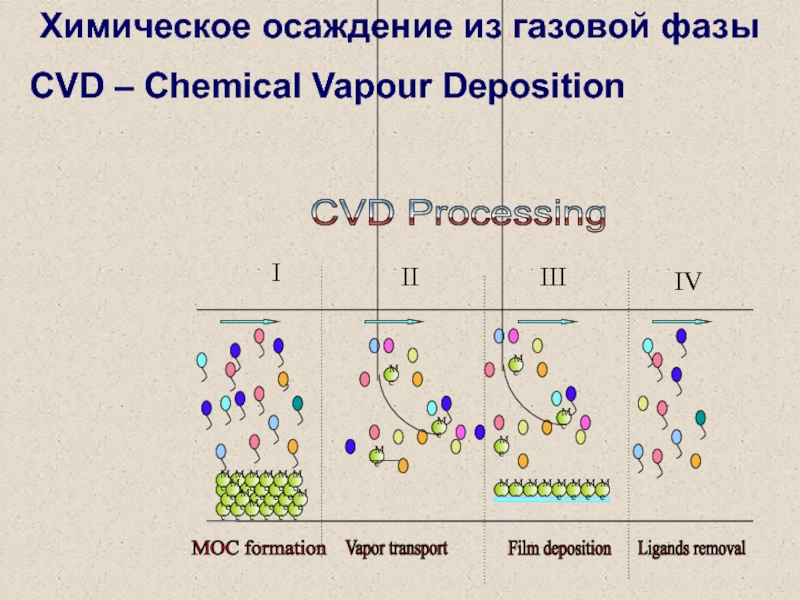
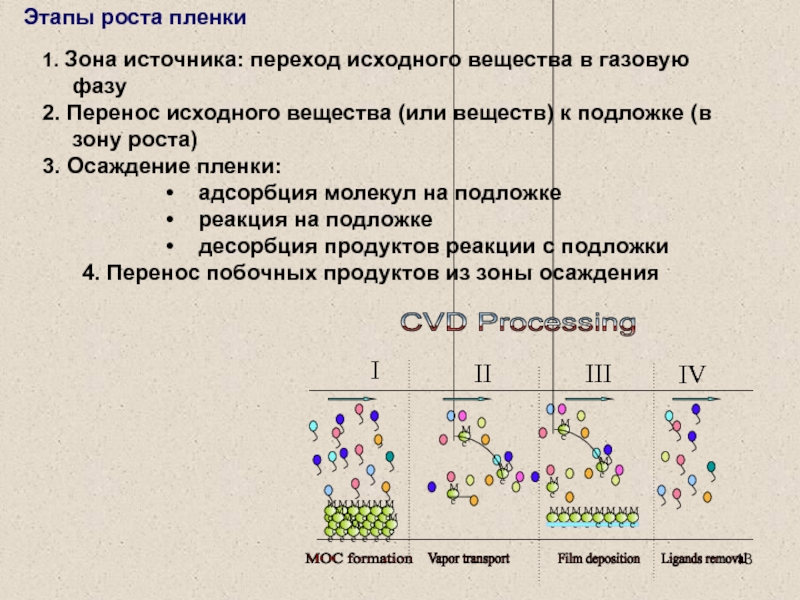
Слайд 13Этапы роста пленки
1. Зона источника: переход исходного вещества в газовую
фазу
2. Перенос исходного вещества (или веществ) к подложке (в зону
роста)
3. Осаждение пленки:
адсорбция молекул на подложке
реакция на подложке
десорбция продуктов реакции с подложки
4. Перенос побочных продуктов из зоны осаждения
IV
Слайд 14Проблематика разработки процессов CVD
Поиск наиболее подходящего исходного вещества или комбинации
веществ для получения пленок, исследование кинетики осаждения в ограниченных пределах
условий и определенных реакторах.
Поиск наилучшей конструкции реактора и аппаратуры в целом, в т.ч. для достижения максимальной производительности процессов CVD, максимальной однородности (равномерности толщины) материала в пределах подложки, повышения безопасности производства.
Снижение дефектности тонких слоев.
Контроль качества слоев и оптимизация процессов.
Слайд 15CVD аппараты состоят из нескольких основных компонентов:
- газораспределительная система
(доставка исходных
веществ в реакционную камеру)
- реактор или реакционная камера
(камера, где
происходит процесс осаждения)
- загрузочный механизм
(система ввода и удаления подложки)
- источник энергии:
резистивный нагрев, радиационный нагрев (галогеновые лампы), индуктивный нагрев, лазер
вакуумная система
система вывода газообразных продуктов реакции из реакционной камеры (ловушки)
Оборудование для контроля параметров процесса осаждения (контроль времени роста пленки, температуры, давления, скорости потоков, и т.д.)
Слайд 16Типы CVD реакторов
Классификация ракторов:
по давлению:
- реакторы атмосферного давления
(РАД, р = 760 мм рт. ст.)
-
реакторы пониженного давления (РПД, р < 760 мм рт. ст.)
- реакторы низкого давления (РНД, р 0.1 – 5 мм рт. ст.).
способу нагрева подложек:
реакторы с «горячими» и «холодными» стенками, в первом случае осуществляется прогрев всего реакционного объема, во втором – только подложки.
производительности:
с точки зрения количества одновременно обрабатываемых подложек реакторы могут быть: индивидуальные, т. е. осаждение происходит на одну подложку, и для нескольких подложек.
Слайд 17Типы CVD реакторов
1 – исходное вещество
2 – подложка
3 – печь
или нагреватель
4 - выхлоп
Слайд 20Типы исходных веществ:
Газообразные (наиболее удобны в использовании)
Жидкие
Твердые
Комбинации (в зависимости от
задачи)
Требования к исходным веществам
Стабильность при комнатной температуре
Достаточная летучесть
Достаточное
парциальное давление (для обеспечения высокой скорости роста пленки)
Температура реакции < Тпл подложки
Синтез необходимых веществ на подложке с легким удалением побочных газообразных продуктов
Низкая токсичность
Низкая стоимость
Слайд 21Рост пленок зависит от:
Переноса газа к поверхности подложки,
Адсорбции газа на
подложке
Скорости реакции на подложке
Перенос продуктов реакции от подложки
Типичные исходные
вещества:
Галогениды: TiCl4, TaCl5, WF6, и др.
Гидриды: SiH4, GeH4, В2Н6, NH3 ….
Металлоорганические соединения:
алкилы - AlMe3, Ti(CH2t-Bu)4
алкоголяты - Ti(OС2Н5)4
диаллиламиды - Ti(NMe2)4
- -дикетонаты: Cu(acac)2
- карбонилы: Ni(CO)4
…..
Слайд 22Типы CVD реакций
Пиролиз (крекинг)
AB(g) ---> A(s) + B(g)
Используют для
получения пленок:
Al, Ti, Pb, Mo, Fe, Ni, B, Zr, C,
Si, Ge,
SiO2, Al2O3, MnO2,
BN, Si3N4, GaN,
Si1-xGex,
Слайд 23- Пленки никеля
Ni(CO)4 Ni + 4CO
- Поликристаллические пленки Si:
SiH4
Si + 2H2 (Тосаж.= 860-920оС)
- Аморфные пленки
Si:
SiH4 а-Si + 2H2 (Тосаж.< 850оС)
- Пленки SiO2
Si(OC2H5)4 SiO2 + 4C2H4 + 2H2O
Слайд 242. Восстановление (реакции с водородом)
AX(g) + 1/2H2(g) A(s) +
HX(g)
Тосаж. в этих процессах ниже, чем при пиролизе.
Водород может использоваться
для финишной очистки поверхности подложки.
Используют для получения пленок
Al, Ti, Sn, Ta, Nb, Cr, Mo, Fe, B, Si, Ge, …
TaB, TiB2,
SiO2,
Nb3Ge, Si1-xGex, . . .
Пример:
WF6(g) + 3H2(g) W(s) + 6HF(g) Тосаж.= 300оC
SiCl4(g) + 2H2(g) Si(s) + 4HCl(g) Тосаж.= 1050-1250оC
Pb(CH3)4(g) + 2H2(g) Pb(s) + 4CH4(g) Тосаж.= 100-125 oC
Слайд 253. Окисление (часто используют кислород)
Используют для получения пленок:
SiO2, Al2O3,
TiO2, Ta2O5, SnO2, ZnO, . . .
Примеры:
Осаждение диоксида кремния SiO2
из смеси силана и кислорода при 450оC (Тосаж. ниже, чем при термическом окислении)
SiH4(g) + O2(g) SiO2(s) + 2H2(g)
SiH4 + 4N2O SiO2 + 2H2O + 4N2
SiH2Cl2 + 2N2O SiO2 + 2N2 + 2HCl
Слайд 264. Реакции получения нитридов с использованием аммиака
Использую для получения пленок:
TiN,
TaN, AlN, BN, ….
AX(g) + NH3(g) AN(s) + HX(g)
3GeH4
+ 4NH3 Ge3N4 + 12H2
3GeCl4 + 16NH3 Ge3N4 + 12NH4Cl
BF3(g) + NH3(g) BN(s) + 3HF(g) (1100оC)
3SiH4 + 4NH3 Si3N4 + 12H2
3SiCl4 + 16NH3 Si3N4 + 12NH4Cl
Слайд 27AX(g) + H2O(g) AO(s) + HX(g)
TiCl4 + 2H2O
TiO2 + 4HCl
SiF4 + 2H2O SiO2 + 4HF
5.
Реакции получения оксидов с использованием паров воды
Использую для получения пленок:
Al2O3, In2O3, SnO2, SiO2, . . .
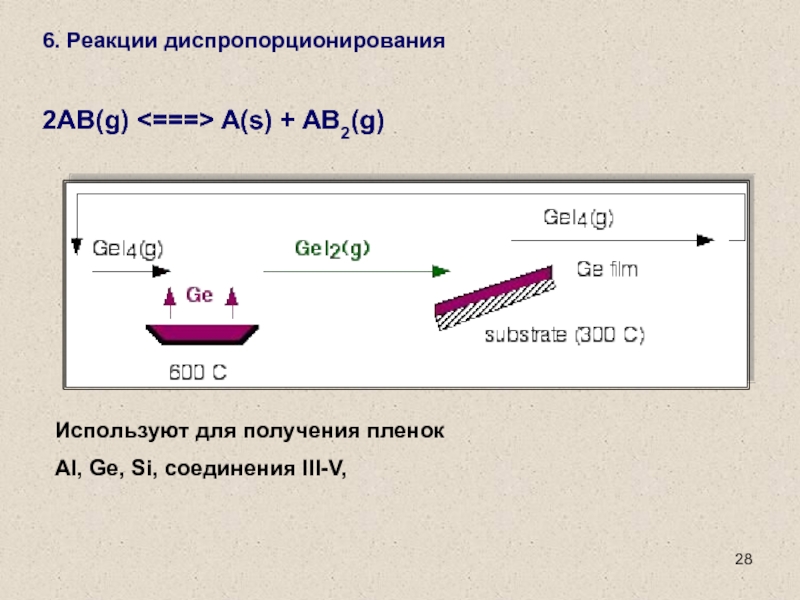
Слайд 286. Реакции диспропорционирования
2AB(g) A(s) + AB2(g)
Используют для получения пленок
Al,
Ge, Si, соединения III-V,
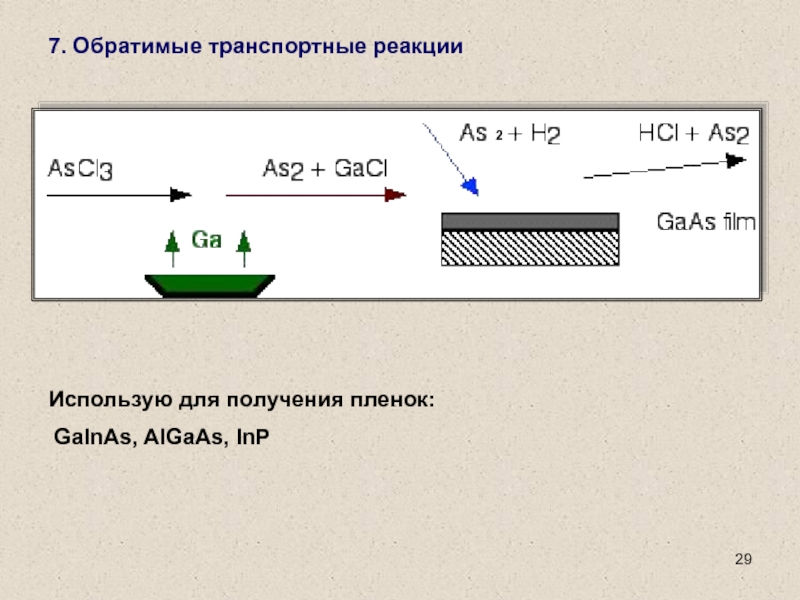
Слайд 297. Обратимые транспортные реакции
Использую для получения пленок:
GaInAs, AlGaAs, InP
2
Слайд 30Описание процессов роста слоев:
Установить количественную связь между скоростью роста слоя
и параметрами процесса CVD:
- температура осаждения пленки (Тосаж.)
- давление в реакционной камере (Робщ., Р(В) )
- линейная скорость газового потока (v)
- соотношения концентрации компонентов в газовой фазе.
Необходимо учитывать:
геометрию реактора
особенности пространственного расположения подложек в реакторе
Тепловой и газодинамический режимы
Эти факторы определяют задачу оптимизации процесса осаждения слоев, которая в конечном счете сводится к определению режимов с максимальной скоростью осаждения слоев с минимальной неоднородностью по толщине пленки на всей поверхности подложки.
Слайд 31Описание процессов роста слоев:
2. Второй зависимостью является взаимосвязь химического состава
слоев от входных параметров процесса.
3. В качестве третьей зависимости –
корреляция между совокупностью свойств (физических, химических функциональных) осажденных слоев и условиями их осаждения.
4. Взаимосвязь физических и химических свойств и функциональных характеристик пленок с их элементным и фазовым составом и структурой (для решения задачи синтеза материала с заранее заданными свойствами).
Слайд 32CVD (APCVD) - химическое осаждение из газовой фазы при атмосферном
давлении
Low Pressure CVD (LPCVD) - химическое осаждение из газовой фазы
при пониженном давлении
Р = 1мТорр – 1 Торр
Plasma Enhanced CVD (PECVD) – плазмохимическое осаждение из газовой фазы
Remote plasma-enhanced CVD (RPECVD) плазмохимическое осаждение из газовой фазы (подложка находится вне зоны плазменного разряда)
Hot Wire CVD (HWCVD) – известно как Catalytic CVD (Cat-CVD) или Hot Filament CVD (HFCVD)
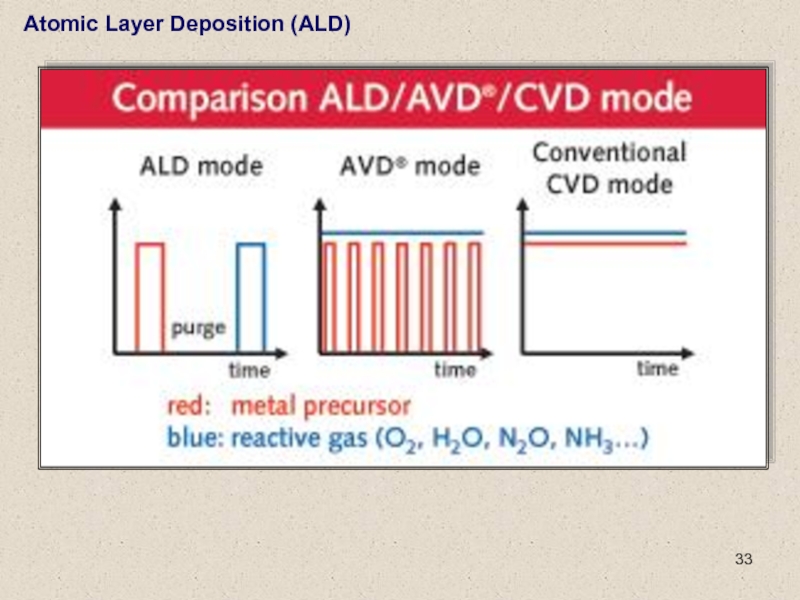
Atomic layer CVD (ALCVD) (также называют Atomic Layer Epitaxy and Atomic layer deposition (ALD)
Слайд 34Laser Enhanced CVD (LECVD) – химическое осаждение их газовой фазы,
стимулированное лазером,
другое название – Photo-assisted CVD (PCVD)
излучение лазера
используют для ускорения реакций на поверхности
2 процесса:
Пиролитический процесс
- нагрев подложки (увеличение Тподл., что приводит к
увеличению скорости реакции)
- Фотолитический процесс
- обычно используют ультрафиолетовое излучение
- диссоциация молекул в газовой фазе увеличивает
реакционную способность исходных веществ
Слайд 35Metalorganic CVD (MOCVD)
другое газвание Organometallic vapor phase epitaxy (OMVPE)
Исходные
вещества: металлоорганические соединения
(соединения содержат связь Ме-С)
Пример: (CH3)3Ga . . .
. триметилгаллий
Преимущества:
- являются летучими соединениями при относительно низких температурах
снижение температуры осаждения
Недостатки:
- загрязнение пленок углеродом
- Высокая токсичность, горючесть
(CH3)3Ga + H3As GaAs + 3CH4
(C2H5)3In + PH3 InP + 3C2H6
(CH3)4Pb + (C2H5)4Sn + (CH3)2Te Pb1-xSnxTe
(CH3)2Cd + H2S CdS + 2CH4
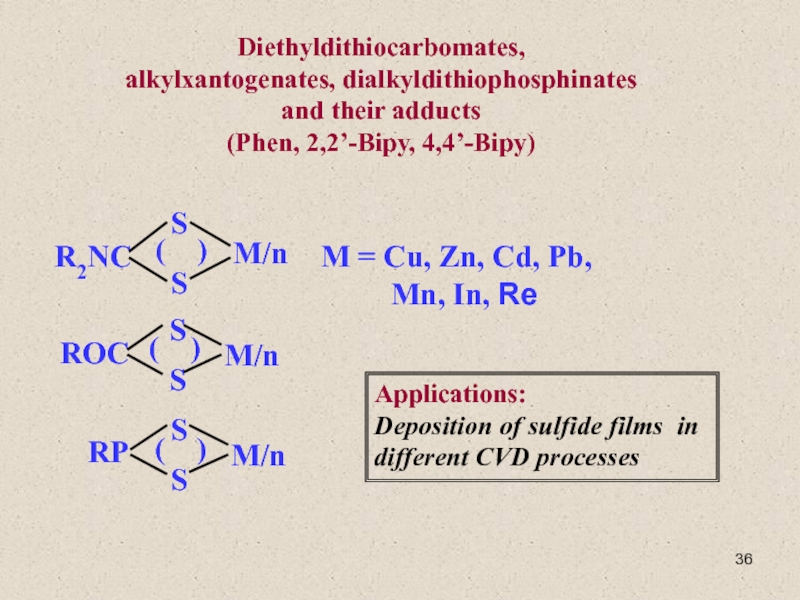
Слайд 36Diethyldithiocarbomates,
alkylxantogenates, dialkyldithiophosphinates
and their adducts
(Phen, 2,2’-Bipy, 4,4’-Bipy)
M
= Cu, Zn, Cd, Pb,
Mn,
In, Rе
Applications:
Deposition of sulfide films in
different CVD processes
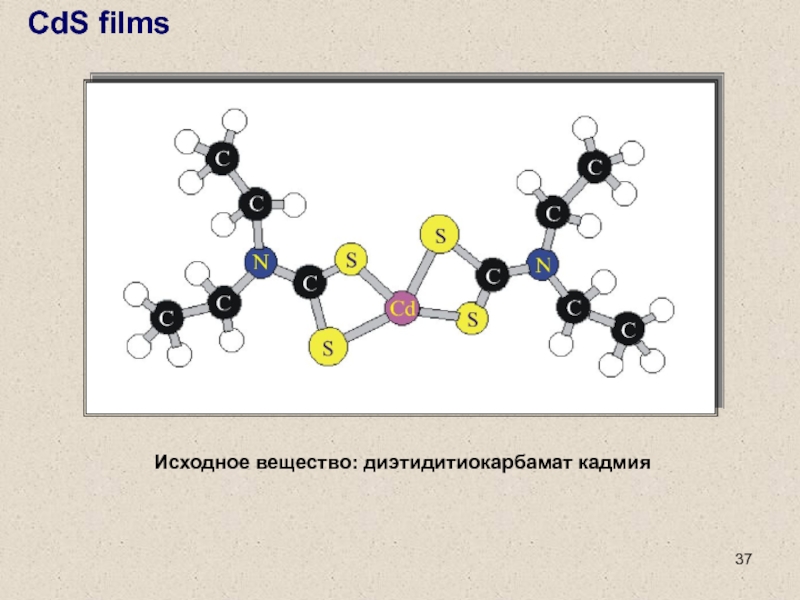
Слайд 37Исходное вещество: диэтидитиокарбамат кадмия
CdS films
Слайд 38CdS films
По сравнению с традиционным процессом:
-понижена температура синтеза
возможность получать многослоевые
структуры Cu2S/CdS/Si(100)
Слайд 43Термическая устойчивость:
Квантово-химический аспект: устойчивость изолированной молекулы МОС зависит от того,
заполнены ли все связывающие молекулярные орбитали МОС электронами и не
содержатся ли электроны на разрыхляющих орбиталях (это правило аналогично правилу устойчивости «октета»).
2) Термодинамический аспект: энтальпийный фактор: энергии связи в МОС, термическая устойчивость растет с увеличением энергий связи металл – радикал/лиганд.
3) Кинетический аспект: распад МОС увеличивается при наличии малой энергии активации распада и при явлении автокатализа продуктами распада – выделяющимся металлом)
Слайд 44Термораспад МОС
1)При реакциях распада МОС первично образуются радикалы в одну
стадию или ступенчато
RnM M + nR
2) Радикалы (лиганды) претерпевают
вторичные реакции:
Дегидрирование (отрыв водорода радикалами)
Распад радикала или лиганда
Рекомбинация или конденсация радикалов или лигандов
Реакции изомеризации
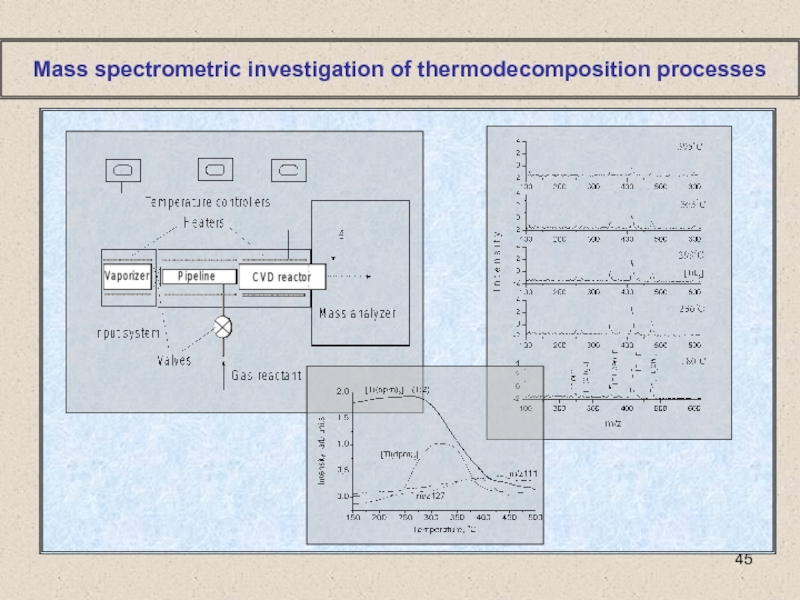
Слайд 45Mass spectrometric investigation of thermodecomposition processes
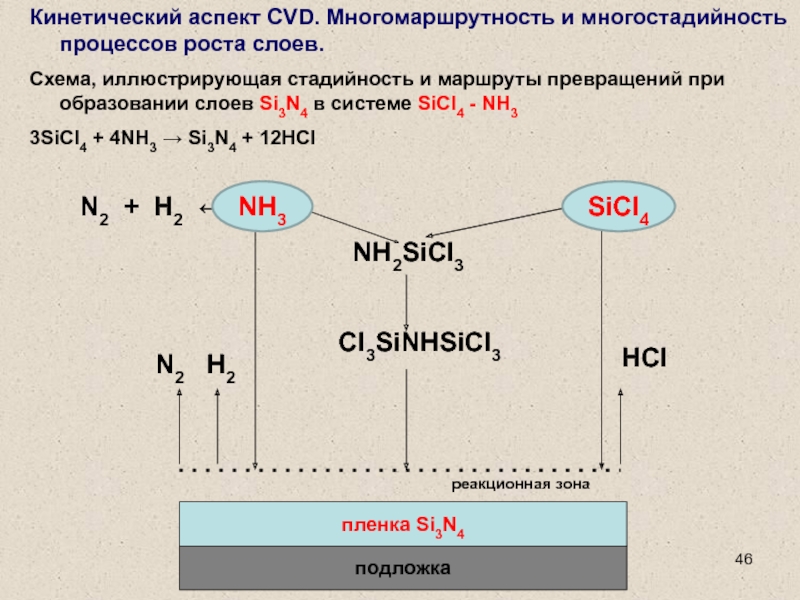
Слайд 46Кинетический аспект CVD. Многомаршрутность и многостадийность процессов роста слоев.
Схема, иллюстрирующая
стадийность и маршруты превращений при образовании слоев Si3N4 в системе
SiCl4 - NH3
3SiCl4 + 4NH3 Si3N4 + 12HCl
реакционная зона
N2 + H2 NH3 SiCl4
NH2SiCl3
Cl3SiNHSiCl3
N2 H2
HCl
NH3
SiCl4
Слайд 47Кинетический аспект CVD. Многомаршрутность и многостадийность процессов роста слоев.
Схема, иллюстрирующая
стадийность и маршруты превращений при образовании слоев Si3N4 в системе
SiH4 - NH3
Превращения в газовой фазе:
2NH3 N2 + 3H2
SiH4 SiH2 + H2
SiH2 + SiH4 Si2H6
Si2H6 2SiH3
nSi2H6 (SiH2)2n + nH2
Поверхностные превращения:
2NH3 2N(ads) + 3H2
NH3 N(ads) + 3H(ads)
2NH3 2NH3(ads) N2(gas)+ 3H2(gas)
SiH4 SiH4(ads)
SiH2 SiH2(ads)
SH3 SiH3(ads)
2NSi2/4NH2 SiN4/3 + 3H2
Слайд 48Обобщенная кинетическая схема образования слоя диэлектрика при CVD
As Bs
F
А и В – исходные реагенты
As и
Bs – реагенты в состоянии адсорбции
I, F – промежуточные продукты в газовой фазе и в адсорбционном слое
С – побочный продукт
DM – тонкий слой диэлектрического материала
A + B DM
Это превращение протекает многостадийно и, в общем случае, по нескольким маршрутам.
1
2
3
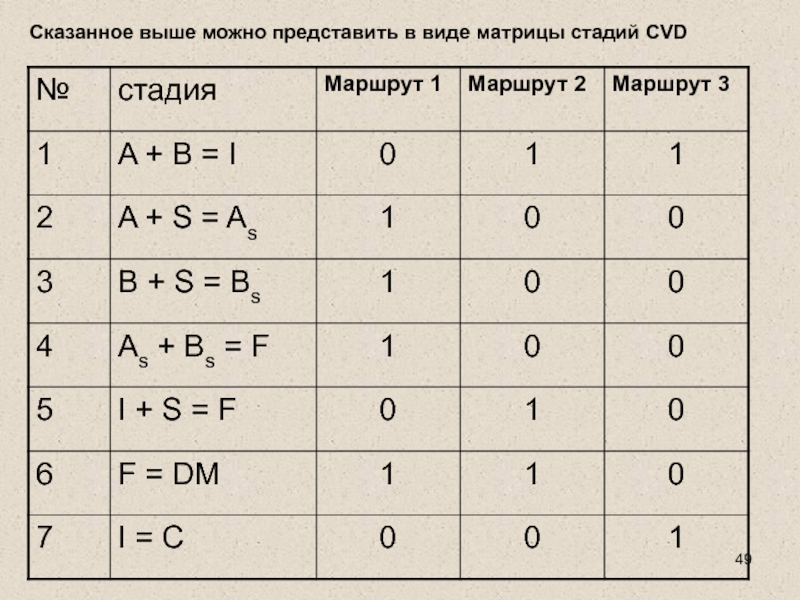
Слайд 49Сказанное выше можно представить в виде матрицы стадий CVD
Слайд 50Рассмотрим три основных маршрута:
Взаимодействие А и В в адсорбционном слое.
Взаимодействие
промежуточного продукта I с поверхностью растущего слоя с образование промежуточного
продукта F, конечное превращение которого в реакционной зоне приводит к образованию структурных единиц диэлектрика.
Образование в газовой фазе промежуточного продукта I и в дальнейшем побочного конечного продукта С.
Процесс роста диэлектрика описывается как сложная реакция, протекающая по трем параллельным маршрутам, каждый из которых является многостадийным.
1 маршрут – стадии 2, 3, 4, 6.
2 маршрут – стадии 1, 5, 6.
3 маршрут – 1 и 7.
Слайд 51Современные прецизионные микроэлектронные технологии требуют высокую воспроизводимость свойств материала и
размеров элементов приборов.
Оптимизация процессов CVD:
Параметры процесса CVD, влияющие на свойства
материала:
Температура осаждения пленки
Концентрация реагентов
Давление в реакционной камере
Скорость подачи реагентов
Геометрия реактора
И т. д.
Слайд 52Синтез пленок SiO2
- Моносилан и кислород (SiH4 + O2) (Тосаж.
673 К)
Пиролиз тетраэтоксисилана (C2H5O)4Si (Тосаж > 923 К)
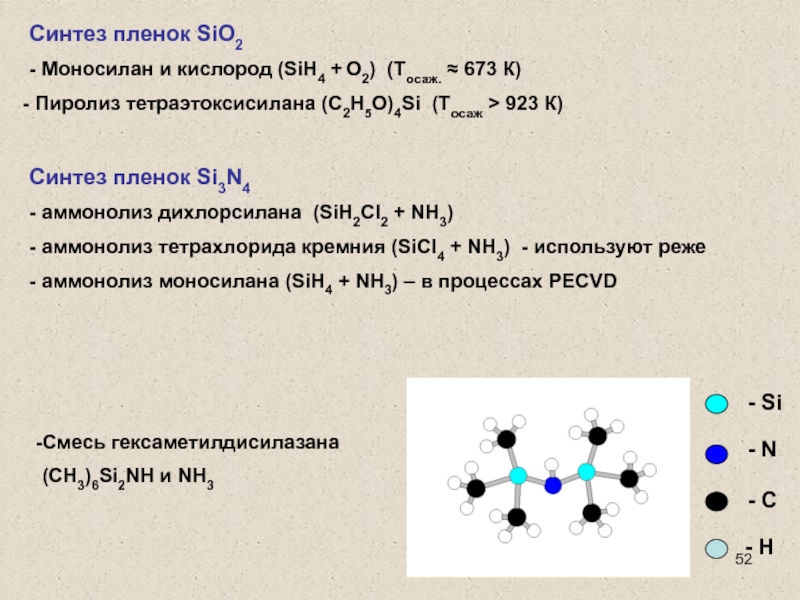
Синтез
пленок Si3N4
- аммонолиз дихлорсилана (SiH2Cl2 + NH3)
- аммонолиз тетрахлорида кремния (SiCl4 + NH3) - используют реже
- аммонолиз моносилана (SiH4 + NH3) – в процессах PECVD
Смесь гексаметилдисилазана
(CH3)6Si2NH и NH3
Слайд 53Синтез слоев нитрида бора BN (h-BN и c-BN)
CVD и LPCVD
BCl3+
NH3 BN + 3HCl (Тосаж. = 773 – 1673 K)
BF3
+ NH3 BN + 3HF
BBr3 + NH3 BN + 3HBr
B2H6 + 2NH3 2BN + 6H2
B2H6 + N2 2BN + 3H2
B10H14 + NH3 BN + B +H2
B3N3H6 3BN + 3H2
B3N3H3Cl3 3BN + 3HCl
(C2H5)2HNBH3 + NH3 + N2 BN
PECVD
2BCl3+ N2 + 3H2 2BN + 6HCl (Тосаж.=473 –873K)
BBr3+ NH3 BN + 3HBr
B2H6 + N2 2BN + 3H2
B2H6 + 2NH3 2BN + 6H2
(CH3)2HNBH3 + NH3 BN
(C2H5)3NBH3 + NH3 BN
(CH3)2HN.BH3 +NH3 + Ar BN
(CH3)2HN.BH3 + NH3+ H2 BN
B3N3H6 + (Ar, He, H2) 3BN + 3H2
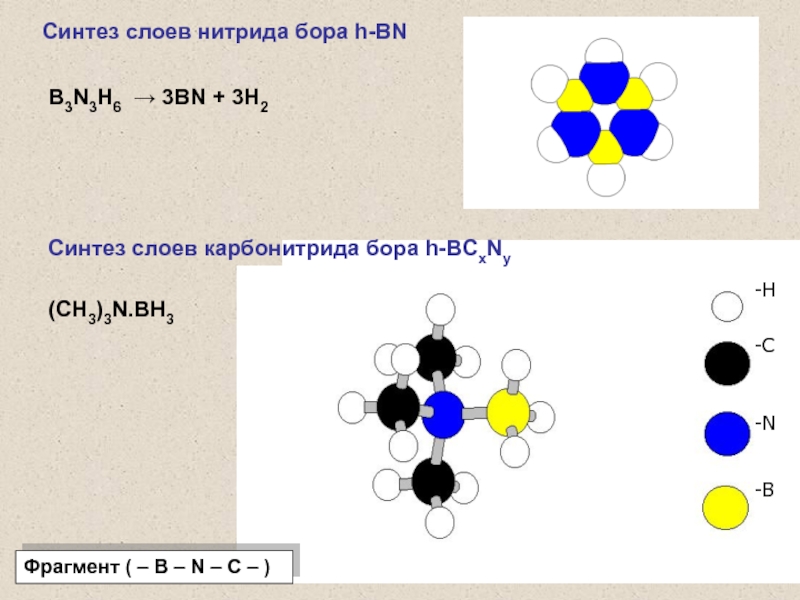
Слайд 54B3N3H6 3BN + 3H2
Синтез слоев нитрида бора h-BN
Синтез слоев
карбонитрида бора h-BСхNу
(CH3)3N.BH3
Фрагмент ( – B – N – C
– )